La enfermedad de Kawasaki (EK) es una vasculitis multisistémica asociada a lesiones en las arterias coronarias. Las infecciones podrían ser un desencadenante de la inflamación. Nuestro objetivo fue describir la presencia de infecciones en los niños con EK y analizar las características clínicas y la presencia de alteraciones coronarias en estos casos.
Pacientes y métodosAnálisis retrospectivo de los pacientes incluidos en la red KAWA-RACE entre 2011 y 2016. Se estudió tanto a los pacientes que tuvieron una identificación microbiológica confirmada (IMC) en el periodo agudo como a los que presentaron antecedente de infección previa reciente (IPR) las 4 semanas anteriores.
ResultadosSe incluyó a un total de 621 niños, de los cuales 101 (16,3%) tuvieron una IMC y 107 (17,2%) una IPR. Encontramos una significativa menor afectación ecocardiográfica en el grupo de IPR respecto a los niños sin infección previa (23 vs. 35%; p 0,01), con menor proporción no significativa de las alteraciones coronarias globales (16 vs. 25%; p 0,054). Sin embargo, no se detectaron diferencias en la proporción de aneurismas en ninguno de los 2grupos (IMC o IPR) respecto al resto de los pacientes sin infecciones asociadas.
ConclusionesEn nuestro estudio no encontramos diferencias en la incidencia de aneurismas coronarios en niños con y sin IMC o IPR, por lo que ante la sospecha de EK debe iniciarse siempre tratamiento, aunque se tenga infección confirmada microbiológicamente.
Kawasaki disease (KD) is a multisystem vasculitis associated with coronary artery abnormalities. Infections could be a trigger of the inflammation. The main aim of this study was to describe the presence of infections in children with KD, and to analyse the clinical characteristics and the presence of coronary abnormalities in these cases.
Patients and methodsA retrospective study was performed within the Kawasaki Diseases Network (KAWA-RACE (2011-2016). An analysis was performed that included patients with positive microbiological findings (PMF) during the acute phase, as well as those with a previous recent infection (PRI) during the 4 weeks preceding KD diagnosis.
ResultsThe study included total of 621 children with KD, with PMF being found in 101 (16.3%) patients, and a PRI in 107 (17.2%). Significantly less echocardiographic abnormalities were found in the in the group with a PRI, when compared to those without a PRI (23 vs. 35%, P=.01) and also a lower proportion of overall coronary artery lesions (16 vs. 25%, P=.054). No significant differences were found in the proportion of aneurysms in either of these groups (PRI or PMF) when compared to those without infection.
ConclusionsIn the present study, no differences were found in the incidence of coronary aneurysms in either of the groups, with or without PRI or PMF. Therefore, if KD is suspected, appropriate treatment should be started despite having a confirmed infection.
La enfermedad de Kawasaki (EK) es una vasculitis aguda autolimitada que afecta a vasos de pequeño y mediano calibre y que habitualmente se desarrolla en la infancia. En la actualidad es la causa más común de enfermedad cardiaca adquirida en niños en nuestro medio1,2. Su incidencia en Europa se sitúa en torno a 8/100.000 de los niños menores de 5 años3,4. Aunque los hallazgos clínicos, de laboratorio y las características epidemiológicas de la enfermedad señalan un origen o desencadenante infeccioso, aún no se ha podido identificar5,6. Se han publicado algunos estudios de asociación de genoma completo (GWAS) en EK y se han identificado varios loci biológicamente plausibles, implicados en la inflamación, la respuesta inmunitaria y el estado cardiovascular2,7,8. Así, una hipótesis razonablemente abierta es que la EK está causada por un agente infeccioso aún por identificar, que produce enfermedad solo en individuos genéticamente predispuestos. Su rareza en los primeros meses de vida y en adultos indica un agente al que estos últimos son inmunes y del cual los lactantes muy pequeños están protegidos por anticuerpos maternos pasivos.
El diagnóstico de la EK es clínico y se realiza mediante los criterios diagnósticos propuestos por la Asociación Americana de Cardiología (AHA)2. La presencia de una infección previa o simultánea, máxime si existe confirmación microbiológica, se puede considerar un diagnóstico alternativo que descarte el de EK. Este aspecto está hoy en día en discusión. El objetivo de este trabajo fue estudiar la existencia de infecciones previas o concomitantes en los niños con diagnóstico de EK en la red española para el estudio de esta enfermedad, KAWA-RACE, y su relación con la presencia de alteraciones coronarias.
Pacientes y métodosEn 2015 se creó una red pediátrica de ámbito nacional para el estudio de la EK (red KAWA-RACE) con el apoyo de las sociedades de infectología pediátrica (SEIP), de reumatología pediátrica (SERPE) y de cardiología pediátrica (SECPPC). Participaron 53 hospitales españoles de todas las regiones, que recogieron los datos epidemiológicos, clínicos y de tratamiento de los pacientes en una base de datos online (REDcap)9. Se diseñó un estudio retrospectivo entre los años 2011 y 2016 en el que se incluyó a los pacientes menores de 16 años que cumplían los criterios diagnósticos de EK según la AHA10 en los hospitales participantes. El estudio cuenta con la aprobación del Comité de Ética.
Se definieron como:
- •
Infección previa reciente (IPR): infección diagnosticada en las 4 semanas previas al diagnóstico de EK sin necesidad de tener una prueba microbiológica positiva que confirme la infección.
- •
Infección microbiológicamente confirmada (IMC): infección diagnosticada durante el periodo agudo de la EK y con una prueba microbiológica positiva.
Se consideraron alteraciones cardiológicas ecocardiográficas todas las posibles afectaciones, incluyendo la presencia de insuficiencias valvulares, pericarditis, signos de miocarditis y afectaciones coronarias. La alteración coronaria incluyó la presencia de hiperrefringencias, ectasias y aneurismas coronarios definidos por los criterios de la AHA2.
Análisis estadísticoEl análisis estadístico se realizó mediante el Statistical Package for the Social Sciences (SPSS), versión 20.0. Los valores fueron expresados como porcentajes para las variables discretas, y como media y desviación estándar (DE) para las variables continuas. Se compararon las características clínicas y analíticas, así como la presencia de alteraciones coronarias en los pacientes con y sin IPR o IMC. Las características clínicas y las variables de laboratorio fueron comparadas empleando el test t de Student, el test U de Mann-Whitney, el test χ2, y el test exacto de Fisher cuando fue apropiado. Un valor de p <0,05 fue considerado como estadísticamente significativo.
ResultadosSe incluyó a un total de 621 pacientes con EK. El 63% fueron varones. La media de edad al diagnóstico fue de 2,8 años (DE=2,4); 494 (79,5%) eran menores de 5 años. Un total de 437 casos fueron clasificados como EK completa (70,4%), 171 como incompleta (27,5%) y 13 como casos atípicos (2,1%). Se hallaron aneurismas coronarios en 60 casos (9,7%), que fueron persistentes en 28 (4,5%) de ellos.
Infecciones previas recientesDel total de 621 casos, refirieron una IPR 107 (17,2%) pacientes. Se detectaron más frecuentemente en primavera (38%; p 0,023). Los pacientes con IPR no difirieron en sexo, edad, tipo de EK, parámetros analíticos, duración total de la fiebre o necesidad de una segunda dosis de inmunoglobulina intravenosa, de los niños sin infección previa (tabla 1). De los 5 criterios clínicos principales, se encontraron diferencias en la presencia de adenopatías, que fue mayor en el grupo de IPR (76 vs. 64%; p 0,01). Se encontró una significativa menor afectación en la ecocardiografía y menor proporción no significativa de alteración coronaria en el grupo de IPR (23 vs. 35%; p 0,01 y 16 vs. 25%; p 0,054, respectivamente), aunque no se encontraron diferencias en la presencia de aneurismas.
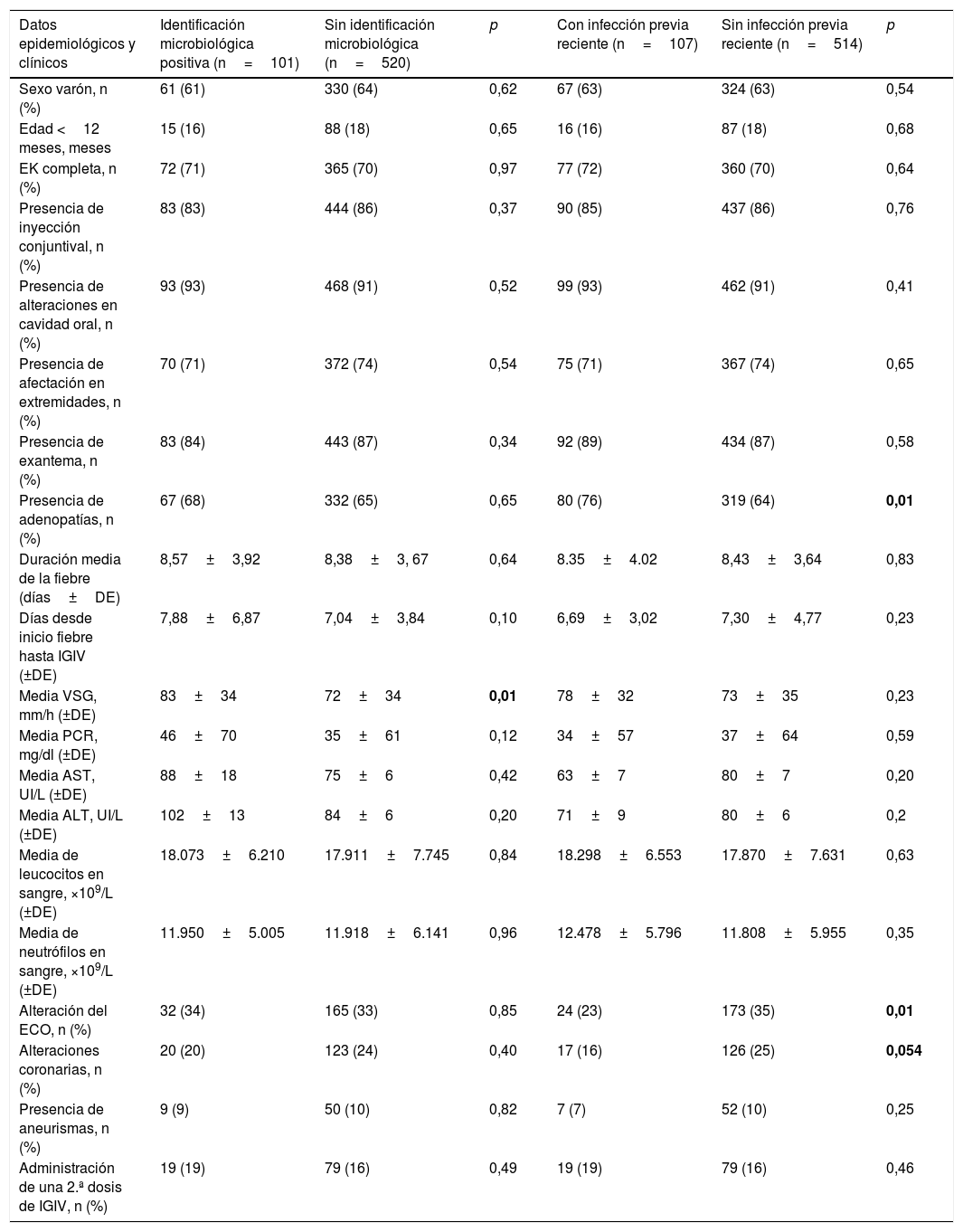
Datos epidemiológicos, clínicos y analíticos en pacientes con enfermedad de Kawasaki con relación a tener o no identificación microbiológica positiva en el periodo agudo de la enfermedad o antecedente de infección en las 4 semanas previas al diagnóstico
| Datos epidemiológicos y clínicos | Identificación microbiológica positiva (n=101) | Sin identificación microbiológica (n=520) | p | Con infección previa reciente (n=107) | Sin infección previa reciente (n=514) | p |
|---|---|---|---|---|---|---|
| Sexo varón, n (%) | 61 (61) | 330 (64) | 0,62 | 67 (63) | 324 (63) | 0,54 |
| Edad <12 meses, meses | 15 (16) | 88 (18) | 0,65 | 16 (16) | 87 (18) | 0,68 |
| EK completa, n (%) | 72 (71) | 365 (70) | 0,97 | 77 (72) | 360 (70) | 0,64 |
| Presencia de inyección conjuntival, n (%) | 83 (83) | 444 (86) | 0,37 | 90 (85) | 437 (86) | 0,76 |
| Presencia de alteraciones en cavidad oral, n (%) | 93 (93) | 468 (91) | 0,52 | 99 (93) | 462 (91) | 0,41 |
| Presencia de afectación en extremidades, n (%) | 70 (71) | 372 (74) | 0,54 | 75 (71) | 367 (74) | 0,65 |
| Presencia de exantema, n (%) | 83 (84) | 443 (87) | 0,34 | 92 (89) | 434 (87) | 0,58 |
| Presencia de adenopatías, n (%) | 67 (68) | 332 (65) | 0,65 | 80 (76) | 319 (64) | 0,01 |
| Duración media de la fiebre (días±DE) | 8,57±3,92 | 8,38±3, 67 | 0,64 | 8.35±4.02 | 8,43±3,64 | 0,83 |
| Días desde inicio fiebre hasta IGIV (±DE) | 7,88±6,87 | 7,04±3,84 | 0,10 | 6,69±3,02 | 7,30±4,77 | 0,23 |
| Media VSG, mm/h (±DE) | 83±34 | 72±34 | 0,01 | 78±32 | 73±35 | 0,23 |
| Media PCR, mg/dl (±DE) | 46±70 | 35±61 | 0,12 | 34±57 | 37±64 | 0,59 |
| Media AST, UI/L (±DE) | 88±18 | 75±6 | 0,42 | 63±7 | 80±7 | 0,20 |
| Media ALT, UI/L (±DE) | 102±13 | 84±6 | 0,20 | 71±9 | 80±6 | 0,2 |
| Media de leucocitos en sangre, ×109/L (±DE) | 18.073±6.210 | 17.911±7.745 | 0,84 | 18.298±6.553 | 17.870±7.631 | 0,63 |
| Media de neutrófilos en sangre, ×109/L (±DE) | 11.950±5.005 | 11.918±6.141 | 0,96 | 12.478±5.796 | 11.808±5.955 | 0,35 |
| Alteración del ECO, n (%) | 32 (34) | 165 (33) | 0,85 | 24 (23) | 173 (35) | 0,01 |
| Alteraciones coronarias, n (%) | 20 (20) | 123 (24) | 0,40 | 17 (16) | 126 (25) | 0,054 |
| Presencia de aneurismas, n (%) | 9 (9) | 50 (10) | 0,82 | 7 (7) | 52 (10) | 0,25 |
| Administración de una 2.ª dosis de IGIV, n (%) | 19 (19) | 79 (16) | 0,49 | 19 (19) | 79 (16) | 0,46 |
Negrita: diferencias estadísticamente significativas.
ALT: alanina aminotransferasa; DE: desviación estándar; ECO: ecocardiografía; EK: enfermedad de Kawasaki; IGIV: inmunoglobulina intravenosa; PCR: proteína C reactiva; VSG: velocidad de sedimentación globular.
Las IPR más frecuentes referidas fueron las siguientes: foco ORL (faringoamigdalitis) (n=65; 61%), gastroenteritis (n=12; 11%), otitis media aguda (n=7; 7%), infección del tracto urinario (n=6; 6%), enfermedad exantemática escarlatiniforme (n=5; 5%) e infección de piel y partes blandas (n=3; 3%). Los pacientes cuya infección previa fue un foco ORL tuvieron aneurismas coronarios en el 10,5% de los casos; esta proporción fue superior al resto del grupo de los niños con IPR (7%; p 0,051).
Infecciones microbiológicamente confirmadasSe identificaron 101 casos (16,3%) que tuvieron una IMC; 9 pacientes tuvieron varias y hubo 4 coinfecciones virales (tabla 2). Las IMC fueron más frecuentes durante la primavera (34% de ellas; p 0,07). Los pacientes con IMC no difirieron en sexo, edad, tipo de EK, criterios diagnósticos clínicos, duración total de la fiebre o necesidad de una segunda dosis de inmunoglobulina intravenosa de los pacientes sin identificación microbiológica (tabla 1). Se objetivó que la velocidad de sedimentación globular se encontraba significativamente más elevada en el grupo con IMC (83 vs. 72mm/h). No se encontraron diferencias en la presencia de alteraciones ecocardiográficas en general, ni de alteraciones coronarias o aneurismas.
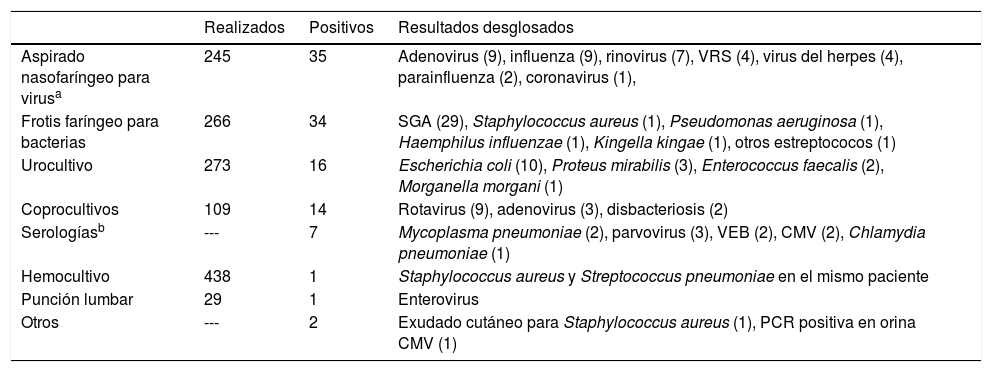
Resultados microbiológicos positivos obtenidos en pacientes con enfermedad de Kawasaki (KAWA-RACE 2011-2016)
| Realizados | Positivos | Resultados desglosados | |
|---|---|---|---|
| Aspirado nasofaríngeo para virusa | 245 | 35 | Adenovirus (9), influenza (9), rinovirus (7), VRS (4), virus del herpes (4), parainfluenza (2), coronavirus (1), |
| Frotis faríngeo para bacterias | 266 | 34 | SGA (29), Staphylococcus aureus (1), Pseudomonas aeruginosa (1), Haemphilus influenzae (1), Kingella kingae (1), otros estreptococos (1) |
| Urocultivo | 273 | 16 | Escherichia coli (10), Proteus mirabilis (3), Enterococcus faecalis (2), Morganella morgani (1) |
| Coprocultivos | 109 | 14 | Rotavirus (9), adenovirus (3), disbacteriosis (2) |
| Serologíasb | --- | 7 | Mycoplasma pneumoniae (2), parvovirus (3), VEB (2), CMV (2), Chlamydia pneumoniae (1) |
| Hemocultivo | 438 | 1 | Staphylococcus aureus y Streptococcus pneumoniae en el mismo paciente |
| Punción lumbar | 29 | 1 | Enterovirus |
| Otros | --- | 2 | Exudado cutáneo para Staphylococcus aureus (1), PCR positiva en orina CMV (1) |
CMV: citomegalovirus; PCR: proteína C reactiva; SGA: estreptococo del grupo A; VEB: virus de Epstein Barr; VRS: virus respiratorio sincitial.
Nuestro estudio pone de manifiesto que el tener una infección reciente o simultánea con la EK es frecuente y que no disminuye el riesgo de desarrollar aneurismas coronarios. La presencia de una IPR es también manifiesta en la literatura5,6,11. Weng et al. realizan un estudio de base poblacional en el que siguen a 285.636 niños con infección por enterovirus y a 285.636 niños sin dicha infección, y encontraron en el grupo de niños expuestos una incidencia de EK un 54% mayor que en el grupo de no expuestos5.
La clínica de muchas de las infecciones más frecuentes en la edad pediátrica se solapa con los criterios clínicos diagnósticos de la EK, lo que dificulta su diagnóstico2. En nuestra serie, encontramos 65/621 (10,5%) pacientes con antecedente de una infección ORL y 6/621 (1%) con enfermedad exantemática escarlatiniforme; ambas infecciones se solapan con los criterios diagnósticos principales de EK. También 12/621 (2%) presentaron una gastroenteritis: está descrito en la literatura que la EK puede asociar síntomas compatibles con este diagnóstico2,3, como ha sido descrito en un estudio español realizado por Sánchez-Manubens et al., que lo encuentran hasta en un 24% de los pacientes3.
Clásicamente ha existido la impresión de que la EK se encuentra sobrediagnosticada12. En nuestro estudio encontramos una menor incidencia de afectación cardiaca en el grupo de pacientes con antecedente de IPR, lo que podría hacer pensar que la EK es una enfermedad sobrediagnosticada también en nuestro medio2, pero no hubo diferencias en la presencia de aneurismas.
En nuestra cohorte, el porcentaje de afectación coronaria y, más concretamente, de aneurismas coronarios (7-10%) fue alto en comparación con las series asiáticas de Japón (0,91%), Corea (1,7%) o Shangai (1,1%), menor que el publicado en EE. UU. (13%) y otros países de nuestro entorno como Holanda (13,5%) o Alemania (17%), pero aproximado al descrito en series de países vecinos como Portugal (8,5%)8-14. No obstante, recientemente Coon et al.15 han publicado datos de 48 hospitales estadounidenses en los que la tasa de diagnósticos de alteraciones coronarias no graves en la EK casi se ha duplicado en los últimos 15 años, sin un cambio significativo en la tasa de resultados cardiacos adversos. En Europa podría estar sucediendo el mismo fenómeno de sobrediagnóstico, lo que hace necesario un análisis acerca de qué lesiones coronarias son clínicamente significativas, para maximizar el beneficio y minimizar el daño en estos niños.
El hecho de que la presencia de adenopatías sea más frecuente en el grupo de IPR, y dado que es un criterio diagnóstico de EK, podría estar contribuyendo a un posible sobrediagnóstico y a que algunos casos sean considerados como EK sin serlo. Nuestros resultados, sin embargo, ponen de manifiesto que sigue siendo un reto el diagnóstico de esta enfermedad. Dado el riesgo de afectación cardiaca que supone no tratar una verdadera EK, consideramos que se debe ser muy cauto y riguroso antes de desaconsejar el tratamiento, sobre todo en los grupos de mayor riesgo, como son los lactantes o los cuadros graves.
Si analizamos la presencia de infecciones simultáneas, en la literatura hay multitud de estudios que han señalado varios virus como desencadenantes de EK, incluyendo virus coxsackie, parainfluenza, virus respiratorio sincitial, metapneumovirus, chikungunya, citomegalovirus y enterovirus, entre otros5,6,11. Algunos estudios describen que hasta la mitad de los casos de EK tienen uno o más virus respiratorios positivos detectados por PCR, si bien su papel patogénico no está claro11. Chang et al. seleccionaron a 226 niños con EK y a 226 niños sanos y realizaron PCR y cultivo para virus respiratorios en secreciones respiratorias. Encontraron presencia de virus en el 50,4% de los enfermos vs. el 16,4% en los sanos (p <0,001) y concluyen que las infecciones víricas se asocian a la EK4.
Por otra parte, no hay que obviar la naturaleza de la infección vírica y la posibilidad de que un sujeto quede de portador asintomático por un periodo variable de tiempo tras una infección viral. La infección por adenovirus puede ser un ejemplo de lo anterior, al ser un virus que solapa sus síntomas con los de la EK y que además tiene la particularidad de elevar de forma importante los reactantes de fase aguda en la analítica, como ocurre también en nuestra serie. Jaggi et al.16 describen la detección de adenovirus en la nasofaringe de pacientes con EK completa, incompleta y sujetos sanos, y encuentran que, en los pacientes con EK completa, la carga viral era significativamente menor que en los clasificados como EK incompleta y concluyen que tener un resultado positivo para adenovirus en un paciente con EK debe ser tomado con precaución, ya que podemos estar delante de un paciente con infección por adenovirus que cumple criterios de EK o ante un paciente con EK en el que se detecta de forma concomitante adenovirus en un portador asintomático.
A pesar de aislar los virus en la fase aguda de los pacientes con EK, está descrita una misma incidencia de alteraciones coronarias en estos casos que en los que no presentan la infección, al igual que ocurre en nuestra cohorte6. En nuestro estudio encontramos 35/621 (5,6%) pacientes con virus respiratorios positivos, cifra considerablemente inferior, pero en nuestra serie tan solo se realizó aspirado nasofaríngeo para virus en 245 (39%) pacientes y no en todos los centros se realiza panel de virus respiratorios por PCR. El carácter retrospectivo de nuestro estudio y la ausencia de un protocolo común de diagnóstico microbiológico constituyen la principal limitación de este trabajo. Para establecer la incidencia real de infecciones en pacientes con EK se deberían realizar de forma sistemática las mismas pruebas microbiológicas a todos los pacientes, pero esto no está estandarizado e incluso las guías de la AHA más recientes, de 2017, lo dejan a criterio del clínico y en función de los síntomas del paciente2.
En definitiva, la presencia de una infección concomitante no descarta el diagnóstico de EK ni en nuestra serie ni en la literatura, lo que pone en duda la teoría del sobrediagnóstico.
En conclusión, no encontramos diferencias en la incidencia de afectación cardiaca en los pacientes con y sin aislamiento microbiológico confirmado, por lo que ante la sospecha de EK debe iniciarse siempre tratamiento, independientemente de que exista sospecha de infección o de que se obtengan resultados microbiológicos positivos. En nuestra serie, las infecciones previas recientes se siguieron de menor incidencia de alteraciones coronarias en los pacientes con diagnóstico de EK, aunque no de aneurismas coronarios. Parece claro que son necesarios estudios prospectivos de calidad que ayuden a establecer el papel de las infecciones en la EK. Esperamos que el reclutamiento prospectivo, ya puesto en marcha en KAWA-RACE y al que animamos a participar a todos los centros de nuestro país, colabore a esclarecer estas incógnitas.
FinanciaciónEl grupo de trabajo KAWA-RACE ha recibido una beca para la investigación de la Sociedad Española de Reumatología Pediátrica (SERPE), convocatoria 2015. Dicho dinero se dedica al desarrollo del grupo de trabajo y a los costes administrativos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Agradecemos a todos los investigadores del grupo de trabajo KAWA-RACE su participación y contribución de pacientes.
Se han enviado resúmenes relacionados con este trabajo al congreso de la AEP en Zaragoza, en junio de 2018, (aceptados como comunicaciones orales) y a la ESPID en Malmö, en mayo de 2018, aceptado como póster sin defensa.