La detección de los defectos de la β-oxidación mitocondrial y de algunas acidurias orgánicas es posible mediante el análisis del perfil de acilcarnitinas en el cribado metabólico neonatal. Pese a la alta sensibilidad del cribado, las concentraciones de carnitina y acilcarnitinas presentan diferencias en los recién nacidos prematuros con respecto a los a término, lo que puede conllevar variaciones en la rentabilidad diagnóstica1. Para una detección más precisa de los errores congénitos del metabolismo en prematuros, sobre todo en los más inmaduros, son necesarios estudios adicionales que amplíen el conocimiento, todavía limitado, de su perfil de carnitina y acilcarnitinas.
Se efectuó un estudio observacional retrospectivo con inclusión de 144 prematuros de muy bajo peso al nacimiento (peso<1.500g), ingresados en la Unidad de Neonatología de nuestro centro durante 6 años, con los siguientes criterios de exclusión: encefalopatía hipóxico-isquémica, hemorragia intraventricular grados iii y iv, y/o disfunción renal o hepática grave. El objetivo del trabajo fue el establecimiento de la media, mediana y percentiles de normalidad de carnitina libre (CL), carnitina total (CT) y ésteres de carnitina en las 2 primeras semanas de vida en esta subpoblación de prematuros.
Previa autorización del Comité Ético, se emplearon para el estudio las muestras de sangre impregnadas en papel obtenidas a los 3-5 días (a las 48h de la primera ingesta oral efectiva) y a los 15 días de vida para el cribado metabólico, de acuerdo con la cronología de muestras del cribado neonatal en prematuros vigente en nuestra comunidad autónoma. El análisis de las concentraciones de CL y acilcarnitinas fue realizado mediante espectrometría de masas en tándem, empleando un equipo de triple cuadripolo (ESI-MS/MS API 2000, applied Biosystems Scienx, Toronto, Canadá), conforme a la metodología descrita por Millington et al.2.
En el estudio se incluyó a 73 mujeres y 71 hombres con edad gestacional media de 30 semanas (rango: 24-36), peso medio de 1.210g (rango: 570-1.490g) y una distribución homogénea entre prematuros de peso adecuado (n=73) y de bajo peso (n=71) para su edad gestacional. El peso medio en los prematuros de peso adecuado fue 1.245g y en los de bajo peso 1.190g.
Las concentraciones medias objetivadas al tercer-quinto día fueron: CL: 29,19μmol/l, CT: 58,09μmol/l y total de acilcarnitinas (tAC): 29,69μmol/l, siendo las concentraciones menores a los 15 días (CL: 22,22μmol/l, CT: 42,65μmol/l y tAC: 20,69μmol/l). En las concentraciones relativas de acilcarnitinas de cadena corta, media y larga se objetiva igualmente un descenso en la segunda muestra con respecto a la primera. Este descenso fue significativo en todos los parámetros excepto para las acilcarnitinas de cadena media. La comparación estadística se realizó mediante la prueba de Wilcoxon. Los percentiles de referencia de CL y de los ésteres de carnitinas en la población se reflejan en la tabla 1.
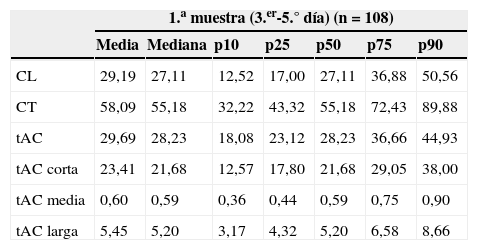
Percentiles de CL, CT, tAC, tACc, tACm y tACl (μmol/l) en prematuros de muy bajo peso al nacimiento
| 1.a muestra (3.er-5.° día) (n=108) | |||||||
|---|---|---|---|---|---|---|---|
| Media | Mediana | p10 | p25 | p50 | p75 | p90 | |
| CL | 29,19 | 27,11 | 12,52 | 17,00 | 27,11 | 36,88 | 50,56 |
| CT | 58,09 | 55,18 | 32,22 | 43,32 | 55,18 | 72,43 | 89,88 |
| tAC | 29,69 | 28,23 | 18,08 | 23,12 | 28,23 | 36,66 | 44,93 |
| tAC corta | 23,41 | 21,68 | 12,57 | 17,80 | 21,68 | 29,05 | 38,00 |
| tAC media | 0,60 | 0,59 | 0,36 | 0,44 | 0,59 | 0,75 | 0,90 |
| tAC larga | 5,45 | 5,20 | 3,17 | 4,32 | 5,20 | 6,58 | 8,66 |
| 2.a muestra (15.° día) (n=81) | Descenso medio entre las 2 muestras | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Media | Mediana | p10 | p25 | p50 | p75 | p90 | p | ||
| CL | 22,22 | 19,52 | 9,55 | 13,26 | 19,52 | 29,27 | 39,55 | 6,97 | p<0,001 |
| CT | 42,65 | 39,18 | 21,60 | 29,48 | 39,18 | 51,20 | 66,08 | 15,44 | p<0,0001 |
| tAC | 20,69 | 19,43 | 10,98 | 14,75 | 19,43 | 24,62 | 29,14 | 9 | p<0,0001 |
| tAC corta | 16,94 | 15,61 | 8,27 | 11,09 | 15,61 | 20,72 | 24,43 | 6,47 | p<0,0001 |
| tAC media | 0,56 | 0,54 | 0,35 | 0,44 | 0,54 | 0,69 | 0,77 | 0,04 | NS |
| tAC larga | 3,39 | 2,96 | 1,67 | 2,15 | 2,96 | 4,04 | 6,11 | 2,06 | p<0,0001 |
CL: carnitina libre; CT: carnitina total; NS: p no significativa; tAC: total de acilcarnitinas; tAc corta: total de acilcarnitinas de cadena corta; tAC media: total de acilcarnitinas de cadena media; tAC larga: total de acilcarnitinas de cadena larga.
La comparación efectuada entre el grupo de prematuros de peso adecuado y el de bajo peso muestra valores más altos de CL, CT y tAC en el segundo grupo durante las 2 primeras semanas de vida, con diferencias significativas a los 3-5 días (CL: 25,65±16μmol/l vs. 32,24±14,4μmol/l, CT: 51,81±22,9μmol/l vs. 63,43±24μmol/l, tAC: 26,65±9,6μmol/l vs. 32,26±12,29μmol/l).
Los escasos trabajos que han evaluado el perfil de carnitina y acilcarnitinas en prematuros han obtenido resultados discordantes. Los niveles menores de CL y acilcarnitinas de cadena corta, media y larga demostrados en prematuros3–5 no fueron refrendados por los resultados obtenidos en otras series6,7.
Mandour et al.7 estudiaron los niveles de CL y acilcarnitinas en prematuros a los 5 y 14 días de vida en relación con un grupo control de neonatos a término, siendo el 39% de los pretérmino de muy bajo peso al nacimiento. La edad gestacional media (32,2 semanas) y el peso medio (1.600±430g) en su población fue mayor que en la nuestra. Las concentraciones medias de CL y acilcarnitinas de cadena media y larga al tercer-quinto día fueron equiparables en ambos estudios, siendo los niveles de acilcarnitinas de cadena corta y tAC menores en nuestra serie. A los 15 días, persiste una concentración similar de CL (22,2μmol/l en nuestro estudio y 21,5μmol/l en Mandour et al.), con niveles menores de acilcarnitinas en nuestra población, probablemente en relación con su menor peso.
Nuestros resultados confirman el descenso a los 15 días de los valores de CL, CT y acilcarnitinas demostrado previamente6–8.
La novedad de nuestro trabajo reside en el establecimiento de los percentiles de referencia de CL y acilcarnitinas en una población de prematuros de muy bajo peso al nacimiento en nuestro medio, como herramienta para una valoración más precisa del cribado neonatal en esta población.