Introducción
Dado que la vacuna triple vírica (TV) se incuba en cultivos celulares de embrión de pollo, su administración podría constituir un riesgo potencial de reacción en pacientes con alergia al huevo. El calendario vacunal recomendado por el Comité Asesor de Vacunas de la Asociación Española de Pediatría (AEP) y aprobado por el Comité Interterritorial del Sistema Nacional de Salud establece la primovacunación frente a sarampión, rubéola y parotiditis (SaRuPa) a los 15 meses y una dosis de recuerdo a los 3 años.
Mientras que en Estados Unidos y Gran Bretaña la alergia al huevo no es una contraindicación de la vacunación TV 1,2, en España se ha venido utilizando en estos niños una vacuna TV alternativa (Triviraten® Laboratorios Berna Biotech®, incubada en células diploides humanas, libre de proteína aviar y neomicina), la cual dejó de producirse a partir de febrero de 2004 debido a que los componentes antisarampión y especialmente antiparotiditis (cepa Rubini) son mucho menos inmunógenos, causando fracasos vacunales al generar títulos de anticuerpos de 2 a 20 veces menores que los de las vacunas TV convencionales 3. Es entonces cuando surge entre los pediatras españoles la cuestión de cómo abordar la vacunación TV en niños alérgicos al huevo.
En mayo de 2004, la Sociedad Española de Inmunología Clínica y Alergia Pediátrica (SEICAP) aconsejó que los niños con anafilaxia al huevo debían recibir, previa realización de pruebas cutáneas, una pauta de vacunación secuencial con dosis crecientes, o bien ser vacunados con Moruviraten®, sin componente frente a parotiditis y que debe ser solicitada como medicamento extranjero 4.
Por otro lado, en septiembre de 2004 el comité asesor de vacunas de la AEP efectuó entre otras las siguientes recomendaciones 5: a) el alergólogo debe establecer el diagnóstico y la gravedad de la alergia al huevo; b) se vacunará con TV estándar en los Centros de Salud, y sólo en el caso de manifestaciones alérgicas graves (anafilaxia) o asma persistente concomitante se administrará en medio hospitalario, permaneciendo en ambos casos al menos 30 min bajo observación, y c) los niños que hayan tenido una reacción anafiláctica con una dosis de TV no deben ser vacunados con la segunda dosis.
No obstante, hasta la fecha no existe en nuestro país ningún estudio publicado que confirme la seguridad de la vacunación TV en alérgicos al huevo. El objetivo del presente trabajo ha sido confirmar la tolerancia de la vacuna TV estándar (incubada en cultivos celulares de embrión de pollo) en pacientes con historia de alergia o sensibilización al huevo.
Material y métodos
Entre noviembre de 2004 y junio de 2005 se realizó vacunación TV incubada en embrión de pollo (Priorix®, GlaxoSmithKline) en 40 niños diagnosticados de alergia al huevo en base a historia sugestiva y positividad de prick cutáneos con extractos de yema, clara, ovoalbúmina y ovomucoide (laboratorios Leti, Barcelona) y/o inmunoglobulinas E (IgE) específicas (Sistema UniCAP®, Pharmacia Diagnostics) para dichos alérgenos.
La administración se llevó a cabo por el Servicio de Medicina Preventiva de nuestro Hospital, tras lo cual los pacientes permanecían bajo observación en nuestra Unidad durante al menos una hora. Además se realizó un estudio descriptivo en relación con la alergia al huevo y factores asociados, analizando los resultados con el programa estadístico SPSS versión 12.0 para Windows.
Resultados
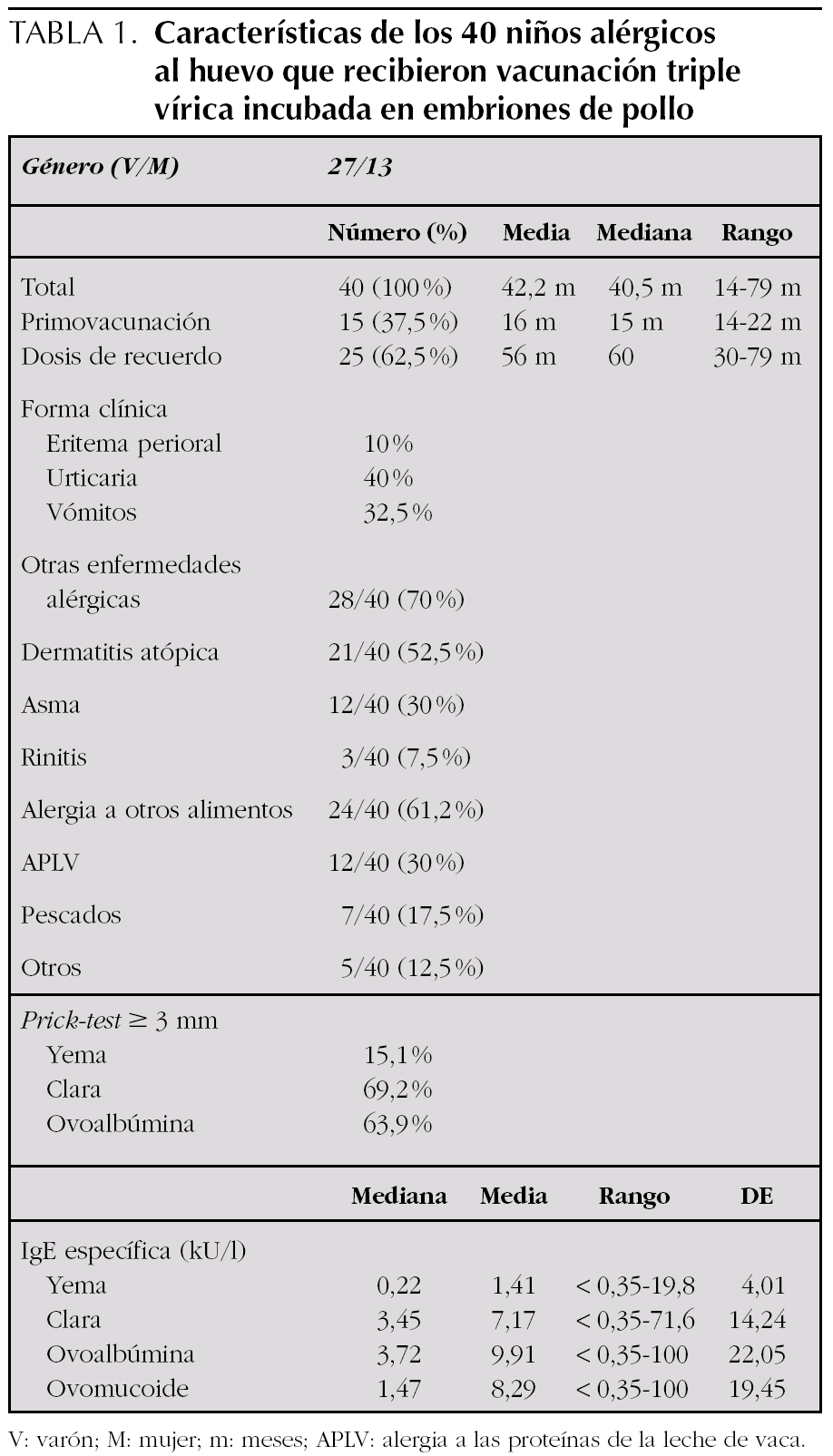
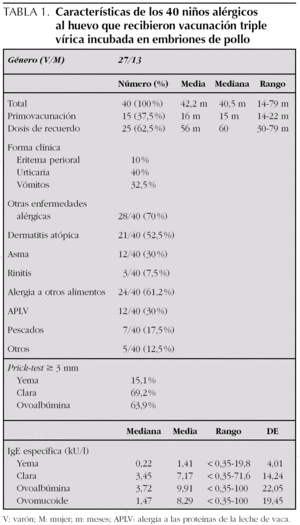
Se aplicó vacunación TV en dosis única a 40 pacientes, 27 niños (67,5 %) y 13 niñas (32,5 %) (tabla 1). El rango de edad osciló entre 14 y 79 meses (media, 42,2 meses). Recibieron la primovacunación 15 pacientes (37,5 %) (media, 16 meses; rango, 14-22 meses) y el resto, que previamente habían sido vacunados con Triviraten®, recibió la dosis de recuerdo (media, 56 meses; rango, 30-79 meses). No hubo ningún tipo de reacción adversa tras la inmunización con TV convencional.
Existía enfermedad alérgica asociada (excluyendo la alergia alimentaria) en 28 de los 40 pacientes: dermatitis atópica 32,5 %, dermatitis atópica y asma 20 %, asma 10 % y rinitis 7,5 %. Presentaban alergia a otros alimentos 24 niños (61,2 %): proteínas de leche de vaca (30 %), pescados (17,5 %), otros alimentos (12,5 %). Tienen antecedentes familiares de atopia en primer grado el 55 %.
La yema se introdujo en la dieta en 32 pacientes entre los 8 a 14 meses (mediana, 10 meses; media, 10,4 meses; desviación estándar [DE], 1,29), con reacción inmediata en 3 casos (dos con vómitos y en otro eritema perioral). En el resto se difirió la introducción de yema debido a que eran pacientes diagnosticados de alergia a proteínas de leche de vaca. La introducción de clara se efectuó entre los 9-15 meses (mediana, 12 meses; media, 12,4 meses; DE, 1,75). La clínica de presentación fue: eritema perioral 10 %, urticaria generalizada 22,5 %, vómitos 15 %, vómitos y urticaria 17,5 %. Nunca habían tomado clara en el momento de la vacunación 13 niños (32,5 %).
El diagnóstico de alergia al huevo se realizó mediante prick-test, CAP y/o prueba de provocación. Presentaron prick-test positivo (≥ 3 mm) 69,2 % para clara, 63,9 % para ovoalbúmina y 15,1 % para yema. Los valores de IgE específica fueron los siguientes: frente a clara: mediana, 3,45 kU/l; media, 7,17 kU/l; DE, 14,2 (rango, < 0,35-71,6 kU/l); frente a ovoalbúmina: mediana, 3,72 kU/l; media, 9,91 kU/l; DE, 22,05 (rango, < 0,35-100 kU/l); frente a ovomucoide: mediana, 1,47 kU/l; media, 8,29 kU/l; DE, 19,4 (rango, < 0,35-100 kU/l), y frente a yema: mediana, 0,22 kU/l; media, 1,41 kU/l; DE, 4,01 (rango, < 0,35-19,8 kU/l).
Discusión
Ya en la década de 1990 existían varios estudios que confirmaban la seguridad de la vacunación TV en niños alérgicos al huevo 1,6-9. En el año 2000 el Comité de Infecciones y Vacunaciones del Colegio de Pediatras Británico y la Sociedad Británica de Alergología e Inmunología Clínica establecieron que la vacunación TV es tan segura como cualquier otra y que no debía retrasarse en niños alérgicos al huevo, sin que sean precisas precauciones adicionales salvo en caso de asma concomitante o reacción anafiláctica previa por TV 2.
Patja et al 10 revisaron las reacciones adversas por vacunación TV en Finlandia, encontrando 73 reacciones potencialmente graves de un total de 2,99 millones de dosis de vacunas administradas entre los años 1982 a 1996, la mayoría en pacientes no alérgicos al huevo.
En 1983 Herman et al 11 comunicaron 2 casos de reacción generalizada (urticaria, angioedema y disnea) en niños alérgicos a clara de huevo vacunados con TV; así mismo, recomendaron efectuar pruebas cutáneas con la vacuna diluida antes de administrarla a niños con reacción grave al huevo. Baxter 12 practicó prick-test e intradermorreacción (IDR) en 150 niños alérgicos al huevo, de los que 145 tuvieron prick-test e IDR negativas y no presentaron reacciones adversas tras la vacunación. Los cinco restantes tuvieron prick positivos, cuatro con IDR negativas, que fueron vacunados sin incidencias, mientras que el último presentó reacción anafiláctica 10 min tras la IDR.
En otro estudio se realizó prick-test con vacuna TV a 410 niños, obteniéndose resultados positivos en cinco de ellos. Posteriormente se vacunó a los niños con TV estándar y cuatro de ellos (que habían tenido prick-test cutáneos negativos) tuvieron una reacción leve, no presentando ninguna reacción posvacunal los 5 niños con prick-test positivos, concluyendo que las pruebas cutáneas con vacuna TV no son predictoras de reacción adversa 13. La recomendación basada en la evidencia de la Asociación Americana de Pediatría (AAP) es no realizar pruebas cutáneas, pues no son útiles para pronosticar qué pacientes pueden tener una reacción grave tras la vacunación 14.
En una revisión de 17 estudios realizados entre 1963 y 1995 que incluía a 1.227 niños alérgicos al huevo que habían recibido TV, sólo dos mostraron reacción generalizada tras ésta (los dos comunicados por Herman en 1983) 1. Todo ello, junto con el hecho de que la vacuna SaRuPa convencional se incuba en cultivos de fibroblastos de embrión de pollo (cuyas proteínas se asemejan más a las del pollo que a las del huevo), nos ha llevado a realizar vacunación con TV en los niños diagnosticados de alergia al huevo, ya fuese primovacunación o dosis de recuerdo en niños que previamente habían recibido Triviraten®.
Varios autores 15-17 han responsabilizado a la gelatina, que actúa como agente estabilizador de algunas vacunas SaRuPa y triple bacteriana (DTP), de las reacciones adversas observadas en algunos pacientes. La concentración de ovoalbúmina es de 0,5-1 ng por dosis de 0,5 ml de TV, mientras que la cantidad de gelatina es 14,5 mg. La sensibilización a la gelatina podría producirse por las vacunaciones previas con DTP 15, no siendo la ausencia de alergia a la gelatina alimentaria predictora de ausencia de reacción vacunal, pues mientras que la gelatina alimentaria es de origen bovino, la presente en vacunas es de origen porcino, que podría tener reacción cruzada con leche de vaca, huevo y pollo 17.
Otro posible desencadenante de reacciones alérgicas es la neomicina utilizada como conservante de las vacunas, que en el caso de la vacuna TV se encuentra a una concentración de 25 mg por dosis de 0,5 ml. Se han descrito reacciones locales y sistémicas por neomicina, pero sólo en algunos casos se ha podido demostrar un mecanismo mediado por la IgE 18.
Las recomendaciones actuales son vacunar con TV convencional a todos los niños según el calendario vigente, independientemente de si son o no alérgicos al huevo 2,5,14. En este contexto, creemos que cuando vuelva a comercializarse una vacuna incubada en células diploides humanas, su papel quedaría reservado a niños que hayan presentado reacción sistémica con la primera dosis de TV, salvo que se confirme que la eficacia del nuevo producto es al menos similar a la de la TV estándar. El único beneficio de Triviraten® sería el estar libre de retrovirus aviares presentes en vacunas estándar 19, aunque este hecho no parece que tenga relevancia clínica 20.
En cuanto al perfil de los pacientes incluidos en este estudio, son niños en los que la introducción de yema es tolerada sin incidencias en la mayoría de los casos, apareciendo los síntomas con las primeras ingestas de clara en forma de reacción perioral y/o urticaria-angioedema, pero raramente ocurren signos de anafilaxia en estos primeros contactos. Una vez hecho el diagnóstico e indicada una dieta exenta de huevo, si los pacientes tienen contacto inadvertido con éste, las reacciones suelen de nuevo ser de carácter leve, siendo imposible predecir qué pacientes presentarán anafilaxia. Tras el período de estudio, hemos continuado vacunando con TV a pacientes alérgicos al huevo con resultados óptimos.
Un importante punto de discusión es la decisión de dónde vacunar a los niños con alergia al huevo demostrada. Sólo se deberían vacunar en centro hospitalario los niños con manifestaciones alérgicas graves con claro componente sistémico y en aquellos alérgicos al huevo con diagnóstico de asma persistente. En el resto de la población alérgica al huevo con manifestaciones clínicas leves (reacciones cutáneas o vómitos), no deben adoptarse medidas distintas a cualquier otra vacunación.
Por último, queda aún por determinar si los alérgicos al huevo tolerarían otras vacunas incubadas en huevos embrionados (fiebre amarilla y antigripal). En el caso de la vacuna antigripal, que contiene 20-45 mg de proteína de huevo por mililitro 21, la recomendación de la AAP es la de no aplicar la vacunación antigripal en alérgicos al huevo, pues aunque las reacciones adversas son raras, debe administrarse anualmente y existe quimioprofilaxis frente al virus influenza 22.
En resumen, en nuestra experiencia la administración de la vacuna TV es segura en niños alérgicos al huevo, que no presentan un riesgo de reacción alérgica mayor que el resto de la población, dato que avalan numerosos estudios. No se debe contraindicar la vacuna TV estándar en estos niños ni debe retrasarse la misma en espera de la recomercialización de la vacuna incubada en células diploides humanas. En estos niños no deben adoptarse medidas extraordinarias para la vacunación TV, salvo en casos de reacción alérgica grave tras la ingestión de huevo o si existe un diagnóstico de asma persistente, que deben ser vacunados en el hospital. No obstante, se sigue recomendando, al igual que con el resto de vacunaciones, que la administración se realice por personal cualificado y en las condiciones adecuadas para atender una eventual reacción adversa.
Agradecimientos
A Cristina Méndez e Inés Tofé por su ayuda en la lectura crítica del trabajo.
Correspondencia: Dr. Javier Torres Borrego.
Unidad de Alergia y Neumología Pediátricas. Servicio de Pediatría.
Hospital Universitario Reina Sofía.
Avda. Menéndez Pidal, s/n. 14004 Córdoba. España.
Correo electrónico: javier.torres.sspa@juntadeandalucia.es
Recibido en diciembre de 2005.
Aceptado para su publicación en enero de 2006.