El tratamiento del derrame pleural paraneumónico complicado (DPC) es controvertido. Las principales guías recomiendan el drenaje, pero con el menor nivel de evidencia. Recientes trabajos han observado buenos resultados solo con antibióticos. Hemos comparado retrospectivamente nuestros resultados en 2 cohortes consecutivas de pacientes tratados con distinto criterio: en el grupo 1 (2005-2009, actitud intervencionista) el drenaje se decidía en función de las características del líquido pleural, de acuerdo con las principales guías; en el grupo 2 (2010-2013, actitud conservadora) el drenaje se decidía en función de la evolución clínica del paciente.
MétodosSe revisaron las historias clínicas de los pacientes tratados por DPC entre 2005 y 2013. Las principales variables analizadas fueron la proporción de pacientes drenados y la duración de la estancia hospitalaria.
ResultadosSe analizó a 109 pacientes (64 grupo 1 y 45 grupo 2). Se colocó un tubo de drenaje en el 83% de los pacientes del grupo 1 y en el 47% de los del grupo 2 (p<0,001). La duración media de la estancia hospitalaria fue de 11,4 días en el grupo 1 y 12,3 días en el grupo 2 (p=0,45). No se observaron otras diferencias destacables.
ConclusiónNuestros resultados coinciden con los de otros estudios recientes que han observado una buena evolución en niños tratados solo con antibióticos y cuestionan la necesidad del drenaje en muchos de los niños que presentan un DPC. Son necesarios ensayos clínicos para identificar las circunstancias en las que se puede obtener un beneficio del drenaje en el DPC.
The treatment of complicated pleural infection (CPI) is controversial. Clinical guidelines recommend drainage, but with the lowest grade of evidence. Recent reports have observed good outcomes with antibiotics alone. We retrospectively compared the outcomes in two consecutive cohorts treated with different policies: the first treated according to pleural fluid charactersitics (2005-2009, interventional-prone, group 1) and the second according to clinical assessment (2010-2013, conservative-prone, group 2).
MethodsThe clinical records of all children treated for CPI in our hospital between 2005 and 2013 were thoroughly reviewed. Primary outcomes were the proportion of children drained and the length of hospital stay (LHS).
ResultsOne hundred and nine patients (64 group 1 and 45 group 2) were analyzed. A chest tube was placed in 83% of patients in group 1 and 47% in group 2 (P<0.001). The mean LHS was 11.4 days for patients in group 1 and 12.3 for patients in group 2 (P=0.45); no differences were observed in other outcomes.
ConclusionOur results add to few recent observations reporting good outcomes in many children treated with antibiotics alone and challenge the need to drain most children with CPI. Clinical trials are now needed to identify when a drainage procedure would be useful.
El derrame y el empiema pleurales son complicaciones ocasionales de la neumonía en niños cuya prevalencia —a tenor de lo publicado1-4— habría aumentado en los últimos años. Los derrames pequeños no requieren procedimientos invasivos para su diagnóstico y manejo, y responden bien al tratamiento exclusivo con antibióticos. El tratamiento de derrames grandes, organizados y purulentos (fase fibropurulenta) continúa siendo objeto de controversia, habiéndose descrito varios abordajes que van del tratamiento conservador con antibióticos a la inserción de un tubo torácico u otras intervenciones quirúrgicas, sobre todo la videotoracoscopia. La mayoría de las guías consideran que el derrame pleural paraneumónico complicado (DPC) no debe tratarse solamente con antibióticos y recomiendan el drenaje5-8; sin embargo, algunas instituciones han observado buenos resultados en muchos de los niños afectados sin necesidad de recurrir a la inserción de un tubo torácico o la cirugía, lo que sugiere que puede ser conveniente un abordaje más individualizado9,10.
Nuestro hospital es el centro de referencia para una población de casi 250.000 niños menores de 15 años cuando se requieren cuidados intensivos o cirugía pediátrica. Muchos niños diagnosticados de DPC son transferidos desde otros hospitales para su evaluación y diagnóstico. En 2010, a resultas de nuestra experiencia y de un estudio reciente9, pasamos de nuestra adherencia anterior a las guías acreditadas, que conllevaba el drenaje de casi todos los casos de DPC, a un manejo más conservador e individualizado. En este artículo informamos de nuestra experiencia en los últimos 9 años, comparando las características de los pacientes, los tratamientos y la evolución de los niños atendidos en nuestro hospital entre 2005 y 2009, cuando se solía insertar un tubo torácico sobre la base de las características del derrame, frente a los de los niños atendidos entre el año 2010 y el 2013, cuyo manejo se llevó a cabo de acuerdo con criterios clínicos integrales, especialmente la gravedad del estado general y la dificultad respiratoria observadas en la exploración física.
Pacientes y métodosSelección de los pacientesLa información de los pacientes menores de 15 años ingresados entre los años 2005 y 2013 inclusive y con diagnóstico al alta de derrame pleural o empiema se obtuvo de la base de datos electrónica de nuestro hospital. Se revisaron retrospectivamente las historias clínicas de estos pacientes para seleccionar a aquellos que desarrollaron derrames pleurales asociados a un diagnóstico de neumonía adquirida en la comunidad. Se excluyó a los pacientes con derrames pleurales asociados a tuberculosis u otras enfermedades. Los derrames paraneumónicos se consideraron DPC si el espacio pleural medido en la radiografía simple de tórax era mayor de 1cm y se observaban loculaciones o detritus en la ecografía pleural. El análisis solo incluyó a pacientes con DPC.
Manejo hospitalarioLos pacientes fueron ingresados desde el servicio de urgencias de nuestro hospital o transferidos desde otros hospitales. Comparamos 2 grupos de pacientes: aquellos ingresados entre 2005 y 2009 (grupo 1), cuya atención se llevó a cabo conforme a las guías de la British Thoracic Society para el tratamiento de la infección pleural en la infancia5, y los ingresados entre 2010 y 2013 (grupo 2), que fueron tratados de acuerdo con el juicio clínico de los pediatras responsables. Los hallazgos clínicos que llevaron a la decisión de drenar el empiema en pacientes del grupo 2 incluyeron el aumento del esfuerzo respiratorio y la sepsis grave o persistente9,10. La fiebre persistente no se consideró razón suficiente para drenar el derrame al haberse descrito que su duración es larga, se practique o no el drenaje9. En la mayoría de los casos, la inserción del tubo torácico fue llevada a cabo por un radiólogo intervencionista asistido por un anestesista. Los tubos, de tipo pigtail y calibre pequeño, se insertaron mediante la técnica de Seldinger, con guía ecográfica en pacientes sometidos a sedación profunda. En menos ocasiones, especialmente en niños ingresados en la unidad de cuidados intensivos (UCI), el tubo fue insertado por un cirujano pediátrico. Por lo general, no se practicaron toracocentesis ni tomografía computarizada. Las decisiones restantes (retirada del tubo, duración del tratamiento antibiótico, alta hospitalaria, etc.) se tomaron de acuerdo con el juicio clínico de los médicos responsables.
Recogida de datosLas historias clínicas de los pacientes seleccionados se revisaron meticulosamente, extrayéndose para cada paciente datos tales como el sexo, la edad, la duración de la estancia hospitalaria (DEH), las comorbilidades, los signos y síntomas, la duración de la fiebre, los resultados de analítica y cultivo de sangre y líquido pleural, los antibióticos administrados, la duración de tratamiento antibiótico, la oxigenoterapia, el ingreso en la UCI, la colocación de tubo de drenaje, las intervenciones quirúrgicas y las complicaciones. No fue posible analizar el estado de vacunación contra neumococo por ser un dato generalmente no registrado.
EvoluciónLas principales variables para la comparación de los grupos 1 y 2 fueron; a) la proporción de niños en los que se colocó un tubo torácico en nuestro hospital, y b) la DEH. Las variables secundarias analizadas fueron los tratamientos empleados, la duración del tratamiento antibiótico y la duración de la fiebre. La duración de la fiebre primaria se calculó como la suma del número de días con fiebre antes del ingreso y el tiempo transcurrido hasta la defervescencia, definido como los días transcurridos entre el ingreso y el primer día con una temperatura menor de 38°C sostenida durante 24 h. La fiebre recurrió en algunos pacientes tras la defervescencia. En estos casos, se calcularon tanto el número total de días con fiebre durante la estancia hospitalaria como el número total de días desde el ingreso hasta la desaparición definitiva de la fiebre.
Análisis estadísticoSe transfirieron los datos al programa SPSS (v17.0 SPSS, Chicago, EE. UU.). El análisis descriptivo incluyó frecuencias y porcentajes para las variables categóricas, y la media ± desviación estándar (DE) y el rango para variables cuantitativas con una distribución normal, o la mediana, el rango intercuartílico (RIC, P25-P75) y el rango para las variables cuantitativas con distribución no normal. Las variables categóricas se compararon mediante el test exacto de Fisher o el de la χ2 de tendencia lineal. Las variables continuas se compararon mediante la prueba de la t de Student (variables con distribuciones normales) o la prueba U de Mann-Whitney (no normales). Los valores de p fueron calculados a 2 colas y el nivel de significación utilizado fue de 0,05.
ÉticaEl estudio fue aprobado por el Comité Ético de Investigación Clínica de nuestro hospital.
ResultadosSelección de pacientesDoscientos niños fueron dados de alta de nuestro hospital con un diagnóstico de derrame pleural entre 2005 y 2013. Veinticuatro de ellos no presentaron etiología infecciosa y 5 recibieron un diagnóstico de tuberculosis. Los 171 niños restantes tuvieron derrames pleurales paraneumónicos y fueron seleccionados para un análisis detallado de sus historias clínicas. Sesenta y dos tuvieron derrames simples y pequeños, y no se consideró que requiriesen una intervención de drenaje. Los otros 109 presentaron derrames grandes y complicados en los que el drenaje estaba indicado según las guías principales. Se consideró que estos 109 pacientes tenían DPC y constituyeron la muestra de nuestro estudio. Sesenta y cuatro niños ingresaron entre 2005 y 2009 (12,8/año) y 45 entre 2010 y 2013 (11,3/año).
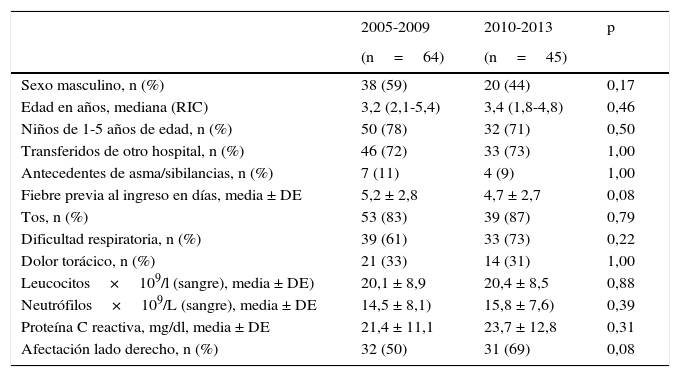
Características de los pacientesLas características principales de los pacientes ingresados se presentan en la tabla 1. El 10% de los pacientes tenía antecedentes de asma o sibilancias recurrentes, una prevalencia muy cercana a la de la población pediátrica general en nuestro país11. Un paciente tenía parálisis cerebral; 2, epilepsia, y otros 2, síndrome de Down. Dos mostraban lesiones de varicela. La mayoría de los pacientes, o bien estaban sanos con anterioridad, o bien habían tenido problemas de salud no relacionados con el desarrollo de la neumonía o del derrame pleural.
Características al ingreso de los niños con derrame pleural complicado
| 2005-2009 | 2010-2013 | p | |
|---|---|---|---|
| (n=64) | (n=45) | ||
| Sexo masculino, n (%) | 38 (59) | 20 (44) | 0,17 |
| Edad en años, mediana (RIC) | 3,2 (2,1-5,4) | 3,4 (1,8-4,8) | 0,46 |
| Niños de 1-5 años de edad, n (%) | 50 (78) | 32 (71) | 0,50 |
| Transferidos de otro hospital, n (%) | 46 (72) | 33 (73) | 1,00 |
| Antecedentes de asma/sibilancias, n (%) | 7 (11) | 4 (9) | 1,00 |
| Fiebre previa al ingreso en días, media ± DE | 5,2 ± 2,8 | 4,7 ± 2,7 | 0,08 |
| Tos, n (%) | 53 (83) | 39 (87) | 0,79 |
| Dificultad respiratoria, n (%) | 39 (61) | 33 (73) | 0,22 |
| Dolor torácico, n (%) | 21 (33) | 14 (31) | 1,00 |
| Leucocitos×109/l (sangre), media ± DE) | 20,1 ± 8,9 | 20,4 ± 8,5 | 0,88 |
| Neutrófilos×109/L (sangre), media ± DE | 14,5 ± 8,1) | 15,8 ± 7,6) | 0,39 |
| Proteína C reactiva, mg/dl, media ± DE | 21,4 ± 11,1 | 23,7 ± 12,8 | 0,31 |
| Afectación lado derecho, n (%) | 32 (50) | 31 (69) | 0,08 |
Todos los pacientes tuvieron fiebre en algún momento de la enfermedad. Antes del ingreso, 2 pacientes tuvieron fiebre de bajo grado (< 38°C) que duró solo un día. En los otros 107, la fiebre (≥ 38°C) duró entre 1 y 10 días. La frecuencia de la tos, la dificultad respiratoria y el dolor torácico se muestran en la tabla 1. Otros signos y síntomas frecuentes fueron (n): vómitos (28), dolor abdominal (23), diarrea (13), cefalea (6) y convulsión febril (2).
En pacientes drenados, los valores medianos (RIC) del líquido pleural fueron: proteína 4g/l (4-5), glucosa 10mg/dl (2-31), leucocitos 3,4×109/L (0,6-22,8). Los cultivos bacterianos fueron positivos en 30 pacientes (28%): se recuperó S. pneumoniae en 17 pacientes (16%: 9 de la sangre, 8 del líquido pleural), S. epidermidis en 4 (3 sangre, 1 líquido pleural), S. pyogenes en 3 (1 sangre, 3 líquido pleural), S. aureus en 2 (1 sangre, 1 líquido pleural) y otras bacterias en 4 pacientes.
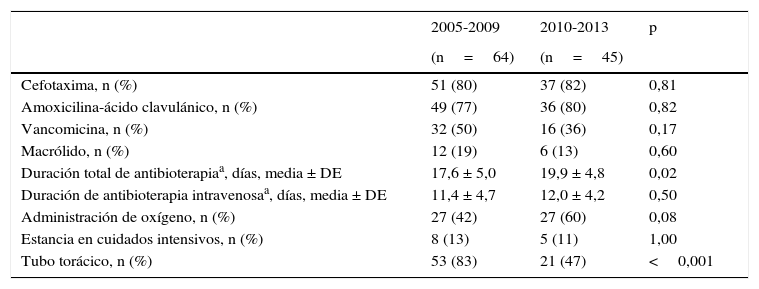
Tratamiento generalLa tabla 2 compara los tratamientos. Por lo general, se suministró más de un antibiótico a los pacientes, incluyendo antibióticos por vía oral antes y/o después de la estancia hospitalaria. Los antibióticos se administraron por un período de 7 a 34 días, con una media de 2 días más en el segundo grupo, y se administraron por vía intravenosa de 0 a 26 días. Cincuenta y cuatro pacientes requirieron oxígeno por una mediana de 4 días (RIC 3-7 días; rango 1-15 días). Trece pacientes fueron ingresados en la UCI pediátrica por una media ± DE de 8,3 ± 6,9 días (rango 1-23 días), pero solo 2 necesitaron ventilación mecánica.
Tratamiento de niños con derrame paraneumónico complicado
| 2005-2009 | 2010-2013 | p | |
|---|---|---|---|
| (n=64) | (n=45) | ||
| Cefotaxima, n (%) | 51 (80) | 37 (82) | 0,81 |
| Amoxicilina-ácido clavulánico, n (%) | 49 (77) | 36 (80) | 0,82 |
| Vancomicina, n (%) | 32 (50) | 16 (36) | 0,17 |
| Macrólido, n (%) | 12 (19) | 6 (13) | 0,60 |
| Duración total de antibioterapiaa, días, media ± DE | 17,6 ± 5,0 | 19,9 ± 4,8 | 0,02 |
| Duración de antibioterapia intravenosaa, días, media ± DE | 11,4 ± 4,7 | 12,0 ± 4,2 | 0,50 |
| Administración de oxígeno, n (%) | 27 (42) | 27 (60) | 0,08 |
| Estancia en cuidados intensivos, n (%) | 8 (13) | 5 (11) | 1,00 |
| Tubo torácico, n (%) | 53 (83) | 21 (47) | <0,001 |
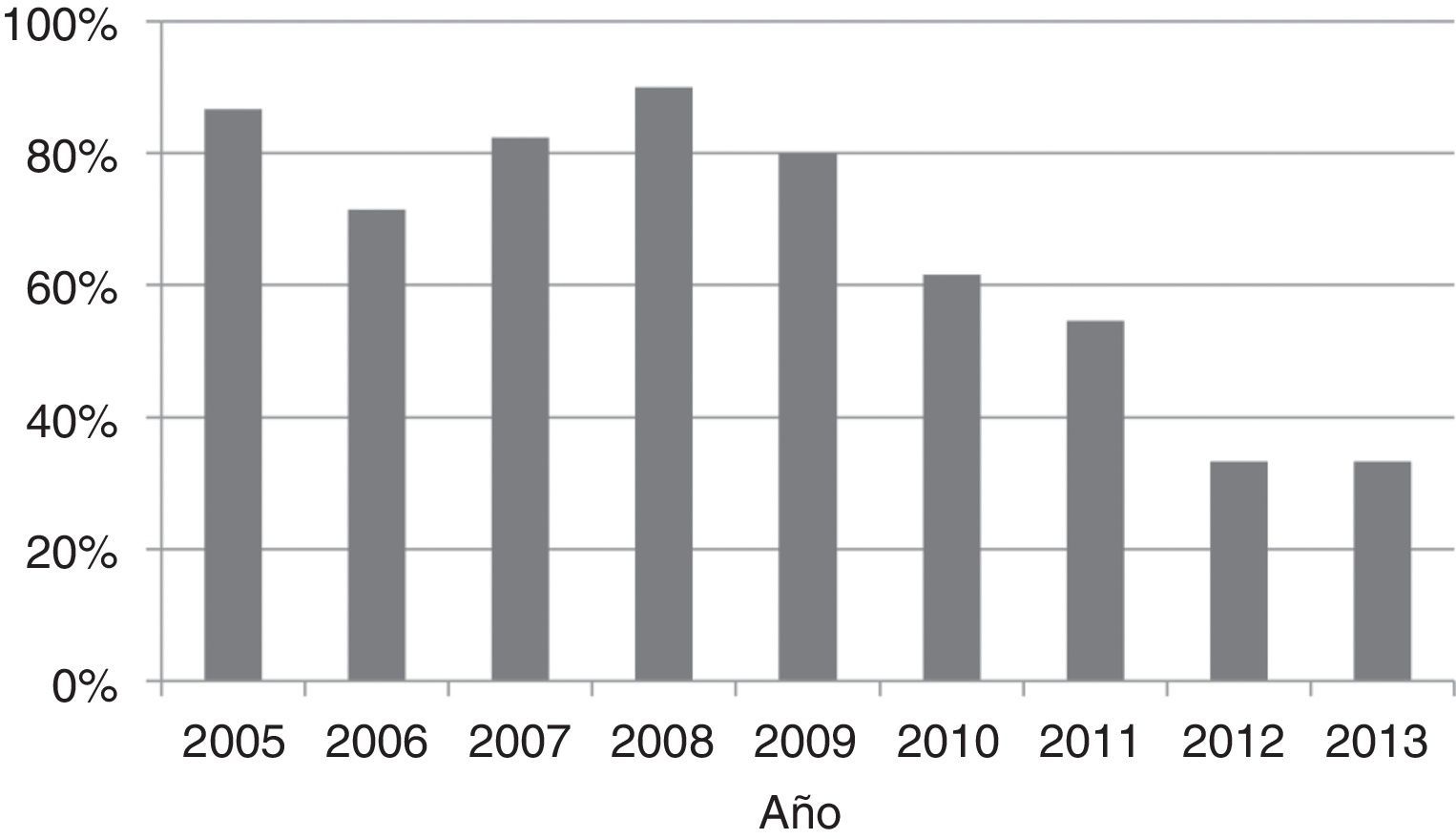
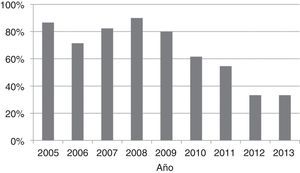
Se colocó un tubo torácico en 74 pacientes (68%) en nuestro hospital, el 83% de los pacientes del grupo 1 y el 47% de los del grupo 2, lo que constituyó la mayor diferencia en el tratamiento de ambos grupos (tabla 2). Se administró uroquinasa al 85% de los pacientes drenados (91% en el grupo 1 y 71% en el grupo 2, p=0,07). No encontramos ninguna tendencia significativa en el porcentaje de pacientes drenados entre 2005 y 2009 (p=0,91), pero sí observamos una reducción progresiva en la colocación de tubos torácicos entre 2009 y 2013 tras el cambio en el criterio de tratamiento del empiema (p=0,006) (fig. 1). Se realizó toracoscopia en un único paciente por fracaso terapéutico tras 9 días con un tubo torácico. Dos pacientes ingresados en nuestro centro en el año 2009 habían sido drenados en el hospital de origen antes de su traslado. La exclusión de estos 2 pacientes no dio lugar a diferencias en las comparaciones de los tratamientos y los resultados.
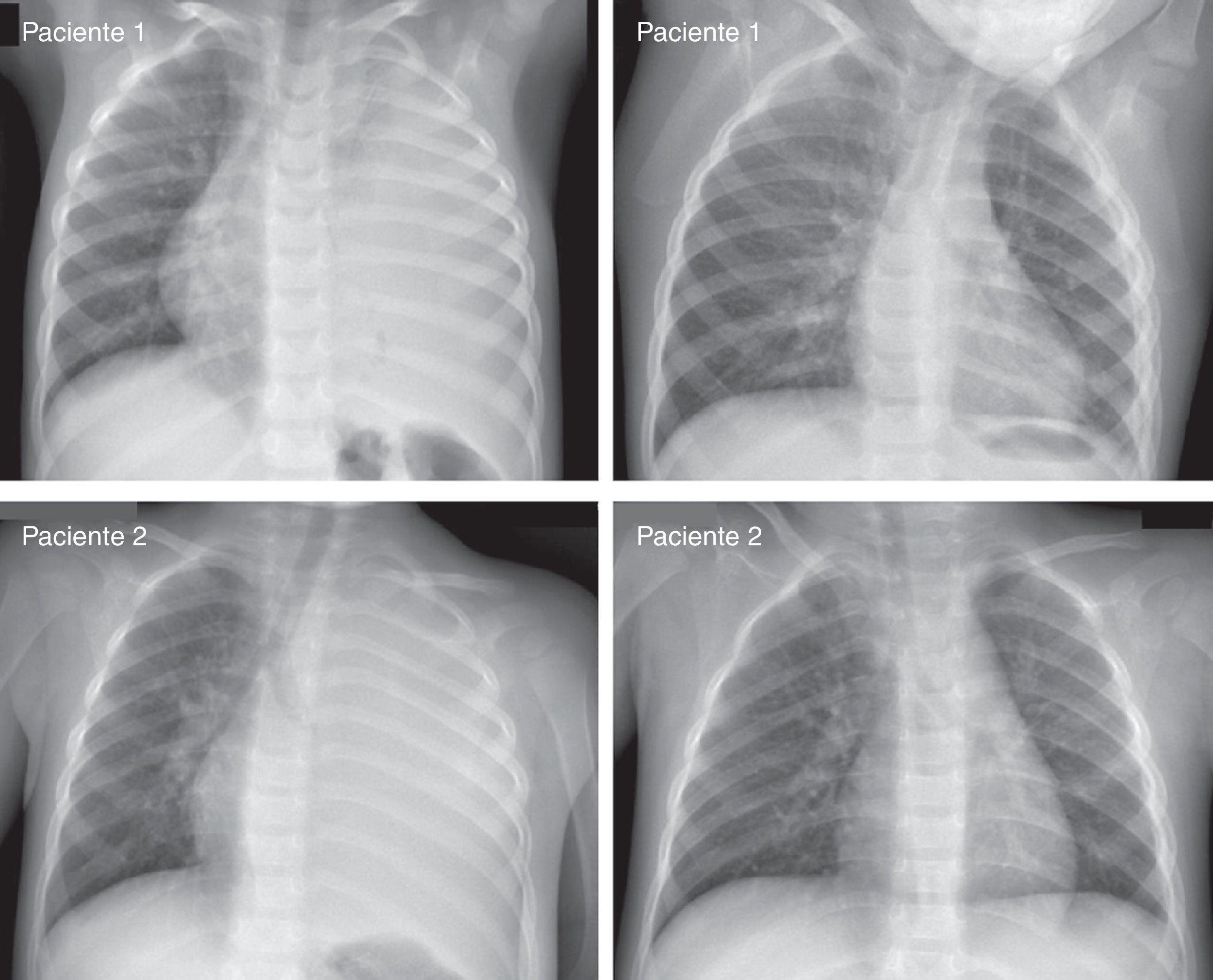
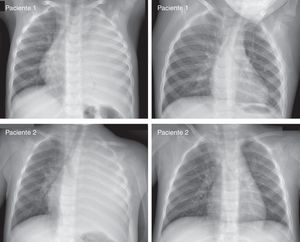
EvoluciónLos resultados principales se presentan en la tabla 3. En 2005 se insertó un tubo torácico en una niña de un año transferida a nuestro centro, pero al día siguiente fue trasladada debido a un derrame pericárdico a otro centro especializado, donde fue tratada con éxito. Se excluyó a esta paciente del análisis de la duración de la antibioterapia y de los resultados. La DEH (media ± DE, 11,8 ± 6,1 días; rango 3-32 días) no difirió significativamente en ambos grupos, ni siquiera al excluirse a los 2 pacientes drenados en otro hospital. La fiebre primaria duró 11,6 ± 5,0 días (rango 1-25 días) y el tiempo transcurrido desde el ingreso hasta la defervescencia osciló entre 0 y 21 días. La fiebre recurrió tras la defervescencia durante la estancia hospitalaria en 22 pacientes tras un período afebril de 1 a 8 días y el nuevo episodio febril duró de 1 a 12 días. No hubo diferencias entre los grupos en el número total de días con fiebre durante la estancia hospitalaria (media de 7,7 días) ni en el número total de días transcurridos desde el ingreso hasta la desaparición total de la fiebre (media de 8,4 días). Un único paciente presentó neumotórax antes de la inserción del tubo torácico. La DEH media fue más larga en niños con neumotórax (18,0 vs. 10,6 días; p<0,001), incluso cuando el análisis incluyó únicamente a los pacientes drenados (18,0 vs. 12,1 días; p<0,001). Aunque la evolución a largo plazo no se documentó sistemáticamente, todos los pacientes se recuperaron y no se observaron daños permanentes en el seguimiento. La figura 2 muestra las radiografías inicial y final de 2 pacientes representativos con DPC masivos que no se drenaron.
Resultados principales en niños hospitalizados por derrame paraneumónico complicado
| 2005-2009 | 2010-2013 | p | |
|---|---|---|---|
| (n=63a) | (n=45) | ||
| Duración de estancia hospitalaria, días, media ± DE | 11,4 ± 5,8 | 12,3 ± 6,7 | 0,45 |
| Tiempo transcurrido hasta la defervescencia desde el ingreso, días, media ± DE | 6,8 ± 4,9 | 6,9 ± 4,2 | 0,86 |
| Tiempo transcurrido hasta la defervescencia desde el ingreso mayor de 12 días, n (%) | 6 (10) | 3 (7) | 0,73 |
| Recurrencia de la fiebre tras la defervescencia, n (%) | 11 (17) | 11 (24) | 0,47 |
| Neumotórax, n (%) | 9 (14) | 8 (18) | 0,60 |
Las características principales de los pacientes drenados y de los no drenados fueron similares al ingreso, aunque los derrames del lado derecho fueron drenados más frecuentemente que los del izquierdo (80% vs. 59%; p=0,02). No hubo diferencias en los antibióticos empleados ni en la duración total de la antibioterapia, si bien los pacientes drenados recibieron antibióticos por vía intravenosa durante más tiempo (12,5 vs. 9,8 días; p=0,004) y requirieron con mayor frecuencia tanto oxígeno (59% vs. 29%; p=0,004) como el ingreso en la UCI (18% vs. 0%; p=0,009). La DEH fue más larga en pacientes drenados (13,5 vs. 8,1 días; p<0,001), incluso excluyendo a los pacientes con neumotórax del análisis (11,1 vs. 8,1 días; p<0,001).
DiscusiónEl diagnóstico y el tratamiento del derrame pleural para neumónico y el empiema sigue siendo un tema controvertido. La infección pleural constituye un espectro que tradicionalmente se ha dividido en fases. Siguiendo las recomendaciones de la BTS y de otros autores, se diagnosticó el DPC (incluyendo el empiema) cuando la fase fibropurulenta se evidenció por la presencia de un derrame grande (> 1cm) con signos ecográficos de organización5,8. Al no estar demostrada la utilidad del análisis bioquímico en el manejo clínico de los niños con derrame pleural paraneumónico, la aspiración de líquido pleural no se realizó por lo general con este único fin5,12. En los casos en los que se dispuso de líquido pleural, los resultados de los estudios bioquímicos y bacteriológicos mostraron claramente que nuestros pacientes estaban afectados de derrame complicado y empiema.
Al contrario de otros estudios cuyo objeto era establecer el mejor procedimiento de drenaje, el nuestro sugiere que el manejo conservador con el uso exclusivo de antibióticos es un tratamiento adecuado para muchos niños con DPC. Nuestro estudio se suma a otros recientes con observaciones similares9,10 y alimenta el debate sobre el mejor tratamiento para el DPC, un debate que se debe, fundamentalmente, a la falta de ensayos clínicos que den respuesta a la cuestión. Una revisión sistemática reciente solo encontró 4 ensayos aleatorizados y concluyó que el tratamiento fibrinolítico puede ser tan efectivo como la videotoracoscopia y más efectivo que el placebo para reducir la DEH en niños que requieren drenaje pleural13. Otra revisión sistemática de estudios que comparan la videotoracoscopia y el drenaje torácico con fibrinolíticos llegó a conclusiones similares14. De acuerdo con estos resultados, y con la mayoría de las guías, se administraron fibrinolíticos a casi todos nuestros pacientes drenados. Sin embargo, no se ha llevado a cabo ningún ensayo que compare el tratamiento conservador e invasivo del DPC. Por lo general, las guías actuales para el DPC no recomiendan el tratamiento exclusivo con antibióticos, si bien esta recomendación se basa en el menor nivel de evidencia5. El DPC es una condición temida por el riesgo de muerte o de secuelas, debido a experiencias del pasado o con pacientes adultos15-17. No obstante, la mortalidad en niños sanos es extraordinariamente baja y la evidencia muestra una excelente evolución funcional y radiológica a largo plazo18-24. En consecuencia, el manejo del DPC debería dirigirse a reducir la morbilidad a corto plazo, las molestias del paciente, la DEH y el coste del tratamiento.
Epaud et al. analizaron la evolución de 65 pacientes con derrame pleural de origen infeccioso. Durante los primeros 15 meses, se insertó un tubo de drenaje sobre la base de las características del derrame pleural (grupo clásico). Durante los siguientes 15 meses, los pacientes fueron sometidos a drenaje sobre la base de los criterios clínicos (grupo conservador). Se colocó un número significativamente menor de tubos torácicos en el grupo conservador (25% vs. 52%; p=0,03). La duración de la temperatura corporal superior a 39°C fue menor en el grupo conservador con respecto al clásico (10 vs. 14 días; p=0,01), sin diferencias significativas en la DEH (16 días vs. 20; p=0,16)9. Más recientemente, Carter et al. publicaron su experiencia de 12 años con el tratamiento conservador del empiema en niños. En pacientes clínicamente estables se inició el tratamiento exclusivo con antibióticos por vía intravenosa. Si el estado clínico del paciente no mejoraba en 48-72 h, se llevaba a cabo un procedimiento de drenaje. Noventa y cinco de los 182 pacientes (52%) fueron tratados exclusivamente con antibióticos, mientras que el 48% de ellos, principalmente aquellos con derrames pleurales grandes o que requirieron cuidados intensivos, fueron sometidos a procedimientos de drenaje. Los pacientes tratados exclusivamente con antibióticos tuvieron una DEH menor, un menor número de días de estancia hospitalaria con fiebre y una duración menor de tratamiento antibiótico por vía intravenosa que los pacientes sometidos a procedimientos de drenaje. Se presentaron 6 complicaciones de procedimientos de drenaje: un paciente tuvo una laceración hepática y 5 desarrollaron neumotórax. Sus resultados indican que algunos niños con derrames paraneumónicos moderados o grandes pueden ser tratados eficazmente mediante la antibioterapia exclusiva: hasta el 23% de los pacientes con desplazamiento mediastínico fueron tratados con éxito de esta manera10. Se han observado resultados similares en pacientes adultos25. Una revisión retrospectiva reciente de casi 15.000 niños ingresados con derrame pleural paraneumónico y empiema mostró una variación significativa en las intervenciones principales empleadas en 40 hospitales infantiles de EE. UU.26. La antibioterapia exclusiva fue la intervención principal en el 52% de los pacientes, oscilando entre el 30 y el 75% según el hospital. Curiosamente, la DEH y los costes fueron más bajos en pacientes tratados solamente con antibióticos que en pacientes sometidos a procedimientos invasivos, a pesar de que la gravedad de su enfermedad era similar sobre la base de la necesidad de ventilación mecánica y de ingreso en la UCI. Estos hallazgos subrayan la importancia de establecer qué pacientes requieren realmente ser drenados.
En conjunto, este y otros estudios indican claramente que la historia natural del DPC en niños tratados con antibióticos y medidas de soporte suele resultar en una recuperación completa. La fiebre es un mal indicador de mejoría, ya que suele persistir durante muchos días antes de remitir, con independencia de la colocación o no de un tubo torácico9,27. No es la remisión de la fiebre, sino una recuperación muy lenta (o simplemente la falta de empeoramiento en los primeros días), lo que apunta a una evolución favorable y precede a la remisión de la fiebre y a la recuperación10. Por otro lado, los tratamientos invasivos tienen riesgos asociados, son más dolorosos y caros, y requieren destreza técnica y recursos adecuados28,29. Observamos la presencia de neumotórax en varios pacientes tras la colocación del tubo torácico, lo que resultó en una DEH significativamente más larga. Desconocemos en qué grado el neumotórax estaba relacionado con la enfermedad o era una complicación iatrogénica de la inserción del tubo torácico, ya que se han descrito ambas posibilidades9,30.
Nuestro trabajo comparte las limitaciones de casi todos los estudios observacionales en este campo, habiéndose realizado en un solo centro con un tamaño muestral reducido. No obstante, los pacientes de ambos períodos de estudio fueron prácticamente iguales al ingreso y la única diferencia en su tratamiento fue el criterio empleado para el drenaje del derrame, que resultó en una menor proporción de colocación de tubos torácicos, una duración total de la antibioterapia (fundamentalmente oral) ligeramente mayor y evoluciones similares. Los pacientes drenados en el grupo 2 posiblemente estaban más graves o no mejoraron con antibióticos. No intentamos establecer en qué pacientes estaba o no indicado el drenaje o las razones complejas en que se basaba esta decisión. La determinación de la intervención a efectuar basándose en el juicio clínico se ha utilizado también en ensayos clínicos en otras enfermedades respiratorias31. Lo que hemos comprobado es que algunos pacientes con DPC pueden ser tratados sin procedimientos invasivos con buenos resultados. Debemos señalar que el cambio de enfoque en relación con el drenaje de pacientes con DPC, de criterios radiológicos a criterios clínicos, no llevó a un cambio rápido sino progresivo en el número de pacientes no drenados. Dado que la interpretación de los hallazgos clínicos es de naturaleza subjetiva, la confianza de los clínicos en el tratamiento conservador aumentó conforme los resultados con este nuevo criterio fueron satisfactorios.
En conclusión, muchos niños con DPC podrían ser tratados con antibióticos, evitando procedimientos invasivos arriesgados, caros y molestos. Son necesarios ensayos clínicos aleatorios para saber en qué circunstancias el drenaje del derrame beneficia realmente a un niño afecto de DPC.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Los resultados preliminares de este trabajo se presentaron en la XXXIV Reunión de la Sociedad Española de Neumología Pediátrica, San Sebastián, 2012.