Las infecciones cutáneas constituyen un motivo de consulta frecuente en dermatología pediátrica. Se revisan las manifestaciones clínicas, el diagnóstico y el tratamiento de los principales cuadros infecciosos bacterianos de la piel, así como de la sobreinfección de las heridas punzantes y por mordedura. Las bacterias más prevalentes en las infecciones cutáneas son Staphylococcus aureus (S. aureus) y Streptococcus pyogenes. El tratamiento es generalmente empírico y solo ante determinadas circunstancias o mala evolución clínica se recomienda el estudio microbiológico. Las infecciones cutáneas superficiales pueden tratarse con antisépticos y antibióticos tópicos (mupirocina o ácido fusídico). El tratamiento sistémico se reserva para formas extensas, graves o con otros factores de riesgo del huésped. En estos casos, el antibiótico de elección dependerá, entre otros factores, de los patógenos sospechados; los más utilizados son penicilina, amoxicilina, amoxicilina-ácido clavulánico y cefalosporinas de primera o segunda generación. Considerando la baja incidencia de S. aureus resistente a la meticilina de adquisición comunitaria en nuestro país, no se recomienda modificar el tratamiento empírico salvo en circunstancias de especial gravedad, recurrencia o antecedente epidemiológico, en cuyo caso el tratamiento recomendado es clindamicina o trimetoprima-sulfametoxazol.
Skin infections are a common cause for dermatological consultations in the paediatric setting. A review is presented of the clinical manifestations, diagnosis and treatment of the main bacterial skin infections, as well as the diagnosis and treatment of super-infected puncture and bite wounds. The most prevalent bacteria in skin infections are Staphylococcus aureus and Streptococcus pyogenes. Treatment is usually empirical, since microbiological studies are only recommended under certain circumstances or lack of improvement with common therapies. Superficial skin infections can be treated with local antiseptics or antibiotics (mupirocin or fusidic acid). Systemic treatment is usually reserved for patients with extensive or severe disease or with other risk factors. Systemic treatment depends on the suspected infecting bacteria, with penicillin, amoxicillin, amoxicillin-clavulanic acid and first or second generation cephalosporin being the most frequently used drugs. Due to the low incidence of community-acquired methicillin-resistant infection by S. aureus in Spain, the use of clindamycin or co-trimoxazole is only recommended after severe disease, relapses or a clear epidemiological background.
La piel es la primera barrera del organismo frente a los agentes externos y las infecciones cutáneas, el motivo más frecuente de consulta en dermatología pediátrica. Los principales factores de riesgo son el deterioro de la integridad de la piel, la falta de higiene, el hacinamiento, la humedad y las inmunodeficiencias.
Las bacterias más prevalentes son Staphylococcus aureus (S. aureus) y Streptococcus pyogenes (S. pyogenes). Ambas pueden producir infecciones cutáneas por inoculación directa, por diseminación hematógena y mediante la producción de toxinas1, como en el síndrome estafilocócico de la piel escaldada por S. aureus y en el síndrome del shock tóxico estafilocócico o estreptocócico.
Según la sistemática de los documentos de consenso, añadiremos la fuerza de la recomendación de las medidas propuestas, siguiendo la clasificación de la Infectious Diseases Society of America (tabla 1)2.
Fuerza de recomendación y calidad de la evidencia
| Fuerza de recomendación | |
| A | Buena evidencia para apoyar el uso de la recomendación |
| B | Moderada evidencia para apoyar el uso de la recomendación |
| C | Mala evidencia para apoyar el uso de la recomendación |
| D | Moderada evidencia para no apoyar el uso de la recomendación |
| E | Buena evidencia para no apoyar el uso de la recomendación |
| Calidad de la evidencia | |
| I | Evidencia de al menos un ensayo clínico controlado aleatorizado bien diseñado |
| II | Evidencia de la menos un ensayo clínico bien diseñado no aleatorizado, de estudios analíticos caso-control o estudio de cohortes (preferiblemente de más de un centro), de series históricas múltiples o de un resultado dramático de experimentos no controlados |
| III | Evidencia de opiniones de autoridades en la materia, basadas en experiencia clínica, estudios descriptivos o informes de comités de expertos |
Tomado de Khan et al.2.
En general, el tratamiento antibiótico de las infecciones cutáneas es empírico3. Solo en algunas circunstancias (quimioterapia, neutropenia, inmunodeficiencia grave, heridas por inmersión, mordeduras de animales, afectación del estado general, sospecha de complicaciones, afectación extensa, sospecha de ectima gangrenoso, fascitis necrosante, pacientes ingresados) o ante una mala evolución es recomendable realizar hemocultivos o cultivos de aspirados, biopsias o exudados. Para elegir el tratamiento deben considerarse la clínica, los microorganismos posiblemente implicados, la localización, extensión y profundidad de la infección, y los antecedentes personales.
Las infecciones cutáneas sin síntomas sistémicos que afectan a las capas superficiales de la piel se tratan habitualmente con antisépticos o antibióticos tópicos; los de mejor cobertura frente a los patógenos habituales son la pomada de mupirocina y la crema o pomada de ácido fusídico. En infecciones por S. aureus sensible a la meticilina con mala respuesta clínica a la mupirocina, la pomada de retapamulina constituye una alternativa válida a partir de los 9 meses de edad4.
La antibioticoterapia sistémica se reserva para determinadas formas clínicas (celulitis), formas extensas, de rápida progresión o diseminadas, casos graves o con afectación del estado general (fascitis necrosante), neonatos, celulitis-adenitis en menores de 3 meses e inmunodeprimidos. En algunas ocasiones, son fundamentales la incisión y el drenaje quirúrgico.
Si se sospecha S. aureus, el antibiótico de elección es la cloxacilina, si bien sus características farmacológicas (administración cada 6 h, baja biodisponibilidad y mal sabor) hacen que sean preferibles la amoxicilina-ácido clavulánico y las cefalosporinas de primera generación (cefadroxilo o cefalexina). En caso de contraindicación para los betalactámicos, los fármacos de elección son la clindamicina (aunque en España solo se comercializa en cápsulas de 150 y 300mg) y la trimetoprima-sulfametoxazol.
Ante la sospecha de S. pyogenes, el antibiótico de elección es la penicilina o la amoxicilina. En los alérgicos a los betalactámicos pueden usarse macrólidos de 16 átomos (josamicina o midecamicina), clindamicina o, en caso de reacción no anafiláctica, cefalosporinas de primera generación.
En las infecciones en que puedan estar implicadas ambas bacterias está indicado el tratamiento con amoxicilina-ácido clavulánico o una cefalosporina de primera generación.
En el momento de la redacción de este documento, ni el cefadroxilo ni la cefalexina, únicas cefalosporinas de primera generación con presentación oral, se comercializan en España en forma de suspensión y solo se dispone de cápsulas de 500mg. Debido a esta circunstancia, las cefalosporinas de segunda generación (cefuroxima, cefaclor), pese a ser algo menos activas frente a los cocos grampositivos que las de primera, pueden considerarse alternativas válidas.
Principales cuadros infecciososImpétigoEl impétigo puede aparecer a cualquier edad y se transmite por autoinoculación y por contacto directo o con objetos contaminados. Produce lesiones epidérmicas no cicatriciales, bien delimitadas, generalmente en zonas expuestas. Puede ser ampolloso o no ampolloso. En la forma no ampollosa, causada por S. pyogenes, S. aureus (solo o como coinfección) y, ocasionalmente, por estreptococos de los grupos C y G, las lesiones evolucionan de mácula a pápula, vesícula y pústula que termina en costra melicérica gruesa. En la forma ampollosa, causada por S. aureus productor de toxina exfoliativa, las lesiones evolucionan a vesículas y estas a ampollas de contenido amarillento, más o menos turbio e incluso purulento, y costra fina. La principal complicación es la propagación local (celulitis, linfadenitis) o, excepcionalmente, sistémica (neumonía, osteoartritis, sepsis).
En los casos leves no complicados pueden emplearse desinfectantes tópicos, mupirocina o ácido fusídico cada 8 h, o retapamulina cada 12 h, durante 5-7 días. Si las lesiones son extensas o hay síntomas sistémicos, se recomienda antibioticoterapia por vía oral con amoxicilina-ácido clavulánico, una cefalosporina de primera o segunda generación, o cloxacilina5.
Dermatitis perianal bacterianaLa dermatitis perianal bacteriana consiste en un eritema alrededor del ano causado por S. pyogenes o con menos frecuencia por S. aureus solo o asociado al anterior6. Presenta un pico de incidencia a los 3-5 años de edad7 y predomina en los varones (70%), aunque las frecuencias se igualan si se incluyen los casos de vulvovaginitis8, que junto con la balanopostitis constituyen la denominada enfermedad perineal.
Se manifiesta como un eritema no elevado, de unos 2-3cm, alrededor del ano, de bordes bien delimitados, que puede asociar prurito, defecación dolorosa, estreñimiento, incontinencia por rebosamiento, hematoquecia y fisuras9. En los niños puede haber balanopostitis y en las niñas vulvovaginitis con secreción y disuria10. No suele producir síntomas generales, a diferencia de lo que ocurre en la celulitis. En la fase aguda (< 6 semanas de evolución) la lesión es roja, brillante, húmeda y dolorosa, y puede presentar una seudomembrana blanquecina. Sin tratamiento, las lesiones se cronifican, con fisuras dolorosas, secreción mucosa o placas psoriasiformes con costra periférica amarillenta. Cuando la causa es estafilocócica, puede haber pústulas y el eritema se extiende hacia la piel adyacente6.
Los pacientes o sus convivientes pueden haber presentado una faringoamigdalitis aguda o una infección cutánea7 en los últimos 3 meses o simultáneamente con la dermatitis perianal, o ser portadores faríngeos o perianales de S. pyogenes7,8. Las recurrencias tras el tratamiento con penicilina o amoxicilina son frecuentes (hasta el 37%)11, sobre todo si hay casos familiares no diagnosticados.
Se cree que la transmisión es por contacto, ya sea por autoinoculación (infección o portador asintomático faríngeo o cutáneo) o por contagio intrafamiliar, en especial si se comparte el agua de la bañera10 o si algún familiar ha presentado faringoamigdalitis aguda o dermatitis perianal7.
El diagnóstico se establece por la clínica y la confirmación es bacteriológica. Deben recogerse muestras de la zona perianal en todos los pacientes (A-II) y muestras faríngeas si hay síntomas (B-III), para realizar el test de diagnóstico rápido antigénico de S. pyogenes (valor predictivo positivo del 100%)7 o un cultivo. Si el resultado del test es negativo, se recomienda realizar el cultivo por la posibilidad de falsos negativos o de S. aureus como causante del cuadro (A-II). Deben investigarse posibles casos en convivientes y realizar un test de diagnóstico rápido o un cultivo a los pacientes sintomáticos (B-III), ya que constituyen una causa frecuente de recurrencias dentro del núcleo familiar.
Aunque se han comunicado buenos resultados con antibioticoterapia tópica en monoterapia (B-II), se recomienda el uso de antibióticos sistémicos en todos los casos (A-II). Si no se dispone de test de diagnóstico rápido o este ha sido positivo, se recomienda tratamiento con penicilina o amoxicilina oral durante 10 días (B-II), que pueden prolongarse hasta 14-21 días según la evolución clínica (C-III)10. Si no hay respuesta tras un ciclo de amoxicilina, o si el test diagnóstico ha sido negativo, y en espera del resultado del cultivo, puede usarse amoxicilina-ácido clavulánico (C-III).
A la hora de elegir la antibioticoterapia inicial, también deben considerarse los antecedentes de infección estreptocócica o estafilocócica en el núcleo familiar (C-II).
En las recurrencias se recomienda cefuroxima11 durante 7-10 días (C-II). La asociación de tratamiento por vía oral y tópico parece disminuir las recurrencias (A-II)6.
Infecciones de los folículos pilosos: foliculitis, forúnculo y ántraxEl principal agente causante de las infecciones de los folículos pilosos es S. aureus, seguido de los bacilos gramnegativos. Son factores predisponentes la obesidad, la diabetes, la hiperhidrosis, la inmunosupresión y la dermatitis atópica.
Clínicamente son lesiones centradas por pelos en la cara, el cuello, las axilas o los glúteos, que van desde una pápula-vesícula con base eritematosa (foliculitis, que afecta al folículo piloso superficial), pasando por nódulos eritematosos pustulosos dolorosos (forúnculo, que se extiende a la dermis profunda), hasta placas eritematosas calientes y dolorosas (ántrax, que afecta al tejido celular subcutáneo circundante).
El diagnóstico es clínico y solo se recomienda el estudio microbiológico en lesiones de mala evolución o atípicas12.
El tratamiento es inicialmente tópico con mupirocina o ácido fusídico y en las formas recurrentes o extensas que no respondan al tratamiento tópico se asociará amoxicilina-ácido clavulánico, clindamicina, cefadroxilo, cefalexina o cefuroxima. Para los forúnculos y ántrax, se recomienda aplicar calor local y valorar la realización de incisión y drenaje quirúrgico.
Linfangitis aguda bacterianaSe define como la inflamación de los vasos linfáticos del tejido celular subcutáneo. Los microorganismos más frecuentemente implicados son S. pyogenes, S. aureus y Pasteurella multocida (P. multocida) (esta última tras mordedura animal). Suele haber afectación sistémica incluso antes de que sean evidentes el característico cordón lineal inflamatorio desde su origen hasta los linfáticos regionales y el edema distal.
El tratamiento empírico en las formas leves a moderadas es la amoxicilina-ácido clavulánico o una cefalosporina de primera o de segunda generación.
ErisipelaEs una infección superficial que afecta a la dermis superior, el tejido celular subcutáneo y a veces al sistema linfático, causada en la mayoría de los casos por S. pyogenes o estreptococos de los grupos B, C o G1,13-18.
Son factores desencadenantes las abrasiones, las úlceras, las infecciones fúngicas intertriginosas de los pies, la obstrucción venosa o linfática y el edema crónico. En los neonatos, la infección puede originarse en el cordón umbilical y extenderse a la pared abdominal.
Su comienzo es agudo, con una placa eritematosa de característicos bordes bien definidos y ligeramente elevados. Ocurre con mayor frecuencia en los miembros inferiores y en la cara, y puede asociarse con linfadenitis regional. Suele haber síntomas generales (fiebre, escalofríos, malestar), a veces precediendo a los signos cutáneos. También son posibles las complicaciones sistémicas (sepsis, síndrome del shock tóxico estreptocócico, endocarditis, etc.), aunque son raras en los pacientes por lo demás sanos. Cuando la infección se resuelve produce descamación e hiperpigmentación.
El diagnóstico es clínico (A-II); los hemocultivos y los cultivos de biopsias cutáneas o de aspirados tienen bajo rendimiento.
El tratamiento consiste en penicilina o amoxicilina por vía oral (A-III)1. Los pacientes con lesiones mayores de 5cm o afectación del estado general, los lactantes y los inmunodeprimidos pueden requerir hospitalización y tratamiento parenteral (A-II). El cuidado de las heridas y sus factores predisponentes son también aspectos importantes del tratamiento (A-II).
CelulitisSe trata de una infección aguda que afecta a la dermis y al tejido celular subcutáneo. Son factores predisponentes los traumatismos, las heridas y las infecciones preexistentes. Aparece como una placa eritematosa, caliente y dolorosa, con límites mal definidos, que en ocasiones presenta flictenas, petequias o necrosis local y puede acompañarse de linfadenitis y síntomas sistémicos17.
Está causada principalmente por S. aureus y S. pyogenes. Otros microorganismos menos frecuentes son Streptococcus agalactiae y bacilos gramnegativos en neonatos y enterobacterias en pacientes inmunodeprimidos.
Su localización puede proporcionar una orientación etiológica: en la región periauricular y la planta del pie con heridas punzantes es más frecuente Pseudomonas aeruginosa y en mordeduras es habitual P. multocida.
El diagnóstico es clínico, pero se recomienda estudio microbiológico en los casos comentados en el apartado de tratamiento general. La ecografía puede ser útil para diferenciar la celulitis de los abscesos aún no fluctuantes.
Debe recomendarse siempre el tratamiento antibiótico sistémico con buena cobertura frente a S. aureus y S. pyogenes. En casos leves y bajo estricta vigilancia, puede considerarse la vía oral con amoxicilina-ácido clavulánico, cloxacilina, cefadroxilo, cefalexina, cefuroxima o clindamicina.
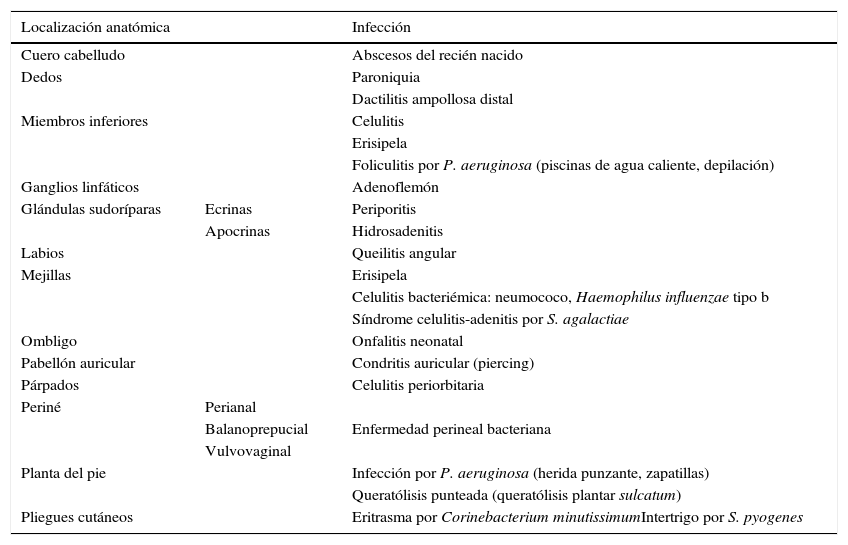
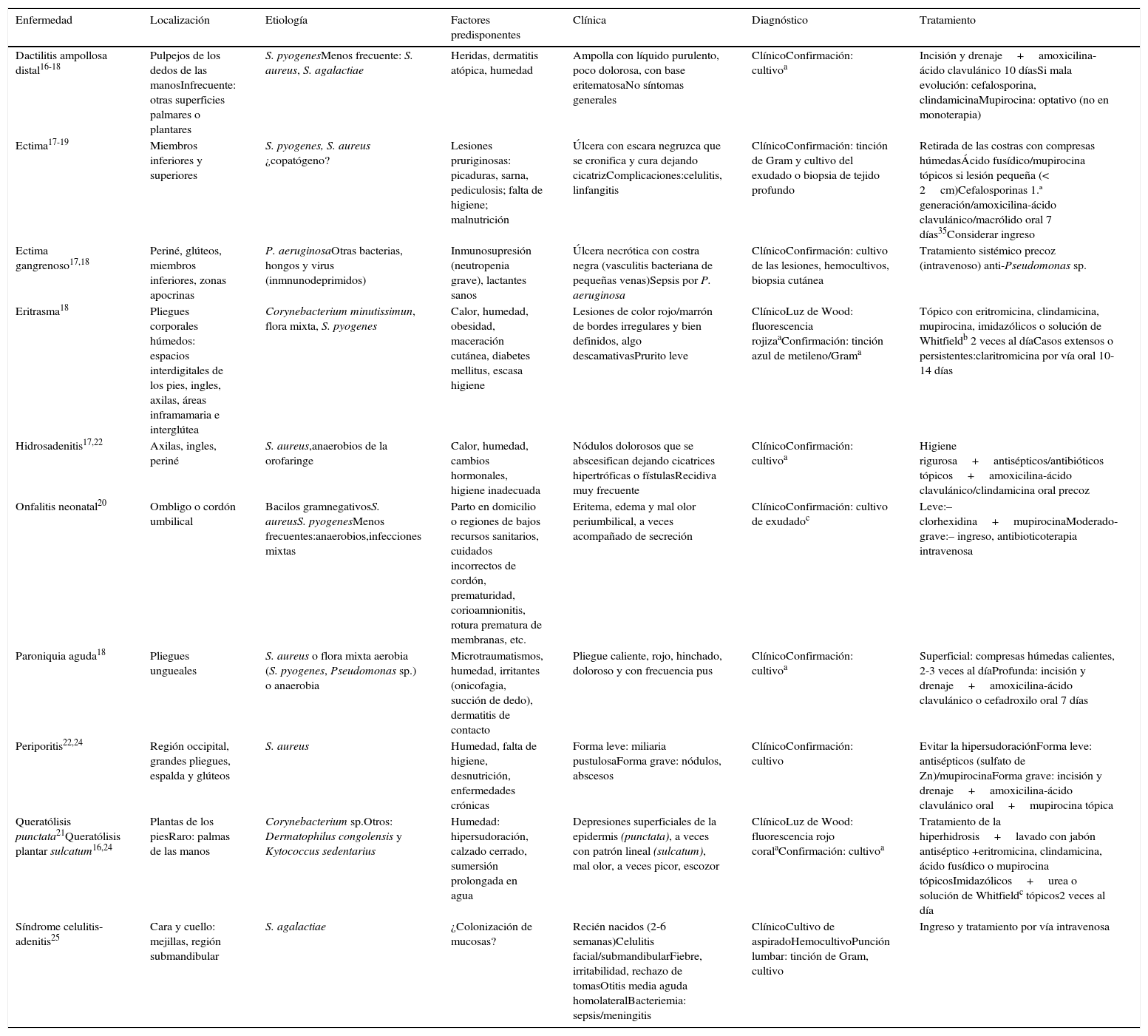
En las tablas 2 y 3 se resumen otros cuadros infecciosos con importancia clínica y en la tabla 4 se detalla la posología de los antiinfecciosos más empleados.
Formas clínicas de las infecciones cutáneas bacterianas más frecuentes según su localización preferente
| Localización anatómica | Infección | |
|---|---|---|
| Cuero cabelludo | Abscesos del recién nacido | |
| Dedos | Paroniquia | |
| Dactilitis ampollosa distal | ||
| Miembros inferiores | Celulitis | |
| Erisipela | ||
| Foliculitis por P. aeruginosa (piscinas de agua caliente, depilación) | ||
| Ganglios linfáticos | Adenoflemón | |
| Glándulas sudoríparas | Ecrinas | Periporitis |
| Apocrinas | Hidrosadenitis | |
| Labios | Queilitis angular | |
| Mejillas | Erisipela | |
| Celulitis bacteriémica: neumococo, Haemophilus influenzae tipo b | ||
| Síndrome celulitis-adenitis por S. agalactiae | ||
| Ombligo | Onfalitis neonatal | |
| Pabellón auricular | Condritis auricular (piercing) | |
| Párpados | Celulitis periorbitaria | |
| Periné | Perianal | |
| Balanoprepucial | Enfermedad perineal bacteriana | |
| Vulvovaginal | ||
| Planta del pie | Infección por P. aeruginosa (herida punzante, zapatillas) | |
| Queratólisis punteada (queratólisis plantar sulcatum) | ||
| Pliegues cutáneos | Eritrasma por Corinebacterium minutissimumIntertrigo por S. pyogenes |
Tomado de Moraga-Llop y Tobeña Rue18
Otras formas clínicas de las infecciones cutáneas bacterianas
| Enfermedad | Localización | Etiología | Factores predisponentes | Clínica | Diagnóstico | Tratamiento |
|---|---|---|---|---|---|---|
| Dactilitis ampollosa distal16-18 | Pulpejos de los dedos de las manosInfrecuente: otras superficies palmares o plantares | S. pyogenesMenos frecuente: S. aureus, S. agalactiae | Heridas, dermatitis atópica, humedad | Ampolla con líquido purulento, poco dolorosa, con base eritematosaNo síntomas generales | ClínicoConfirmación: cultivoa | Incisión y drenaje+amoxicilina-ácido clavulánico 10 díasSi mala evolución: cefalosporina, clindamicinaMupirocina: optativo (no en monoterapia) |
| Ectima17-19 | Miembros inferiores y superiores | S. pyogenes, S. aureus ¿copatógeno? | Lesiones pruriginosas: picaduras, sarna, pediculosis; falta de higiene; malnutrición | Úlcera con escara negruzca que se cronifica y cura dejando cicatrizComplicaciones:celulitis, linfangitis | ClínicoConfirmación: tinción de Gram y cultivo del exudado o biopsia de tejido profundo | Retirada de las costras con compresas húmedasÁcido fusídico/mupirocina tópicos si lesión pequeña (< 2cm)Cefalosporinas 1.ª generación/amoxicilina-ácido clavulánico/macrólido oral 7 días35Considerar ingreso |
| Ectima gangrenoso17,18 | Periné, glúteos, miembros inferiores, zonas apocrinas | P. aeruginosaOtras bacterias, hongos y virus (inmnunodeprimidos) | Inmunosupresión (neutropenia grave), lactantes sanos | Úlcera necrótica con costra negra (vasculitis bacteriana de pequeñas venas)Sepsis por P. aeruginosa | ClínicoConfirmación: cultivo de las lesiones, hemocultivos, biopsia cutánea | Tratamiento sistémico precoz (intravenoso) anti-Pseudomonas sp. |
| Eritrasma18 | Pliegues corporales húmedos: espacios interdigitales de los pies, ingles, axilas, áreas inframamaria e interglútea | Corynebacterium minutissimun, flora mixta, S. pyogenes | Calor, humedad, obesidad, maceración cutánea, diabetes mellitus, escasa higiene | Lesiones de color rojo/marrón de bordes irregulares y bien definidos, algo descamativasPrurito leve | ClínicoLuz de Wood: fluorescencia rojizaaConfirmación: tinción azul de metileno/Grama | Tópico con eritromicina, clindamicina, mupirocina, imidazólicos o solución de Whitfieldb 2 veces al díaCasos extensos o persistentes:claritromicina por vía oral 10-14 días |
| Hidrosadenitis17,22 | Axilas, ingles, periné | S. aureus,anaerobios de la orofaringe | Calor, humedad, cambios hormonales, higiene inadecuada | Nódulos dolorosos que se abscesifican dejando cicatrices hipertróficas o fístulasRecidiva muy frecuente | ClínicoConfirmación: cultivoa | Higiene rigurosa+antisépticos/antibióticos tópicos+amoxicilina-ácido clavulánico/clindamicina oral precoz |
| Onfalitis neonatal20 | Ombligo o cordón umbilical | Bacilos gramnegativosS. aureusS. pyogenesMenos frecuentes:anaerobios,infecciones mixtas | Parto en domicilio o regiones de bajos recursos sanitarios, cuidados incorrectos de cordón, prematuridad, corioamnionitis, rotura prematura de membranas, etc. | Eritema, edema y mal olor periumbilical, a veces acompañado de secreción | ClínicoConfirmación: cultivo de exudadoc | Leve:– clorhexidina+mupirocinaModerado-grave:– ingreso, antibioticoterapia intravenosa |
| Paroniquia aguda18 | Pliegues ungueales | S. aureus o flora mixta aerobia (S. pyogenes, Pseudomonas sp.) o anaerobia | Microtraumatismos, humedad, irritantes (onicofagia, succión de dedo), dermatitis de contacto | Pliegue caliente, rojo, hinchado, doloroso y con frecuencia pus | ClínicoConfirmación: cultivoa | Superficial: compresas húmedas calientes, 2-3 veces al díaProfunda: incisión y drenaje+amoxicilina-ácido clavulánico o cefadroxilo oral 7 días |
| Periporitis22,24 | Región occipital, grandes pliegues, espalda y glúteos | S. aureus | Humedad, falta de higiene, desnutrición, enfermedades crónicas | Forma leve: miliaria pustulosaForma grave: nódulos, abscesos | ClínicoConfirmación: cultivo | Evitar la hipersudoraciónForma leve: antisépticos (sulfato de Zn)/mupirocinaForma grave: incisión y drenaje+amoxicilina-ácido clavulánico oral+mupirocina tópica |
| Queratólisis punctata21Queratólisis plantar sulcatum16,24 | Plantas de los piesRaro: palmas de las manos | Corynebacterium sp.Otros: Dermatophilus congolensis y Kytococcus sedentarius | Humedad: hipersudoración, calzado cerrado, sumersión prolongada en agua | Depresiones superficiales de la epidermis (punctata), a veces con patrón lineal (sulcatum), mal olor, a veces picor, escozor | ClínicoLuz de Wood: fluorescencia rojo coralaConfirmación: cultivoa | Tratamiento de la hiperhidrosis+lavado con jabón antiséptico +eritromicina, clindamicina, ácido fusídico o mupirocina tópicosImidazólicos+urea o solución de Whitfieldc tópicos2 veces al día |
| Síndrome celulitis-adenitis25 | Cara y cuello: mejillas, región submandibular | S. agalactiae | ¿Colonización de mucosas? | Recién nacidos (2-6 semanas)Celulitis facial/submandibularFiebre, irritabilidad, rechazo de tomasOtitis media aguda homolateralBacteriemia: sepsis/meningitis | ClínicoCultivo de aspiradoHemocultivoPunción lumbar: tinción de Gram, cultivo | Ingreso y tratamiento por vía intravenosa |
Posología de los antibióticos orales más usados en las infecciones cutáneas bacterianasa
| Fármaco | Posología | Dosis máxima |
|---|---|---|
| Penicilina V | 25-50mg/kg/d cada 6h | 3g/d |
| Cloxacilina | 50mg/kg/d cada 6h | 4g/d |
| Amoxicilina (± ácido clavulánico) | 50-60mg/kg/d cada 8-12h | 3g/d |
| Cefadroxilo | 25-50mg/kg/d cada 12h | 1g/d |
| Cefalexina | 20-25mg/kg/d cada 6h | 2g |
| Cefuroxima | 3 meses-5 años: 15mg/kg/d cada 12h5-12 años: 125mg/12h> 12 años: 250mg/12h | 4g/d |
| Cefaclor | 20mg/kg/d cada 8h | 1g/d |
| Claritromicina | 15mg/kg/d cada 12h | 1g/d |
| Josamicina | 30-50mg/kg/d cada 12h | 1g/d |
| Midecamicina | 35-50mg/kg/d cada 8-12h | 1,8g/d |
| Clindamicina | 10-30mg/kg/d cada 6h | 1,8g/d |
| Trimetoprima-sulfametoxazol (TMP-SMX) | 6-12mg TMP/kg/d cada 12h30-60mg SMX/kg/d cada 12h | TMP: 320mg/dSMX: 1600mg/d |
La mayoría de las sobreinfecciones de heridas por mordedura producen manifestaciones clínicas en las primeras 12 h, generalmente eritema, dolor o algún tipo de secreción por la herida. En las mordeduras humanas, la fiebre superior a 38°C, el absceso y la linfangitis son criterios establecidos de sobreinfección, así como la presencia de al menos 4 de los siguientes criterios: eritema mayor de 3cm desde el borde, dolor a la palpación, inflamación, drenaje purulento o leucocitosis superior a 12.000 células/ml.
En las sobreinfecciones de las heridas punzantes en el pie la clínica suele empezar en los primeros 5-7 días si la infección es estafilocócica y después de 7 días si está producida por Pseudomonas. Es importante descartar la afectación ósea y de los tejidos profundos23,24.
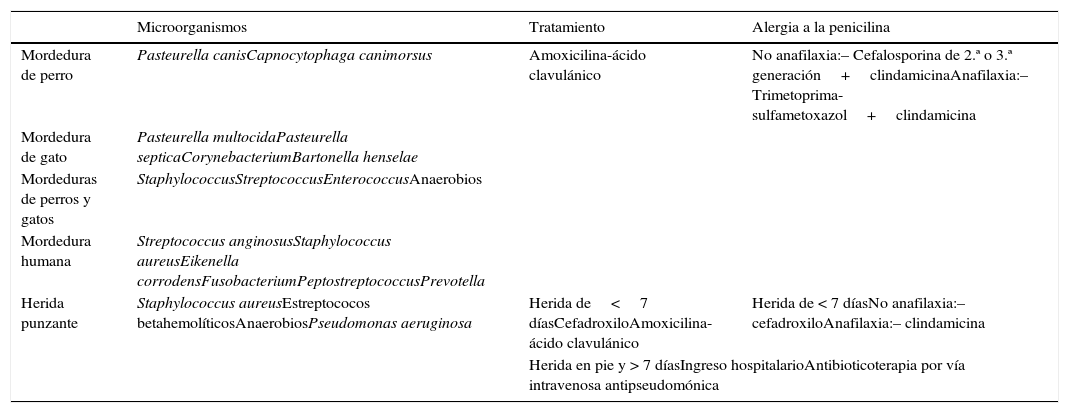
Además de las medidas locales de limpieza y desbridamiento, se recomienda tratamiento antibiótico profiláctico solo en los casos contemplados en la tabla 5 (A-I) y según las pautas expuestas en la tabla 6.
Indicaciones de profilaxis antibiótica en mordeduras y heridas punzantes25
| Mordeduras de gato y humanasMordeduras de perro con retraso en atención de > 8hMordeduras de perro en manos, pies y caraHeridas punzantes profundasHeridas con aplastamiento, edema o que requieran desbridamientoHeridas con afectación de tendones, músculos o articulacionesHeridas con fracturas subyacentesHeridas punzantes en la planta del pie con retraso en atención de > 24h, con gran contaminación o tejido desvitalizadoEnfermedad de base: inmunodepresión, riesgo de endocarditis, neumopatía crónica, hepatopatía crónica, diabetes mellitus |
Tomado de Bangert et al.25.
Infecciones secundarias a mordeduras y heridas punzantes23
| Microorganismos | Tratamiento | Alergia a la penicilina | |
|---|---|---|---|
| Mordedura de perro | Pasteurella canisCapnocytophaga canimorsus | Amoxicilina-ácido clavulánico | No anafilaxia:– Cefalosporina de 2.ª o 3.ª generación+clindamicinaAnafilaxia:– Trimetoprima-sulfametoxazol+clindamicina |
| Mordedura de gato | Pasteurella multocidaPasteurella septicaCorynebacteriumBartonella henselae | ||
| Mordeduras de perros y gatos | StaphylococcusStreptococcusEnterococcusAnaerobios | ||
| Mordedura humana | Streptococcus anginosusStaphylococcus aureusEikenella corrodensFusobacteriumPeptostreptococcusPrevotella | ||
| Herida punzante | Staphylococcus aureusEstreptococos betahemolíticosAnaerobiosPseudomonas aeruginosa | Herida de<7 díasCefadroxiloAmoxicilina-ácido clavulánico | Herida de < 7 díasNo anafilaxia:– cefadroxiloAnafilaxia:– clindamicina |
| Herida en pie y > 7 díasIngreso hospitalarioAntibioticoterapia por vía intravenosa antipseudomónica | |||
Tomado de Álvez González23
Siempre deben considerarse las medidas estándar de profilaxis frente a la rabia, el tétanos y el resto de las enfermedades transmisibles por heridas.
Staphylococcus aureus resistente a la meticilina adquirido en la comunidadEpidemiologíaEn los Estados Unidos, donde hasta el 80% de los estafilococos aislados de pacientes ambulatorios son resistentes a la meticilina, la infección por S. aureus resistente a la meticilina adquirido en la comunidad (SARM-AC) supone un problema de salud pública25. En España, algunos estudios sobre población pediátrica arrojan una frecuencia de resistencia a la meticilina en S. aureus de entre el 9 y el 14,8%26-29, pero no se dispone de estudios de ámbito nacional. La frecuencia en los neonatos se ha investigado en la Comunidad de Madrid30 entre 2007 y 2009, siendo del 3,3%.
El papel de la resistencia a la meticilina como indicador de gravedad está empezando a ser cuestionado y cada vez se otorga mayor relevancia a otros factores de virulencia, como la leucocidina de Panton-Valentine (LPV)32, aunque la mayoría de las cepas que la producen también son resistentes a meticilina31,33. El SARM de adquisición hospitalaria se asocia a determinados genotipos que condicionan resistencia a múltiples antibióticos, lo que no ocurre con SARM-AC, que solo en raras ocasiones presenta resistencia a los macrólidos y las lincosamidas27,31,33.
Clínica y diagnósticoAunque pueden causar neumonía, sepsis y osteoartritis, la mayoría de las infecciones por SARM-AC se limitan a la piel y los tejidos blandos.
No existen criterios clínicos que ayuden a diferenciar las infecciones cutáneas producidas por S. aureus sensible a meticilina de las causadas por SARM34, si bien en estas últimas son más frecuentes el fracaso terapéutico y la formación de abscesos y necrosis con costra superficial negruzca similar a una picadura de araña3. Dadas las implicaciones para el tratamiento, es importante el diagnóstico de abscesos difíciles de detectar en la exploración, por lo que se recomienda el uso de ecografía para el estudio de lesiones sugestivas aún no fluctuantes (C-III). Si es posible, se recomienda tomar muestras para cultivo, determinación de LPV y caracterización genética.
TratamientoLa baja incidencia actual de SARM-AC en nuestro medio no justifica el cambio de las pautas de antibioticoterapia empírica. Sin embargo, hay circunstancias en las que debe considerarse, como celulitis extensa, abscesificada o necrosante, presencia de abscesos recurrentes en el niño o sus convivientes, mala respuesta al tratamiento convencional, procedencia del paciente de zonas de alta endemia (Asia, América o Europa del Este) o convivencia con portadores conocidos (C-III).
En las infecciones menores no supuradas (impétigo, sobreinfección leve de heridas, etc.), suele ser suficiente el tratamiento tópico con mupirocina35 (A-III). En los abscesos cutáneos es fundamental la incisión y drenaje quirúrgico precoz, que se ha mostrado eficaz en pacientes por lo demás sanos con infecciones no complicadas para conseguir la curación total sin antibioticoterapia adyuvante35-38 (A-II). El tratamiento antibiótico sistémico se recomienda en el resto de las infecciones localizadas, como adyuvante si el drenaje ha sido incompleto, si hay afectación local intensa (abscesos mayores de 5cm) y en los pacientes menores de 2 años o con otros factores de riesgo (inmunodepresión, dermatitis atópica moderada-grave, etc.) (A-III).
El fármaco de primera elección es la clindamicina por vía oral, que además inhibe la producción de LPV35 (A-II). La trimetoprima-sulfametoxazol es una alternativa eficaz en regiones donde haya alta resistencia a la clindamicina (A-II), en caso de intolerancia a esta o cuando su presentación en cápsulas no se ajuste a las necesidades del paciente. Debe evitarse el linezolid en las infecciones leves-moderadas, por su alto precio y por la posibilidad de efectos adversos y desarrollo de resistencias. La presencia de LPV no exige cambios en la actitud terapéutica, aunque se asocia a mayor necesidad de incisión y drenaje quirúrgico3,31.
Si el tratamiento empírico se inicia con alguno de estos fármacos, se recomienda el desescalado a un betalactámico tan pronto como pueda demostrarse su sensibilidad.
Estudio y tratamiento de los portadoresSe estima que el 19,3% de la población española está colonizada por S. aureus, de los que solo el 1,3% son SARM39. La zona de colonización más frecuente son las fosas nasales, pero también se han descrito portadores axilares, inguinales e intestinales40. Considerando la baja incidencia de SARM en nuestro medio, no se recomienda el estudio sistemático de convivientes, reservándose para brotes en comunidades definidas (familias, instituciones, etc.) y para infecciones recurrentes3 (C-III). En estos casos, el tratamiento descolonizador del niño y sus convivientes portadores se realizará con mupirocina nasal cada 12 h y lavados corporales y del cuero cabelludo con jabón de clorhexidina al 4% durante 5-10 días (C-III). En caso de fracaso terapéutico con mupirocina, se empleará ácido fusídico tópico cada 12 h asociado a trimetoprima-sulfametoxazol por vía oral durante 7 días3,35 (C-III).
PrevenciónEl mecanismo principal de transmisión parece ser el contacto íntimo piel con piel40. Las medidas generales de prevención consisten en minimizar el riesgo de traumatismos cutáneos (uso de protecciones durante la práctica de actividades deportivas, etc.) (C-III), mantener las heridas limpias y tapadas (A-III), el lavado de manos e higiene corporal frecuentes (A-III), evitar compartir toallas y ropa (A-III) y la eliminación adecuada de objetos contaminados35,40 (C-III).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.