Valorar la efectividad del tratamiento con hormona de crecimiento (GH) en niños pequeños para la edad gestacional (PEG) sin crecimiento recuperador (talla al iniciar la terapia<−2,5 DE), en la Comunidad Valenciana, entre el 01/01/2003 y el 31/12/2013, y comparar los resultados con los ya publicados.
Material y métodosLos datos antropométricos de los PEG que constituyeron la muestra de estudio se recogieron retrospectivamente de los documentos de solicitud de tratamiento existentes en la Consejería de Sanidad de Valencia.
ResultadosUn total de 115 sujetos comenzaron a tratarse entre el 01/01/2003 y el 31/12/2013, con dosis de GH de 0,035±0,004mg/kg/día, a una edad de 8,10±2,75 años y con una talla de −3,14±0,59 DE. Talla alcanzada tras 2 años de terapia (n=115, edad: 10,50±2,72 años): −2,11±0,66 DE; y tras 4 años (n=96, edad: 12,65±2,46 años): −1,76±0,75 DE. Esta última mejoría de talla coincide con edades a las que suele producirse el estirón puberal. Solo 35 de los 115 niños finalizaron el crecimiento, en el periodo de estudio, a una edad de 16,22±1,19 años. Este subgrupo no consiguió normalizar la talla adulta (−2,22±0,86 DE), ni alcanzar su talla diana (−1,72±0,75 DE); no obstante, hubo una buena aproximación a la talla del progenitor más bajo (−1,95±1,28 DE). El 42,9% de estos 35 casos experimentaron un incremento de estatura superior a 1 DE.
ConclusionesLa muestra estudiada no obtiene una respuesta de crecimiento tan satisfactoria como las de otras series publicadas. Probablemente, estos resultados mejorarían iniciando el tratamiento más precozmente, e individualizando las dosis según las características del paciente.
To analyse the effectiveness of growth hormone (GH) therapy in short-stature children born small for gestational age (SGA) without catch-up growth (height at the beginning of treatment<−2.5 SDS), in Valencia (Spain), between 01/01/2003 and 12/31/2013; and to compare our findings with previously published data.
Materials and methodsAnthropometric data from the SGA children were obtained from the database of the «Ministry of Health of Valencia». These data were retrospectively reviewed.
ResultsA total of 115 SGA children, with a mean age of 8.10±2.75 years and height of −3.14±0.59 SDS started treatment (dose: 0.035±0.004mg/kg/day) between January 1st, 2003 and March 31st, 2013. After 2 years of therapy (n=115, age: 10.50±2.72 years) the height SDS was −2.11±0.66; and after 4 years (n = 96, age: 12.65±2.46 years) of −1.76±0.75 SDS. This latest improvement in stature matches ages at which the growth spurt usually occurs. Only 35 out of 115 children reached adult height, although impaired (−2.22±0.86 SDS), and failed to achieve their target height (−1.72 ±0.75 SDS). However, this sub-group grew to near the height of the shorter parent (−1.95 ±1.28 SDS), and 42,9% of these 35 cases increased their stature by more than 1 SDS.
ConclusionsThe studied sample did not achieve satisfactory growth results, as in other published series. Our findings might be improved by starting treatment earlier, and with doses individualised according to patient characteristics.
Pequeño para la edad gestacional (PEG) es aquel recién nacido cuyo peso o longitud se encuentran 2 o más desviaciones estándar (DE) por debajo de la media establecida para su población de referencia, según su sexo y edad gestacional1. Son producto de una alteración en el crecimiento intrauterino, cuya causa se desconoce en el 40% de los casos2.
Aproximadamente, el 90% de estos niños presenta un crecimiento recuperador espontáneo durante los primeros 2 años de vida, aunque en los que son, además, pretérmino puede retrasarse hasta los 3-4 años1. El 10% restante no realizará este catch-up por motivos que, en la mayoría de las ocasiones, se desconocen3,4. Se ha apuntado como posibles causas la disminución de la masa celular en el momento del nacimiento y alteraciones de las vías endocrino-metabólicas implicadas en el crecimiento posnatal, sobre todo del eje GH-IGF-1. Sin embargo, la mayoría de los PEG presentan unos valores de hormona del crecimiento (GH) normales o incluso elevados en los test de estímulo5, lo que indica que existe cierto grado de resistencia periférica a la acción de la GH, o bien una GH con actividad biológica disminuida.
El equipo de Job fue pionero en emplear la hormona de crecimiento recombinante humana (rhGH) para tratar el retraso de crecimiento posnatal que presentaban algunos niños PEG6,7, y sentó las bases de investigaciones posteriores, en las que se demuestra que la rhGH parece ser un tratamiento efectivo y seguro para reducir parcialmente el déficit de talla adulta de los sujetos PEG. Sin embargo, la respuesta al tratamiento es muy variable de unos trabajos a otros, hecho que se cree que pueda estar en relación con la heterogeneidad etiológica del PEG8–11.
El uso de esta hormona para tratamiento del PEG con talla baja fue aprobado por la Food and Drug Administration (FDA) en julio de 2001 y por la European Agency for the Evaluation of Medicinal Products (EMA) en junio de 20031. La Agencia Española del Medicamento (AEM) sigue los criterios de la EMA.
El rango de dosis de rhGH recomendado en el PEG es más alto que en el déficit de GH, y se sitúa entre 0,035 y 0,067mg/kg/día1. Esto es así porque, como ya se ha apuntado antes, en el PEG no suele haber una secreción disminuida de GH, sino cierto grado de resistencia periférica a su acción.
En la Comunidad Valenciana, desde que se aprobó esta indicación de rhGH, no existe ningún trabajo sobre la efectividad del tratamiento en sujetos PEG. En este artículo, exponemos los resultados de crecimiento en una muestra de niños tomada a lo largo de 10 años.
Objetivos- a)
Evaluar la efectividad de la hormona de crecimiento en niños PEG de nuestra zona, entre el 01/01/2003 y el 31/12/2013, según la proporción de estos que alcanzaron su talla diana al final del tratamiento, o bien el carril correspondiente, en caso de no haber acabado la terapia.
- b)
Comparar los resultados obtenidos con los publicados por otros grupos tanto nacionales como internacionales.
Se ha utilizado la información recogida en los documentos de solicitud de inicio, renovación y finalización de tratamiento con rhGH, remitidos al Comité Asesor de Hormona de Crecimiento de la Comunidad Valenciana por todas las Unidades de Endocrinología Pediátrica de los hospitales de las 3 provincias, entre el 01/01/2003 y el 31/12/2013.
Para tener acceso a esta información se obtuvo el permiso del CEIC de la Fundación de Investigación del Hospital Clínico Universitario de Valencia. Quedó clasificado como un estudio observacional posautorización otros diseños (OPA-OD) según las directrices de la Orden SAS/3470/2009, de 16 de diciembre del Ministerio de Sanidad. Los OPA-OD son estudios no prospectivos en los que, por la amplitud o antigüedad de la muestra, no se exige un consentimiento informado de los sujetos que la componen, siempre y cuando se respete el anonimato. Asimismo, dio su consentimiento la Consejería de Sanidad de la Comunidad Valenciana, puesto que es en su sede donde están guardados y custodiados dichos documentos y, por tanto, donde se realizó la recogida de datos.
La muestra de estudio se obtuvo aplicando los siguientes criterios:
- a)
Inclusión: únicamente se tomaron los casos de PEG que cumplían estrictamente todos los requisitos que a continuación se especifican:
- -
Peso o longitud al nacer inferior a −2 DE.
- -
Haber mantenido desde siempre una talla por debajo de −2,5 DE.
- -
No haber iniciado la pubertad.
- -
Haber recibido tratamiento con la hormona durante 2 años, como mínimo.
- -
- b)
Exclusión: de todos los que cumplieron los criterios de inclusión, se eliminó a los sujetos cuya talla diana se desconocía, y aquellos en los que el tratamiento se suspendió antes de lo previsto por aparición de reacciones adversas o por mala cumplimentación.
Se estudiaron retrospectivamente las siguientes variables:
- 1.
Dosis de GH pautada (mg/kg/día).
- 2.
Datos auxológicos familiares: DE de talla diana (TD) y DE de la talla del progenitor más bajo.
- 3.
Datos auxológicos de cada caso: edad decimal en años, DE de talla y de velocidad de crecimiento (VC). En concreto, estos datos se tomaron en 5 fases del tratamiento: 1.ª) antes de comenzar, 2.ª) tras un año de tratamiento, 3.a) tras 2 años de tratamiento, 4.ª) durante el último año que recibieron la terapia, 5.ª) talla adulta.
Todas las DE de los datos auxológicos mencionados fueron unificadas según las Tablas del Estudio Transversal Español de Crecimiento de 201012,13 (TD, talla del progenitor más bajo y tallas de cada caso en las 5 fases del estudio) y del Estudio Longitudinal Español de 1978/200014 (para la VC, teniendo en cuenta, además, el estadio madurativo del sujeto).
Se consideró que el sujeto había alcanzado la talla adulta cuando su velocidad de crecimiento era inferior a 2cm/año, o bien se había producido el cierre de las metáfisis de crecimiento.
Métodos estadísticosPara describir las características basales de la muestra se utilizó la media y la DE. Para evaluar la efectividad del tratamiento, se comparó la media de talla lograda en cada fase del estudio con la inmediatamente anterior, utilizando la prueba t de muestras relacionadas con corrección de Bonferroni. El test t de Student de muestras independientes se usó para confrontar la media de talla adulta con la de la TD (ambas variables presentaron una distribución normal), y la prueba U de Mann-Whitney, para comparar la media de talla adulta con la del progenitor más bajo (en este caso, se usó un test no paramétrico porque la distribución de las DE de la talla del progenitor más bajo no fue normal).
Se consideraron resultados estadísticamente significativos cuando el valor de p<0,05. Para realizar las operaciones estadísticas se utilizó en programa SPSS versión 20®.
ResultadosLos documentos de solicitud de tratamiento con GH remitidos al Comité Asesor de la Comunidad Valenciana en el periodo de estudio constituyeron un total de 1.361, pero únicamente 134 cumplieron los criterios de inclusión. Los 1.216 restantes correspondían a solicitudes denegadas por no cumplir los criterios requeridos para PEG o tratarse de documentos de adultos o pediátricos de indicaciones distintas a las estudiadas (déficit de GH, síndrome de Turner, síndrome de Prader-Willi, insuficiencia renal, alteraciones del gen SHOX).
Hubo 19/134 casos que presentaron alguna causa de exclusión. En 14/19, no se dispuso de la talla media parental. En 2/19, se especificó claramente una falta de cumplimiento por parte de la familia: fue el propio médico prescriptor quien comunicó al Comité la supresión del tratamiento. En 3/19, se retiró por la aparición de trastornos supuestamente relacionados con la hormona: un caso de epifisiólisis de cadera izquierda que requirió cirugía, otro de enfermedad de Perthes y un tercero que presentó hiperglucemia mantenida durante meses. Por tanto, la muestra de casos útiles quedó compuesta por 115 sujetos, de los cuales 60 eran niños y 55 niñas, todos ellos de origen caucásico.
La dosis media de GH empleada fue de 0,035±0,004mg/kg/día. Los 115 casos recibieron un mínimo de 2 años de tratamiento (como se exigía para poder entrar en el estudio), solo 96/115 alcanzaron la 4.a fase (3 o más años de tratamiento) y únicamente se dispuso de información relativa a la talla adulta en 35/115 sujetos.
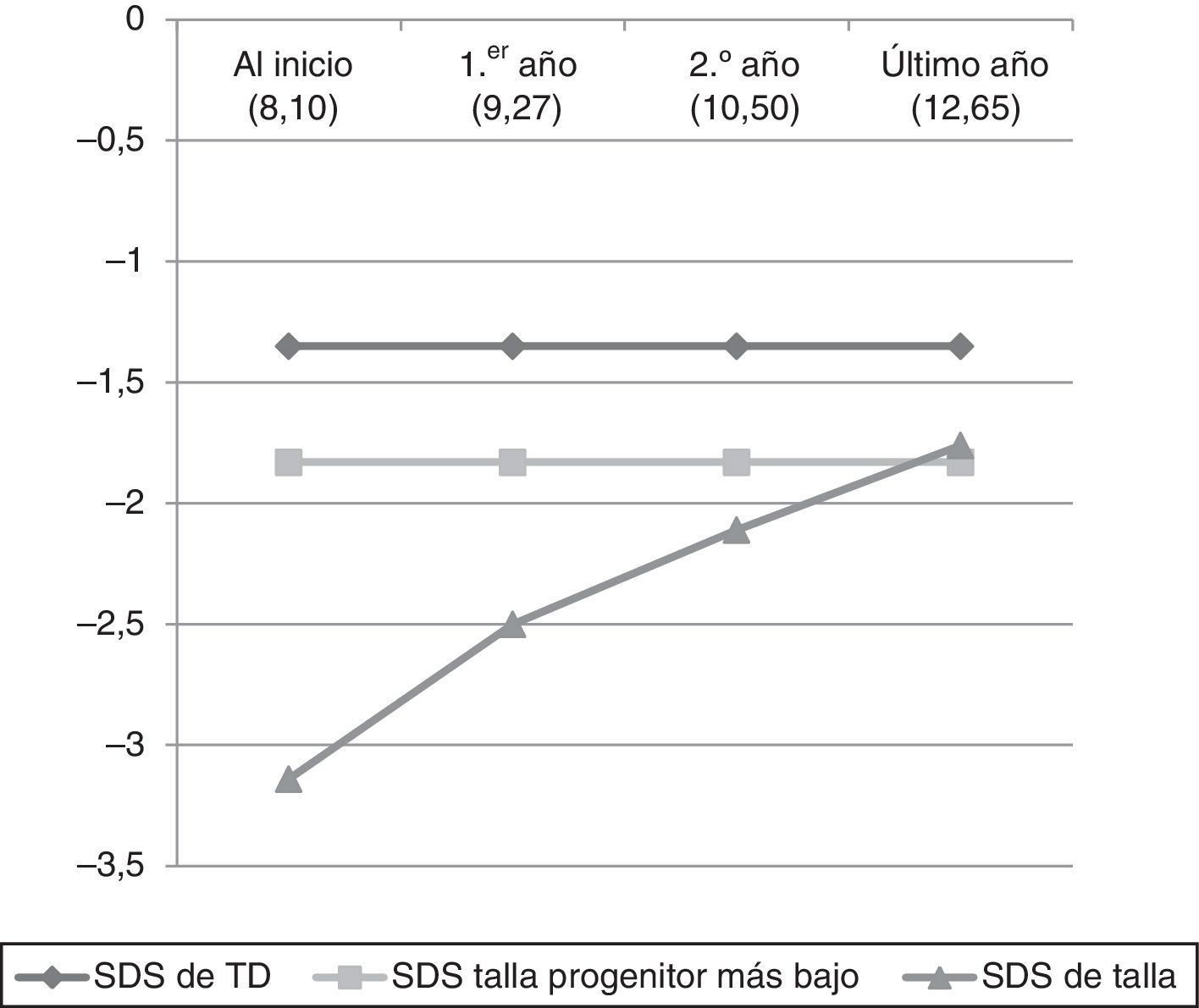
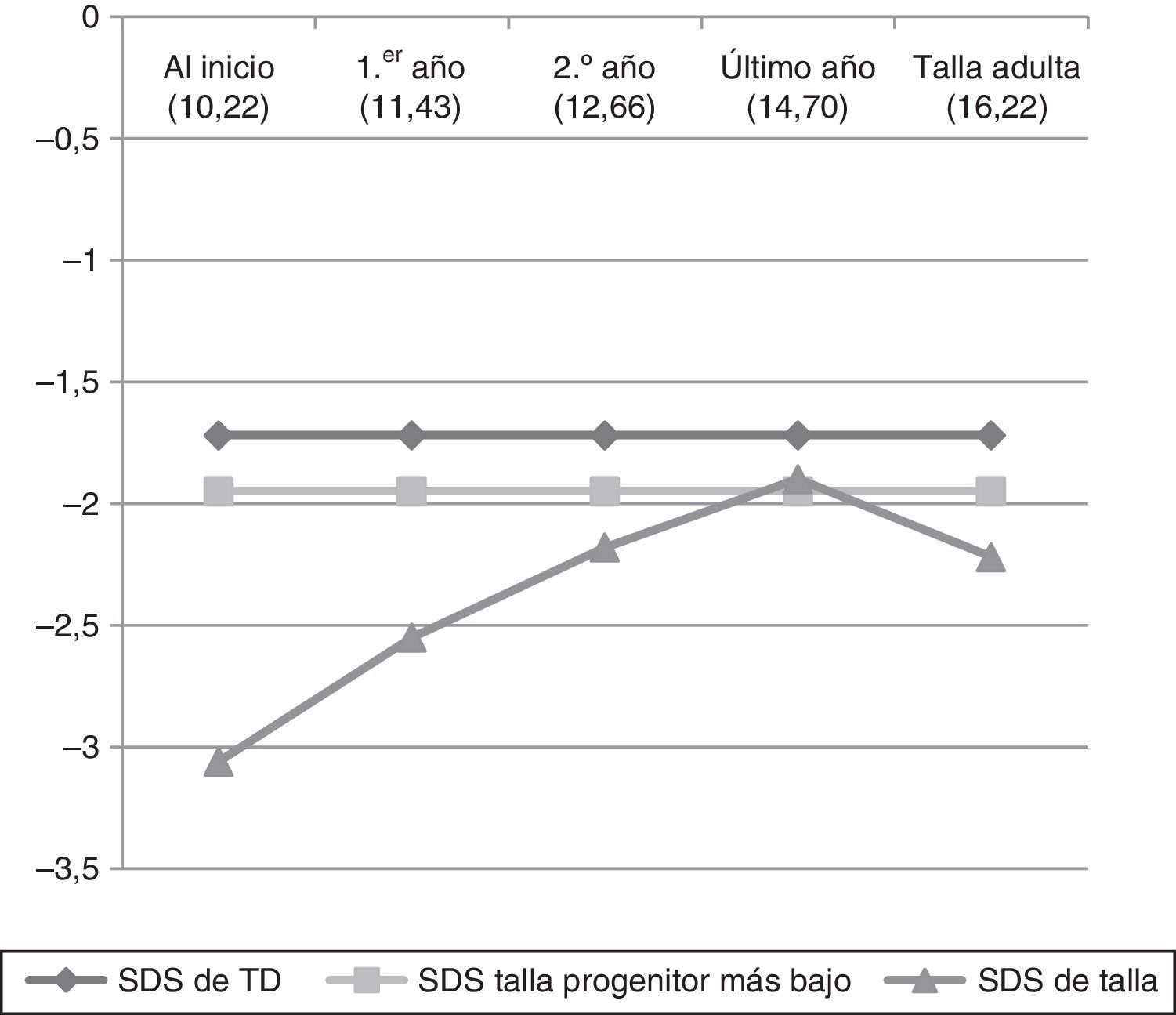
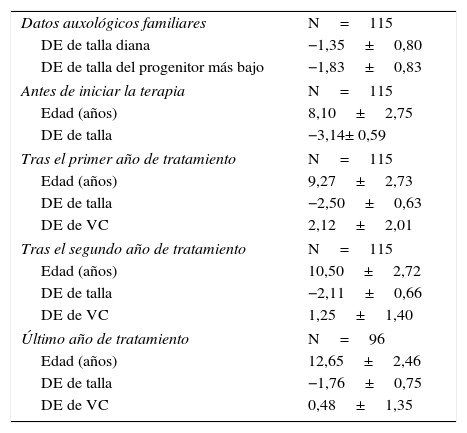
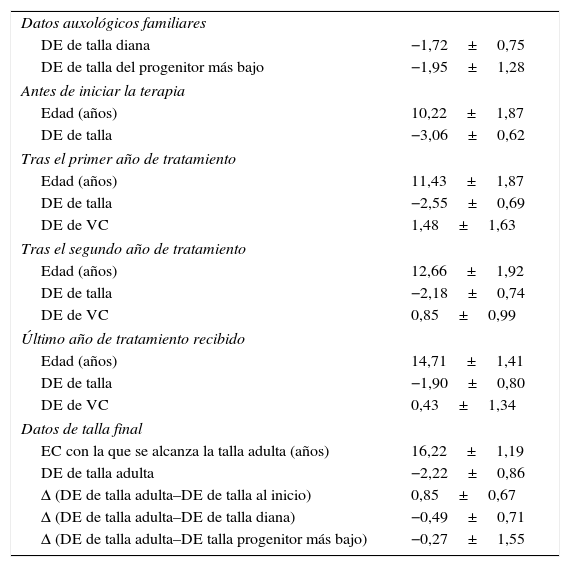
En la tabla 1 y figura 1 viene reflejada la evolución de la talla y VC de los casos que no han llegado aún a la talla adulta. Mientras que en la tabla 2 y figura 2 queda expuesta a evolución de los 35 niños que alcanzaron la estatura adulta, durante el periodo de estudio.
Datos auxológicos de la muestra a lo largo del estudio (media±desviación estándar)
| Datos auxológicos familiares | N=115 |
| DE de talla diana | −1,35±0,80 |
| DE de talla del progenitor más bajo | −1,83±0,83 |
| Antes de iniciar la terapia | N=115 |
| Edad (años) | 8,10±2,75 |
| DE de talla | −3,14± 0,59 |
| Tras el primer año de tratamiento | N=115 |
| Edad (años) | 9,27±2,73 |
| DE de talla | −2,50±0,63 |
| DE de VC | 2,12±2,01 |
| Tras el segundo año de tratamiento | N=115 |
| Edad (años) | 10,50±2,72 |
| DE de talla | −2,11±0,66 |
| DE de VC | 1,25±1,40 |
| Último año de tratamiento | N=96 |
| Edad (años) | 12,65±2,46 |
| DE de talla | −1,76±0,75 |
| DE de VC | 0,48±1,35 |
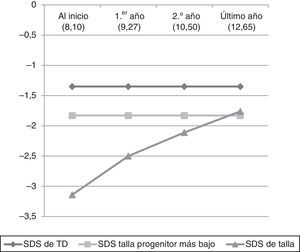
Representación gráfica de la evolución de las medias del DE de la talla en las primeras 4 fases del estudio. Los valores numéricos que aparecen entre paréntesis corresponden a la media de la edad cronológica en años en cada etapa del tratamiento. Muestra al inicio (115 sujetos), 1.er año (115 sujetos), 2.° año (115 sujetos), último año (96 sujetos).
Datos auxológicos de los 35 casos que alcanzaron la talla final (media±desviación estándar)
| Datos auxológicos familiares | |
| DE de talla diana | −1,72±0,75 |
| DE de talla del progenitor más bajo | −1,95±1,28 |
| Antes de iniciar la terapia | |
| Edad (años) | 10,22±1,87 |
| DE de talla | −3,06±0,62 |
| Tras el primer año de tratamiento | |
| Edad (años) | 11,43±1,87 |
| DE de talla | −2,55±0,69 |
| DE de VC | 1,48±1,63 |
| Tras el segundo año de tratamiento | |
| Edad (años) | 12,66±1,92 |
| DE de talla | −2,18±0,74 |
| DE de VC | 0,85±0,99 |
| Último año de tratamiento recibido | |
| Edad (años) | 14,71±1,41 |
| DE de talla | −1,90±0,80 |
| DE de VC | 0,43±1,34 |
| Datos de talla final | |
| EC con la que se alcanza la talla adulta (años) | 16,22±1,19 |
| DE de talla adulta | −2,22±0,86 |
| Δ (DE de talla adulta–DE de talla al inicio) | 0,85±0,67 |
| Δ (DE de talla adulta–DE de talla diana) | −0,49±0,71 |
| Δ (DE de talla adulta–DE talla progenitor más bajo) | −0,27±1,55 |
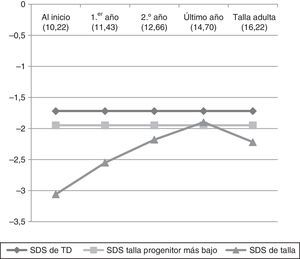
Desde el inicio de la terapia hasta la 4.ª fase del estudio se observó un incremento de talla estadísticamente significativo (p<0,0001). Como se puede ver en la figura 1, se alcanza, e incluso se rebasa, la media de talla del progenitor más bajo y parece que la tendencia es ir aproximándose a la TD. Al analizar, por separado, los 35 casos que llegaron a la talla final, durante las primeras 4 fases del tratamiento sucede lo mismo que en el resto del grupo, es decir, el incremento de talla es estadísticamente significativo (p<0,0001), pero a partir de la 4.ª fase se frena llamativamente el crecimiento y se alcanza un valor de talla adulta bajo (−2,22±0,86 DE). Al comparar la talla adulta con la TD (−1,72±0,75 DE), se encontraron diferencias estadísticamente significativas (t de Student: valor de t=−2,545; p=0,013), pero cuando se confronta con la del progenitor más bajo (−1,95±1,28 DE) no se hallaron diferencias (U de Mann-Whitney: valor de Z=−0,582; p=0,561).
El 42,9% de los 35 casos que alcanzaron la estatura adulta experimentaron un incremento de talla superior a 1 DE con la terapia.
DiscusiónEste es el primer trabajo que expone resultados de crecimiento de niños PEG valencianos tratados con rhGH.
Aunque en el protocolo de nuestra comunidad autónoma no se concede GH a sujetos afectos de algunos síndromes (Silver Russell, Noonan, Down), no podemos decir que la muestra sea homogénea, ya que, los criterios de tratamiento no aseguran que se excluya a todos los niños sindrómicos, ni tampoco a los afectos de determinadas displasias óseas (sobre todo, de aquellas que clínicamente no son muy manifiestas en los primeros años de vida). No obstante, lo que se ha pretendido en este estudio es valorar la respuesta, en general, de los sujetos tratados con GH bajo el epígrafe de PEG. Hay que recalcar que se ha trabajado retrospectivamente sobre documentos de solicitud de tratamiento y no sobre pacientes. Por tanto, solo fue posible saber si el sujeto tenía rasgos fenotípicos anómalos si el médico que efectuaba la petición de GH lo especificaba (estos casos no se incluyeron en el estudio). Esta heterogeneidad de la muestra puede haber influido en los resultados obtenidos. Quizá, en trabajos prospectivos futuros que aborden este tema, sería de utilidad recoger la presencia de rasgos sindrómicos, así como las medidas de los segmentos corporales de los niños PEG al inicio del tratamiento, y no solo la talla.
Se puede decir que nuestros niños lograron un incremento estadísticamente significativo de la DE de talla en las primeras 4 fases del tratamiento (p<0,0001); sin embargo, en el subgrupo de 35 casos que llegan a la talla final, a partir de esta 4.ª fase, se aprecia una llamativa deceleración del crecimiento, con un valor de talla final bajo (−2,22±0,86 DE). Por tanto, al contrario de lo que sucede en otras series publicadas15–17, los PEG de nuestra muestra que llegaron a la talla adulta no consiguieron normalizarla, ni tampoco aproximarse a la TD. No obstante, lograron que su DE de estatura se acercara bastante a la del progenitor más bajo. En ninguno de los trabajos revisados se ha tenido en cuenta la evaluación de la talla adulta con relación a la del progenitor más bajo. Se ha considerado de interés realizar tal comparación, en este estudio, dados los subóptimos resultados de estatura adulta obtenidos.
Se ha analizado qué circunstancias han podido influir en la pobre respuesta de crecimiento lograda en los PEG valencianos. Los modelos de predicción de respuesta a la rhGH del PEG publicados por Ranke et al.18,19 ponen de manifiesto que los factores con mayor influencia en el crecimiento, durante el primer año de terapia, son la edad de inicio y la dosis empleada; mientras que en el segundo año, lo más relevante es el incremento de la VC conseguido durante el primero. Todos estos factores han sido desfavorables en nuestro grupo.
En nuestra casuística, los niños empiezan el tratamiento una edad superior a la referida por otras series15–17,20 con mejores resultados (tabla 3). Especialmente tardía fue la edad de los 35 casos que alcanzaron la talla final (10,22±1,87 años). Se insiste en la importancia de iniciar la terapia cuanto antes16,21,22 para obtener buenas respuestas; es más, parece que este es uno de los factores más influyentes9,17,19,23. Una justificación a este comienzo tardío podría ser que la muestra engloba a sujetos que ya eran mayores cuando se implantó la indicación de tratamiento en España, en el 2003. Otra posibilidad, quizá con mayor peso, es una remisión tardía de los niños desde Atención Primaria a la consulta de Endocrinología.
Comparación de los resultados obtenidos en nuestra muestra de PEG con los de otros estudios
| Datos previos a iniciar el tratamiento con rhGH | KIGS20 (n=65) Mediana (P10/P90) | Van Pareren et al.17 (n=28) | Carrascosa et al.15 (n=49) | Güemes-Hidalgo et al.16 (n=52) | Nuestra muestra (n=115) |
|---|---|---|---|---|---|
| Edad cronológica (años) | 7,9 (3,6/11,9) | X±DE 7,9±1,9 | X±DE H: 7,8±1,8 M: 6,5±1,4 | X±DE 5,90±2,29 | X±DE 8,10±2,75 |
| DE de talla | (Prader) −3,6 (−5,0/−2,6) | (Prader) −2,9±0,8 | −3,3±0,6 | −3,12±0,62 | −3,14±0,59 |
| Dosis de rhGH pautada (mg/kg/día) | 0,035 (0,022/0,061) | X: 0,033 | 0,0319±0,0035 | Rango: 0,033-0,045 | 0,035±0,004 |
| Tras el 1.er año de tratamiento | KIGS20 (n=65) Mediana (P10/P90) | Van Pareren et al.17 (n=28) | Carrascosa et al.15 (n=49) | Güemes-Hidalgo et al.16 (n=45) | Nuestra muestra (n=115) |
|---|---|---|---|---|---|
| DE de talla | (Prader) −3,0 (4,6/−2,0) | No consta | ΔDE talla en 1 año: 0,8±0,3 | X: −2,2 P5: −2,4 P95: −1,9 | X±DE: −2,50±0,63 |
| DE de VC | (cm/año) 7,5 (5,6/10,0) | No consta | X±DE 4,5±1,8 | X: 3,22 P5: 2,59 P95: 3,85 | X±DE: 2,12±2,01 |
| Tras el 2.° año de tratamiento | KIGS20 (n=65) Mediana (P10/P90) | Van Pareren et al.17 (n=28) | Carrascosa et al.15 (n=49) | Güemes-Hidalgo et al.16 (n=36) | Nuestra muestra (n=115) |
|---|---|---|---|---|---|
| DE de talla | No consta | X±DE: −1,5±0,7 | ΔDE talla en 2 años: 1,2±0,4 | X: −1,8 P5: −2,0 P95: −1,5 | X±DE: −2,11±0,66 |
| DE de VC | No consta | No consta | X±DE: 2,0±1,4 | X: 2,28 P5: 1,7 P95: 2,87 | X±DE: 1,25±0,66 |
| Talla adulta | KIGS20 (n=65) Mediana (P10/P90) | Van Pareren et al.17, (n=28) | Carrascosa et al.15 (n=49) X±DE | Güemes-Hidalgo et al.16 | Nuestra muestra (n=35) X±DE |
|---|---|---|---|---|---|
| Edad cronológica (años) | 16,8 (14,7/18,3) | X: 15,8 | H: 17,4±0,8 M: 15,4±0,8 | − | 16,22±1,19 |
| DE de talla | (Prader) −2,1 (−3,5/−1,3) | X±DE: −1,1±0,8 | −1,7±0,7 | − | −2,22±0,86 |
| Δ (DE talla adulta–DE talla inicial) | (Prader) 1,3 (0,2/2,6) | X: 1,8 | 1,6±0,8 | − | 0,85±0,67 |
| Δ (DE talla adulta–DE talla media parental) | (Prader) −1,0 (2,4/0,0) | No consta | −0,4±0,8 | − | −0,49±0,71 |
| Δ (DE talla adulta–DE talla progenitor más bajo) | No consta | No consta | No consta | − | −0,27±1,55 |
DE: desviación estándar; X: media.
La media de dosis de rhGH que se usó en nuestros niños (0,035±0,004mg/kg/día) fue similar a la empleada por otros grupos15–17,20 (tabla 3), situada en el límite bajo del rango recomendado en el PEG1,24. Se ha visto que cuanto más alta es la dosis utilizada, dentro de los límites terapéuticos, mejores resultados se obtienen1,25,26. No obstante, si el paciente empieza a tratarse entre los 4 y los 6 años de edad, con 0,033mg/kg/día, se logran muy buenas respuestas. Sin embargo, en el caso de los niños prepuberales de talla extremadamente baja (inferior a −3 DE) y en aquellos que comienzan la terapia a edades ya muy cercanas a la pubertad se precisarán dosis más altas (≥0,055mg/kg/día)27,28. Ambas circunstancias se dan en el subgrupo de 35 casos que alcanza la talla finalpues iniciaron el tratamiento a una edad media de 10,22 años, con una talla de −3,06 DE. Quizá, si se hubieran empleado dosis de rhGH en el rango alto de lo recomendado se podrían haber mejorado los resultados de crecimiento.
El DE de VC obtenido por nuestros PEG en los primeros 12 meses de tratamiento es claramente inferior al de otros grupos15–17,20 (tabla 3). Lógicamente, este factor viene condicionado por los ya expuestos (edad de comienzo tardío y dosis de rhGH subóptimas).
La información realmente interesante de este estudio es la que aporta el subgrupo de 35 casos que alcanza la talla adulta. No obstante, se ha mostrado el perfil evolutivo de la estatura del resto de los casos para resaltar que, hasta la 4.ª fase, es muy similar al de estos 35 sujetos. Es decir, las gráficas de las figuras 1 y 2 son prácticamente superponibles. Se considera importante destacar este dato, puesto que, en la 4.ª fase, los sujetos presentan una edad media (12,65 años) que es muy probable que coincida con el momento de su estirón puberal; por tanto, la mejoría de la DE de talla que se produce en esta fase (DE −1,76±0,75) podría ser debida a este hecho, más que al tratamiento. Quizá, por este motivo, en los 35 casos que alcanzan la talla adulta se aprecia una pérdida de DE de estatura respecto a la fase previa, por el cese brusco del crecimiento tras el estirón puberal. Cabría esperar que los resultados de talla adulta de la parte de la muestra que aún no ha llegado a ella sean parecidos a los de aquellos que ya la han logrado. No obstante, no podremos asegurarlo hasta que se obtengan las tallas adultas de los 115 casos.
ConclusionesLa muestra estudiada de niños PEG valencianos tratados con rhGH por talla baja no obtiene una respuesta de crecimiento tan satisfactoria como los de otras series publicadas. Aunque mejora su DE de estatura, no logran aproximarse a su TD y quedan con una DE semejante a la del progenitor más bajo. Se cree que estos resultados subóptimos se deben a la edad avanzada de los niños al comenzar la terapia y a no haber ajustado la dosis de rhGH al alza ante un comienzo tan tardío, según lo recomendado en la bibliografía. Para mejorar nuestros resultados, se considera primordial que el pediatra de Atención Primaria remita a los PEG con DE de talla<−2,5 en torno a los 4 años, para poder iniciar el tratamiento cuanto antes, así como individualizar las dosis según las características del paciente.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A todo el personal de la Conselleria de Sanitat, en especial a Carmen Albelda y a M. Antonia Grau. A los profesionales médicos de todos los hospitales de la Comunidad Valenciana que remitieron los documentos de solicitud de tratamiento con hormona de crecimiento a la Conselleria de Sanitat, ya que estos han constituido el material de estudio de este trabajo.