Conocer el perfil de prescripción de anticatarrales en las consultas de Pediatría de Atención Primaria en el Área V del Servicio de Salud del Principado de Asturias y valorar su idoneidad.
Material y métodosEstudio transversal, descriptivo y retrospectivo. Se analizaron las prescripciones para el tratamiento de los procesos respiratorios en 6 consultas de Pediatría de Atención Primaria en el Área Sanitaria V del Servicio de Salud del Principado de Asturias en el año 2011. Se valoraron la idoneidad de los tratamientos prescritos mediante las fichas técnicas de los fármacos y las indicaciones clínicas según el diagnóstico, siguiendo las recomendaciones de guías clínicas, protocolos o en su defecto la bibliografía disponible más actual.
ResultadosSe analizaron 424 anticatarrales: 249 antitusígenos, 155 mucolíticos y 20 clasificados en otros. La media de edad de los pacientes es de 5 años. Un 85,1% de las prescripciones se consideran inadecuadas. El 11,6% de ellos fueron prescritos fuera de ficha técnica. Se consideraron inadecuados el 82,8% de los asociados al diagnóstico R74 y el 73% al R05. Todos los fármacos de los menores de 6 años se consideraron inadecuados. El 99,4% de los mucolíticos/otros y el 75,1% de los antitusígenos se consideraron inadecuados.
ConclusionesSe observa un alto porcentaje de prescripción de fármacos anticatarrales en menores de 14 años en nuestro medio, encontrándose un 85% de las prescripciones inadecuadas. Los niños deberían recibir solo medicamentos con una relación beneficio-riesgo favorable; para ello es necesario mejorar la información sobre el uso pediátrico y promover acciones formativas dirigidas a los padres y a los profesionales sanitarios.
To evaluate cold and cough medications and their suitability in children in Primary Health Care in Area V of the Asturian Health Service.
Material and methodsA cross-sectional, descriptive and retrospective study was conducted in which an analysis was performed of the respiratory diseases and the prescriptions of 6 Primary Health Care paediatricians who worked in Area V of the Asturian Health Service in 2011. An evaluation was made on the suitability of these medications. An analysis was also made of the drug datasheet and clinical recommendations (clinical guidelines, protocols or reports).
ResultsA total of 424 cold and cough drugs: 249 antitussives, 155 mucolytics, and 20 “others” were analyzed. The mean age was 5 years old. There was a total of 85.1% unsuitable prescriptions. Off-label drugs were used in 11.6%. The prescribing was considered unsuitable in 82.8% of prescriptions associated with R74, and 73% of R05. All of the prescription drugs in children under 6 years old were unsuitable. Mucolytics/“others” were not suitable in 99.4%, nor antitussives in 75.1%.
ConclusionsThere is a high level of cold and cough drugs being prescribed in children, with 85% of these being unsuitable. Children should only receive drugs with a good risk and benefit ratio. Pediatricians should try to improve the information about pediatric drug use and spread this information to parents, doctors and nurses.
En los últimos años ha existido controversia sobre el empleo de anticatarrales debido al uso y venta libre de muchos preparados farmacéuticos de dudosa eficacia terapéutica y con riesgo potencial de intoxicaciones en la edad pediátrica1,2.
En el año 2008, la Food and Drug Administration emitió una recomendación para evitar la administración de cualquier medicamento para la tos o el catarro en niños menores de 2 años por el riesgo de efectos secundarios, estando pendiente su decisión acerca del uso de anticatarrales entre los 2 y 11 años en la actualidad3,4. En otros países, como Canadá, Reino Unido, Australia, Bélgica y Holanda, también se ha desaconsejado su uso en los menores de 6 años, prohibiendo la dispensación libre de estos fármacos5.
La última Encuesta Nacional de Salud Española del 2011-2012 observó que el 48,2% de la población de entre 0-15 años había consumido en las 2 semanas previas medicamentos para aliviar los síntomas asociados a una infección respiratoria aguda (excluidos analgésicos-antitérmicos y antibióticos), no habiendo sido recetados por el médico en más de la cuarta parte de las ocasiones6.
A esto se suma que la ingesta accidental de anticatarrales continúa siendo un motivo de consulta frecuente como intoxicación en Urgencias de Pediatría y que el uso de medicamentos en condiciones diferentes de las autorizadas sigue siendo una realidad en los pacientes pediátricos. En nuestro país, el Ministerio de Sanidad califica de uso incorrecto la utilización en condiciones no autorizadas y advierte de los riesgos legales que esta práctica supone7,8.
Atendiendo a estas premisas, nos ha parecido oportuno realizar un estudio para conocer el perfil de prescripción de anticatarrales en las consultas de Pediatría de Atención Primaria (AP), recogiendo los datos desde las historias clínicas elaboradas por los profesionales que atienden a la población pediátrica en nuestra región.
Material y métodosCaracterísticas del estudioEstudio transversal, descriptivo y retrospectivo, donde se analizan los procesos respiratorios y sus prescripciones mediante la revisión de historias clínicas a través de OMI-AP (programa de historia clínica electrónica usado en nuestra comunidad autónoma en los centros de salud) en 6 consultas de Pediatría de AP en el Área Sanitaria V del Servicio de Salud del Principado de Asturias entre el 1 de enero y el 31 de diciembre del 2011.
Dicha área corresponde a los concejos de Gijón, Carreño y Villaviciosa, con población mayoritariamente urbana, atendiendo a una población de 31.111 menores de 14 años en el año 2011. Consta de 14 zonas básicas de salud, con un total de 32 médicos pediatras. Se seleccionan de manera aleatoria 6 consultas con disponibilidad de acceso en horario de tarde y 3 días al mes de lunes a viernes (16 lunes, 5 martes, 5 miércoles, 4 jueves y 6 viernes).
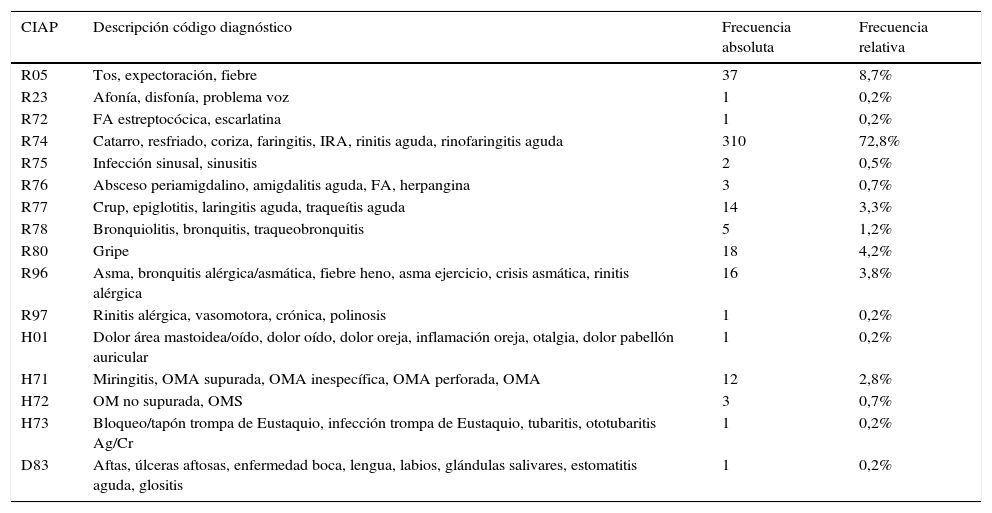
Se analizan los pacientes con procesos respiratorios, recogiendo las siguientes variables: 1) datos del paciente: fecha de nacimiento, edad, sexo, alergia medicamentosa, enfermedad crónica y/o tratamientos crónicos; 2) motivo de consulta y número de consultas por el mismo proceso; 3) diagnóstico: código CIAP-1 seleccionado por el médico (tabla 1), y 4) datos de prescripción: si estaban recibiendo medicación en el momento de la consulta, el médico prescriptor que atiende la visita analizada, el principio activo y/o nombre comercial del fármaco prescrito en dicha visita, su presentación y posología.
Frecuencia de los códigos CIAP-1 asociados al uso de anticatarrales
| CIAP | Descripción código diagnóstico | Frecuencia absoluta | Frecuencia relativa |
|---|---|---|---|
| R05 | Tos, expectoración, fiebre | 37 | 8,7% |
| R23 | Afonía, disfonía, problema voz | 1 | 0,2% |
| R72 | FA estreptocócica, escarlatina | 1 | 0,2% |
| R74 | Catarro, resfriado, coriza, faringitis, IRA, rinitis aguda, rinofaringitis aguda | 310 | 72,8% |
| R75 | Infección sinusal, sinusitis | 2 | 0,5% |
| R76 | Absceso periamigdalino, amigdalitis aguda, FA, herpangina | 3 | 0,7% |
| R77 | Crup, epiglotitis, laringitis aguda, traqueítis aguda | 14 | 3,3% |
| R78 | Bronquiolitis, bronquitis, traqueobronquitis | 5 | 1,2% |
| R80 | Gripe | 18 | 4,2% |
| R96 | Asma, bronquitis alérgica/asmática, fiebre heno, asma ejercicio, crisis asmática, rinitis alérgica | 16 | 3,8% |
| R97 | Rinitis alérgica, vasomotora, crónica, polinosis | 1 | 0,2% |
| H01 | Dolor área mastoidea/oído, dolor oído, dolor oreja, inflamación oreja, otalgia, dolor pabellón auricular | 1 | 0,2% |
| H71 | Miringitis, OMA supurada, OMA inespecífica, OMA perforada, OMA | 12 | 2,8% |
| H72 | OM no supurada, OMS | 3 | 0,7% |
| H73 | Bloqueo/tapón trompa de Eustaquio, infección trompa de Eustaquio, tubaritis, ototubaritis Ag/Cr | 1 | 0,2% |
| D83 | Aftas, úlceras aftosas, enfermedad boca, lengua, labios, glándulas salivares, estomatitis aguda, glositis | 1 | 0,2% |
CIAP: Clasificación Internacional de Atención Primaria; FA: faringoamigdalitis aguda; IRA: infección respiratoria de vías altas; OMA: otitis media aguda; OMS: otitis media serosa.
Se ha valorado la idoneidad de los tratamientos prescritos teniendo en cuenta 2 aspectos:
- 1.
Los datos que figuran en las fichas técnicas disponibles en la página web de la Agencia Española de Medicamentos y Productos Sanitarios, o en su defecto en los prospectos disponibles en el Vademécum 2012, de todos aquellos fármacos empleados en procesos del aparato respiratorio, incluyéndose los siguientes subgrupos de la clasificación ATC: R01B correspondiente a los descongestionantes nasales de uso sistémico y R05 que incluye los preparados para tos y resfriado.
- 2.
Por otro lado, se ha valorado la idoneidad de los tratamientos prescritos en los pacientes estudiados, siguiendo las recomendaciones de guías clínicas, protocolos o en su defecto la bibliografía disponible más actual según el cuadro clínico que presentan, clasificándolos de este modo según se considere inadecuado o adecuado. El uso de los fármacos analizados no se recomiendan en los pacientes con asma, bronquiolitis aguda, bronquitis aguda, gripe, laringitis aguda, neumonía, otitis media serosa, sinusitis aguda y tos ferina9-24. En los casos de cuadros catarrales, el uso de antitusígenos no está recomendado en menores de 6 años, aunque podría ser una alternativa bajo control médico en algunos pacientes mayores de 6 años25.
El análisis estadístico se efectuó mediante el programa informático SPSS versión 15.0 con licencia de uso. Se calcularon frecuencias absolutas y relativas para las variables cualitativas y se calcularon medias, medianas e intervalos de confianza del 95% de las medias para las variables cuantitativas. Para la comparación de grupos se utilizaron los test de la chi al cuadrado y el análisis mediante regresión logística binaria (variables cualitativas). Se consideraron diferencias estadísticamente significativas cuando el nivel de significación (p) era menor de 0,05.
ResultadosDatos generales de la muestraSe analizó a un total de 1.889 pacientes en 2.659 consultas por procesos respiratorios, con 2.583 prescripciones farmacológicas. En 726 consultas no se realizó ninguna prescripción. El diagnóstico más frecuente fue la infección respiratoria alta/R74 (42,5% de las consultas), seguido del asma/R96 (16,9%).
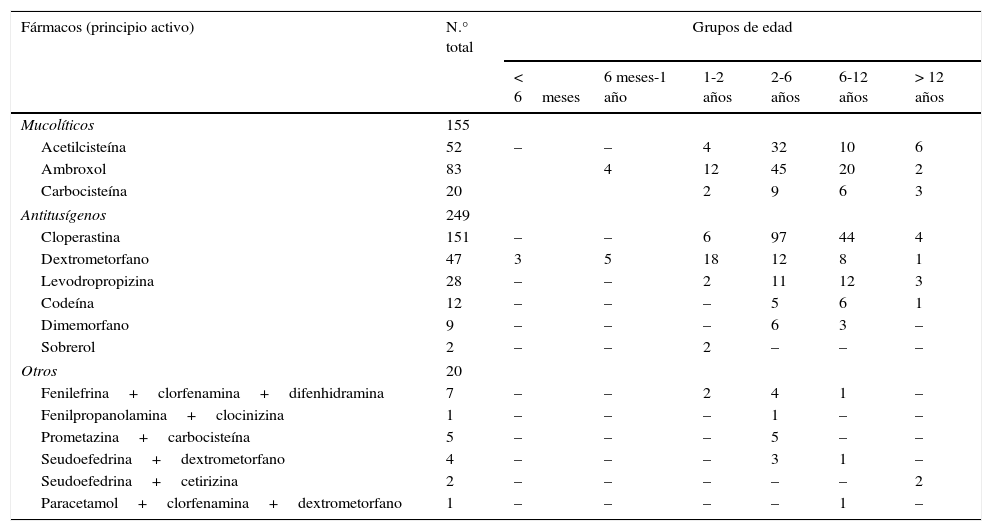
Análisis de los anticatarrales prescritosEn este artículo se analizaron 424 anticatarrales (16,4% de todas las prescripciones registradas): 249 antitusígenos (9,6% del total), 155 mucolíticos (6%) y 20 clasificados en otros (0,7%) (tabla 2), prescritos en un total de 354 pacientes. En el 23,7% de las consultas, el paciente ya estaba tomando alguna medicación prescrita con anterioridad por el mismo proceso. De estos fármacos, 14 antitusígenos, 4 mucolíticos y 5 del grupo otros estaban prescritos en la visita previa y no se suspendieron.
Distribución de principios activos prescritos (subgrupos terapéuticos R01B y R05)
| Fármacos (principio activo) | N.° total | Grupos de edad | |||||
|---|---|---|---|---|---|---|---|
| < 6meses | 6 meses-1 año | 1-2 años | 2-6 años | 6-12 años | > 12 años | ||
| Mucolíticos | 155 | ||||||
| Acetilcisteína | 52 | – | – | 4 | 32 | 10 | 6 |
| Ambroxol | 83 | 4 | 12 | 45 | 20 | 2 | |
| Carbocisteína | 20 | 2 | 9 | 6 | 3 | ||
| Antitusígenos | 249 | ||||||
| Cloperastina | 151 | – | – | 6 | 97 | 44 | 4 |
| Dextrometorfano | 47 | 3 | 5 | 18 | 12 | 8 | 1 |
| Levodropropizina | 28 | – | – | 2 | 11 | 12 | 3 |
| Codeína | 12 | – | – | – | 5 | 6 | 1 |
| Dimemorfano | 9 | – | – | – | 6 | 3 | – |
| Sobrerol | 2 | – | – | 2 | – | – | – |
| Otros | 20 | ||||||
| Fenilefrina+clorfenamina+difenhidramina | 7 | – | – | 2 | 4 | 1 | – |
| Fenilpropanolamina+clocinizina | 1 | – | – | – | 1 | – | – |
| Prometazina+carbocisteína | 5 | – | – | – | 5 | – | – |
| Seudoefedrina+dextrometorfano | 4 | – | – | – | 3 | 1 | – |
| Seudoefedrina+cetirizina | 2 | – | – | – | – | – | 2 |
| Paracetamol+clorfenamina+dextrometorfano | 1 | – | – | – | – | 1 | – |
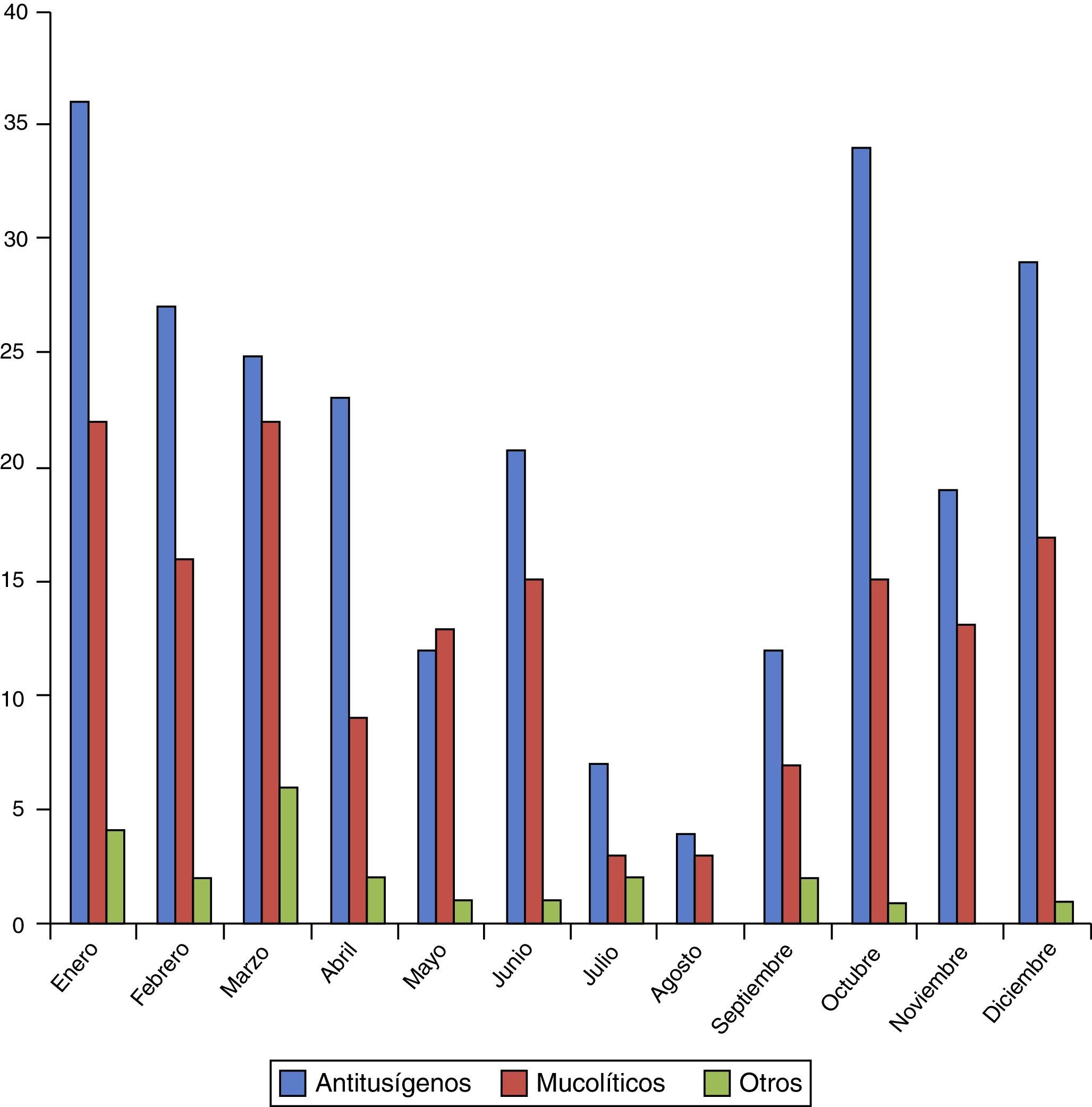
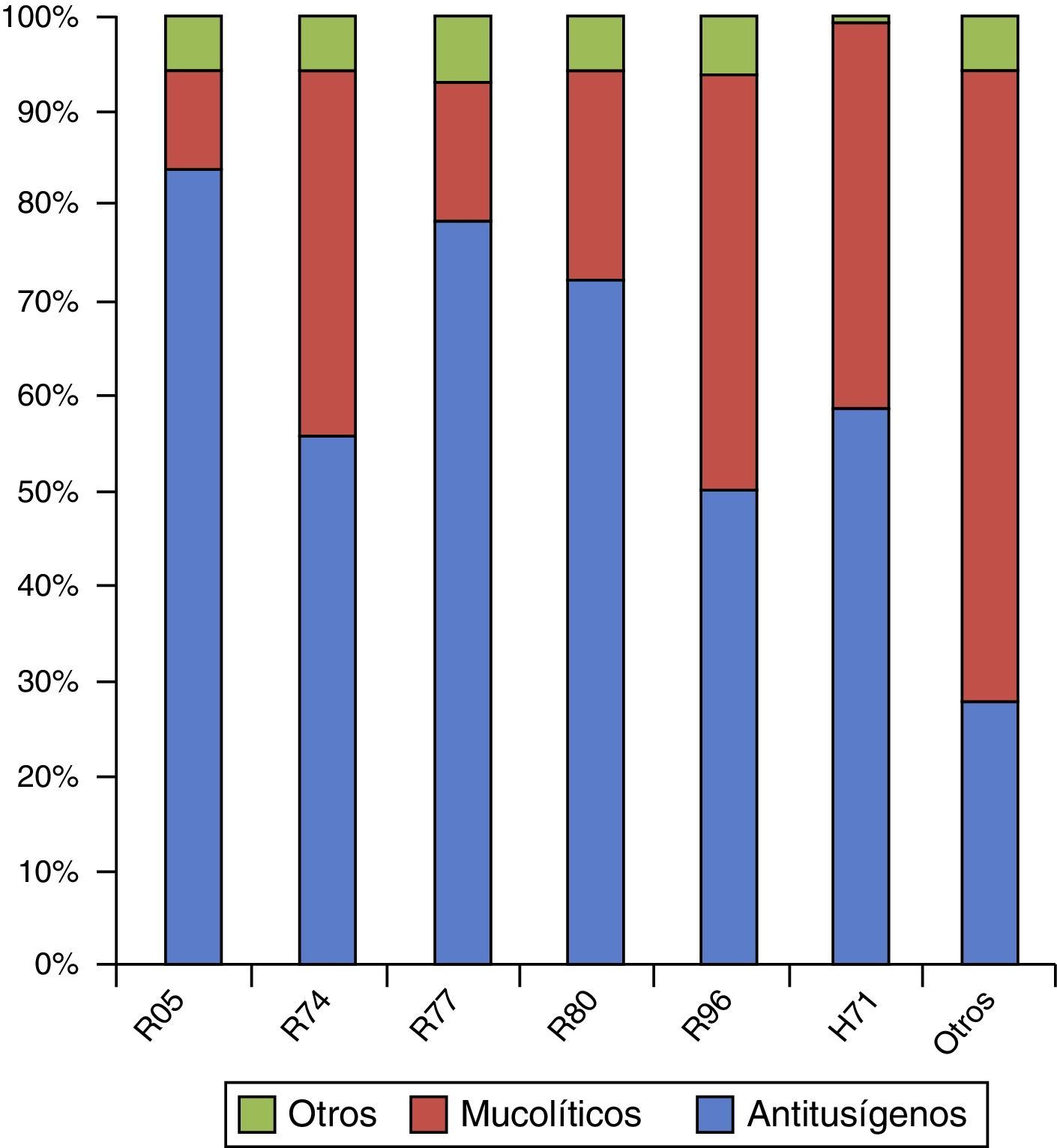
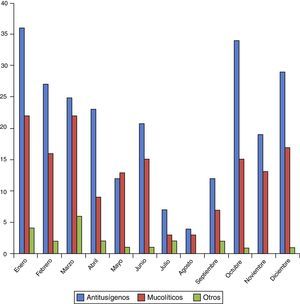
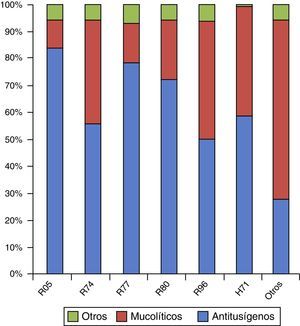
El diagnóstico más frecuente en este grupo es el R74 (72,8%), seguido del R05 (8,7%) (tabla 1). La distribución por meses y por códigos CIAP-1 se observa en las figuras 1 y 2.
Los pacientes que recibieron estos fármacos eran varones en un 51,9% y mujeres en el 48,1% de los casos, presentaban algún problema predisponente el 27%. La media de edad de los pacientes es de 5 años (1-171 meses). Estos pacientes fueron valorados por un pediatra en el 83,1% de las ocasiones y por un médico de familia en el 16,9%.
Variabilidad de la idoneidad del tratamientoAnálisis descriptivoEn el análisis inicial realizado para valorar la idoneidad teniendo en cuenta criterios clínicos e indicaciones en ficha técnica se observa un 85,1% de prescripciones inadecuadas. Estas corresponden al 75,1% de los antitusígenos (187), al 100% de los mucolíticos (155) y al 95,5% del grupo otros (19). De estos fármacos, el 11,6% de ellos fueron prescritos a edades no indicadas en la ficha técnica, fundamentalmente en menores de 2 años (tabla 3).
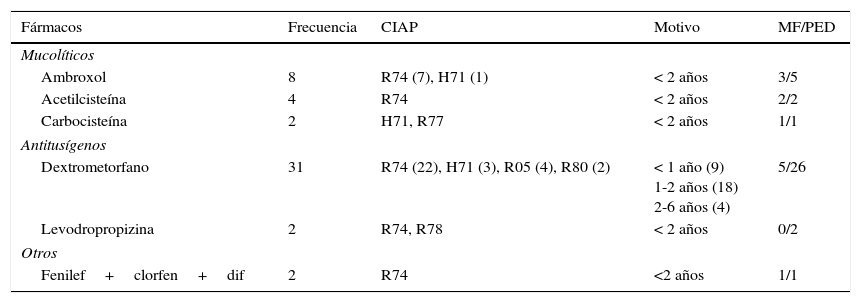
Fármacos prescritos en condiciones no autorizadas en ficha técnica
| Fármacos | Frecuencia | CIAP | Motivo | MF/PED |
|---|---|---|---|---|
| Mucolíticos | ||||
| Ambroxol | 8 | R74 (7), H71 (1) | < 2 años | 3/5 |
| Acetilcisteína | 4 | R74 | < 2 años | 2/2 |
| Carbocisteína | 2 | H71, R77 | < 2 años | 1/1 |
| Antitusígenos | ||||
| Dextrometorfano | 31 | R74 (22), H71 (3), R05 (4), R80 (2) | < 1 año (9) 1-2 años (18) 2-6 años (4) | 5/26 |
| Levodropropizina | 2 | R74, R78 | < 2 años | 0/2 |
| Otros | ||||
| Fenilef+clorfen+dif | 2 | R74 | <2 años | 1/1 |
CIAP: Clasificación Internacional de Atención Primaria; MF: médico de familia; PED: pediatra.
En los pacientes diagnosticados de R05 y R74 el tratamiento es inadecuado en el 73 y el 82,8%, respectivamente. Se observan diferencias estadísticamente significativas cuando comparamos los tratamientos inadecuados en los pacientes diagnosticados de R05 (p=0,029) frente a los no diagnosticados de R05, al igual que ocurre con aquellos etiquetados de R74 (p=0,027), no pudiendo establecerse mediante regresión logística si existe mayor o menor riesgo de tratamiento inadecuado asociado al diagnóstico.
Variabilidad por consultaExisten diferencias estadísticamente significativas entre la idoneidad de los tratamientos prescritos a los pacientes atendidos en la consulta 5 (p=0,006) frente a los que son valorados en las otras consultas, pero estas diferencias no se confirman, por lo que no puede establecerse una relación de mayor o menor riesgo de recibir tratamiento inadecuado en dicha consulta.
Variabilidad por grupos de edadEntre los grupos de edad, menores de 6 años y mayores de 6 años, se observa una diferencia estadísticamente significativa (p=0,000). Se tomó como punto de corte los 6 años, dado que es el límite en el que se consideraría como alternativa posible el uso de este grupo de fármacos, por lo que el tratamiento en los menores de 6 años se considera inadecuado en todos los casos. En el análisis mediante regresión logística no se observan diferencias estadísticamente significativas.
Variabilidad por tipo de médicoSi tenemos en cuenta el tipo de médico se observa una diferencia estadísticamente significativa entre los pediatras y los médicos de familia (p=0,038), objetivándose un 83,5% de prescripciones inadecuadas en los primeros y un 93,1% en los segundos, sin poder establecerse una relación de mayor o menor riesgo de recibir tratamiento inadecuado según el médico prescriptor.
Variabilidad por fármacos o grupos de fármacosSe encuentran diferencias estadísticamente significativas (p=0,000) comparando los antitusígenos (75,1% inadecuados) frente a los otros fármacos anticatarrales (99,4%), observándose un mayor porcentaje de tratamientos adecuados en el grupo de antitusígenos (IC del 95%, 99,3-100%) mediante regresión logística.
DiscusiónLas consultas por procesos respiratorios suponen gran parte de la carga asistencial en el día a día del pediatra de AP, implican una elevada morbilidad y hasta un 59,3% de los motivos de reducción de la actividad diaria de los pacientes y sus familias26. Este hecho se refleja en el estudio realizado en el 2006 en Asturias, donde un 44,8% de los diagnósticos analizados correspondían al aparato respiratorio y, dentro de estos, la infección respiratoria alta (R74) era el diagnóstico más frecuente, con un 23,1% sobre el total27. En nuestro estudio, el diagnóstico más frecuente también ha sido el R74 (42,5%), seguido del R96 o asma/rinitis alérgica (16,9%) (tabla 1).
Por lo general, los procesos respiratorios agudos son benignos y autolimitados; su tratamiento consiste en medidas no farmacológicas y de soporte. Sin embargo, existe una gran variedad de medicamentos que se han empleado en un intento de contrarrestar los síntomas. Su utilización no se recomienda por norma general dados su dudosa eficacia y el riesgo no desdeñable de toxicidad, sobre todo en menores de 6 años1,28. La ingesta accidental de anticatarrales por parte de menores de 4 años es un motivo de consulta frecuente como intoxicación en Urgencias de Pediatría, cerca del 75% de estos niños precisa tratamiento y casi la mitad debe permanecer al menos unas horas en el hospital7. En el estudio de Morales et al.8, los medicamentos del grupo R (aparato respiratorio) supusieron el 26,5% del total, es decir, una cuarta parte de los fármacos que toman los niños cuando acuden a las visitas en Urgencias. En nuestro trabajo, un 16,4% de las prescripciones realizadas fueron de medicamentos anticatarrales, en su mayoría antitusígenos y mucolíticos.
Por otro lado, un elevado porcentaje de los medicamentos que se utilizan en niños, tanto en Europa como en Estados Unidos, no están autorizados para su uso en este grupo de edad. Según datos de la Agencia Europea de Medicamentos, en el período 1995-2005 la situación no ha mejorado respecto a años anteriores en cuanto al número de medicamentos con información pediátrica, que es aproximadamente un tercio de los aprobados8. El uso de fármacos off-label, es decir, cuando la prescripción se realiza al margen de lo aprobado o autorizado en la ficha técnica, se calcula entre un 20 y un 80% de todas las prescripciones29-31. En nuestro estudio se analiza la idoneidad de los tratamientos prescritos teniendo en cuenta, por un lado, las autorizaciones en ficha técnica, principalmente la edad y, por otro, las indicaciones clínicas. El 85% de los fármacos anticatarrales prescritos han sido en condiciones no idóneas, debido a prescripciones off-label en el 13,2% de los antitusígenos, el 9% de los mucolíticos y el 10% del grupo otros. La causa más frecuente fue la edad inferior al límite autorizado, afectando a los menores de 2 años. Los estudios acerca de prescripciones off-label son muy heterogéneos en cuanto a la metodología, lo que dificulta la comparación de los resultados, hecho que observamos en nuestra muestra y en otros estudios, como el de Olsson et al.32, donde las cifras de prescripciones off-label son inferiores.
En el resto de los casos, el motivo fue la ausencia de indicación clínica, ya que los anticatarrales no están indicados en los pacientes con asma, bronquiolitis aguda, bronquitis aguda, gripe, laringitis aguda, neumonía, otitis media serosa, sinusitis aguda y tos ferina9-24. Debemos recordar que en los casos de cuadros catarrales el uso de estos fármacos podría ser una alternativa válida de tratamiento bajo control médico en casos seleccionados en mayores de 6 años25.
Por estos motivos, nos planteamos si el uso de estos fármacos está siendo adecuado en nuestro medio. En este sentido, debemos recordar que, para un uso racional de medicamentos, la Organización Mundial de la Salud33, en 1985, estableció que es preciso: a) recetar el medicamento apropiado; b) que se disponga de este oportunamente y a un precio asequible; c) que se dispense en las condiciones debidas, y d) que se tome en la dosis indicada y en los intervalos y durante el tiempo prescritos. El medicamento apropiado ha de ser, por tanto, eficaz y de calidad e inocuidad aceptables.
En nuestro estudio, el subgrupo más prescrito dentro de los anticatarrales son los antitusígenos. La distribución es bastante similar a la recogida por Cano Garcinuño et al.1, siendo la cloperastina el fármaco líder, utilizado desde hace más de medio siglo, con acción central y antihistamínica, cuya eficacia clínica en Pediatría no ha sido suficientemente estudiada5,34. El dextrometorfano es, a su vez, uno de los más empleados en niños como se refleja en la encuesta realizada en el País Vasco34 y en nuestra muestra el segundo en frecuencia. En líneas generales es un fármaco seguro y con amplio margen terapéutico, pero su sobredosificación o ingesta tóxica puede producir efectos secundarios graves sobre el sistema nervioso central y, en ocasiones, incluso la muerte35. Su eficacia antitusígena no se ha demostrado y, por el contrario, se ha convertido en una droga de uso recreacional en niños mayores y adolescentes en muchos países5. Debido a la falta de eficacia y el riesgo de efectos adversos graves, la Asociación Americana de Pediatría no recomienda el uso de dextrometorfano en niños36. La codeína, cuarto fármaco prescrito en nuestro estudio, se considera un «gold standard» en el tratamiento de la tos, aunque no hay estudios que avalen su uso en niños, sobre todo en lactantes y niños pequeños que tienen un mayor riesgo de toxicidad36. Los descongestionantes orales son vasoconstrictores que actúan a nivel de la mucosa, pero también tienen efectos sistémicos (cardiovasculares y neurológicos), cuya eficacia no ha sido demostrada37. En nuestro estudio se registraron varios productos que contienen fenilefrina y seudoefedrina.
Al analizar la idoneidad de las prescripciones, encontramos que el mayor porcentaje de tratamientos inadecuados tiene lugar en los casos con diagnóstico R05 y R74 respecto a los otros diagnósticos recogidos, probablemente por ser los más frecuentes en relación con el uso de estos fármacos. Asimismo, la edad fue un factor importante en estos análisis. Los mayores porcentajes de tratamientos inadecuados, como cabía esperar, ocurren por debajo de los 6 años. La elevada prescripción de anticatarrales y su relación inversa con la edad es una pauta que se ha mantenido en España desde hace al menos 30 años, y que se ha podido apreciar tanto en estudios pequeños en consultas como en estudios poblacionales1,38. Por tanto, debemos estar alerta en este grupo de edad, donde la dosificación recomendada está, principalmente, extrapolada de las dosis empleadas para los adultos, sin considerar las diferencias existentes de este rango de edad respecto a fisiología, biodisponibilidad y toxicidad medicamentosa37.
Algunos estudios previos han encontrado diferencias en la prescripción entre pediatras y médicos generales, siendo los primeros menos proclives a prescribir anticatarrales en los lactantes1,8. En nuestro estudio, las diferencias a este respecto señalan un mayor porcentaje de tratamiento adecuado en el caso de prescriptores pediatras, pero sin diferencias estadísticamente significativas. En Ontario, una encuesta realizada a los médicos que atendían población pediátrica recoge que el 16% de los médicos generales y el 4% de los pediatras recomiendan fármacos anticatarrales para sus pacientes con edades entre 0-6 meses, y que este porcentaje se eleva al 38 y el 14% en los niños entre 6-12 meses39. En una encuesta realizada en el País Vasco se demuestra que, aunque existen abundantes datos que desaconsejan el empleo de anticatarrales, la prescripción de estos fármacos es habitual entre los pediatras de AP; el 67,5% de los pediatras encuestados prescribían antitusígenos habitualmente34.
A su vez, encontramos diferencias al analizar los antitusígenos frente a los mucolíticos/otros. Se han considerado más tratamientos adecuados en el primer grupo que en el segundo, lo que se explicaría por la ausencia de indicación en los casos donde se han empleado fármacos del grupo mucolíticos/otros y la posibilidad en algunos casos de aceptar como alternativa terapéutica los antitusígenos en mayores de 6 años.
Nuestro estudio tiene limitaciones a pesar de seleccionar una muestra aleatoria. El tamaño muestral puede ser o no representativo de las prescripciones que se hacen de anticatarrales, pero consideramos que sí demuestra la situación actual en la que el uso de estos fármacos es frecuente a pesar de su escasa eficacia y su posible toxicidad. La fortaleza de nuestro trabajo se basa en la recogida de los datos de prescripción a través de las historias clínicas, y ligados a un diagnóstico clínico.
Para concluir, debemos resaltar la importancia de que los niños reciban solo medicamentos con probada eficacia y con una relación beneficio-riesgo favorable. Para evitar las prescripciones inadecuadas, además de promover acciones formativas para convencer a los propios pediatras, deberemos trabajar con los padres, informándoles sobre la eficacia real y los posibles efectos secundarios de estos fármacos para así tomar una decisión conjunta médico-padres individualizada en cada caso. La actitud del médico debería ser no recomendar este tipo de medicamentos basándose en los datos actualmente disponibles40. Pueden darse situaciones en que los padres deseen, a pesar de todo, que su hijo reciba algún tipo de medicación, en esta situación, el pediatra debería recurrir a aquellos fármacos que presenten un mejor perfil de seguridad40.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A todos los pediatras de AP del Área V del Servicio de Salud del Principado de Asturias, por su labor diaria, por su accesibilidad y su apoyo en la realización de este trabajo.