Cow's Milk-related Symptom Score (CoMiSS) es una herramienta práctica para evaluar la alergia a la proteína de la leche de vaca (APLV) en los lactantes teniendo en cuenta su sintomatología, a pesar de que el diagnóstico de APLV debe ser confirmado posteriormente por un especialista en pediatría y/o gastroenterología y nutrición pediátricas. El presente estudio tiene como objetivo comparar los resultados de la herramienta CoMiSS en lactantes diagnosticados de alergia a las APLV IgE y noIgE mediada.
Material y métodosEstudio multicéntrico, transversal, tipo encuesta realizado entre pediatras de toda España. Se les pidió que obtuvieran la puntuación CoMiSS en lactantes en el momento del diagnóstico de APLV y 7días después de iniciar el manejo nutricional con una fórmula extensamente hidrolizada (FEH). Se consideró positiva una puntuación CoMiSS ≥12.
ResultadosParticiparon en el estudio 294 pediatras (edad media: 51años). Se registró la puntuación CoMiSS en 1.176 lactantes con APLV (edad media±DE: 6,4±4,9meses), el 66,8% (n=745) no-IgE mediada. La puntuación CoMiSS media total mostró una mayor disminución en el grupo con alergia IgE mediada que en el grupo no-IgE mediada (−9,06±5,74 frente a −6,00±4,05; p<0,0001). Las puntuaciones medias de los síntomas individuales, llanto y regurgitación mostraron reducciones significativamente mayores en el grupo APLV no-IgE mediada, mientras que el eccema atópico en la cabeza y los brazos, la urticaria y los síntomas respiratorios mostraron reducciones significativamente mayores en el grupo IgE mediada. La puntuación CoMiSS total mostró una mayor disminución en el grupo con APLV muy grave en comparación con las graves, moderadas y leves.
ConclusiónEsta encuesta muestra que en los lactantes diagnosticados con APLV, solo un tercio tenía una puntuación CoMiSS positiva ≥12puntos en el momento del diagnóstico, lo que respalda un uso inadecuado de la herramienta CoMiSS. Se recomiendan acciones para aumentar el conocimiento del valor de CoMiSS para la evaluación de la APLV.
The Cow's Milk-related Symptom Score (CoMiSS) is a practical tool to assess for cow's milk protein allergy (CMPA) in infants based on clinical manifestations, although the diagnosis of CMPA should be confirmed subsequently by a specialist in pediatrics and/or pediatric gastroenterology and nutrition. The aim of this study was to compare CoMiSS results in infants diagnosed with IgE-mediated and non-IgE-mediated CMPA.
Material and methodsMulticenter, cross-sectional survey study with participation of pediatricians throughout Spain. Pediatricians were directed to apply the CoMiSS to infants at the time of diagnosis of CMPA and 7days after initiating nutritional management with an extensively hydrolyzed formula (EHF). We interpreted a CoMiSS score of 12 or greater as positive.
ResultsA total of 294 pediatricians (mean age, 51years) participated in the study. The analysis included CoMiSS results for 1176 infants with CMPA (mean [SD] age: 6.4 [4.9] months), of who 66.8% (n=745) had non-IgE-mediated CMPA. We found a greater decrease in the mean score in the IgE-mediated group compared to the non-IgE-mediated group (mean [SD] −9.06 [5.74] vs −6.00 [4.05]; P<.0001). When it came to individual symptoms, there were significantly greater reductions in the mean scores for crying and regurgitation in the non-IgE-mediated group, and, conversely, significantly greater reductions in the scores for atopic eczema in the head and arms, urticaria and respiratory symptoms in the IgE-mediated group. There was also a greater decrease in the total CoMiSS score in infants with very severe CMPA compared to infants with severe, moderate and mild CMPA.
ConclusionThis survey showed that only one third of infants diagnosed with CMPA had a positive CoMiSS result of 12points or greater at the time of diagnosis, which suggests an inadequate use of the CoMiSS. We recommend the implementation of strategies to increase knowledge of the utility of the CoMiSS for the assessment of CMPA.
La alergia a la proteína de la leche de vaca (APLV) afecta al 2%-6% de la población pediátrica1, y es la alergia alimentaria diagnosticada con mayor frecuencia en lactantes durante el primer año de vida2. En el estudio EuroPrevall, realizado en una cohorte de niños reclutados desde el nacimiento en nueve países europeos, la incidencia global de la APLV confirmada mediante prueba de provocación en menores de 2años fue del 0,54%3. No obstante, la mayoría de los niños afectados adquieren tolerancia a la leche de vaca con el tiempo, con un descenso en la prevalencia de APLV al 1% a los 6años de edad4. Los efectos adversos provocados por el consumo de la leche de vaca se deben a una respuesta inmunitaria que puede estar mediada por anticuerpos IgE (IgE mediada, reacción de hipersensibilidad tipoI) u otros mecanismos (noIgE mediada). En la población española se ha descrito una incidencia de APLV IgE mediada del 0,36% durante el primer año de vida5.
El diagnóstico de la APLV supone un reto debido a su amplio espectro clínico, que implica al aparato digestivo, la piel y el aparato respiratorio. No es difícil que se haga un diagnóstico incorrecto de APLV en la práctica diaria debido a la falta de síntomas específicos y la alta proporción de diagnósticos basados en la experiencia clínica sin confirmación mediante pruebas complementarias, tales como las pruebas de exclusión-provocación, el prick test o la detección de anticuerpos IgE frente a las proteínas de la leche de vaca6. El diagnóstico erróneo puede llevar a restricciones alimentarias innecesarias, que a su vez pueden afectar al crecimiento y el desarrollo cuando no se usan fórmulas hipoalergénicas, aumentando el estrés familiar y la carga para el sistema sanitario. El infradiagnóstico y el retraso diagnóstico también tienen efectos perjudiciales para la salud del lactante, con síntomas persistentes, retraso del crecimiento y riesgo de deficiencias de micronutrientes. Además, el sobrediagnóstico de la APLV puede implicar costes significativos por el uso excesivo de las distintas fórmulas especiales disponibles para su manejo7.
En septiembre de 2014, un grupo de expertos en el manejo de niños con problemas gastrointestinales y/o enfermedades atópicas participó en un taller celebrado en Bruselas (Bélgica) y desarrolló por consenso un sistema de puntuación para la evaluación de la APLV basada en su sintomatología, la Cow's Milk-related Symptom Score (CoMiSS™)8. La puntuación CoMiSS es una herramienta fácil de usar, rápida y corta, que evalúa la presencia y la intensidad del llanto y la regurgitación, la consistencia de las deposiciones y las manifestaciones cutáneas y respiratorias. Es un instrumento útil para la valoración de la APLV, que ayuda a establecer su diagnóstico, especialmente en casos de alergia noIgE mediada, y que puede emplearse para monitorizar la mejora de los síntomas8. Para identificar a los lactantes con riesgo de APLV, se acepta el punto de corte arbitrario de ≥12 propuesto y utilizado como criterio de inclusión en el ensayo original9. Numerosos estudios han evaluado la utilidad de la CoMiSS en diferentes contextos, principalmente en lactantes con síntomas posiblemente relacionados con la APLV, así como antes y después de la eliminación de la leche de vaca, en la APLV IgE mediada y noIgE mediada, como herramienta diagnóstica independiente, en lactantes considerados sanos y en pacientes con afecciones distintas a la APLV10-16. También se han publicado varios artículos de revisión que ofrecen una síntesis detallada de los resultados de estos estudios clínicos17-19. Un metaanálisis que incluía 14 estudios y 1.238 niños con aplicación de un punto de corte de ≥12 mostró una sensibilidad combinada del 64% y una especificidad del 75%, con un área bajo la curva ROC de 0,786, demostrando el potencial de la puntuación CoMiSS para la valoración de la APLV y la monitorización de la respuesta a la dieta exenta de leche de vaca20.
Sin embargo, hasta donde sabemos, no se ha realizado ningún estudio en España para evaluar la utilidad clínica de la puntuación CoMiSS. Por lo tanto, el objetivo principal del estudio fue determinar si el uso de esta puntuación podría ayudar a los pediatras españoles en la evaluación de los lactantes con APLV, comparando los resultados de la CoMiSS en lactantes diagnosticados de APLV tanto IgE mediada como noIgE mediada y con distintos niveles de gravedad.
MétodosDiseño y participantesSe llevó a cabo un estudio observacional, multicéntrico y transversal tipo encuesta en pediatras españoles con objeto de recoger datos sobre el uso de la CoMiSS en lactantes diagnosticados de APLV en la práctica clínica real.
Podían participar los pediatras de atención primaria del sistema nacional de salud español o de centros privados de toda España, siempre y cuando su práctica diaria habitual incluyera el manejo ambulatorio de al menos 10lactantes. Los participantes se reclutaron a partir de la información disponible en la base de datos de pediatras clínicos gestionada por Laboratorios OrdesaS.L. Alrededor del 50% del total de los pediatras que ejercen la especialidad en España están registrados en la base de datos. Se enviaron invitaciones individuales a los pediatras solicitando su participación en el estudio, destacando su naturaleza voluntaria y anónima. A continuación, se envió un cuaderno electrónico de recogida de datos a aquellos pediatras que dieron su consentimiento informado por escrito. El trabajo de campo duró 6meses y se llevó a cabo entre enero y septiembre de 2023.
Procedimientos del estudio y recogida de datosSe pidió a los participantes que completaran el cuestionario CoMiSS recogiendo datos retrospectivos de los últimos 6meses para obtener la puntuación de los lactantes en el momento del diagnóstico de APLV basado en la práctica clínica habitual del pediatra, los síntomas recogidos en la anamnesis y la exploración física, así como 7días después del inicio de la dieta de exclusión con fórmula extensamente hidrolizada (FEH). Se excluyó a los pacientes que requerían alimentación con fórmula elemental. Los datos presentados en este estudio se registraron en el transcurso de la práctica clínica habitual en el mundo real, facilitando el cuestionario de la puntuación CoMiSS a los pediatras sin informarles de que se trataba de este instrumento y sin ofrecer formación previa para su uso.
La puntuación CoMiSS es una herramienta sencilla de evaluación en la que se valoran los siguientes cinco síntomas: duración diaria del llanto, número y volumen de episodios de regurgitación, consistencia de las heces, presencia y gravedad de eccema atópico o urticaria, y presencia y gravedad de síntomas respiratorios. El llanto, las regurgitaciones y las manifestaciones cutáneas se puntúan con una escala de0 a6, en la que la gravedad aumenta con cada punto y el 6 representa la mayor gravedad posible. La consistencia de las deposiciones se puntúa, según la clasificación obtenida con la Bristol Stool Scale (BSS)21, como 0 para deposiciones normales (tipos3 y4), 2 para deposiciones blandas (tipo5), 4 para deposiciones duras (tipos1 y2) o semilíquidas (tipo6) y 6 para deposiciones líquidas (tipo7). Las manifestaciones cutáneas también se puntúan en una escala de 0 a 6 e incluyen la presencia de eccema atópico (con afectación de cabeza-cuello-tronco y/o manos-brazos-piernas-pies). Los síntomas respiratorios se puntúan en una escala de 0 a 3, en la que 0 corresponde a su ausencia, 1a síntomas leves, 2a síntomas moderados y 3a síntomas graves. La puntuación total de la CoMiSS oscila entre 0 y 33puntos, y valores en la escala total de 12 o más puntos se consideran indicativos de APLV.
En el formulario del estudio también se recogían datos demográficos del lactante, sobre el diagnóstico de APLV IgE mediada o noIgE mediada establecido por cada pediatra basándose en su experiencia y práctica clínica habitual, la edad al diagnóstico y la gravedad de los síntomas. Esta última se evaluó mediante una escala Likert de 4 puntos (leve, moderada, grave y muy grave). También se registró el tiempo transcurrido hasta la mejora de los síntomas tras el inicio de la alimentación con FEH. La primera sección del cuestionario recogía datos sobre las características demográficas de los pediatras, el tipo de consulta, el centro de trabajo y el número de pacientes menores 2años que atendían al mes.
Análisis estadísticoLos datos categóricos se expresan como frecuencias y porcentajes y los continuos como media y desviación estándar (DE) o, si la distribución no era normal, mediana y rango intercuartílico (RIC). Las diferencias en la distribución de las variables entre los grupos de APLV IgE mediada y noIgE mediada, así como los cambios en los distintos ítems de la herramienta CoMiSS entre el día0 (antes de introducir cambios en la alimentación del lactante) y el día7 (tras la introducción de la FEH) se compararon mediante la prueba de Kruskal-Wallis, la prueba U de Mann-Whitney y el análisis de varianza (ANOVA) según sus condiciones de aplicación. La significación estadística se fijó en p<0,05. El análisis de los datos se realizó con el software Statistical Analysis Systems, versión 9.4 (SAS Institute, Cary, NC, EE.UU.).
ResultadosPediatras participantesEn el estudio participaron 294 pediatras (51,4% mujeres) con una edad media de 51años (DE: 11,2). La mayoría (82,6%) trabajaban en entornos urbanos, el 51,7% en un centro público, el 22,4% en una clínica privada y el 23,1% en entornos tanto públicos como privados. Por añadidura, el 55,4% trabajaban en centros de salud, el 18,7% en consultas externas hospitalarias y el 25,8% en clínicas privadas. El número mediano de lactantes atendidos por mes fue de 150 (RIC: 100-200).
Características de los lactantesLa muestra del estudio incluyó a 1.176 lactantes diagnosticados de APLV por sus pediatras. El 55,7% eran varones, con una mediana de edad de 5meses (RIC: 3-9). La mediana de edad en el momento del diagnóstico de APLV fue de 2meses (RIC: 1-4). Se registró APLV noIgE mediada en el 66,8% de los lactantes (n=745) y APLV IgE mediada en el 33,2% (n=371). En el grupo con APLV noIgE mediada, solo se realizaron pruebas de provocación en el 56,4% de los casos. La gravedad de la APLV se consideró leve en el 22,9% de los lactantes (n=262), moderada en el 58% (n=664), grave en el 17,3% (n=198) y muy grave en el 1,8% (n=21). En todos los casos, se indicó alimentación con FEH.
Evolución de la puntuación CoMiSS antes y después de introducir una fórmula extensamente hidrolizadaSe registró una puntuación CoMiSS total de 12puntos o superior en el 33,1% de los lactantes en el día0 y en el 1,7% en el día7. La proporción de lactantes con una puntuación inferior a 12puntos aumentó del 66,9% en el día0 al 98,3% en el día7. La mediana de la puntuación CoMiSS total disminuyó de 10 (RIC: 7-13) a 3puntos (RIC: 1-5) tras la introducción de la FEH.
Los cambios en los distintos ítems de la puntuación CoMiSS entre los días0 y7 se muestran en la tabla 1. Las puntuaciones medias de todos los síntomas disminuyeron entre el día0 y el7, y las diferencias fueron estadísticamente significativas en todos, excepto la consistencia de las heces. La reducción fue particularmente importante en los ítems correspondientes al llanto y la regurgitación, con un aumento notable en el porcentaje de lactantes que lloraban una hora o menos al día (del 16,7% al 57,1%) y en el de lactantes con cero a dos episodios de regurgitación al día (del 23,7% al 63,8%). El porcentaje de niños con deposiciones normales aumentó del 24,6% al 58,2%. Las proporciones de pacientes con eccema atópico moderado y grave que afectaba tanto a la cabeza-cuello-tronco como a los brazos-manos-piernas-pies disminuyeron del 24,1% al 2,9% y del 15,9% al 2,3%, respectivamente. Además, en el día7, el 97,9% de los lactantes no presentaban urticaria y el 91,4% no presentaban síntomas respiratorios.
Diferencias en las puntuaciones de los ítems de la CoMiSS en la muestra de estudio antes y después de iniciar la dieta de eliminación
| Variables | Día 0, n (%) | Día 7, n (%) |
|---|---|---|
| Puntuación total, media (DE) | 9,95 (4,81) | 3,16 (2,98) |
| p<0,0001 | ||
| Llanto | ||
| ≤ 1 hora/día | 181 (16,7) | 617 (57,1) |
| De 1 a 1,5 horas/día | 143 (13,2) | 299 (27,6) |
| De 1,5 a 2 horas/día | 148 (13,6) | 102 (9,4) |
| De 2 a 3 horas/día | 201 (15,8) | 32 (3,0) |
| De 3 a 4 horas/día | 188 (17,3) | 22 (2,0) |
| De 4 a 5 horas/día | 121 (11,1) | 3 (0,3) |
| ≥ 5 horas/día | 103 (9,5) | 6 (0,6) |
| Sin datos | 91 (7,7) | 95 (8,1) |
| Puntuación, media (DE) | 2,78 (1,90) | 0,68 (1,02) |
| p=0,004 | ||
| Regurgitación | ||
| 0 a 2 episodios/día | 258 (23,7) | 697 (63,8) |
| De ≥ 3 a ≤ 5 episodios de volumen pequeño | 248 (22,8) | 290 (26,5) |
| > 5 episodios con volumen >1 cucharadita de café | 136 (12,5) | 66 (6,0) |
| > 5 episodios de volumen pequeño ±la mitad del alimento recibido en <la mitad de las tomas | 155 (14,2) | 21 (1,9) |
| Regurgitaciones continuas de volumen pequeño >30minutos después de cada toma | 139 (17,8) | 16 (1,5) |
| Regurgitación de entre la mitad y todo el volumen del alimento recibido en la mitad de las tomas, como mínimo | 102 (9,4) | 1 (0,1) |
| Regurgitación de todo el alimento después de cada toma | 50 (4,6) | 2 (0,2) |
| Sin datos | 88 (7,5) | 83 (7,1) |
| Puntuación, media (DE) | 2,16 (1,84) | 0,52 (0,86) |
| p=0,0298 | ||
| Deposiciones (escala de Bristol) | ||
| Tipo 1 y 2 (deposiciones duras) | 116 (6,6) | 140 (12,8) |
| Tipo 3 y 4 (deposiciones consistentes) | 269 (24,6) | 635 (58,2) |
| Tipo 5 (deposiciones blandas) | 260 (23,7) | 275 (25,2) |
| Tipo 6 (deposiciones semilíquidas no asociadas a infección) | 291 (26,6) | 33 (3,0) |
| Tipo 7 (deposiciones líquidas) | 159 (14,5) | 8 (0,7) |
| Sin datos | 81 (6,9) | 85 (7,2) |
| Puntuación, media (DE) | 2,29 (1,67) | 1,19 (1,57) |
| p=0,1974 | ||
| Manifestaciones cutáneas | ||
| Eccema atópico | ||
| Cabeza-cuello-tronco | ||
| Ausente | 549 (50,0) | 737 (68,4) |
| Leve | 285 (26,0) | 309 (28,7) |
| Moderado | 237 (21,6) | 30 (2,8) |
| Grave | 27 (2,5) | 1 (0,1) |
| Sin datos | 78 (6,7) | 99 (8,4) |
| Puntuación, media (DE) | 0,77 (0,87) | 0,35 (0,54) |
| p<0,0001 | ||
| Brazos-manos-piernas-pies | ||
| Ausente | 656 (61,5) | 819 (78,7) |
| Leve | 241 (22,6) | 198 (19,0) |
| Moderado | 151 (14,1) | 21 (2,0) |
| Grave | 19 (1,8) | 3 (0,3) |
| Sin datos | 109 (9,3) | 135 (11,5) |
| Puntuación, media (DE) | 0,56 (0,80) | 0,24 (0,49) |
| p<0,0001 | ||
| Urticaria | ||
| No | 865 (77,4) | 1056 (97,9) |
| Sí | 253 (22,6) | 23 (2,1) |
| Sin datos | 58 (4,9) | 97 (8,2) |
| Puntuación, media (DE) | 1,36 (2,51) | 0,13 (0,87) |
| p<0,0001 | ||
| Síntomas respiratorios | ||
| Sin síntomas respiratorios | 821 (73,8) | 993 (91,4) |
| Leves | 198 (17,8) | 86 (7,9) |
| Moderados | 87 (7,8) | 6 (0,6) |
| Graves | 7 (0,6) | 1 (0,1) |
| Sin datos | 63 (5,4) | 90 (7,6) |
| Puntuación, media (DE) | 0,35 (0,65) | 0,09 (0,32) |
| p<0,0001 | ||
CoMiSS: Cow's Milk-Related Symptom Score; DE: desviación estándar.
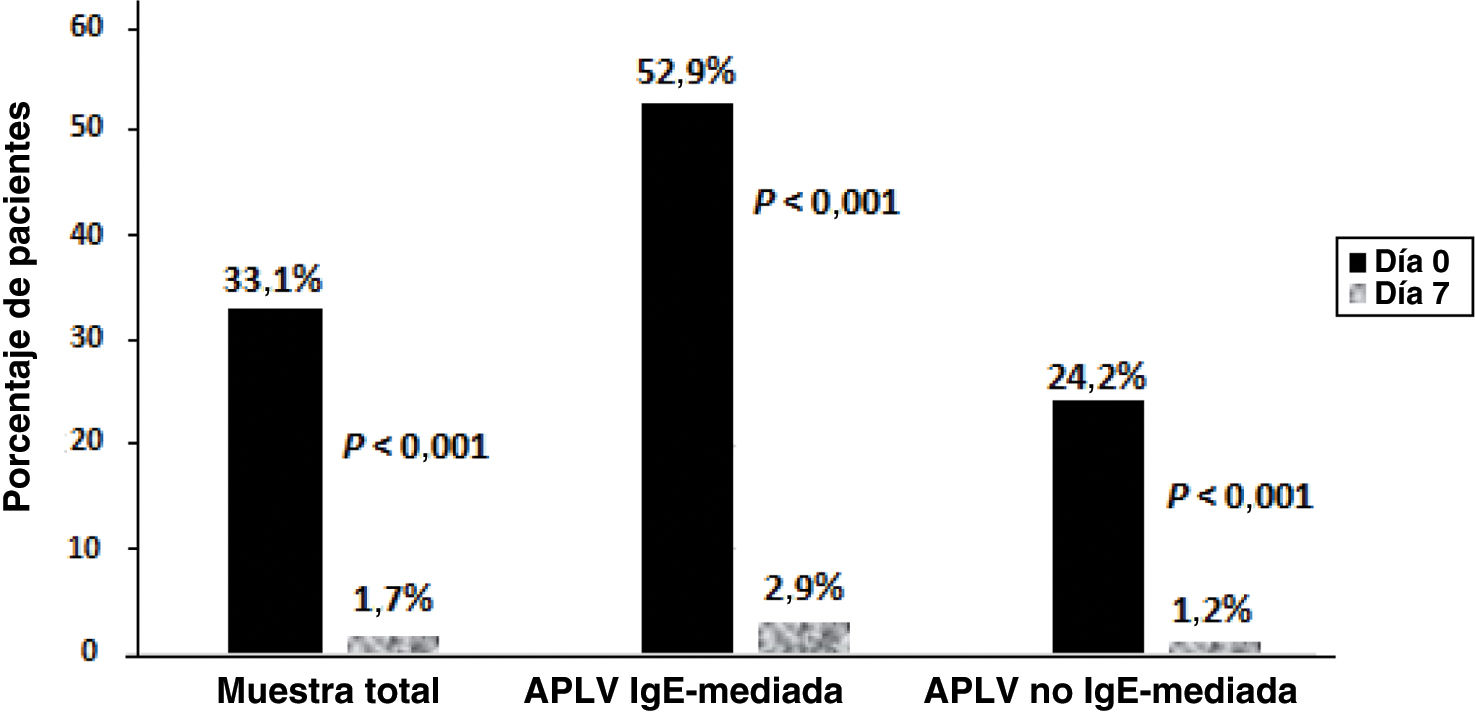
En el grupo de APLV IgE mediada, la media de la puntuación CoMiSS en el día0 fue de 12 (DE: 5,2), disminuyendo a 3,4 (DE: 3,4) en el día7 (p<0,001). Los valores correspondientes para la APLV noIgE mediada fueron 8,9 (DE: 4,1) y 3,1 (DE: 2,8), respectivamente (p<0,001). También hubo diferencias significativas en el porcentaje de lactantes con una puntuación igual o superior a12 entre los grupos de APLV IgE mediada y noIgE mediada: 52,9% y 24,27%, respectivamente (fig. 1) (p<0,05).
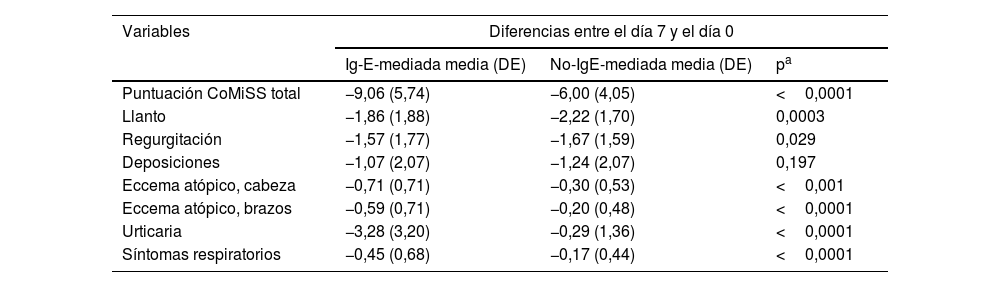
La comparación de las puntuaciones medias mostró diferencias estadísticamente significativas entre los grupos de APLV IgE mediada y noIgE mediada en los cambios en los síntomas relacionados con la APLV entre los días0 y7 (tabla 2). La media de la puntuación CoMiSS total mostró un aumento mayor en el grupo de APLV IgE mediada que en el grupo de APVL noIgE mediada (media [DE]: −9,06 [5,74] vs. −6,00 [4,05]); p<0,0001). Sin embargo, en el análisis de las puntuaciones de cada síntoma se observaron reducciones significativamente mayores en el llanto y la regurgitación en el grupo de APLV noIgE mediada, mientras que las reducciones en el eccema atópico en cabeza y brazos, urticaria y síntomas respiratorios fueron significativamente mayores en el grupo de APLV IgE mediada.
Cambio en la media de la puntuación CoMiSS según el diagnóstico de APLV
| Variables | Diferencias entre el día 7 y el día 0 | ||
|---|---|---|---|
| Ig-E-mediada media (DE) | No-IgE-mediada media (DE) | pa | |
| Puntuación CoMiSS total | −9,06 (5,74) | −6,00 (4,05) | <0,0001 |
| Llanto | −1,86 (1,88) | −2,22 (1,70) | 0,0003 |
| Regurgitación | −1,57 (1,77) | −1,67 (1,59) | 0,029 |
| Deposiciones | −1,07 (2,07) | −1,24 (2,07) | 0,197 |
| Eccema atópico, cabeza | −0,71 (0,71) | −0,30 (0,53) | <0,001 |
| Eccema atópico, brazos | −0,59 (0,71) | −0,20 (0,48) | <0,0001 |
| Urticaria | −3,28 (3,20) | −0,29 (1,36) | <0,0001 |
| Síntomas respiratorios | −0,45 (0,68) | −0,17 (0,44) | <0,0001 |
APLV: alergia a la proteína de la leche de vaca; CoMiSS: Cow's Milk-Related Symptom Score; DE: desviación estándar.
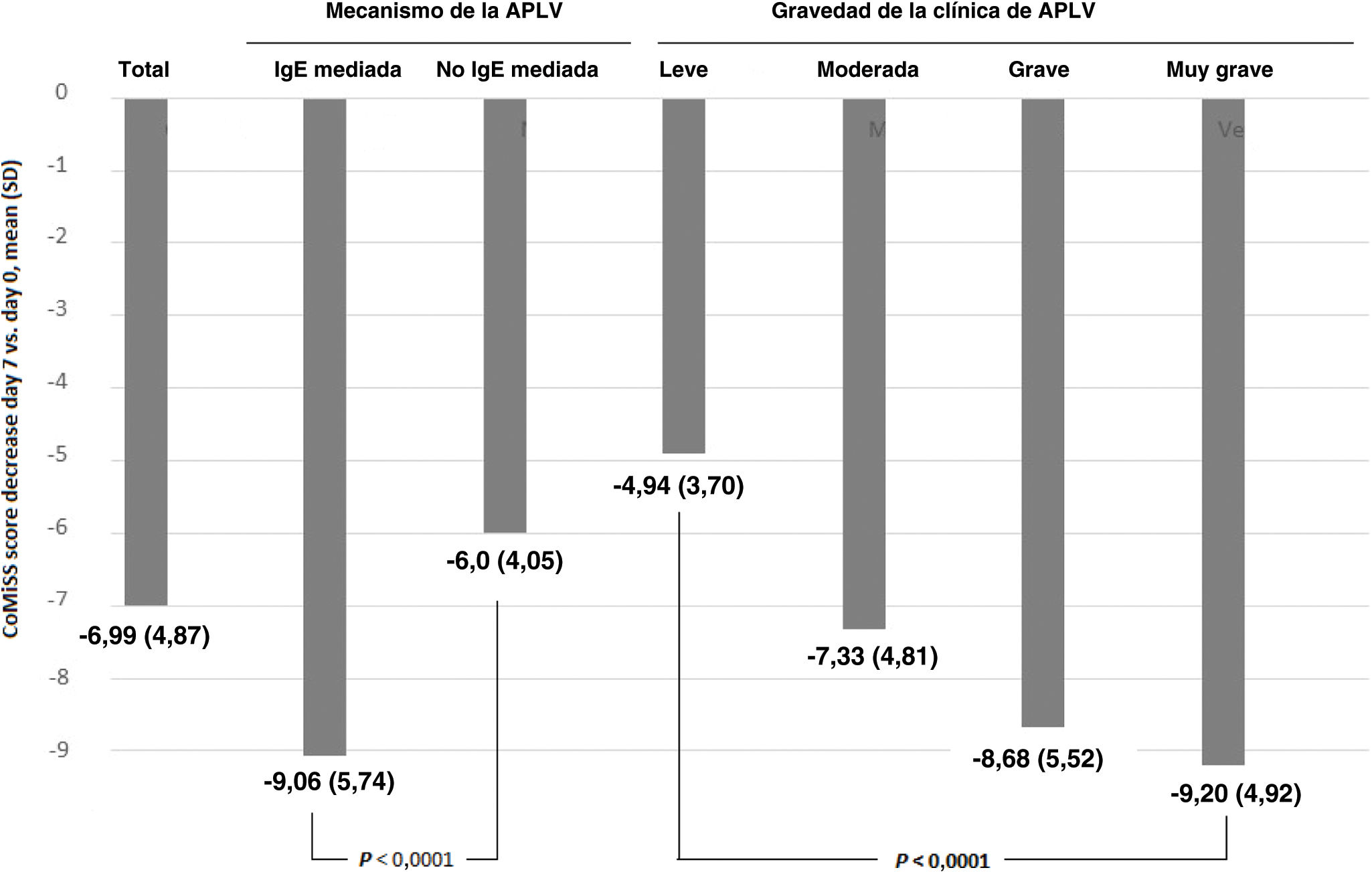
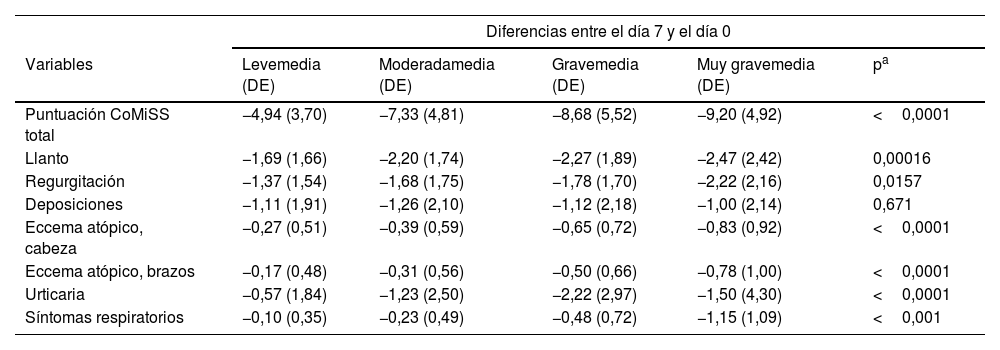
En el análisis de las puntuaciones CoMiSS según el nivel de gravedad de la APLV se observaron diferencias estadísticamente significativas entre los grupos con clínica leve, moderada, grave y muy grave. Como se muestra en la tabla 3, la media de la puntuación CoMiSS total mostró una disminución mayor en el grupo de APLV muy grave (−9,20 [DE: 4,92]) en comparación con los grupos restantes. Al analizar por separado los cambios en los síntomas asociados a la APLV, se observaron diferencias significativas entre los días7 y0 en todos los síntomas, excepto en las deposiciones. En general, las reducciones en las puntuaciones fueron mayores en los grupos de síntomas graves en comparación con el resto (tabla 3).
Cambios en las puntuaciones CoMiSS según la gravedad de los síntomas de APLV
| Diferencias entre el día 7 y el día 0 | |||||
|---|---|---|---|---|---|
| Variables | Levemedia (DE) | Moderadamedia (DE) | Gravemedia (DE) | Muy gravemedia (DE) | pa |
| Puntuación CoMiSS total | −4,94 (3,70) | −7,33 (4,81) | −8,68 (5,52) | −9,20 (4,92) | <0,0001 |
| Llanto | −1,69 (1,66) | −2,20 (1,74) | −2,27 (1,89) | −2,47 (2,42) | 0,00016 |
| Regurgitación | −1,37 (1,54) | −1,68 (1,75) | −1,78 (1,70) | −2,22 (2,16) | 0,0157 |
| Deposiciones | −1,11 (1,91) | −1,26 (2,10) | −1,12 (2,18) | −1,00 (2,14) | 0,671 |
| Eccema atópico, cabeza | −0,27 (0,51) | −0,39 (0,59) | −0,65 (0,72) | −0,83 (0,92) | <0,0001 |
| Eccema atópico, brazos | −0,17 (0,48) | −0,31 (0,56) | −0,50 (0,66) | −0,78 (1,00) | <0,0001 |
| Urticaria | −0,57 (1,84) | −1,23 (2,50) | −2,22 (2,97) | −1,50 (4,30) | <0,0001 |
| Síntomas respiratorios | −0,10 (0,35) | −0,23 (0,49) | −0,48 (0,72) | −1,15 (1,09) | <0,001 |
Los cambios medios en las puntuaciones CoMiSS en la muestra total y en los subgrupos de lactantes clasificados según el mecanismo de la APLV y la gravedad de los síntomas se muestran en la figura 2.
Tiempo transcurrido hasta observar mejoría en los síntomasEl tiempo medio hasta observar mejoría en los síntomas fue de 7,1días (DE: 5,7). La mejora percibida se categorizó como «muy grande» en 533 casos (46,5%), «grande» en 497 (43,4%), «moderada» en 106 (9,3%) y «pequeña» en 9 (0,8%).
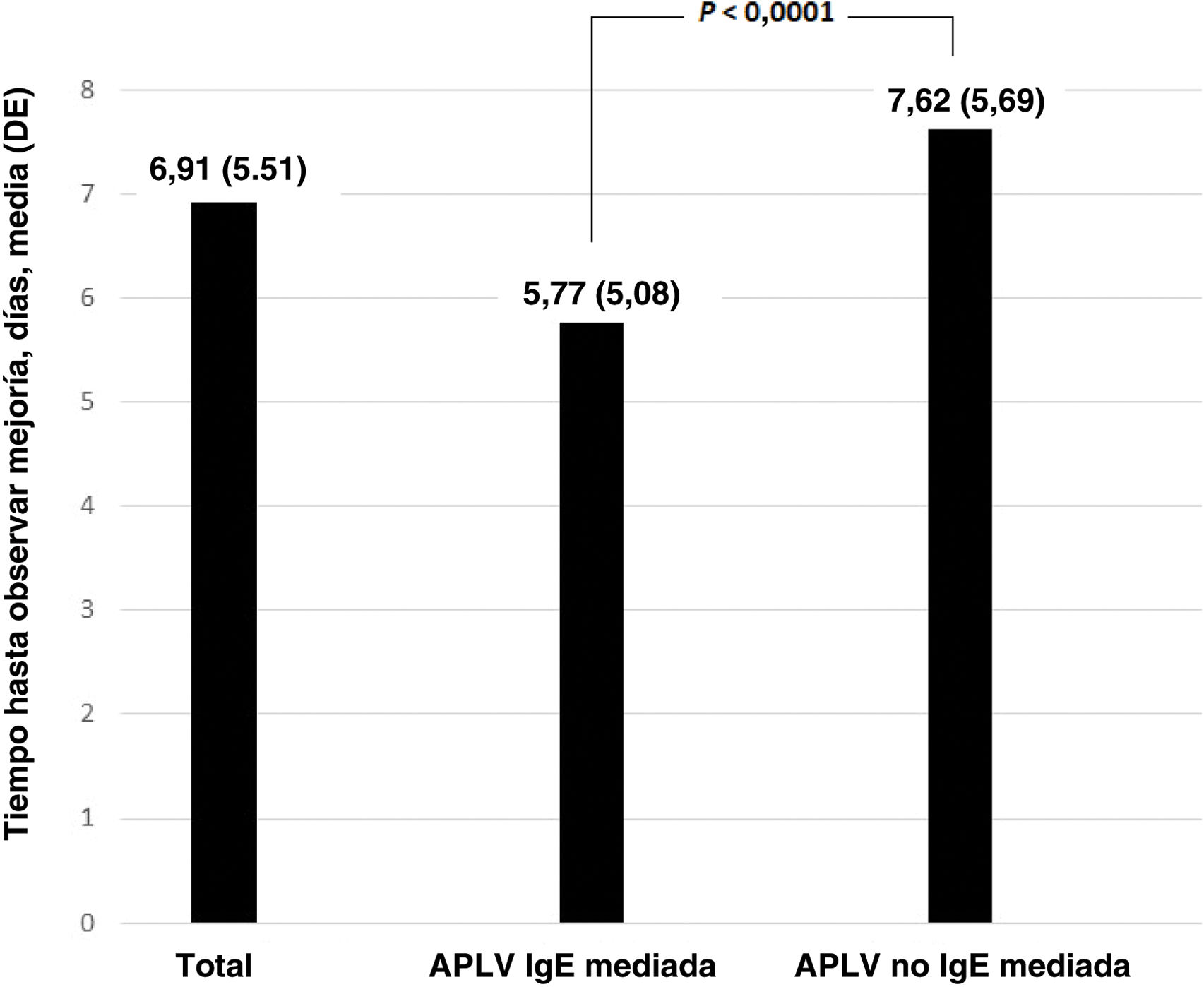
La mediana del tiempo transcurrido hasta observar mejoría no se asoció a tener una puntuación CoMiSS negativa (<12) o positiva (≥12) en el día0 (mediana [RIC]: 6 [3-8] días vs. 5 [3-7] días; p=0,301) ni a la gravedad de la clínica de APLV (mediana [RIC]: leve, 7 [4-9] días; moderada, 6 [3-7] días; grave, 5 [3-10] días; muy grave, 7 [1,5-14] días; p=0,345), aunque el tiempo hasta la mejoría fue mayor en el grupo con síntomas muy graves. En cambio, el tiempo hasta observar mejoría sí fue significativamente más largo en el grupo de APLV noIgE mediada que en el de APLV IgE mediada (fig. 3).
DiscusiónUno de los principales hallazgos del estudio fue el pequeño porcentaje de la muestra con una puntuación CoMiSS positiva (≥12), del 33,1%, a pesar de que la APLV se había diagnosticado previamente en todos los pacientes. Esto sugiere un posible uso inadecuado de la herramienta en casos no mediados por IgE. No obstante, algunos investigadores han advertido que las guías internacionales22 desarrolladas para apoyar a los médicos en el diagnóstico de APLV noIgE mediada en lactantes pueden estar contribuyendo al sobrediagnóstico de esta afección22. En un análisis secundario del ensayo clínico aleatorizado Enquiring About Tolerance (EAT), realizado en 1.303 lactantes, la prevalencia de los síntomas establecidos en la guía international Milk Allergy in Primary Care (iMAP) para el manejo de la alergia a la leche en atención primaria23 fue del 38% para síntomas leves-moderados a los 3meses y del 74% desde los 3 a los 12meses24. Una de las principales preocupaciones con respecto al sobrediagnóstico de la APLV noIgE mediada es su contribución a una restricción excesiva de alimentos durante el primer año de vida, un periodo clave en el crecimiento y el desarrollo inmunológico. A pesar de ello, las guías pueden ser útiles para los médicos si se siguen rigurosamente y si de hecho se realizan las pruebas de provocación. En nuestro estudio solo se realizaron pruebas de provocación en el 56% de los casos de APLV noIgE mediada, por lo que es probable que algunos de los pacientes incluidos no fueran realmente alérgicos a la leche de vaca25.
Se ha debatido cuál es el punto de corte de la CoMiSS más adecuado para reconocer la presencia de síntomas de alergia a la leche de vaca en lactantes. El grupo de expertos que desarrolló el instrumento original ha propuesto reducir el punto de corte basal de 12 a 10puntos, además de la inclusión del angioedema y la sustitución de la escala de Bristol por la de Bruselas (Brussels Infants and Toddlers Stool Scale [BITSS]) para evaluar la consistencia de las heces26. Son necesarios estudios adicionales para determinar si al cambiar el punto de corte y realizar otras pequeñas modificaciones mejoran la sensibilidad y la especificidad de la puntuación CoMiSS. En cualquier caso, otros autores continúan recomendando el punto de corte de 12puntos como el más adecuado para identificar a los lactantes que podrían beneficiarse de una dieta exenta de leche de vaca27. Hay consenso de que la APLV es poco probable con una puntuación CoMiSS de 6 o inferior8,26,27. En el presente estudio se aplicó el punto de corte convencional (CoMiSS ≤12puntos) para considerar los resultados positivos.
La evolución en la puntuación CoMiSS difirió entre los grupos de APLV IgE mediada y APLV noIgE mediada, con valores más altos en el momento del diagnóstico además de una reducción mayor a los 7días del inicio de la FEH en el primer grupo. En el análisis de los síntomas individuales de la CoMiSS, el llanto y la regurgitación mostraron reducciones significativamente mayores en el grupo de APLV noIgE mediada, mientras que el eccema atópico, la urticaria y los síntomas respiratorios mostraron reducciones mayores en el grupo de APLV IgE mediada. Estos hallazgos son consistentes con el hecho de que los síntomas cutáneos y respiratorios son manifestaciones observadas con frecuencia en los lactantes con APLV IgE mediada en comparación con el amplio espectro de síntomas gastrointestinales poco específicos que podrían sugerir una APLV noIgE mediada. En la práctica clínica, a menudo es difícil distinguir entre la APLV mediada por IgE y la nomediada por IgE en base a los síntomas y la exploración física. Sin embargo, las diferencias en los resultados de la CoMiSS entre los grupos de APLV IgE mediada y de APLV noIgE mediada encontradas en nuestro estudio deben interpretarse teniendo en cuenta que los diagnósticos fueron reportados por los propios pediatras y que no se investigaron las pruebas o procedimientos utilizados para establecer la clasificación de la APLV.
Otro de los hallazgos fue el tiempo significativamente más largo hasta la mejoría de los síntomas tras iniciar la dieta de eliminación con FEH en lactantes diagnosticados de APLV noIgE mediada en comparación con los diagnosticados de APLV IgE mediada. Según el algoritmo del documento de consenso sobre la APLV no mediada por IgE de la Asociación Española de Pediatría, se puede esperar mejoría con la dieta de eliminación tras un periodo de tiempo variable en función de la presentación clínica, de entre 1 y 5días en las formas agudas, de 1 a 2semanas en los casos de eccema o hemorragia gastrointestinal, y de 2 a 4semanas en los casos de estreñimiento, diarrea y retraso del crecimiento28.
En el análisis de la distribución de las puntuaciones CoMiSS según el nivel de gravedad de la clínica (clasificada como leve, moderada, grave y muy grave), se observaron diferencias estadísticamente significativas, con reducciones mayores de las puntuaciones para los distintos síntomas, en particular el llanto, la regurgitación, la urticaria y las molestias respiratorias en las categorías graves. Otros estudios han encontrado un descenso en los valores de la CoMiSS en lactantes con sospecha de APLV tras el inicio de una intervención nutricional12, así como reducciones más pronunciadas en lactantes con una prueba de provocación positiva que en aquellos con una prueba negativa10, pero la asociación entre la gravedad de los síntomas y la magnitud de la reducción en la puntuación CoMiSS tras la introducción de la FEH no se había evaluado previamente.
Los presentes resultados deben interpretarse teniendo en cuenta algunas limitaciones del estudio. El sesgo de selección puede haber afectado a la representatividad de la muestra y a la validez externa de los resultados. La muestra no fue aleatoria ni se estratificó proporcionalmente al número de especialistas en pediatría registrados en las 17comunidades autónomas del país. No obstante, los 294 participantes proporcionaron información valiosa sobre un grupo extenso de lactantes menores de 2años diagnosticados de APLV a los que se aplicó la herramienta CoMiSS antes de la introducción de una FEH y 7días después. En este sentido, la muestra bajo estudio, de 1.176 lactantes, es la más grande registrada hasta la fecha. La clasificación de la APLV fue reportada por los pediatras participantes, pero el cuestionario no incluía preguntas específicas sobre el enfoque utilizado para establecer el diagnóstico de APLV IgE mediada frente al de APLV noIgE mediada. Por otra parte, como no se realizaron pruebas de provocación para el diagnóstico de la APLV en todos los casos, es posible que se haya sobreestimado la incidencia de la APLV, lo que podría explicar el porcentaje limitado de niños con puntuaciones CoMiSS positivas. Además, el intervalo de 7días entre las dos valoraciones con la CoMiSS fue corto, y no se sabe si los resultados podrían haberse visto afectados si se hubiera prolongado más.
ConclusiónLa encuesta realizada revela que solo un tercio de los lactantes con sospecha de APLV en base a la clínica tuvieron una puntuación CoMiSS positiva (≥12puntos). En los casos de APLV IgE mediada, las medias de las puntuaciones CoMiSS fueron significativamente más altas en el momento del diagnóstico en comparación con los casos noIgE mediados, y también mostraron reducciones mayores una semana después de introducir una FEH. El diagnóstico de APLV debe reconsiderarse detenidamente en pacientes con puntuaciones CoMiSS negativas, especialmente en aquellos con sospecha de alergia no mediada por IgE, siguiendo las recomendaciones publicadas por la ESPGHAN. Un mayor conocimiento y experiencia con la CoMiSS como herramienta de referencia podría mejorar su fiabilidad y su utilidad en la práctica clínica para la valoración de la APLV.
FinanciaciónProyecto financiado por Laboratorios Ordesa S.L.
Conflicto de interesesA.S.-O. es empleada de Laboratorios Ordesa S.L., que contribuyó a la financiación del estudio. En cualquier caso, Laboratorios Ordesa S.L. no participó en absoluto en el análisis o interpretación de los datos. Los autores restantes no declaran ningún conflicto de intereses.
Los autores expresan su agradecimiento a todos los pediatras que participaron en el estudio, a K Access Health Projects por su apoyo en el análisis estadístico de los datos y a la doctora Marta Pulido por la revisión del manuscrito y asistencia editorial.
Presentación previa en la 56 Reunión Anual de la ESPGHAN, Milán, 15-18 de mayo de 2024, y en el 70 Congreso de la AEP, Córdoba, 6-8 de junio de 2024.