La etiología del trastorno por déficit de atención-hiperactividad (TDAH) es multifactorial: factores genéticos, ambientales y biológicos (neurotransmisores: sistema dopaminérgico). El hierro es fundamental para un correcto funcionamiento del sistema dopaminérgico. La ferropenia es frecuente en niños con TDAH y su corrección podría ser útil como tratamiento de estos pacientes.
ObjetivosAnalizar la posible relación entre ferropenia y síntomas de inatención, hiperactividad e impulsividad presentes en pacientes con TDAH, así como el posible beneficio del tratamiento con hierro.
Pacientes y métodosEstudio prospectivo en niños diagnosticados de TDAH según criterios DSM-IV, cognitivamente normales, no anémicos. Se usaron escalas específicas (SNAP-IV, EDAH) y se determinó la ferritina sérica. Aquellos con ferritina ≤ 30ng/ml recibieron tratamiento con sulfato ferroso (4mg/kg/día) durante 3 meses, analizándose posteriormente su eficacia.
ResultadosSe analizó a 60 pacientes, edad media: 9,02 años (rango: 6-14). El subtipo inatento fue el más frecuente (53,3%); el 63,3% presentó ferropenia, siendo más frecuente entre los inatentos (38 vs. 22; p<0,02). Diecisiete pacientes completaron el tratamiento con hierro. De los 8 del subtipo no inatento, en 7 el tratamiento no fue efectivo y en uno la respuesta fue parcial. De los 9 del subtipo inatento, el tratamiento fue eficaz en el control total de los síntomas en 5, parcialmente eficaz en 3 e ineficaz en un paciente. La probabilidad de obtener respuesta completa tras tratamiento con hierro fue mayor en pacientes con TDAH inatento (p=0,02).
ConclusionesEl tratamiento con suplementos férricos puede ser una alternativa eficaz en el tratamiento de pacientes con TDAH y ferropenia, especialmente en aquellos con subtipo inatento.
The aetiology of attention deficit hyperactivity disorder (ADHD) is attributed to different factors: genetic, environmental, and biological (neurotransmitters: dopaminergic system). Iron is essential for the correct functioning of the dopaminergic system. Iron deficiency is common in patients with ADHD, and its correction may be useful in the treatment.
ObjectivesTo analyse a possible relationship between iron deficiency and symptoms of inattention, hyperactivity and impulsivity in ADHD patients, and the potential benefit of iron therapy.
Patients and methodsA prospective study was conducted on non-anaemic and cognitively normal children, newly diagnosed with ADHD, according to DSM-IV criteria. Specific scales were used (SNAP-IV, ADHS) and serum ferritin was determined. Those with ferritin ≤ 30ng/ml were treated with ferrous sulphate (4mg/kg/day) for 3 months, with its effect quantified being subsequently quantified.
ResultsA total of 60 patients, with a mean age of 9.02 years (range: 6-14), were analysed. The inattentive subtype was the most frequent one (53.3%). Almost two-thirds (63.3%) had iron deficiency, which was more frequent among the inattentive group (38 vs 22, P<.02). The iron treatment was completed by 17 patients. The treatment was not effective in 7 of the 8 non-inattentive subtypes, with a partial response in the remaining one. Of the 9 inattentive subtypes: the treatment was successful in the total control of symptoms in 5 of them, partially effective in other 3, and ineffective in one patient. The probability of complete response after treatment with iron was higher in inattentive patients with ADHD (P=.02).
ConclusionsTreatment with iron supplements can be an effective alternative to treat patients with ADHD and iron deficiency, especially the inattentive subtype.
El hierro es necesario para un adecuado desarrollo del sistema nervioso central (SNC), desempeñando un papel importante en la sinaptogénesis, dendritogénesis, mielinización, metabolismo energético cerebral y en los sistemas de neurotransmisión (sistemas dopaminérgico, serotoninérgico y GABAérgico)1. Desde hace 4 décadas son muchos los estudios que han comprobado, ya sea mediante tests neuropsicológicos o pruebas neurofisiológicas, que la ferropenia en niños (incluso sin anemia) se ha relacionado con alteraciones del desarrollo psicomotor, problemas conductuales-emocionales y diversos trastornos del aprendizaje que incluyen el retraso del lenguaje, la dislexia, la discalculia, los problemas de memoria visuoespacial y la inatención2-4. Parece que los 2 primeros años de vida son un «periodo crítico» en el que unos adecuados niveles de hierro a nivel del SNC son necesarios para un correcto desarrollo psicomotor5. En escolares, el tratamiento con hierro de niños ferropénicos (con y sin anemia) parece corregir en muchas ocasiones el trastorno neurocognitivo secundario6,7.
El hierro ejerce un papel fundamental en el adecuado funcionamiento del sistema dopaminérgico, en particular al ser coenzima de la tirosina hidroxilasa (encargada de la síntesis de dopamina) y de la monoaminoxidasa (encargada de la degradación de dopamina). El hierro se localiza a nivel cerebral junto a las neuronas dopaminérgicas y parece que su déficit (ferropenia) disminuye la densidad de receptores D2 y D4, al igual que altera su funcionamiento8. A nivel comportamental, la alteración del metabolismo de la dopamina se traduce en trastornos en la memoria, aprendizaje, atención, inhibición y funciones ejecutivas, por lo que no es de extrañar que la dopamina se considere clave en la fisiopatología del trastorno por déficit de atención e hiperactividad (TDAH)9.
El TDAH es la enfermedad neuropsiquiátrica más frecuente en la infancia y adolescencia, afectando al 4,5% de los escolares españoles10. Se caracteriza por la combinación variable de síntomas de inatención, inquietud motriz e impulsividad, en una intensidad que provoca alteraciones funcionales en varios ámbitos de la vida del paciente. Se pueden diferenciar 3 subgrupos: el TDAH de predominio inatencional, el TDAH hiperactivo y el TDAH mixto. La etiología del TDAH es multifactorial, siendo probablemente el resultado de la combinación de factores genéticos (tasa de heredabilidad: 0,76), factores ambientales y factores biológicos (neurotransmisores). Las evidencias que apuntan a una posible disfunción dopaminérgica son varias: la mayoría de los genes implicados están relacionados con el metabolismo de la dopamina (gen del receptor D2, gen del receptor D4 DRD4, gen del transportador de dopamina DAT1…), es la diana terapéutica de los principales tratamientos farmacológicos (metilfenidato y dexanfetamina) y los recientes estudios de neuroimagen funcional muestran una disfunción dopaminérgica a nivel de los circuitos frontoestriatales.
En los últimos años, varios estudios demuestran que existe una relación hierro-dopamina-TDAH, proporcionando evidencias cada vez más consistentes que relacionan el TDAH con el metabolismo del hierro11. En cambio, la eficacia de la corrección de la ferropenia mediante suplementos férricos en los pacientes con TDAH ha sido escasamente estudiada, por lo que el objetivo de nuestro trabajo ha sido analizar el impacto de la ferropenia en los síntomas de pacientes con TDAH y el posible beneficio de la corrección mediante suplementos férricos de los depósitos de hierro en el control de la sintomatología de este trastorno.
Pacientes y métodosEl estudio fue prospectivo e incluyó a todos los pacientes de 6-17 años de edad diagnosticados de TDAH en el Servicio de Neurología Infantil del Hospital Niño Jesús de Madrid. Todos los pacientes fueron diagnosticados por un neurólogo infantil de acuerdo con los criterios de «Diagnostic and Statistical Manual of Mental Disorders-Fourth Edition» (DSM-IV). Los síntomas se cuantificaron mediante test específicos de TDAH: a los padres se les aplicó la escala de Swanson, Nolan y Pelham (SNAP-IV) y a los profesores se les aplicó la Escala de Evaluación del Trastorno por Déficit de Atención e Hiperactividad (EDAH)12 En la anamnesis se preguntó por la presencia de comorbilidad neurológica (alteraciones del desarrollo psicomotor, trastornos de aprendizaje, tics y epilepsia), comorbilidad psiquiátrica y específicamente por la presencia de los criterios diagnósticos del síndrome de piernas inquietas (SPI)13. Se excluyó a todos aquellos pacientes con alteración cognitiva (cociente intelectual < 85), anemia, enfermedades orgánicas que justificaran la clínica del TDAH y aquellos que hubieran recibido tratamiento en los últimos 6 meses con suplementos férricos, metilfenidato o atomoxetina.
La ferropenia se determinó mediante la cuantificación de ferritina sérica, que es un compuesto que se relaciona con las reservas totales de hierro del organismo, siendo el marcador más precoz de ferropenia14. Valores por debajo de 10-12ng/ml reflejan que los depósitos en la médula ósea son insuficientes, por lo que se desarrollará anemia; pero la sintomatología neurológica por disminución de hierro a nivel del SNC puede aparecer antes de la presencia de anemia.
En todos los pacientes, se realizó una analítica de sangre en la que se determinó hemograma, ferritina, hormonas tiroideas (TSH y T4 libre), así como un electroencefalograma (EEG) de vigilia según el sistema internacional (10-20).
Aquellos pacientes con ferropenia se les ofreció tratamiento con sulfato ferroso (4mg/kg/día, máximo 80mg/día) durante 3 meses; con control analítico (hemograma y ferritina) y clínico posterior (incluyendo escalas SNAP-IV y EDAH).
El análisis estadístico se realizó mediante el software SPSS vs.12.0 para la comparativa entre los síntomas de aquellos pacientes con y sin ferropenia, y para comparar la eficacia del tratamiento con suplementos férricos entre el grupo del TDAH inatento y el TDAH no inatento, usando la prueba de la chi al cuadrado de Pearson.
ResultadosEl número de pacientes incluidos en el estudio fue 60: 12 niñas y 48 niños, con una media de edad de 9,02 años (rango 6-14). El subtipo inatento fue el más frecuente (53,3%). La mayoría de los pacientes (63,33%) presentaron ferropenia. La hemoglobina, el hematocrito y el volumen corpuscular medio fueron normales para su edad en todos los pacientes del estudio. Las características clínicas de los grupos con y sin ferropenia se describen en la tabla 1.
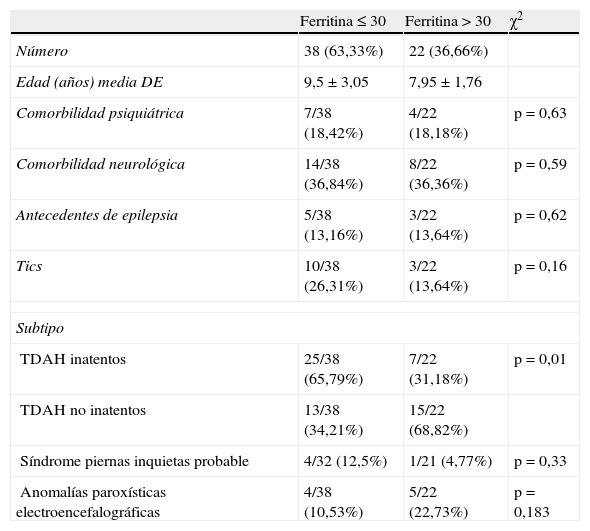
Características clínicas de los pacientes (según niveles de ferritina)
| Ferritina ≤ 30 | Ferritina>30 | χ2 | |
| Número | 38 (63,33%) | 22 (36,66%) | |
| Edad (años) media DE | 9,5 ± 3,05 | 7,95 ± 1,76 | |
| Comorbilidad psiquiátrica | 7/38 (18,42%) | 4/22 (18,18%) | p=0,63 |
| Comorbilidad neurológica | 14/38 (36,84%) | 8/22 (36,36%) | p=0,59 |
| Antecedentes de epilepsia | 5/38 (13,16%) | 3/22 (13,64%) | p=0,62 |
| Tics | 10/38 (26,31%) | 3/22 (13,64%) | p=0,16 |
| Subtipo | |||
| TDAH inatentos | 25/38 (65,79%) | 7/22 (31,18%) | p=0,01 |
| TDAH no inatentos | 13/38 (34,21%) | 15/22 (68,82%) | |
| Síndrome piernas inquietas probable | 4/32 (12,5%) | 1/21 (4,77%) | p=0,33 |
| Anomalías paroxísticas electroencefalográficas | 4/38 (10,53%) | 5/22 (22,73%) | p=0,183 |
Al comparar los pacientes con y sin ferropenia, el subtipo inatento fue el más frecuente entre aquellos con valores de ferritina sérica < 30ng/ml (67,79% vs. 31,18%; p=0,01). No encontramos diferencias estadísticamente significativas en el resto de variables clínicas. Encontramos más pacientes con criterios clínicos compatibles con SPI probable en el grupo de pacientes con ferropenia (12,5% vs. 4,77%), aunque sin llegar a alcanzar una significación estadística.
Ocho de los pacientes habían presentado un cuadro de epilepsia previo que estaba controlado en el momento del diagnóstico (13,33%). Solo uno de ellos estaba recibiendo tratamiento antiepiléptico durante el estudio (levetiracetam). En el EEG se objetivaron anomalías epileptiformes subclínicas en 9 pacientes (15%), de los cuales la mayoría no habían presentado previamente crisis epilépticas (7/9).
De los 38 pacientes a los que se les ofreció tratamiento con suplementos férricos, solo aceptaron iniciarlo 17 (44,74%). A los 3 meses se realizó un control clínico en el que se volvieron a cuantificar los síntomas mediante escalas específicas (SNAP-IV y EDAH), y se comparó con su situación basal. La respuesta al tratamiento se clasificó como: «no respuesta» en aquellos pacientes en que el tratamiento con suplementos férricos no había mejorado la sintomatología, por lo que se inició tratamiento específico con estimulantes (metilfenidato); «respuesta parcial» en aquellos en que se había producido una mejoría parcial de los síntomas pero que requirieron iniciar tratamiento específico con estimulantes (metilfenidato), y «respuesta completa» en aquellos pacientes en que el control de los síntomas había sido completo (cuantificado por escalas específicas de TDAH) y no necesitaron tratamiento con estimulantes.
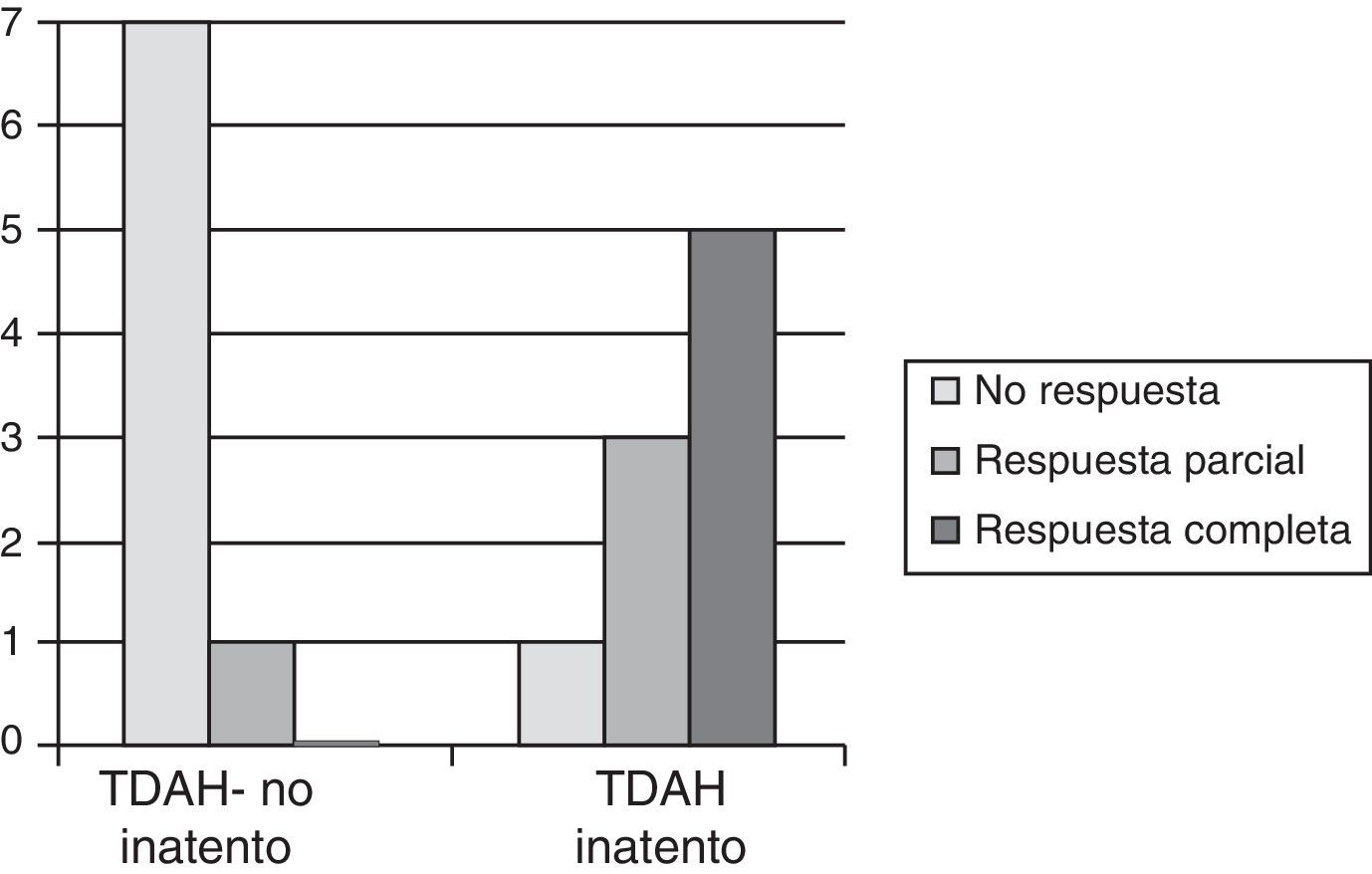
De manera global, en estos 17 pacientes, los efectos del tratamiento fueron: respuesta completa en 5 (29,41%), «respuesta parcial» en 4 (23,53%) y «no respuesta» en 8 (47,06%). Al comparar la eficacia del tratamiento entre el subtipo inatento y el subtipo no inatento (hiperactivo y mixto), los suplementos férricos fueron más efectivos en el grupo de TDAH inatento (fig. 1). Así, de los 8 pacientes del subtipo no inatento, el tratamiento no fue efectivo en 7 («no respuesta») y en uno la respuesta fue parcial. De los 9 del subtipo inatento, la respuesta al tratamiento fue completa en 5 (55%), la respuesta fue parcial en 3 y en uno el tratamiento no fue eficaz en uno («no respuesta»). La probabilidad de obtener una respuesta completa de los síntomas tras el tratamiento con suplementos férricos fue mayor en los pacientes con TDAH inatento (5 pacientes) que en los TDAH no inatento (ningún paciente) (χ2 p=0,02).
De los 2 pacientes con probable SPI que recibieron tratamiento con hierro, en ninguno desapareció la sintomatología, aunque los valores de ferritina sérica tras los suplementos de hierro por vía oral seguían siendo menores de 30ng/ml. Ninguno de los pacientes que recibieron tratamiento con hierro refirieron efectos secundarios de consideración.
ConclusionesLa ferropenia parece alterar el funcionamiento del sistema dopaminérgico en el SNC y contribuye en la aparición de síntomas de inatención, hiperactividad e impulsividad característicos de los pacientes con TDAH. En la literatura médica son varios los estudios que relacionan el hierro en la fisiopatología del TDAH:
- –
Cortese en 2011 realizó estimaciones del hierro cerebral mediante resonancia magnética craneal en 18 niños con TDAH y 18 controles, objetivando concentraciones inferiores de hierro a nivel talámico en los pacientes con TDAH15.
- –
Varios estudios de casos-control objetivan que la ferropenia (definida por niveles bajos de ferritina sérica) es más frecuente en los niños con TDAH que en controles sanos16-18.Aunque hay varios estudios que no han encontrado relación entre el TDAH y la ferritina19,20, un reciente metaanálisis realizado por Tan en 2011 de los 5 principales estudios concluyó que los niveles bajos de ferritina sérica se relacionan con mayor susceptibilidad de presentar TDAH en la infancia (p=0,003)11.
- –
La ferritina se ha relacionado inversamente con la severidad del TDAH en varios estudios, de manera que los niños con valores más bajos de ferritina sérica fueron los más inatentos, impulsivos e hiperactivos21-24.
- –
También se ha demostrado una correlación positiva entre ferritina y una sensibilidad al tratamiento con psicoestimulantes, de manera que sería necesaria una mayor cantidad de medicación estimulante en niños con TDAH y ferropenia para controlar los síntomas22.
- –
Hasta el 65-80% de los niños con TDAH presentan algún tipo de trastorno comórbido, especialmente psiquiátrico. En 2 estudios la ferropenia se relacionó significativamente con mayor probabilidad de presentar comorbilidades psiquiátricas: grado de oposicionismo17 y trastornos de comportamiento23.
En nuestro estudio, el 63,3% de los pacientes con TDAH presentaron niveles de ferritina sérica inferiores a 30ng/ml, un porcentaje algo menor que el descrito en estudios previos21 pero que refleja la alta incidencia de ferropenia en este grupo de pacientes.
Aunque estos hallazgos indican que el tratamiento con hierro podría suponer una mejora en los síntomas de TDAH, son muy pocos estudios los que han evaluado el tratamiento con hierro en estos pacientes. Aparte de comunicaciones de casos aislados en los que refieren mejoría de los síntomas tras el tratamiento con hierro por vía oral25, solo hay 2 trabajos que hayan estudiado la eficacia del tratamiento con suplementos férricos en los pacientes con TDAH. El primero en proponer tratamiento con hierro fue Sever, en 1997, en 14 niños de 7-11 años diagnosticados de TDAH a los que les administró citrato ferroso durante 30 días (5mg/kg/día), independientemente de los valores de ferritina. Se cuantificó la sintomatología antes y después del tratamiento mediante la escala Conners Rating Scale para padres y profesores. Encontraron que el aumento de la ferritina sérica se relacionó con una disminución de la sintomatología de TDAH según los padres, no encontrando esta relación en las valoraciones de los profesores26. El segundo trabajo es un estudio caso-control publicado en 2008 por Konofal en 23 pacientes no anémicos de 5-8 años de edad con ferritina sérica < 30ng/ml27. Comparó un grupo de 18 pacientes a los que se les administró sulfato ferroso (80mg/día) durante 12 semanas con un grupo de 5 pacientes a los que se les administró placebo. Objetivó un descenso significativo en las puntuaciones obtenidas en la escala Attention Deficit Hyperactivity Disorder Rating Scale (ADHD-RS) de padres (p<0,008) y en la impresión clínica global (p<0,01), sin encontrar diferencias en las puntuaciones de la escala Conners Rating Scale para padres y profesores. El tratamiento fue especialmente efectivo en disminuir los valores de inatención de la ADHD-RS.
La definición de «ferropenia» basándonos en los valores de ferritina sérica es muy variable según los diferentes estudios, variando entre 12-45ng/ml28. Nosotros nos hemos basado el estudio realizado por Konofal et al., en que consideran que tienen ferropenia aquellos valores de ferritina sérica ≤ 30ng/ml27. En otras afecciones, como el SPI, hay estudios que recomiendan iniciar tratamiento con suplementos férricos en caso de valores de ferritina ≤ 50ng/ml29,30. Aunque la cifra de ferritina sérica de 30ng/ml puede parecer muy elevada y en muchos casos se considera normal, lo que determina la necesidad de un tratamiento con suplementos férricos es la cantidad de hierro en el líquido cefalorraquídeo (LCR), que se encuentra en forma de ferritina. De hecho, se he demostrado que los valores de ferritina sérica pueden ser normales en sujetos con escasa ferritina en el LCR31.
En nuestra serie, el tratamiento durante 3 meses con suplementos férricos consiguió un control completo de los síntomas en 5 de los 17 pacientes tratados (29,41%). Al analizar por subtipos, el tratamiento fue efectivo (desaparición de la sintomatología sin necesidad de tratamiento con estimulantes) en el 55% de los inatentos y en ninguno de los otros subgrupos; se obtuvo una respuesta parcial en el 33,3% de los inatentos y en el 12,5% de los no inatentos, y no produjo ningún cambio en la sintomatología en el 11,1% de los inatentos y en el 87,5% del grupo de los no inatentos. Por tanto, la probabilidad de obtener una respuesta completa tras los suplementos férricos fue mayor en los pacientes con TDAH inatentos (p=0,02).
En nuestra muestra, la ferropenia fue más frecuente en los pacientes con TDAH subtipo inatento (65,79% vs. 31,18%; p=0,01). Aunque la relación hierro y TDAH se ha estudiado en varios estudios, hay muy pocas referencias en cuanto a los subtipos de TDAH. Hay 2 trabajos que, al contrario que el nuestro, encuentran una relación entre el grado de ferropenia y el grado de hiperactividad-impulsividad, aunque sin alcanzar significación estadística21,23. En cambio, numerosos estudios afirman que la ferropenia en niños sanos se asocia a problemas de atención, lo que sería compatible con los hallazgos de nuestro trabajo3,5,7.
En los últimos años hay cada vez mayor evidencia de una relación bidireccional entre epilepsia y TDAH. Así, el 30-40% de los pacientes epilépticos presentan sintomatología característica de TDAH, siendo este el principal trastorno neuropsiquiátrico en niños escolares epilépticos32. Asimismo, en pacientes con TDAH es más frecuente que presenten anomalías epilépticas electroencefalográficas en vigilia que en la población general: 6-7,5%33,34, alcanzando en sueño incluso el 51%35. Probablemente compartan una misma base fisiopatológica, aunque los motivos de esta relación continúan sin conocerse por completo36. En nuestra serie, el 13,3% refería historia previa de epilepsia y el 15% presentaba anomalías epileptiformes en el EEG. Estos porcentajes, algo mayores que los descritos en otras series, pueden deberse a la naturaleza de nuestro centro, un hospital de tercer nivel con una unidad específica para el tratamiento de epilepsia infantil, lo que hace que muchos de los pacientes seguidos tengan historia previa de epilepsia.
El otro trastorno en el que también existe una relación bidireccional con el TDAH es el SPI, de forma que un 25% de los niños con SPI tienen criterios diagnósticos de TDAH y un 12-35% de los niños con TDAH presentan síntomas de SPI14. El SPI se caracteriza por una necesidad urgente de mover las piernas habitualmente acompañada de una sensación desagradable, síntomas que mejoran con el movimiento y empeoran en reposo y al final del día. Ambos trastornos comparten un similar mecanismo fisiopatológico basado en la ferropenia y en el trastorno del sistema dopaminérgico37. En los niños con TDAH, la ferropenia es un factor de riesgo para desarrollar SPI38 y un estudio demostró que en aquellos pacientes con TDAH que asociaban SPI los valores de ferritina eran menores15. Aunque parece demostrado que el aporte de suplementos orales de hierro mejora los síntomas de SPI en los pacientes con ferropenia, no lo hemos objetivado en nuestra serie (ninguno de los 2 pacientes tratados mejoraron la sintomatología de SPI). Podría deberse a que, a pesar de los suplementos de hierro, fueron los 2 únicos pacientes que no alcanzaron valores de ferritina mayores de 30ng/ml.
El TDAH es un cuadro clínico de una enorme heterogeneidad clínica resultante de la combinación de varios subtipos clínicos y una alta comorbilidad neurológica y psiquiátrica. Además, su fisiopatología es compleja y en ella intervienen numerosos factores ambientales, biológicos y genéticos. La consecuencia de esta complejidad es que «no hay 2 pacientes TDAH iguales». Por tanto, no podemos esperar que la ferropenia sea un hallazgo constante en los niños con TDAH, pero sí que sea un factor causal en algunos de los pacientes con TDAH.
Las limitaciones de nuestro estudio son fundamentalmente el escaso tamaño de la muestra, no haber podido obtener información de parte del profesorado y no haber comparado la eficacia del tratamiento con un grupo control al que se le administrara placebo.
Este es el primer estudio publicado en nuestro conocimiento en el que se estudia la relación de la ferropenia en función de los distintos subtipos de TDAH. Hemos encontrado una clara relación entre niveles bajos de ferritina y el subtipo inatento, de modo que los TDAH inatentos fueron los que más frecuentemente presentaron ferropenia y los que mejor respondieron al tratamiento con suplementos férricos. Aunque son necesarios más estudios doble ciego sobre la eficacia de los suplementos de hierro por vía oral en los pacientes con TDAH, consideramos que el tratamiento con suplementos férricos puede ser una alternativa eficaz en el tratamiento de pacientes con TDAH y ferropenia, especialmente en aquellos con subtipo inatento.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.