Monitorear la presión parcial de CO2 (PCO2) en los recién nacidos que requieren ventilación permitiría evitar hipocapnia e hipercapnia. La medición de CO2 espirada (ETCO2) es una alternativa poco implementada en esta población.
ObjetivoEvaluar la relación entre la ETCO2 y la PCO2 en recién nacidos.
MétodosEstudio de corte transversal, comparativo entre dos métodos de medición de PCO2, el convencional mediante análisis de muestras sanguíneas y el estimado mediante ETCO2. Se incluyeron recién nacidos internados que requerían ventilación mecánica convencional. La medición de ETCO2 se realizó mediante un ventilador neonatal Graph Net Neo-TECME®, con capnógrafo incorporado y se obtuvo el gradiente ETCO2-PCO2. Se realizaron análisis de correlación y gráficos de Bland-Altman para estimar la concordancia.
ResultadosSe analizaron 277 muestras (ETCO2/PCO2) en 83 recién nacidos. Los valores promedios de ETCO2 y PCO2 fueron de 41,36 mmHg y 42,04 mmHg. Hubo correlación positiva y significativa entre ETCO2 y PCO2 en el análisis global (r = 0,5402; p < 0,001) y en el de cada unidad (p < 0,001). La media de las diferencias fue de 0,68 mmHg (IC 95%- 0,68 a 1,95) y no resultó significativa. Se observó error sistemático positivo (PCO2 > ETCO2) en dos de las unidades, mientras que en la tercera la diferencia fue negativa (PCO2 < ETCO2)
DiscusiónLa correlación entre ETCO y PCO2 es significativa, si bien los valores obtenidos no resultan equivalentes y la diferencia varía entre 0,1 mmHg a 20 mmHg. Asimismo, observamos errores sistemáticos de signo diferente (positivo o negativo) entre las instituciones.
Monitoring the partial pressure of CO2 (PCO2) in newborns who require ventilation would allow avoiding hypocapnia and hypercapnia. The measurement of end-tidal carbon dioxide (ETCO2) is an alternative rarely implemented in this population.
ObjectiveTo evaluate the relationship between ETCO2 and PCO2 in newborns.
MethodsCross-sectional study comparing two PCO2 measurement methods, the conventional one by analysis of blood samples and the one estimated by ETCO2. The study included hospitalized newborns that required conventional mechanical ventilation. The ETCO2 was measured with a Tecme GraphNet® neo, a neonatal ventilator with an integrated capnography, and we obtained the ETCO2-PCO2 gradient. We conducted correlation and Bland-Altman plot analyses to estimate the agreement.
ResultsA total of 277 samples (ETCO2/PCO2) from 83 newborns were analyzed. The mean values of ETCO2 and PCO2 were 41.36 mmHg and 42.04 mmHg. There was a positive and significant correlation between ETCO2 and PCO2 in the overall analysis (r = 0.5402; p < .001) and in the analysis of each unit (p < .001). The mean difference was 0.68 mmHg (95% CI, −0.68 to 1.95) and was not significant. We observed a positive systematic error (PCO2 > ETCO2) in 2 of the units, and a negative difference in the third (PCO2 < ETCO2).
DiscussionThe correlation between ETCO and PCO2 was significant, although the obtained values were not equivalent, with differences ranging from 0.1 mmHg to 20 mmHg. Likewise, we found systematic errors that differed in sign (positive or negative) between institutions.
La monitorización de la presión arterial parcial de CO2 (PaCO2) en los recién nacidos (RN) enfermos, especialmente en aquellos que requieren ventilación, es importante para optimizar el manejo de los pacientes y evitar complicaciones, ya que tanto la hipocapnia como la hipercapnia están implicadas como factores causantes de leucomalacia periventricular1,2, hemorragia intracraneal3 y displasia broncopulmonar3,4. A su vez, las fluctuaciones en la PaCO2 se asocian a peores resultados en el neurodesarrollo5.
Si bien el análisis de los gases en sangre arterial es el «estándar de oro» para el monitoreo de la PaCO2, sabemos que su uso requiere de extracciones dolorosas, es costoso, puede conducir a anemia iatrogénica6 por extracciones repetidas con mayor necesidad de transfusiones y solo brinda una fotografía de un momento determinado.
Una alternativa es el monitoreo transcutáneo de PCO2 (TcCO2), pero este resulta dificultoso en niños pequeños debido a la inmadurez de su piel, necesidad de calibraciones repetidas, el riesgo de quemaduras e infecciones7,8, sumado a la falta de disponibilidad en la mayoría de las unidades de cuidados intensivos neonatales (UCIN) en nuestro medio.
La medición del CO2 al final de la espiración o «end tidal CO2» (ETCO2) es una alternativa de utilidad. Esta técnica ha sido ampliamente aplicada en el ámbito de la cirugía y la anestesia en pacientes adultos y pediátricos, utilizándose como guía para confirmar la correcta posición del tubo endotraqueal, así como en el control de la ventilación y situación cardiopulmonar del paciente9–11. Sin embargo, su uso en las UCIN o en salas de parto en los RN que requieren reanimación ha sido poco implementado, quizá debido a que en RN hay datos controvertidos sobre la correlación entre ETCO2 y PaCO2 y el impacto que puede tener la severidad de la enfermedad pulmonar sobre dicha relación12–16.
El gradiente entre el ETCO2 y PaCO2 puede verse afectado por el grado de severidad de la insuficiencia respiratoria, pero estos datos no están bien evaluados en neonatos ventilados17,18.
La capnografía volumétrica permite estimar el espacio muerto fisiológico en adultos. Según la ecuación de Bohr modificada es posible evaluar la relación entre el espacio muerto (VD) calculado y el volumen tidal (Vt)18, tanto inspiratorio como espiratorio. En adultos se considera que el índice normal de espacio muerto fisiológico y volumen tidal (VD/Vt) es de 0,20-0,35. En pacientes adultos con injuria pulmonar aguda, este índice aumenta a 0,44-0,55 y se asocia con elevada mortalidad19. Desafortunadamente estas posibilidades de información son aún limitadas en neonatos. Los problemas técnicos que generan el espacio muerto del sensor, los tiempos de respuesta y las pérdidas peritubo son limitaciones evidentes en los neonatos, especialmente en los prematuros de muy bajo peso20.
Si bien se ha explorado la correlación entre la gasometría arterial y los métodos no invasivos en RN, existe diversidad en los reportes y muchas variaciones en la literatura científica21. Aun así, los resultados parecen prometedores y pueden aportar datos valiosos para futuros estudios, que son necesarios para consolidar los métodos no invasivos como una alternativa confiable y viable a la gasometría en sangre arterial.
El objetivo primario de este estudio es evaluar y reportar la relación entre la ETCO2 y la PCO2 en neonatos con necesidad de ventilación mecánica en tres unidades de cuidado intensivo neonatal de Argentina.
Material y métodosSe realizó un estudio de corte transversal y comparativo entre dos métodos de medición de PCO2, el convencional mediante gasometría en muestras sanguíneas y el estimado mediante ETCO2.
Se incluyeron en el estudio RN internados en las UCIN de la Clínica Universitaria Reina Fabiola, Clínica y Maternidad CERHU y Hospital Provincial de Rosario, entre agosto del 2019 y julio del 2020, que requerían ventilación mecánica convencional y/o ventilación manual con tubo endotraqueal, sin limitaciones de peso al nacer, edad gestacional ni edad posnatal. Se excluyeron los RN en ventilación con alta frecuencia.
La selección de la muestra fue por conveniencia y relacionada con la disponibilidad de equipos para medir ETCO2 en cada unidad.
La medición de ETCO2 se realizó mediante un ventilador neonatal Graph Net Neo- TECME® (Córdoba, Argentina), con capnógrafo incorporado para medir CO2 espirada -Capnostat 5 (Respironics Inc., EE. UU.), de flujo lateral adaptado al sensor de flujo (sensor dual).
La medición de PCO2 se obtuvo de muestras de sangre arteriales (PaCO2), capilares (PcCO2), o venosas (PvCO2); dichas extracciones se realizaron de acuerdo con el criterio clínico del médico tratante. En este estudio observacional no se tomaron muestras de sangre originadas por la investigación, sino que solo se registraron las obtenidas durante la atención del paciente.
A los fines de estandarizar la obtención de las muestras sanguíneas, todos los responsables de esta actividad en cada unidad recibieron indicaciones específicas sobre el método de extracción de la muestra y su envío al laboratorio para procesamiento.
El análisis de gases en sangre se realizó de acuerdo con el equipo disponible en el laboratorio de cada centro: Cobas b 121 (Roche®), Cobas b 221 (Roche®) y Epoc Reader (Epocal®).
Al finalizar la extracción de la muestra de sangre indicada en cada caso, se registró el valor del ETCO2, y dicho valor se comparó con el obtenido en el laboratorio (PCO2 arterial, venosa o capilar), obteniendo el gradiente ETCO2-PCO2.
Si bien la unidad de estudio fueron las mediciones comparativas, en cada caso se consignaron las variables relacionadas con el RN, su condición y tipo de muestra sanguínea. Se recolectaron peso al nacer, edad gestacional (EG), edad posnatal, enfermedad que condicionaba la ventilación mecánica, fracción inspirada de oxígeno (FiO2) y sitio de extracción de la muestra.
La lectura de CO2 del monitor de ETCO2 no fue utilizada para tomar decisiones clínicas.
Para el análisis de los datos se usaron estadísticos descriptivos (medidas de tendencia central y dispersión; rango, media, mediana, modo, desviación estándar [DE], proporciones o porcentajes e intervalo de confianza [IC]). Las comparaciones se realizaron mediante ANOVA, test de Student y χ2 con corrección de Fisher y Yates, según correspondiera; se evaluó para cada caso la normalidad en la distribución de los datos mediante gráficos y estadísticamente (Kolmogorov-Smirnov). Se realizaron análisis de correlación de Pearson para la muestra global y para las obtenidas de cada una de las tres unidades participantes. Adicionalmente, se realizaron gráficos de Bland-Altman para estimar la concordancia entre los métodos de medición y se calcularon los sesgos de la medición. El análisis estadístico se realizó con el programa InfoStat (Universidad Nacional de Córdoba, Argentina) y en todos los casos el nivel de significación fue del 5%.
El estudio fue aprobado por los Comités de Ética de Investigación en cada una de las instituciones participantes, y dado que el mismo no modificó el cuidado clínico de los RN, y la ETCO2 es un método estándar no invasivo de los cuidados de terapia intensiva, los respectivos Comités Institucionales de Ética de la Investigación dictaminaron la eximición de administrar y obtener consentimiento informado para el estudio.
Todos los procedimientos se realizaron según la Guía de las buenas prácticas de investigación clínica en seres humanos, la Declaración de Helsinki, y las correspondientes leyes provinciales. Se mantuvo la confidencialidad de los datos de acuerdo con la Ley 25326/2000 de Protección de los Datos Personales.
ResultadosSe analizaron 277 muestras (ETCO2/PCO2) comparativas en 83 RN.
El peso promedio de los RN evaluados fue de 2.017 g con una DE ± 853 g (valores extremos entre 660 a 4.220 g); la EG media fue 32 ± 4 semanas. El 52,4% de los pacientes eran masculinos y el 47,6% de sexo femenino.
En la tabla 1 se presenta distribución del número de pacientes y muestras por cada centro (identificados como A, B y C).
Las características comparativas en relación con EG, peso al nacer, FiO2 > 30% y sitio de extracción de las muestras entre las tres instituciones se presentan en la tabla 2, observándose que en el centro B, los RN participantes tuvieron mayor EG y peso al nacer, mientras que en la unidad del centro C se obtuvieron mayor cantidad de muestras arteriales. No hubo diferencias en relación con la necesidad de O2 al evaluar las mediciones entre centros.
El diagnóstico de síndrome de dificultad respiratoria (SDR) fue el más frecuente durante las mediciones, con un 60% de los casos (166 observaciones).
Los valores promedios de ETCO2 y PCO2 fueron de 41,36 mmHg y 42,04 mmHg, respectivamente (tabla 3).
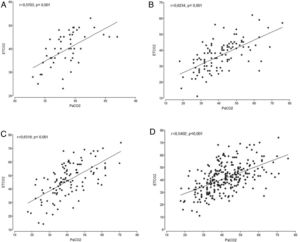
Se observó una correlación positiva y significativa entre ETCO2 y PCO2 en el análisis global de todas las muestras con un r = 0,5402 (p < 0,001) y en las correspondientes a cada una de las tres instituciones (p < 0,001). En el centro C se observó el mayor valor de r = 0,6319, seguido por centro B r = 0,6234 y el centro A r = 0,5703. (Fig. 1).
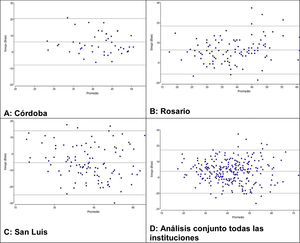
A través del método de Bland-Altman se realizó el análisis de concordancia entre los valores de PCO2 y ETCO2 (Fig. 2). Globalmente la media de las diferencias fue de 0,68 mmHg con un IC 95% entre -0,68 a 1,95 y, por lo tanto, no resultó significativo (valor p 0,289). Sin embargo, al evaluar cada institución de modo individual se encontraron ciertas diferencias: en centros A y B se observó una diferencia o error sistemático positivo (PCO2 mayor a ETCO2), mientras que en el centro C dicha diferencia o error sistemático fue negativo (PCO2 menor a ETCO2). En la tabla 4 se presentan estas diferencias entre los valores de PCO2 y ETCO2 con sus respectivos IC 95% en cada institución y en forma global.
Diferencia promedio, desviación e IC en la medición de CO2 mediante PCO2 y ETCO2
| Diferencias entre valor PCO2 y ETCO2 | |||||
|---|---|---|---|---|---|
| media | Desviación estándar | IC 95% inf | IC 95% sup | Valor p | |
| Centro A | 6,14 | 7,41 | 4,06 | 8,22 | < 0,001 |
| Centro B | 4,49 | 9,21 | 2,73 | 6,24 | < 0,001 |
| Centro C | -5,42 | 10,06 | -7,29 | -3,54 | < 0,001 |
| Global | 0,68 | 10,6 | -0,68 | 1,95 | 0,2892 |
IC: intervalo de confianza; inf: inferior; sup: superior.
Finalmente, calculamos para cada unidad la frecuencia de los valores sin sesgo o diferencias (PCO2 = ETCO2) y la frecuencia de sesgo negativo (PCO2 < ETCO2) o positivo (PCO2 > ETCO2), según su magnitud según intervalos establecidos en forma arbitraria. En la tabla 5 se presentan los resultados. En los centros A y B, el porcentaje de valores de ETCO2 superiores a PCO2 fue del 16 y 35%, respectivamente, pero en el centro C esta diferencia ocurrió en el 70% de las muestras. Desde otra perspectiva, si aceptáramos como irrelevantes diferencias de medición menores a ± 5 mmHg, solo 103 de las 277 observaciones (37%) se encontraron en un rango de diferencias aceptables.
Distribución de las diferencias en los centros entre valores de PCO2 y ETCO2
| Diferencia entre valores | Centro A51muestras | Centro B112 muestras | Centro C114 muestras | |
|---|---|---|---|---|
| PCO2< ETCO2 | < -20 mmHg | 0 | 1 (1%) | 7 (6%) |
| de -10,1 a -20 mmHg | 0 | 9 (8%) | 31 (27%) | |
| de -5,1 a -10 mmHg | 2 (4%) | 13 (12%) | 27 (24%) | |
| de -0,1 a -5 mmHg | 6 (12%) | 16 (15%) | 15 (13%) | |
| Total | 8 (16%) | 39 (35%) | 80 (70%) | |
| PaCO2= ETCO2 | cero | 3 (6%) | 8 (7%) | 0 |
| PCO2> ETCO2 | de 0,1 a 5 mmHg | 17 (33%) | 26 | 12 |
| de 5,1 a 10 mmHg | 9 (18%) | 17 | 8 | |
| de 10,1 a 20 mmHg | 11 (21%) | 19 | 9 | |
| > a 20 | 3 (6%) | 3 | 0,9 | |
| Total | 40 (78%) | 65 (58%) | 34 (30%) |
En forma preliminar exploramos el efecto de la edad gestacional, el peso al nacer y el sitio de extracción de la muestra (arterial vs. capilar o venosa) sobre la relación PCO2/ETCO2.
El grupo de RN ≤ 32 semanas tuvo menor correlación (r = 0,5445) que la de los RN > a 32 semanas (r = 0.5681); para el peso no se observaron diferencias significativas.
Los RN con FiO2 ≥ 30% tuvieron mayor correlación (r = 0,6100) que los RN con FiO2 < 30% (r = 0,5533), si bien ambas fueron significativas (p = 0,0177). Con respecto a los valores de CO2 y su efecto en la relación, no observamos diferencias cuando separamos a las observaciones como aquellas con CO2 < o ≥ 45 mmHg. Asimismo, el sitio de extracción de la muestra también modificó el grado de correlación (p < 0,0001); en las muestras arteriales dicha relación fue superior (r = 0,6471) que la observada en las muestras de vena o capilar (r = 0,5684).
DiscusiónNuestros resultados muestran como en otros estudios que la correlación entre ETCO2 y PCO2 es significativa. Los valores de correlación obtenidos en estas tres unidades (r 0,54) son algo más bajos que los reportados en la literatura, donde se han reportado valores entre 0,70 a 0,8021–24. La mayoría de las revisiones más recientes destacan la amplia variabilidad en los resultados25,26.
En nuestro estudio multicéntrico se ha observado que el comportamiento de la relación ETCO2 y PCO2 fue diferente entre los centros. Los análisis de concordancia mostraron sesgos o diferencias sistemáticas positivas en dos instituciones y negativa en otra de las unidades. Si bien no podemos afirmar la causa de estas variaciones, las mismas podrían deberse al tipo de equipamiento usado para el procesamiento de la sangre o bien al mayor porcentaje de muestras arteriales en el centro de San Luis. Existe evidencia de que el tipo de muestras modifica la correlación27, y en nuestro estudio, el 68 y 80% de las muestras de las dos instituciones con sesgo positivo fueron venosas o capilares.
El único parámetro de gravedad o mayor compromiso respiratorio en los casos analizados fue el requerimiento de ≥ FiO2 30%. En tal sentido, los RN con FiO2 ≥ 30% tuvieron una leve mejor correlación, a diferencia de lo establecido en publicaciones previas27. No encontramos efecto con relación al valor de CO2.
Más allá de los hallazgos y su significación estadística, desde el punto de vista clínico la pregunta es si podemos confiar en ETCO2 como un estimador seguro del valor de laboratorio de PCO2, que nos permita frente a un RN ventilado tomar decisiones clínicas confiables, y de este modo prevenir la hipocapnia e hipercapnia sin tener que realizar extracciones de sangre frecuentes. En tal sentido, impresiona que los valores, al menos obtenidos en forma aislada, son equivalentes en muy pocos casos y que la diferencia entre ambos puede variar entre 0,1 mmHg hasta más de 20 mmHg. Sin embargo, este estudio no ha analizado las tendencias en valores secuenciales frente al mismo recién nacido, las cuales podrían ser de utilidad clínica al marcar un descenso o ascenso de los valores, más allá del nivel inicial.
La PaCO2 es un parámetro importante en pacientes críticamente enfermos y ventilados mecánicamente. Para limitar los procedimientos invasivos o para una monitorización más continua de la PaCO2, las alternativas actuales son la capnografía o la monitorización transcutánea. Cada uno de estos tiene ventajas y limitaciones. La capnografía ofrece la medición de la PCO2 al final de la espiración y tiene la ventaja de no ser invasivo y ofrecer continuidad, si bien en pacientes con enfermedad pulmonar a menudo puede diferir como en nuestro estudio. La medición transcutánea de PCO2 puede ser confiable, si bien el daño en la piel del RN por el calor ha limitado su uso.
Nuestro estudio presenta limitaciones relacionadas con el limitado número de mediciones observadas en tres unidades neonatales en forma aislada. Sin embargo, aporta nuevos datos a los ya publicados por otros autores y alerta sobre la posibilidad de variaciones no predecibles, como ocurrió entre los diferentes centros, donde las relaciones observadas fueron diferentes. Esto podría indicar que, por el momento, cada centro debería validar el uso de estos monitores antes de asumir como válidos para su unidad los valores de correlación observados en otros estudios. Asimismo, refuerza la necesidad de continuar estableciendo o identificando las causas de dichas variaciones.
Son aún necesarios nuevos estudios para consolidar los métodos no invasivos como una alternativa fiable y viable a la gasometría en sangre arterial. Continúa siendo clave investigar en nuevas tecnologías que permitan tomar decisiones clínicas informadas y brindar seguridad en el cuidado de los RN críticamente enfermos.
FinanciaciónLa investigación fue financiada y auspiciada por la Sociedad Iberoamericana de Neonatología SIBEN. No existieron becas ni otros subsidios.
Conflicto de interesesLos autores no presentan ningún conflicto de intereses.