Los pacientes con parálisis cerebral moderada-grave precisan de sus cuidadores para realizar las actividades básicas de la vida diaria (ABVD).
ObjetivosDescribir la presencia de comorbilidades, la percepción de dificultad de los cuidadores para las ABVD y analizar la influencia del grado de afectación motora, el estado nutricional y otras alteraciones neurológicas.
MétodosEstudio transversal y observacional. Se estudió a pacientes con parálisis cerebral grados III-IV-V según el Sistema de Clasificación de la Función Motora Gruesa (GMFCS). Se registraron las comorbilidades y se estudió la composición corporal mediante antropometría y bioimpedanciometría. Además, se hizo una encuesta de carga del cuidador sobre ABVD (10 ítems que exploran las diferentes actuaciones: higiene, vestido, transferencias, sueño y alimentación). Se estudió qué variables influyen más en la percepción de dificultad para las ABVD.
ResultadosMuestra de 69 pacientes (50,7% mujeres, edad media de 10,46 ± 0,4 años), con los siguientes grados de GMFCS: grado III 36,2% (N = 25), grado IV 29,0% (N = 20) y grado V 34,8% (N = 24). Se halló relación entre la puntuación de carga del cuidador y el grado GMFCS (p = 0,003) y la discapacidad intelectual (p < 0,001). Además, independientemente del grado de GMFCS y de la discapacidad intelectual, existe mayor dificultad para las ABVD en relación con valores más bajos en peso (Z) (p = 0,028), masa grasa (kg) (p = 0,035), masa grasa (%) (p = 0,094) e índice de masa corporal (Z) (p = 0,086).
ConclusionesAdemás del grado de afectación motora y de la discapacidad intelectual, el estado nutricional es uno de los factores modificables que influyen en la dificultad del cuidador para realizar las ABVD en los pacientes con parálisis cerebral.
Patients with moderate-severe cerebral palsy require the support of their caregivers to carry out the activities of daily living (ADLs).
ObjectivesTo describe the comorbidities, need for care in children with cerebral palsy and to analyse the influence of the degree of motor involvement, nutritional status and other neurological disorders.
MethodsCross-sectional and observational study. Patients with cerebral palsy degrees III-IV-V according to the Gross Motor Function Classification System (GMFCS) have been studied. A record of comorbidities has been made and body composition has been studied using anthropometry and bioimpedance. In addition, a caregiver burden survey on ADLs has been carried out (10 items on the different actions: hygiene, clothing, transfers, sleeping and feeding). Which variables have the greatest influence on the perception of difficulty in performing ADLs have been studied.
ResultsA total of 69 patients (50.7% women, mean age 10.46 ± 0.4 years) were analysed, with GMFCS grades: grade III 36.2% (N=25), grade IV 29.0% (N=20), grade V 34.8% (N=24). A relationship was found between the caregiver burden score and GMFCS grade (P=0.003) and intellectual disability (P<0.001). However, regardless of the degree of GMFCS and intellectual disability, there is greater difficulty in performing ADLs in relation to lower values in weight (Z-score) (P=0.028), fat mass (kg) (P=0.035), fat mass (%) (P=0.094), body mass index (Z-score) (P=0.086).
ConclusionsIn addition to the degree of clinical impairment, nutritional status is a factor that influences the caregiver's difficulty in performing the ADLs in cerebral palsy patients on which we can act to improve this problem.
La parálisis cerebral es la causa más frecuente de discapacidad motora en la edad pediátrica. El concepto parálisis cerebral se refiere a un trastorno del desarrollo del movimiento y la postura que es atribuido a una lesión no progresiva que ocurre en un cerebro en desarrollo en la época fetal o en los primeros años.
El estudio europeo Surveillance of Cerebral Palsy in Europe1 estableció la prevalencia de parálisis cerebral en 2-3/1.000 recién nacidos vivos. Este estudio recomienda la edad mínima para el diagnóstico de la parálisis cerebral en 3 años y la edad óptima en 5 años.
Los pacientes con parálisis cerebral presentan con frecuencia múltiples comorbilidades asociadas que afectan a la salud mental y física tanto del propio paciente como del cuidador, con un gran consumo de tiempo y recursos2. Entre estas comorbilidades, la alteración nutricional es una de las más frecuentes y sobre la que, además, se puede actuar directamente3.
En este sentido, debe procurarse que estos pacientes presenten el mejor estado nutricional posible, que les permita desarrollar sus funciones motoras, capacidades de cognición, comunicación e interacción social y, por lo tanto, el desarrollo neuropsicológico globalmente2,4, además de prevenir la aparición de malnutrición y otras enfermedades carenciales5. Aunque parece evidente que una mayor afectación motora dificultará el cuidado de los pacientes con parálisis cerebral, se desconoce en qué medida la situación nutricional puede influir en el manejo de sus cuidadores6.
Los objetivos de este trabajo son estudiar la prevalencia de comorbilidades en una población con parálisis cerebral moderada-grave y analizar la percepción de dificultad que tienen los cuidadores para desarrollar las actividades básicas de la vida diaria (ABVD) con estos pacientes, así como su posible relación con el estado nutricional, la afectación motora y otras alteraciones neurológicas.
Material y métodosSe realizó un estudio transversal, observacional, descriptivo y analítico. La población a estudio estuvo constituida por pacientes de entre 4 y 15 años afectos de parálisis cerebral moderada-grave con espasticidad procedentes de la Unidad de Neuropediatría de un hospital de tercer nivel.
Se incluyó a los pacientes clasificados en niveles III-IV-V del Sistema de la Clasificación de la Función Motora Gruesa (GMFCS) de Palisano7, modificada de acuerdo con la Clasificación Internacional del Funcionamiento de la Organización Mundial de la Salud, que divide a los pacientes en grupos en función de su grado de afectación motora. Se excluyó a aquellos pacientes que decidieron no participar en el estudio por decisión propia o de sus tutores, a aquellos que no estaban en el rango de edad del estudio o que no cumplieran los criterios diagnósticos de parálisis cerebral.
El estudio fue aprobado antes de su desarrollo por el Comité de Ética regional (CEICA; PI16/039). Todos los pacientes o sus tutores firmaron un consentimiento informado.
Tras comprobar que se cumplían los criterios para ser seleccionados, se contactó con ellos o con sus tutores para concertar una visita en consulta, donde se les realizó una entrevista clínica y una exploración para recoger variables relacionadas con el estado clínico, antropometría y hábitos nutricionales. Los ítems sobre las variables neurológicas (déficit visual, hipoacusia, discapacidad intelectual, etc.) se extrajeron de los datos del historial clínico neuropediátrico de los pacientes y fueron consensuados con el neuropediatra.
Con una encuesta rápida se detectaron problemas relacionados con la alimentación. La encuesta consistía en 4 preguntas (resultado positivo ≥ 2 ítems): ¿tarda en comer más de 30 min?, ¿el momento de la comida es estresante para el cuidador o hijo?, ¿gana peso adecuadamente?, ¿presenta síntomas respiratorios durante o tras la comida? Se incluyó como pacientes con disfagia a aquellos con 2 o más ítems positivos en la encuesta (y cuyos problemas tuvieran relación con la deglución/ingesta), a los que tenían una videofluoroscopia compatible y a los portadores de gastrostomía por problemas de alimentación derivados de la deglución.
Se encuestó a los cuidadores para valorar la percepción de dificultad que referían a la hora de hacer con su hijo las ABVD. Para ello, se empleó un cuestionario en castellano validado para cuidadores de pacientes con parálisis cerebral de grado moderado-grave8. Este cuestionario consta de 10 ítems (sobre aseo, transferencias, alimentación, vestir y sueño) en los que se puntúa entre 0 y 3 puntos (fácil-muy difícil) en función de la dificultad (máxima dificultad 30 puntos).
El diagnóstico de estreñimiento se estableció según criterios clínicos para el diagnóstico del estreñimiento en el niño Roma IV9 junto con la escala de morfología fecal de Bristol10. Entre los pacientes con reflujo gastroesofágico se incluyó a aquellos con pH-metría positiva y a aquellos con clínica clara de reflujo (regurgitaciones y vómitos frecuentes).
Para el estudio antropométrico se tomó el peso y la talla, calculada mediante la fórmula de estimación de Stevenson et al.11 a partir de la altura de rodilla: Talla = (altura de la rodilla×2,69) + 24,2cm. Para recoger estos datos se emplearon una báscula (peso) y un cáliper (altura de rodilla). Se estimaron las puntuaciones estándar (Z) para los valores antropométricos según el Estudio de Crecimiento de Carrascosa et al. (2010)12, siguiendo las recomendaciones de la European Society for Paediatric Gastroenterology, Hepatology and Nutrition (ESPGHAN) de 2017 de emplear los estándares poblacionales de referencia. Se calculó el índice de masa corporal (IMC) y el peso para la talla (índice de Waterlow = W) para catalogar el estado nutricional del paciente en función del peso: W = peso actual/peso ideal (p50) para la talla×100.
Se valoró la composición corporal de los pacientes con bioimpedanciometría (BIA) mediante un bioimpedanciómetro modelo Akern BIA-101 Anniversary. Mediante este método se obtienen datos referentes a agua total (extra- e intracelular), masa grasa, masa celular (masa total de células vivas, funcionantes y metabólicamente activas) y masa libre de grasa (masa magra y masa ósea)13,14. Para ello se aplica una corriente alterna imperceptible mediante electrodos adheridos a la piel, con la que se detecta la resistencia (oposición al paso de corriente eléctrica) y reactancia (demora en la conducción causada por las membranas celulares, interfaces tisulares y sustancias no iónicas)13. La metodología con la que se realizó la BIA se describió con mayor precisión en una publicación previa15. En esa publicación se explicó también la forma en la que se ajustó la masa magra de los pacientes a su talla, edad y sexo para lograr el concepto de «masa magra con respecto al ideal» (masa magra ideal).
Para el análisis estadístico se empleó el programa SPSS Statics V21.0. Se ha realizado un estudio descriptivo, con los resultados expresados en media ± desviación estándar/IC 95% (variables cuantitativas) o frecuencias (variables cualitativas). Se comprobó la normalidad de la muestra (test de Kolmogorov-Smirnov y Saphiro-Wilk). Posteriormente se hizo un contraste de hipótesis empleando múltiples estadísticos: test de χ2 y test de Fisher (variables cualitativas), t de Student (muestras paramétricas, variables cuantitativa y cualitativa dicotómica), U de Mann Whitney (muestras no paramétricas, variables cuantitativa y cualitativa dicotómica), ANOVA y comparación de Bonferroni (muestras paramétricas, variables cuantitativa y cualitativa no dicotómica), Kruskal-Wallis (muestras no paramétricas, variables cuantitativa y cualitativa no dicotómica). Por último, se estudió la correlación entre la puntuación en la escala del cuidador y las diferentes variables antropométricas y de composición corporal con r de Pearson (paramétrico) y rho de Spearman (no paramétrico). Tal y como se describe en una publicación previa, los pacientes de esta muestra presentaban diferentes rasgos antropométricos y de composición corporal en función de su grado de afectación motora según la escala GMFCS15, por lo que se elaboró un modelo estadístico multivariante que incluyó las diferentes variables de antropometría y de composición corporal junto con las variables de afectación motora y neurológica que mantuvieron relación estadística con la puntuación obtenida en la escala del cuidador (grado de escala GMFCS y discapacidad intelectual) para discriminar el verdadero peso de estas variables nutricionales.
ResultadosEl número de pacientes que cumplieron los criterios de inclusión fueron 82, aunque 13 rechazaron participar o resultaron ilocalizables, por lo que la muestra final fue de 69 pacientes, con un reclutamiento final del 84,2%. El 50,7% (N = 35) eran mujeres. Al catalogar a los pacientes en los diferentes grados de la escala GMFCS, la distribución fue: grado III 36,2% (N = 25), grado IV 29,0% (N = 20) y grado V 34,8% (N = 24). La edad media era 10,46 ± 0,4 años (grado III 10,83 ± 0,7 años; grado IV 10,89 ± 0,8 años; grado V 9,73 ± 0,7 años; p = 0,380).
En la tabla 1 se detalla la prevalencia de las diferentes comorbilidades halladas en la muestra. La prevalencia de comorbilidades en los pacientes con parálisis cerebral moderada-grave fue alta; destacaron la discapacidad intelectual, la ausencia de control de esfínteres, el déficit visual, la disfagia, la sialorrea y el estreñimiento. Además, se observó una mayor frecuencia de discapacidad intelectual, ausencia de lenguaje, sialorrea y mal control de esfínteres en los pacientes con una mayor afectación motora.
Prevalencia de comorbilidades en pacientes con parálisis cerebral en función de la escala GMFCS
| Total % (n) | Grado III (%) | Grado IV (%) | Grado V (%) | p | |
|---|---|---|---|---|---|
| Discapacidad intelectual | 78,3 (54) | 44 | 95 | 100 | <0,001 |
| Ausencia de lenguaje | 40,6 (28) | 0 | 35 | 87,5 | <0,001 |
| Ausencia de control de esfínteres | 74 (51) | 24 | 70 | 95,8 | <0,001 |
| Déficit visual | 59,4 (41) | 56 | 65 | 58,3 | 0,822 |
| Hipoacusia | 11,6 (8) | 12 | 10 | 12,5 | - |
| Crisis en últimos 12 meses (Epilepsia) | 17,4 (12) | 16 | 10 | 17,4 | 0,415 |
| TDAH | 8,7 (6) | 24 | 0 | 0 | - |
| TEA | 5,8 (4) | 0 | 20 | 0 | - |
| Sialorrea | 44,9 (31) | 20 | 45 | 70,2 | 0,002 |
| Disfagia | 56,5 (39) | 36 | 50 | 83,3 | 0,003 |
| Reflujo gastroesofágico | 24,6 (17) | 8 | 10 | 54,2 | <0,001 |
| Estreñimiento | 66,7 (46) | 60 | 60 | 79,2 | 0,274 |
TDAH: trastorno de déficit de atención e hiperactividad; TEA: trastorno del espectro autista.
La escolarización de los pacientes fue: GMFCS III (32% modalidad ordinaria, 36% con adaptación curricular y el 32% especial), GMFCS IV (5% normal, 5% con adaptación y el 90% especial), GMFCS V (100% especial) (p ˂ 0,001).
La media de horas de rehabilitación/fisioterapia que recibían semanalmente los pacientes era de 3,83 ± 1,64 h realizadas por un profesional; 1,83 ± 2,59 h realizadas por la familia en domicilio y 5,66 ± 3,12 h en total, sin encontrar diferencias significativas entre los grupos según escala GMFCS. Acudía a logopedia de forma regular el 64% de los pacientes grado III, el 95% de grado IV y el 100% de grado V (p < 0,001).
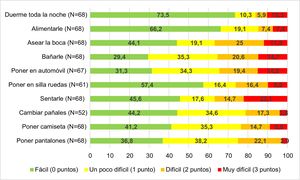
Se pasó una encuesta para medir la dificultad que tenían los padres/tutores para las ABVD, excepto en un caso, en el que la barrera idiomática hacía poco valorables los resultados. La puntuación media en la encuesta del cuidador fue de 8,97 ± 5,90 puntos: grado III 5,79 ± 1,02; grado IV 9,45 ± 1,44; grado V 11,75 ± 0,98 (p = 0,003). En los pacientes con discapacidad intelectual se encontró una puntuación de 9,17 ± 0,66, mientras que en aquellos sin esa discapacidad fue de 2,93 ± 0,67 (p < 0,001). No se encontró relación entre la puntuación en la escala del cuidador y que los pacientes presentaran hipoacusia, déficit visual o ausencia de lenguaje. En la figura 1 se presenta la percepción de dificultad que tienen los padres/tutores a la hora de realizar diferentes ABVD con sus hijos.
En la tabla 2 se muestra la correlación entre la puntuación obtenida en la escala de dificultad del cuidador para ABVD y las diferentes variables antropométricas y de composición corporal. En esta tabla se puede observar que existía correlación inversa y significativa entre la mayor parte de las variables antropométricas y de composición corporal y la puntuación obtenida en la escala de dificultad para ABVD del cuidador, de forma que esto se cumple tanto en las variables absolutas como en aquellas que ajustan su valor en función de edad y sexo (peso [z], IMC, índice de Waterlow). Sin embargo, al ajustar esta correlación en función del grado de la escala GMFCS de los pacientes y la existencia de discapacidad intelectual, las variables en las que dicha relación persistía significativa fueron el peso (Z) y la masa grasa, también con una clara tendencia en el IMC (Z).
Correlación entre las variables antropométricas y de composición corporal y la puntuación obtenida en la escala de dificultad para ABVD del cuidador
| Antropometría | |||
|---|---|---|---|
| r | p* | p** | |
| Talla (cm) | −0,187 | 0,130 | 0,501 |
| Talla (Z) | −0,280 | 0,021 | 0,219 |
| Peso (kg) | −0,283 | 0,019 | 0,128 |
| Peso (Z) | −0,435 | <0,001 | 0,028 |
| IMC (kg/m2) | −0,361 | 0,003 | 0,124 |
| IMC (Z) | −0,359 | 0,003 | 0,086 |
| Índice Waterlow (peso) | −0,334 | 0,005 | 0,186 |
| Bioimpedanciometría-composición corporal | |||
| Masa grasa (kg) | −0,354 | 0,003 | 0,035 |
| Masa grasa (%) | −0,279 | 0,021 | 0,094 |
| Masa magra (kg) | −0,247 | 0,042 | 0,270 |
| Masa magra (%) | 0,311 | 0,010 | 0,059 |
| Masa magra (% ideal) | −0,151 | 0,219 | 0,830 |
r: correlación entre variables antropométricas/composición corporal y escala de dificultad para ABDV del cuidador.
Los pacientes con parálisis cerebral moderada-grave presentan una elevada prevalencia de comorbilidades, que aumenta en relación con el grado de afectación motora16, tal y como ocurre en la muestra. Todas estas comorbilidades conllevan una serie de cuidados y terapias que requieren un manejo coordinado entre atención primaria y especializada, aunque el peso fundamental va a recaer en la figura del cuidador, que va a precisar de tiempo, atención y habilidades técnicas para llevarlos a cabo.
En la actualidad se empieza a prestar atención a la figura del cuidador y es probable que en los próximos tiempos alcance una mayor relevancia. Diferentes estudios han relacionado la prevalencia de comorbilidades y su gravedad directamente con la calidad de vida de los cuidadores, así que su adecuado enfoque, diagnóstico y tratamiento puede ayudar a mejorar esta situación17,18. De esta forma, debería tenerse cada día más en cuenta al cuidador como una figura fundamental que puede presentar problemas de salud, tanto físicos como mentales, derivados de la atención diaria del paciente con parálisis cerebral y que merece una atención personalizada e individualizada19. En estos pacientes existen muchos factores no modificables que pueden afectar a la calidad de vida del cuidador, de los que el problema motor y las alteraciones del comportamiento son los que ejercen un papel más determinante20.
Como era de esperar en los resultados del estudio, la percepción de dificultad para las ABVD por los cuidadores de los pacientes con parálisis cerebral se incrementa conforme aumenta el grado de GMFCS y en aquellos casos con diagnóstico de discapacidad intelectual. Sin embargo, resulta interesante que las variables que valoran el peso y el estado nutricional, independientemente del sexo y de la edad de los pacientes, presentan una relación significativa y negativa con la puntuación obtenida en la escala de dificultad para las ABVD del cuidador. Un mayor peso (Z), IMC (Z) y grasa corporal disminuyen la percepción de dificultad de los cuidadores para las ABVD. Los pacientes con parálisis cerebral presentan mayor alteración nutricional en relación con el grado de GMFCS15 y, a su vez, el grado de GMFCS y la discapacidad intelectual se relacionan con la dificultad para las ABVD. Por todo ello, los resultados del presente estudio se tenían que analizar intentando anular en lo posible la influencia del estado clínico en la relación entre el estado nutricional y la dificultad para las ABVD. Esto es importante ya que, en contra de lo que se habría pensado inicialmente, un mayor peso en estos pacientes no parece ser un problema para estas ABVD para sus cuidadores. De hecho, un mejor estado nutricional, independientemente del grado de afectación motora y de la edad, facilitará estas tareas. La afectación motora y la discapacidad intelectual son los 2factores con mayor influencia sobre la carga del cuidador, pero son difícilmente modificables, mientras que el estado nutricional de los pacientes con parálisis cerebral sí que es mejorable. Por todo esto, los resultados del presente estudio avalan las recomendaciones de la ESPGHAN sobre la necesidad de sistematizar el soporte nutricional en los pacientes pediátricos con parálisis cerebral3.
Otro factor importante sobre el que se puede actuar es el sueño. Existen estudios que destacan la presencia de una mayor prevalencia de problemas relacionados con el sueño en pacientes con parálisis cerebral y que parecen incrementarse con el grado de la escala GMFCS, lo que puede afectar también a la calidad de vida del cuidador del paciente con parálisis cerebral moderada-grave21. En la muestra estudiada, parecen encontrarse dificultades para el cuidado relacionadas con el descanso nocturno en más de un 25% de los casos, aunque sin relación con el estado nutricional. Algunas de estas complicaciones relacionadas con el sueño, como el síndrome de apnea obstructiva, insomnio y otras alteraciones de los patrones del sueño que producen despertares múltiples o periodos cortos de sueño, pueden y deben intentar resolverse, dada la importante repercusión que tienen en la calidad de vida del paciente y del cuidador17,21.
La disfagia es otro factor modificable muy prevalente en la parálisis cerebral que condiciona la calidad de vida del paciente y del cuidador, y tanto en esta muestra como en otras series tiende a aumentar su frecuencia y gravedad con el incremento del problema motor22. La disfagia en estos pacientes está en relación con la presencia de problemas nutricionales, de forma que debe plantearse un abordaje integral del problema disfagia-nutrición16,23. Afortunadamente existen recursos para manejar este problema mediante el empleo de espesantes, la adecuación de texturas, el apoyo de logopedia y la colocación de gastrostomías cuando es necesario24. Un tercio de los pacientes grado V de esta muestra eran portadores de gastrostomía, aunque no existían diferencias en la situación nutricional de los pacientes con o sin gastrostomía. Esto puede deberse al retraso en su colocación o a la mayor afectación motora y neurológica de estos pacientes15.
Algunas terapias complementarias, como la rehabilitación, fisioterapia y logopedia, resultan muy útiles para el desarrollo y bienestar de los pacientes con parálisis cerebral25, aunque debe tenerse en cuenta que requieren un tiempo y una regularidad de asistencia que condiciona los horarios de los cuidadores y que precisan de múltiples desplazamientos. Aunque parece clara su utilidad en diferentes aspectos relacionados con la situación neuromotora26, en este trabajo no se ha hallado relevancia entre el número de horas dedicadas a estas y un cambio sustancial en la puntuación de la escala de dificultad para ABVD del cuidador. Otro factor que parece beneficiar la calidad de vida del paciente y sus cuidadores es la escolarización adaptada a las necesidades del paciente18. En el presente estudio todos los pacientes se encontraban escolarizados.
Pese a que no se ha evaluado, otra carga importante es la económica, que, además, se asocia con el grado de afectación motora y neurológica de los pacientes27. Un estudio multicéntrico europeo estableció que ni una excelente situación económica ni disponer del equipo adecuado eran factores determinantes para prevenir el desarrollo de estrés y otros problemas psicológicos en los cuidadores20. Sin embargo, una revisión sobre la calidad de vida en cuidadores de pacientes con parálisis cerebral concluyó que las frecuentes alteraciones en la calidad de vida y su salud física y mental podían mejorarse trabajando la autoeficacia28, es decir, la capacidad y confianza de los propios cuidadores en sí mismos para realizar adecuadamente las ABVD.
Una de las limitaciones de este estudio es no disponer de mayor número de pacientes para obtener mayor potencia estadística y hacer más análisis por grupos. Sin embargo, la muestra la compone la mayor parte de los pacientes controlados en una unidad de referencia de parálisis cerebral. Sería interesante en próximos trabajos aumentar el número de pacientes en cada grupo de GMFCS, así como medir la repercusión que puede tener una adecuada intervención nutricional en la escala de dificultad para ABVD del cuidador.
A modo de conclusión, puede decirse que la parálisis cerebral es una enfermedad crónica que asocia múltiples comorbilidades que requieren de un manejo multidisciplinar y que precisa que los cuidadores directos del paciente estén correctamente formados y entrenados. Los profesionales sanitarios facilitarán en la medida de lo posible la labor del cuidador para mejorar su calidad de vida y el pronóstico del paciente. La prevalencia de comorbilidades, la necesidad de cuidados y la dificultad percibida por el cuidador para las ABVD se incrementan con el grado de afectación motora y la discapacidad intelectual. Además, de manera independiente, el estado nutricional es uno de los factores modificables que influyen en la dificultad del cuidador para las ABVD en estos pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.