Presentamos una revisión de la evidencia sobre pronóstico de la bronquiolitis aguda, factores de riesgo de formas graves, escalas de valoración de síntomas o gravedad y riesgo de asma postbronquiolitis. En pacientes ingresados son factores de riesgo documentados de estancias prolongadas o ingreso en UCIP: la displasia broncopulmonar y/o enfermedad pulmonar crónica, la prematuridad, las cardiopatías congénitas y la edad menor de 3 meses. Otros factores de riesgo menos documentados son la exposición a tabaco, el antecedente de ventilación mecánica neonatal, la lactancia materna de menos de 4 meses, la coinfección vírica y otras enfermedades crónicas. Son marcadores de gravedad: el aspecto tóxico, la taquipnea, la hipoxia, la presencia de atelectasia o infiltrado en la radiografía de tórax, el trabajo respiratorio aumentado, los signos de deshidratación, la taquicardia y la fiebre. Aunque existen diversos modelos predictivos de gravedad, ninguno ha mostrado suficiente validez predictiva como para recomendar su uso en la práctica clínica. Contamos con diversas escalas de valoración de síntomas o gravedad, ninguna ha demostrado ser más válida o precisa como para recomendar su aplicación preferente en la práctica clínica. Parece existir una consistente y fuerte asociación entre ingreso por bronquiolitis y episodios de sibilantes recurrentes en los primeros 5 años de vida. Sin embargo, no está claro si en años posteriores dicha asociación se prolonga, existiendo información discordante sobre la asociación entre bronquiolitis y asma.
We present a review of the evidence on prognosis of acute bronchiolitis, risk factors for severe forms, symptom or severity scores and risk of post-bronchiolitis asthma. Documented risk factors of long stay or PICU admission in hospitalized patients are: bronchopulmonary dysplasia and/or chronic lung disease, prematurity, congenital heart disease and age less than 3 months. Other less well documented risk factors are: tobacco exposure, history of neonatal mechanical ventilation, breastfeeding for less than 4 months, viral co-infection and other chronic diseases. There are several markers of severity: toxic appearance, tachypnea, hypoxia, atelectasis or infiltrate on chest radiograph, increased breathing effort, signs of dehydration, tachycardia and fever. Although we have some predictive models of severity, none has shown sufficient predictive validity to recommend its use in clinical practice. While there are different symptom or severity scores, none has proven to be valid or accurate enough to recommend their preferable application in clinical practice. There seems to be a consistent and strong association between admission due to bronchiolitis and recurrent episodes of wheezing in the first five years of life. However it is unclear whether this association continues in subsequent years, as there are discordant data on the association between bronchiolitis and asthma.
Presentamos una revisión de la evidencia sobre pronóstico de la bronquiolitis aguda: factores de riesgo de formas graves, escalas de valoración de síntomas o gravedad y riesgo de asma postbronquiolitis. Esta revisión forma parte de la documentación elaborada para la «Conferencia de Consenso sobre bronquiolitis aguda», en el que se sustenta el estudio de idoneidad del proyecto titulado «Variabilidad e idoneidad del manejo diagnóstico y terapéutico de la bronquiolitis aguda» (estudio «aBREVIADo»: BRonquiolitis-Estudio de Variabilidad, Idoneidad y ADecuación). La metodología de la revisión ha sido publicada en un artículo previo de esta serie1.
IntroducciónLa bronquiolitis aguda (BA) es la principal causa de ingreso por infección respiratoria aguda (IRA) de vías bajas en el niño menor de 2 años. Es una entidad respiratoria de diagnóstico clínico, que se presenta habitualmente con rinitis, dificultad respiratoria, tos, rechazo de alimentación, irritabilidad y, en lactantes muy pequeños, apneas. Estos hallazgos clínicos, junto con la existencia de sibilantes y/o crepitantes en la auscultación, permiten realizar el diagnóstico. La BA tiene lugar en lactantes menores de 2 años, más frecuentemente entre los 3–6 meses de vida, en asociación con epidemias de infecciones virales en los meses de otoño e invierno, principalmente por el virus respiratorio sincitial (VRS).
La carga de la enfermedad es importante. La mayoría de los lactantes se infectan por el VRS en los primeros años de vida, aunque solo una parte de ellos presentan síntomas de BA. La mayoría de los casos son autolimitados, persistiendo los síntomas entre 3–7 días, pudiendo ser manejados en su domicilio con medidas sintomáticas. El ingreso hospitalario suele estar motivado por la necesidad de recibir cuidados como la administración de oxígeno suplementario, la aspiración de secreciones o la alimentación enteral o parenteral. Excepcionalmente los pacientes con BA pueden presentar fallo respiratorio y precisar asistencia respiratoria. En función del nivel de cuidados que requiera el paciente podemos clasificar las BA como leves (manejo ambulatorio), moderadas (precisan hospitalización) o graves (presentan fallo respiratorio que requiere ventilación asistida).
Los niños de menor edad y los que tienen problemas médicos previos (prematuridad, cardiopatía congénita, enfermedad pulmonar crónica o displasia broncopulmonar, etc.) son más susceptibles de tener enfermedad grave y mayor riesgo de ingreso hospitalario o asistencia respiratoria. La identificación de factores de riesgo o marcadores clínicos de gravedad puede resultar útil en la toma de decisiones médicas, fundamentalmente para la indicación o no de ingreso hospitalario, pero también para la selección de pacientes susceptibles de la realización de pruebas diagnósticas o la instauración de procedimientos terapéuticos. En los últimos años ha surgido un especial interés por identificar factores de riesgo de BA grave, en relación con la disponibilidad de intervenciones preventivas de alto coste (anticuerpos monoclonales frente al VRS), para las que se propone un uso restringido.
La decisión de ingresar o no a un paciente con BA tiene un carácter multifactorial. En ella influyen factores como la comorbilidad previa, el grado de afectación del paciente y las condiciones sociofamiliares. No obstante, la decisión de ingreso está sujeta a una gran variabilidad, no correlacionándose siempre con la gravedad del paciente. Algo parecido nos puede ocurrir con la duración de la estancia hospitalaria. Sin embargo, la necesidad de ventilación mecánica (VM) podría ser un indicador más robusto de gravedad.
Por otra parte, existen distintas variables clínicas asociadas a gravedad, algunas de ellas aceptablemente precisas que pueden ser empleadas para clasificar el nivel de afectación de los pacientes, indicar o no su ingreso o la instauración de determinados procedimientos diagnósticos o terapéuticos. La consideración de estas variables, tanto de forma aislada como integradas en escalas clínicas o modelos predictivos, pueden facilitar la toma decisiones del paciente con BA, siempre y cuando, demuestren su utilidad clínica.
En cuanto a la evolución de los pacientes con BA, se ha observado que un importante porcentaje de ellos presentan síntomas respiratorios recurrentes en los años que siguen a la infección. Este hallazgo se ha documentado fundamentalmente en pacientes hospitalizados, tanto con BA en general, como con BA o IRA bajas producidas por VRS u otros virus. Se ha sugerido que la BA podría originar una hiperreactividad bronquial, que se manifestaría posteriormente en forma de sibilantes recurrentes. La trascendencia clínica de este potencial riesgo sería elevada, si tenemos en cuenta la alta frecuencia de la BA.
Existe un debate sobre si el daño primario lo produce la infección pulmonar aguda o es solo la manifestación de una predisposición genética o ambiental a morbilidad respiratoria previamente existente. En este debate tiene especial importancia el hecho de que la exposición habitualmente valorada en los estudios epidemiológicos sea el ingreso hospitalario. El ingreso en el curso de la BA puede ser interpretado como un indicador de una mayor gravedad de la infección aguda (en cuyo caso sería una exposición) o como la expresión de una predisposición previa a problemas respiratorios (en cuyo caso sería un efecto). Resulta, por lo tanto, complejo diferenciar ambos fenómenos, especialmente cuando los estudios se inician en el episodio de hospitalización.
Se ha propuesto que el VRS podría desempeñar un papel propio en el desarrollo de asma, bien de forma directa o bien desencadenando cambios en la fisiología pulmonar de pacientes especialmente predispuestos. Junto al efecto citopático del virus en el epitelio respiratorio, jugarían un papel fundamental la respuesta inflamatoria del huésped, en la que intervienen fenómenos de inmunidad humoral y celular. El interés despertado por esta asociación se ha acrecentado por la disponibilidad de medidas preventivas frente a la infección por VRS. No obstante, antes de plantear cualquier intervención al respecto debería aclararse el papel de la infección, los mecanismos fisiopatogénicos implicados, así como la eficacia de las medidas preventivas en la reducción del riesgo de asma. Hay que tener en cuenta que la asociación entre BA y asma no parece exclusiva del VRS, habiéndose encontrado con otros virus, incluso con mayor intensidad.
No obstante, el interés de ofrecer un pronóstico sobre el riesgo de asma en los pacientes con BA se ve limitado por la ausencia de intervenciones que, instauradas precozmente tras el episodio, permitan interferir en el curso evolutivo de los pacientes. Asimismo, aunque se dispone de información sobre diversos cofactores que aumentan el riesgo de asma, la utilidad clínica de los mismos no está claramente establecida, por lo que, por el momento, cualquier orientación pronóstica o recomendación preventiva debería ser aplicable al conjunto de pacientes con BA.
Factores pronósticos y marcadores de gravedad en la BAA la hora de evaluar el pronóstico de los pacientes con BA nos interesa identificar tanto los factores de riesgo que se asocian a formas graves de la enfermedad, como las variables clínicas presentes al inicio del cuadro que muestran el grado de afectación y que orientan en el juicio pronóstico y manejo del paciente.
La evidencia sobre estos factores de riesgo procederá idealmente de estudios de cohortes de pacientes con BA atendidos a nivel ambulatorio u hospitalario, en los que se evalúe la duración de la enfermedad, la presencia de síntomas o signos de compromiso respiratorio, el riesgo de ingreso y la necesidad de procedimientos diagnósticos o terapéuticos. También podemos obtener información, aunque de menor calidad, a partir estudios de casos y controles, transversales y ecológicos.
Estos estudios deberán proporcionarnos estimaciones, a ser posible ajustadas, del riesgo de padecer BA de curso moderado-grave. Complementariamente, nos ofrecerán estimaciones del efecto atribuible en medidas cuantitativas de gravedad: duración de síntomas, estancia hospitalaria, necesidades de oxígeno, escalas de síntomas, etc.
Mayor interés clínico tendrán los trabajos en los que se evalúa la capacidad predictiva de factores de riesgo o marcadores clínicos de gravedad, de forma aislada o integrados en modelos predictivos, en relación con eventos relevantes como el ingreso hospitalario, la estancia hospitalaria prolongada, la necesidad de ingreso en UCI o la VM. Estos estudios nos ofrecerán estimadores de validez como la sensibilidad, especificidad, valores predictivos y cocientes de probabilidades.
Volumen de la evidenciaSe han revisado 31 estudios que analizan pacientes ingresados, 11 estudios pacientes de UCI, 11 estudios casos atendidos en servicios de Urgencias o a nivel ambulatorio y 3 estudios mixtos o de base poblacional. Los diseños predominantes son los estudios de cohortes prospectivos2–24 (23) o retrospectivos25–47 (22), los estudios de casos y controles48–55 (8), los estudios transversales56,57 (2) y ecológicos58 (1). En la tabla 1 se presentan las principales características y resultados de estos trabajos. La calidad predominante es de tipo medio-baja, utilizando estimadores ajustados de efecto solo en 14 estudios3,11,13,14,25–27,30,37,43,46,47,49,54, algunos de ellos con ajuste incompleto. Los pacientes son en su mayoría niños menores de 2 años, muchos de ellos restringidos a los primeros meses de vida, con diagnósticos de BA en 31 estudios, de cualquier etiología (21 estudios) o solo las relacionados con el VRS (10 estudios), o bien IRA de vías bajas (11 estudios; 9 de ellos por VRS). Algunos trabajos incluyen infecciones por VRS sin especificar diagnóstico clínico (10 estudios), frecuente en estudio de pacientes ingresados en UCI.
Tabla simplificada de evidencias sobre factores pronósticos de gravedad en bronquiolitis
| Comparación | N (CE/CC) | E | D | Medida de efecto | RGC¿ | EE | Efecto | IC95% (p) | Calidad. Comentarios |
| Autor año | |||||||||
| Factores pronóstico de gravedad | |||||||||
| Pacientes ingresados | 2/5 (a, e); | ||||||||
| Opavsky2 (PICNIC) 1995 | 689 | H | CP | ||||||
| Cardiopatía | Ingreso en UCI | Se 17% | Es 93% | ||||||
| Prematuridad | Ingreso en UCI | Se 33% | Es 83% | ||||||
| Edad ≤4 meses | Ingreso ≥4 días | Se 46% | Es 59% | Validez modelos de Green (SatO2 y edad): Se 98% Es 47%; y McConochie (VRS A o B, edad <3 meses, factores de riesgo y prematuridad): Se 77%, Es 76% | |||||
| Factores de riesgo | Ingreso ≥4 días | Se 28% | Es 97% | ||||||
| Wang3 (PICNIC) 1995 | 689 | H | CP | 2/5 (c, d, e); <2 años o >2 años con enfermedad cardiaca o pulmonar; ingresos por IRA baja VRS+ | |||||
| Raza india | Ingreso en UCI | 16%¿ | ORa | 3,1 | 1,0–9,2 | ||||
| Apneas | Ingreso en UCI | 16%¿ | ORa | 6,5 | 3–14,1 | ||||
| Edad <6 semanas | Ingreso en UCI | 16%¿ | ORa | 3,8 | 1,8–8 | Días de estancia asociada a las mismas variables (1,2–1,3 días) además de prematuridad 1,1 días (1,0–1,3); cardiopatía 1,4 (1,2–1,6) e inmunodepresión 1,7 (1,4–2,2) | |||
| Enfermedad pulmonar crónica | Ingreso en UCI | 16%¿ | ORa | 2,7 | 1,2–6 | ||||
| Hipoxia al ingreso | Ingreso en UCI | 16%¿ | ORa | 2,9 | 1,1–5,9 | ||||
| Condensación pulmonar | Ingreso en UCI | 16%¿ | ORa | 3,7 | 1,9–6,9 | ||||
| Langley4 1997 | 1603 | H | CP | 2/5 (a, e); <2 años; >2 años con enfermedad pulmonar o cardiaca o inmunosupresión; ingreso por IRA baja VRS+; ninguna medida de prevención redujo el riesgo de contagio | |||||
| Adquisición nosocomial | Mortalidad atribuible al VRS | 0,42% | RR | 10,4 | 3–36,4 | ||||
| Estancia atribuible al VRS (días) | 5 | DM | 5 | (p=0,0001) | |||||
| Moler25 1999 | 802 | H | CR | Estancia ≥7 días | 4/5 (a, c, d, e); <2 años; ingresados por IRA baja VRS+; validez predictiva del modelo conjunto: área curva ROC 0,89 | ||||
| Estancia ≥7 días | Fallo de medro | 3,2% | ORa | 6,4 | 3,1–13,2 | ||||
| DBP o hernia diafragmática | 4,3% | ORa | 5,1 | 2,5–10,6 | |||||
| Aspiración, laringomalacia o HRB | 9% | ORa | 5,3 | 2,7–10,3 | |||||
| Cardiopatía congénita | 3,7% | ORa | 4,3 | 2,1–9,0 | |||||
| Prematuridad | 16% | ORa | 2,5 | 1,5–4,3 | |||||
| Otras enfermedades crónicas | 6,6% | ORa | 2,3 | 1,2–4,3 | |||||
| Brooks 1999 | 16/32 | H | CC | Ingreso UCI | 2/5 (a, d); <1 año; ingresados por infección por VRS; >35 SG; área curva ROC del modelo predictivo 50% | ||||
| Ingresados UCI vs. no ingresados | Frecuencia respiratoria (media) | 50 | DM | 13 | (p=0,02) | ||||
| SatO2 (media) | 93% | DM | -5 | (p=0,01) | |||||
| El-Radhi5 1999 | 90 | H | CP | 2/5 (a, c); 1–12 meses; ingresados por BA | |||||
| Fiebre (>38°C) | Duración del ingreso (días) | 2,7 | DM | 1,5 | (p<0,005) | ||||
| Necesidad de O2 o VM | 29% | OR | 6,1 | 2,3–16,4 | |||||
| RX tórax alterada | 14,8% | OR | 8,9 | 3,2–25,2 | |||||
| Bonillo-Perales26 2000 | 455 | H | CR | 3/5 (a,c,e); <2 años; ingresos por BA en Andalucía de 1997–2000; diferencias en la estancia entre casos VRS+ y VRS- solo entre los no prematuros (DM 1,2 días); no se detallan los riesgos basales de algunos análisis. Media de estancia+1 DE: 11 días | |||||
| Prematuridad | Ingreso UCI | 3,1% | ORa | 2,67 | 1,01–7,56 | ||||
| Estancia prolongada (>11 días) | ‐ | ORa | 2,39 | 1,26–4,52 | |||||
| Edad <6 semanas | Ingreso UCI | ‐ | ORa | 1,68 | 1,04–8,19 | ||||
| Cardiopatía con hiperaflujo | Estancia prolongada (>11 días) | ‐ | ORa | 8,5 | 2,37–30,47 | ||||
| VM neonatal | Estancia prolongada (>11 días) | ‐ | ORa | 4,26 | 1,52–11,92 | ||||
| González27 2000 | 61 | H | CR | 3/5 (a, c, e); <2 años; ingresos por BA; gravedad según escala (FR, sibilancias, cianosis, pO2, pCO2 y pH; no especifica rangos): moderado/grave vs. leve; RGC es riesgo conjunto de la muestra | |||||
| Rechazo tomas | Escala grave-moderada vs. leve | 47%¿ | ORa | 4,08 | 1,1–16,8 | ||||
| Vómitos | Escala grave-moderada vs. leve | 47%¿ | ORa | 4,22 | 1,1–25,3 | ||||
| Espiración alargada | Gravedad clínica (escala) | 47%¿ | ORa | 5,35 | 1,14–24,30 | ||||
| Shazberg6 2000 | 150 | H | CP | Riesgo de otitis media aguda | IA | 53% | 0/5; <2 años; ingreso por BA; no diferencias casos con o sin otitis | ||
| Kaneko28 2001 | 157 | H | CR | 3/5 (a, c, e); <4 años; ingresos por IRA baja VRS+; gravedad: necesidad de oxígeno (SatO2 <90% o dificultad respiratoria intensa) o VM | |||||
| Edad <3 meses | Necesidad de O2 o VM | 13%¿ | OR | 59,9 | 14,7–244 | ||||
| Cardiopatía congénita | Necesidad de O2 o VM | 13%¿ | OR | 99,2 | 8,5–1160 | ||||
| Neves Barreira7 2001 | 487 | H | CP | 3/5 (a, c, d); <2 años; ingresados por IRA baja VRS+; no diferencias por subtipos en RX tórax, gravedad, oxígeno | |||||
| Subtipo de VRS A vs. B | Estancia media (días) | 6,16 | DM | 0,69 | (p=0,26) | ||||
| Aguilera Olmos29 2002 | 2/5 (a, b); CE: <1 mes; CC: >1 mes; ingresados por BA | ||||||||
| Edad <1 mes | 108/587 | H | CR | Ingreso UCI | 9,8% | IA | 19,4% | (p=0,004) | |
| Chan30 2002 | 216 | H | CR | 2/5 (c, d); <2 años; ingresados por BA VRS+; ajuste multivariante incompleto | |||||
| Prematuridad | Hipoxemia (SatO2<90%) | 14,3% | ORa | 1,2 | 1,1–1,6 | ||||
| Eriksson8 2002 | 1.503 | H | CP | 3/5 (a, c, d); ingresos por infección VRS; estudio de riesgo de ingreso (ver tabla); mayor riesgo en epidemias de inicio precoz que tardío. Comparación calculada respecto casos sin factores de riesgo >2 meses (682); no hay control multivariante | |||||
| Displasia broncopulmonar | 49 | Ingreso en UCI | 9,4% | OR | 3,86 | 1,97–7,56 | |||
| Cardiopatas | 59 | Ingreso en UCI | 9,4% | OR | 2,73 | 1,40–5,32 | |||
| Prematuro sin displasia | 108 | Ingreso en UCI | 9,4% | OR | 5,03 | 3,13–8,08 | |||
| Sin factor de riesgo: <2 meses | 530 | Ingreso en UCI | 9,4% | OR | 1,9 | 1,40–2,78 | |||
| Fasheh-Youssef9 2002 | 98 | H | CP | 2/5 (a, c); <12 meses; ingresados por BA; respuesta a salbutamol: descenso de un punto en la escala clínica del Hospital San Juan de Dios; no hay ajuste multivariante | |||||
| Respuesta salbutamol (escala) | Duración ingreso (días) | 4,7 | DM | -0,6 | ns | ||||
| Infiltrado en RX tórax | Duración ingreso (días) | 3,8 | DM | 1,4 | (p=0,01) | ||||
| Purcell31 2002 | 2.396 | H | CR | 2/5 (a, c); <6,5 años (95% <2 años); ingresados por BA o neumonía VRS+; Hemocultivos contaminados 0,5%; LCR: 0% | |||||
| Cribado infección bacteriana | Riesgo de Infección Urinaria | IA | 1,1% | ||||||
| Smyth32 2002 | 276 | H | CR | 1/5(c); ingresos o atendidos en Urgencias (38) por infección por VRS; cociente ARNm IL8 / HGPRT: ARNm de interleukina-8 y ARNm del gen HGPRT. RGC: riesgo global | |||||
| Genotipos VRS A y B | Necesidad de O2 o VM | 59%¿ | ns | ||||||
| Cociente ARNm IL8/HGPRT | Necesidad de O2 o VM | 59%¿ | OR | 1,15 | 1,06–1,24 | ||||
| Horn33 2003 | 304 | H | CR | 3/5 (a, c, d); <12 meses; ingresado por BA o neumonía por VRS o virus no especificado; escala gravedad: «Pediatric Comprehensive Severity Index» (PCSI); hallazgos similares con intubación y estancia hospitalaria; sobreajuste del efecto de prematuridad con el PCSI | |||||
| Prematuro ≤32 SG | Ingreso en UCI | 27,9% | IA | 1,67 | 0,7–3,8 | ||||
| Prematuro 33–35 SG | Ingreso en UCI | 27,9% | IA | 2,42 | 1,1–5,2 | ||||
| Edad en días | Ingreso en UCI (por cada día) | β | 0,007 | (p=0,0003) | |||||
| Escala PCSI al ingreso | Ingreso en UCI (por cada punto) | β | 0,116 | (p<0,0001) | |||||
| Willson34 2003 | 684 | H | CR | 2/5 (c, e); <12 meses; ingresado por BA o neumonía VRS+ | |||||
| Cardiopatías congénitas | Estancia media | 4 | DM | 3,7 | (p<0,001) | ||||
| Otras anomalías congénitas | Estancia media | 4 | DM | 6,7 | (p<0,001) | RGC: riesgo en niños sin factores de riesgo | |||
| Prematuridad | Estancia media | 4 | DM | 2,7 | (p<0,001) | ||||
| Fjaerli35 2004 | 764 | H | CR | 3/5 (a, b, c); <2 años; ingreso por BA VRS+; no ajuste multivariante | |||||
| Algún factor de riesgo | 77 | Duración ingreso (días) | 4 | DM | 4 | (p<0,001) | |||
| Prematuridad | 58 | Duración ingreso (días) | 4 | DM | 4 | (p<0,001) | Factores de riesgo: prematuridad, DBP, cardiopatía, enfermedad neuromuscular, respiratoria o inmunológica | ||
| Trisomía 21 | 7 | Duración ingreso (días) | 4 | DM | 3,5 | (p<0,001) | |||
| Duppenthaler10 2004 | 729 | H | CP | 3/5 (a, c, d); ingresados <24 meses; cohorte de estudio de ingresos por IRA por VRS; comparación de ingresos de niños con cardiopatías hemodinámicamente significativas vs. otros; no ajuste multivariante | |||||
| Cardiopatía hemodin. significativa | 10/719 | Ingreso UCIP | 11% | IA | 50% | (p=0,003) | |||
| Días de oxígeno | 2 | DM | 3 | (p=0,023) | |||||
| VM | 1,8% | IA | 20% | (p=0,016) | |||||
| Purcell62 2004 | 3.308 | H | CR | 2/5 (a, c); <6,5 años (95% <2 años); ingreso por IRA baja VRS+; 3 o más factores se asocia con ingreso en UCIP: 67,4% vs. 0,4%, OR: 22,2 (11,6–42,4); no se realiza ajuste multivariante | |||||
| Edad <6 semanas | Ingreso en UCI | 3,2% | IA | 15,9% | (p<0,001) | ||||
| Prematuridad | Ingreso en UCI | 3,2% | IA | 17,3% | (p<0,001) | ||||
| Cardiopatía | Ingreso en UCI | 3,2% | IA | 33% | (p<0,001) | ||||
| Enfermedad neurológica | Ingreso en UCI | 3,2% | IA | 23,7% | (p<0,001) | ||||
| Weigl37 2004 | 1.316 | H | CR | 1/5 (c); <2 años; ingresados por IRA baja comunitaria | |||||
| Enfermedad de base | Días de ingreso | 7¿ | β | 0,414 | (p<0,001) | VRS+ no asociada directamente sino por verse en niños más pequeños. Ni RX tórax con infiltrados ni proteína C reactiva asociada | |||
| Entidad de la infección | Días de ingreso | 7¿ | β | 0,135 | (p<0,001) | ||||
| Prematuridad | Días de ingreso | 7¿ | β | 0,156 | (p=0,002) | RGC: mediana de días de ingreso global; β coeficientes del modelo de regresión lineal de los días del logaritmo neperiano de los días de ingreso; no se especifica si se han corregido | |||
| Tiraje | Días de ingreso | 7¿ | β | 0,101 | (p=0,015) | ||||
| Edad (días) | Días de ingreso | 7¿ | β | -0,00097 | (p<0,001) | ||||
| Año de estudio (1996–2000) | Días de ingreso | 7¿ | β | -0,061 | (p=0,001) | ||||
| Bradley11 2005 | 206 | H | CP | 4/5 (a, c, d, e); <1 año; BA VRS+; todos menos 8 ingresados; RGC: corresponde al riesgo medio de toda la muestra | |||||
| Edad (por cada mes menos) | SatO2 mínima (%) | 92%¿ | DMa | -0,4 | 0,1–0,7 | ||||
| Raza blanca vs. otras | SatO2 mínima (%) | 92%¿ | DMa | -2,5 | 0,3–4,6 | ||||
| Domingo38 2005 | 271 | H | CR | Ingreso >3 días | 2/5 (a, c); <2 años; ingresados BA (67% VRS+); escala de gravedad propia (Hospital San Juan de Dios; 0–16 puntos); no se realiza ajuste multivariante; los datos no permiten calcular riesgos basales | ||||
| Ingreso >3 días vs. ≤3 días | Escala gravedad ingreso | 5,7 | DM | 0,7 | (p=0,031) | ||||
| Prematuridad | OR | 2,6 | 1,2–5,6 | ||||||
| Fiebre | OR | 2,2 | 1,3–4 | ||||||
| Edad (meses) | 3,4 | DM | 0,7 | (p=0,003) | |||||
| Escala gravedad máxima | 5,9 | DM | 1,35 | (p<0,001) | |||||
| Sritippayawan12 2006 | 71 | H | CP | 4/5 (b, c, d, e); <5 años; ingreso por IRA baja; análisis ajustado invertido para la cotinina en orina (ningún caso sin cotinina tuvo SatO2 baja); ajuste probablemente insuficiente | |||||
| VRS+ vs. VRS- | 19/52 | SatO2 inicial <92% | 11% | OR | 4,47 | 1,27–15,80 | |||
| Cotinina en orina | SatO2 inicial <92% | 33% | OR | 28,3 | 1,3–618,4 | ||||
| Willwerth39 2006 | 691 | H | CR | 2/5 (c, d); <6 meses; ingresados por BA; factores de riesgo de apnea: <1 mes (a términos) <48 semanas posgestacional (pretérminos) o apnea antes del ingreso | |||||
| Factores de riesgo de apnea | Riesgo de apnea | 2,7%¿ | Se 100% | Es 64% | |||||
| Chatzimichael13 2007 | 240 | H | CP | 3/5 (a, c, e); 6–24 meses; peso al nacer >2kg y no tabaco materno en gestación; ingresados por BA VRS+ | |||||
| Lactancia materna <4 meses | Escala RDAI modificada ≥15 pts | 28% | ORa | 6,1 | 3,4–10,7 | ||||
| Exposición a tabaco | Escala RDAI modificada ≥15 pts | 37% | ORa | 2,2 | 1,1–3,6 | ||||
| Fodha40 2007 | 81 | H | CR | 3/5 (a, b, c); <1 año; ingreso por BA VRS+; sin ajuste multivariante; no se encuentran diferencias en función del subtipo de VRS (A o B) ni de la carga viral | |||||
| Prematuridad o bajo peso | Ingreso UCI | 19% | OR | 6,7 | 2,4–18,5 | ||||
| Duración ingreso >7 días | 34% | OR | 4,1 | 1,6–10,9 | |||||
| Edad <28 días al ingreso | Ingreso UCI | 12% | OR | 10,5 | 3,4–32,5 | ||||
| Duración ingreso >7 días | 30% | OR | 4,0 | 1,6–10,0 | |||||
| Simon14 2007 | 406 | H | CP | 4/5 (a, c, d, e); ingresos por infección por VRS de prematuros (cohorte expuesta) y no prematuros (cohorte control); no se identifican en análisis multivariante factores de riesgo de mortalidad. El 11,4% de los prematuros recibieron palivizumab; estudio asistido por Abbott | |||||
| Prematuridad (<37 SG) | Ingreso en UCI | 8% | ORa | 1,73 | 1,08–2,72 | ||||
| Apnea | 7% | ORa | 2,80 | 1,91–4,10 | |||||
| VM | ORa | 4,73 | 1,96–11,94 | ||||||
| Cardiopatía congénita | Ingreso en UCI | ORa | 2,97 | 1,81–4,82 | |||||
| Displasia broncopulmonar | VM | ORa | 5,42 | 2,00–14,17 | |||||
| Richard49 2008 | 88/92 | H | CC | 2/5 (a, e); <1 año; ingresos BA grave en UCI (casos) y corta estancia (controles); estudio financiado por fabricante de técnica de identificación de virus respiratorios (PCR); Escaso papel de la coinfección en relación a otros factores de riesgo. Enfermedad crónica: DBP, cardiopatía o inmunodeficiencia | |||||
| Coinfección vírica (24,4%) | Ingreso en UCI | ORa | 2,7 | 1,2–6,2 | |||||
| Edad <42 días | Ingreso en UCI | ORa | 4,6 | 2,1–10 | |||||
| Prematuridad | Ingreso en UCI | ORa | 7,5 | 3,3–16,6 | |||||
| Enfermedad crónica subyacente | Ingreso en UCI | ORa | 21,6 | 2,4–196 | |||||
| Pacientes ingresados en UCI | |||||||||
| Bont15 2000 | 30 | I | CP | 3/5 (a,c,e); <12 meses; insuficiencia respiratoria con VRS+; IL-12 | |||||
| IL-12 (en cultivo de sangre) | Duración VM | ρ | -0,62 | (p<0,001) | |||||
| Índice ventilatorio medio 1.er día | Duración VM | ρ | 0,47 | (p=0,013) | |||||
| Hanna16 2003 | 130 | I | CP | 2/5 (a, c); lactantes ingresados en UCI por BA VRS+; sodio <136 mmol/l 33%; <130 11% | |||||
| Hiponatremia <130 mmol/l | 10 | Crisis convulsivas | 0% | IA | 40% | ||||
| Eisenhut17 2004 | 54 | I | CP | 2/5 (a, c, e); <7 meses; ingresados en UCIP por insuficiencia respiratoria con VRS+; el diseño no permite valorar el riesgo asociado a transaminasas altas; asociación con cardiopatía congénita (análisis multivariante p<0,01) | |||||
| Transaminasas elevadas | 22/26 | Exitus | 0% | IA | 27,2% | (p<0,01) | |||
| Duración VM (días) | 3,5 | DM | 7,1 | (p<0,01) | |||||
| Cardiopatía congénita | 27% | RR | 3,18 | 1,76–5,74 | |||||
| Kho41 2004 | 236 | I | CR | 2/5 (a, c); <2 años; ingresos en UCI por BA o neumonitis viral; no asociación VRS+ con complicaciones neurológicas | |||||
| VRS+ vs. VRS- | Estancia en UCIP | 2,2 | DM | 1,1 | (p<0,005) | ||||
| Almeida18 2005 | 29 | I | CP | 2/5 (a, c); pacientes <12 meses con BA en UCI con VM; correlación de índice ventilatorio con duración de VM y PaCO2 | |||||
| Índice ventilatorio >37 2.° día | VM >7 días | OR | 6,6 | 1,3–37,2 | |||||
| Chevret42 2005 | 134 | I | CR | Exitus | 3/5 (a, c, e); lactantes ingresados UCIP por BA; No hay ajuste multivariante; el número bajo de exitus no permite valorar la capacidad predictiva de las variables | ||||
| Exitus vs. resto | 4/130 | Edad gestacional (SG) | 38 | DM | -6 | (p=0,006) | |||
| Peso al nacer (g) | 2.930 | DM | -1.405 | (p=0,005) | |||||
| Edad (días) | 44 | DM | 35 | (p=0,046) | |||||
| FiO2 máxima | 40% | DM | 60% | (p=0,003) | |||||
| Flamant43 2005 | 151 | I | CR | 3/5 (a, b, c); <1 año; ingresados en UCIP por insuficiencia respiratoria por infección VRS; no hay variables predictivas de mortalidad | |||||
| DBP | ECMO | 9,2%¿ | ORa | 11,8 | 2,2–63,1 | ||||
| DBP | Duración de VM ≥ 6 días | 51%¿ | ORa | 11,9 | 1,4–100 | ||||
| Edad gestacional <32 SG | Duración de VM ≥ 6 días | 51%¿ | ORa | 4,2 | 1,3–13,7 | RGC: corresponde al riesgo de toda la muestra | |||
| Colonización bacteriana traqueal | Duración de VM ≥ 6 días | 51%¿ | ORa | 3,4 | 1,5–7,7 | ||||
| Oxigenoterapia neonatal | Duración de VM ≥ 6 días | 51%¿ | ORa | 3,4 | 1,2–10,4 | ||||
| Kneyber44 2005 | 82 | I | CR | 3/5 (a, c, d); <12 meses; ingreso UCIP por IRA baja VRS+; infección bacteriana: hemocultivo o aspirado traqueal; efecto paradójico: prematuros menor riesgo infección bacteriana | |||||
| Prematuridad | VM | 11,8% | IA | 41,5% | (p=0,003) | ||||
| Infección pulmonar bacteriana | 41% | IA | 11,8% | (p=0,05) | |||||
| Thorburn19 2006 | 165 | I | CP | 4/5 (a, b, c, d); lactantes ingresados en UCI con VM por BA VRS+; no diferencias en mortalidad | |||||
| Crecimiento bacteriano en LBA | Días de VM (medianas) | 4 | DM | 2 | (p<0,01) | ||||
| Almeida20 2007 | 29 | I | CP | 2/5 (a, c); pacientes <12 meses con BA en UCI con VM; correlación + de Vd/Vt (espacio muerto/volumen corriente) PaCO2 e índice de oxigenación | |||||
| Cociente Vd/Vt | Cociente PaO2/FiO2 <200 | DM | − | (p=0,03) | |||||
| López Guinea45 2007 | 284 | I | CR | 2/5 (a, c); <2 años; ingreso en UCI por BA; factores de riesgo: <6 semanas, prematuridad, enfermedad crónica pulmonar o neurológica u otra, cardiopatía o inmunodeficiencia; mortalidad solo asociada a enfermedad crónica grave previa. No ajuste multivariante | |||||
| Pausas de apnea | VM | 20% | IA | 36% | (p<0,01) | ||||
| Estancia UCI (días) | 4,7 | DM | 1,7 | (p=0,001) | |||||
| RX tórax complicada | VM | 13% | IA | 34% | (p=0,0001) | ||||
| Estancia UCI (días) | 4,1 | DM | 1,9 | (p=0,001) | |||||
| Factores de riesgo | VM | 22% | IA | 38% | (p<0,05) | ||||
| Pacientes ambulatorios/urgencies | |||||||||
| Shaw21 1991 | 213 | U | CP | 3/5 (a, c, e); <13 meses; atendidos en Urgencias por BA; RGC: riesgo global | |||||
| Aspecto tóxico | Ingreso hospitalario | 35%¿ | RR | 4,56 | 2,71–7,69 | ||||
| Edad gestacional <34 | Ingreso hospitalario | 35%¿ | RR | 2,55 | 1,86–3,50 | Análisis disciminante multivariante: aspecto tóxico (Se 76%; Es 76%), edad gestacional <34 semanas (Se 27%; Es 95%), edad <3 meses (Se 38%; Es 83%), FR ≥70 (Se 29%; Es 95%), SatO2 <95% (Se 32%; Es 98%) y atelectasia Rx tórax (Se 21%; Es 98%); validez modelo global: Se 76%; Es 91%; VPP: 81%; VPN 88% | |||
| Edad <3 meses | Ingreso hospitalario | 35%¿ | RR | 1,93 | 1,36–2,74 | ||||
| FR ≥70 | Ingreso hospitalario | 35%¿ | RR | 2,60 | 1,90–3,57 | ||||
| SatO2 <95% | Ingreso hospitalario | 35%¿ | RR | 3,44 | 2,38–4,98 | ||||
| Atelectasia Rx tórax | Ingreso hospitalario | 35%¿ | RR | 2,70 | 1,97–3,70 | ||||
| Kuppermann22 1997 | 156/261 | U | CP | 2/5 (a, c); <24 meses; atendidos en Urgencias por fiebre | |||||
| Fiebre con BA vs. sin BA | Bacteriemia | 5,4% | IA | 1,1% | (p=0,049) | ||||
| Infección urinaria | 13,6% | IA | 1,9% | (p=0,001) | |||||
| Andrade23 1998 | 42 | A | CP | Otitis aguda (Timpanocentesis) | IA | 53% | 3/5 (a, c, d); 2–24 meses; ingresan 50% | ||
| Trefny50 2000 | 99/73 | A | CC | Ingreso vs. ambulatorio | 0/5; <12 meses; infección por VRS (la mayoría bronquiolitis) ingresadas (casos) o ambulatorias (controles); no diferencias riesgo de ingreso por prematuridad o cardiopatía | ||||
| Ingreso vs. ambulatorio | Atopia familiar | 35% | OR | 3,15 | 1,54–6,44 | ||||
| Edad (media) | 6,2 | DM | -1,7 | (p<0,001) | |||||
| Levine56 2004 | 1.248 | U | ET | 4/5 (a, b, c, d); <60 días; atendidos en Urgencias por fiebre; infección bacteriana grave: bacteriemia, ITU, meningitis bacteriana o enteritis bacteriana | |||||
| Fiebre con VRS+ vs. VRS- | Infección bacteriana grave | 12,5% | ORa | 0,58 | 0,33–0,99 | ||||
| Fiebre con BA vs. sin BA | Infección bacteriana grave | 12,5% | OR | 0,53 | 0,28–1,01 | ||||
| Martínez-Baylach51 2004 | 229 | U | CC | 2/5 (a, b); <1 año; atendidos en Urgencias por BA; comparación <4 meses con >8 meses; no ajuste multivariante | |||||
| Edad <4 meses | Ingreso hospitalario | 5,4% | IA | 31,6% | (p<0,001) | ||||
| Ingreso en UCI | 3,6% | IA | 15,8% | (p<0,001) | |||||
| Walsh46,47 2004 | 118 | U | CR | 3/5 (c, d, e); atendidos en Urgencias por BA (la mayoría <2 años); evaluación de predicción de ingreso: muestra derivación (118) y validación (182); RGC: riesgo global en muestra derivación | |||||
| Trabajo respiratorio | Ingreso hospitalario | 69%¿ | ORa | 3,39 | 1,29–8,92 | ||||
| Deshidratación (punto por grado) | Ingreso hospitalario | 69%¿ | ORa | 2,54 | 1,34–4,82 | ||||
| Edad (por cada mes) | Ingreso hospitalario | 69%¿ | ORa | 0,86 | 0,76–0,97 | ||||
| Taquicardia (>percentil 97) | Ingreso hospitalario | 69%¿ | ORa | 3,78 | 1,05–13,57 | Riesgo en muestra validación 24%; validación: Se 91%, Es 60%; ¿corrigiendo por riesgo, Se 91%, Es 83% | |||
| Somech52 2006 | 113/82 | A | CC | Ingreso vs. ambulatorio | 0/5; lactantes ingresados (casos) o ambulatorios (controles) con IRA por VRS; ningún antecedente de riesgo se asoció a ingreso (edad, peso al nacer, edad gestacional, asma familiar, tabaco, guardería, número hermanos); implicación de las variables estudiadas en la decisión de ingreso | ||||
| Ingreso vs. ambulatorio | Escala de Wang (media) | 4,1 | DM | 3,8 | (p<0,001) | ||||
| SatO2 | 97,9 | DM | -5,5 | ||||||
| Auscultación anormal | 9,7% | OR | 29,46 | 12,62–68,79 | |||||
| RX tórax anormal | 34,1% | OR | 25,31 | 10,80–59,31 | |||||
| Fiebre | 34,1% | OR | 13,64 | 6,62–28,08 | |||||
| Voets24 2006 | 378 | U | CP | 2/5 (a, c); 0,5–24 meses; atendidos en Urgencias por BA VRS+ | |||||
| Edad <6 meses | Ingreso hospitalario | 18,8% | RR | 2,70 | 1,98–3,68 | ||||
| FR >45 | Ingreso hospitalario | 14,6% | RR | 4,38 | 3,16–6,06 | ||||
| SatO2 <95% | Ingreso hospitalario | 14,7% | RR | 4,75 | 3,47–6,51 | Validez del modelo (al menos un criterio): Se 86%; Es 91%; CP+ 9,55 | |||
| Al-Shawwa53 2007 | 367 | A | CC | 2/5 (a, b); <2 años; atendidos por BA a nivel ambulatorio; No control de diferencias asociadas a tratamientos recibidos por grupos; RGC: riesgo de ingreso conjunto | |||||
| VRS+ | Ingreso hospitalario | 17% | OR | 5,39 | 2,7–10,6 | ||||
| Exposición a tabaco | Ingreso hospitalario | 17%¿ | OR | 2,39 | 1,2–4,9 | ||||
| Rovira Girabal57 2008 | 127 | U | ET | 4/5 (a, b, d, e); <90 días; atendidos en Urgencias por BA con fiebre (≥38°C); infección orina (4,7%) neumococo en hemocultivo (1,6%); LCR | |||||
| BA febril <28 días vs. 29–90 días | Urocultivo positivo (sonda) | 2,1% | OR | 5,47 | 1,05–28,52 | ||||
| Otros estudios | |||||||||
| Shay58 2001 | 1.806 | P | Ec | 3/5 (a, b, e); registro de mortalidad; en 1997 tasa por 100.000 nacidos vivos asociada a diagnóstico de BA en <5 años 0,65 y <1 año 2,4 | |||||
| Raza negra vs. blanca | Mortalidad/100.000 <1 año | 2,4 | RR | 2,4 | 2,1–2,7 | ||||
| Sexo masculino vs. femenino | Mortalidad/100.000 <1 año | 2,4 | RR | 1,5 | 1,3–1,6 | ||||
| Holman54 2003 | 229/2.336 | P | CC | 4/5 (a, b, c, d); estadísticas de mortalidad asociada a diagnóstico de BA | |||||
| Peso nacer <1.500 | Mortalidad asociada a BA | ORa | 13,9 | 5,2–37 | |||||
| Peso nacer 1.500–2.499g | Mortalidad asociada a BA | ORa | 3,0 | 1,7–5,3 | Otras variables asociadas a mortalidad son 2.° o más hijos vs. 1.°, edad materna <24 años vs. >24 años; educación materna <11 años; estas variables sugieren la existencia de un factor socioeconómico no controlado | ||||
| Apgar 5min 0–7 | Mortalidad asociada a BA | ORa | 4,5 | 2,1–9,6 | |||||
| Tabaco en gestación | Mortalidad asociada a BA | ORa | 1,6 | 1,0–2,6 | |||||
| Struck55 2004 | 91 | H/U | CC | 3/5 (c, d, e); <3 años; IRA baja por VRS subgrupo A ambulatorios o ingresados; gravedad por grupos neumonía o SatO2 <91 | |||||
| VRS subgrupo A; conglomerado 2 vs. 3 del gen de la proteína C | 35/21 | Gravedad (neumonía o SatO2<91) | 26%¿ | OR | 7 | 1,6–49 | |||
A: ambulatorio; BA: bronquiolitis aguda; CC: casos y controles; CCI: coeficiente de correlación intraclase; CIE: códigos de la clasificación internacional de enfermedades; CP: cohortes; CR: cohortes retrospectivo; E: entorno asistencial; Ec: estudio ecológico; ECA: ensayo clínico aleatorizado; EE: estimador de efecto; EPC: enfermedad pulmonar crónica; ET: estudio transversal; D: diseño epidemiológico; DBP: displasia broncopulmonar; DM: diferencia de medias; DMa: DM ajustada; DP: diferencia de porcentajes; H: hospital; I: cuidados intensivos; IA: incidencia acumulada; IRA: infección respiratoria aguda; K: kappa; Kp: kappa ponderado; LBA: lavado broncoalveolar; MPV: metapneumovirus; N (CE/CC): tamaño muestral (cohorte expuesta o casos / cohorte control o controles); ns: no significativo; P: poblacional; PCR: reacción en cadena de la polimerasa; RDAI: Respiratory Distress Assessment Instrument; RDI: razón de densidades de incidencia; RGC: riesgo grupo control; SG: semanas de gestación; U: servicio de Urgencias; VM: ventilación mecánica; VRS: virus respiratorio sincitial; β: coeficiente de regresión; ρ: coeficiente de correlación.
Los tamaños muestrales de los estudios con población ingresada, de Urgencias o ambulatoria son relativamente amplios (mediana 255) y mayores que los trabajos con pacientes de UCI (mediana 106).
Las medidas de efecto más empleadas son el ingreso hospitalario (para pacientes ambulatorios o de Urgencias), el ingreso en UCI, la estancia hospitalaria y la saturación (SatO2) o necesidad de oxígeno (para pacientes ingresados). Otras medidas utilizadas han sido la aparición de apneas, otras complicaciones y escalas clínicas de gravedad. Para pacientes de UCI, la necesidad o duración de la VM, la estancia en UCI y la mortalidad. Algunos trabajos han evaluado el riesgo de infección bacteriana asociado a formas de BA febriles22,56,57.
En cuanto a los factores pronósticos evaluados, podemos distinguir los factores de riesgo existentes antes de la aparición de la BA y las variables clínicas presentes al diagnóstico, que se asocian a gravedad e influyen en la toma de decisiones (y por lo tanto modifican directamente las medidas de efecto), que podemos utilizarlas como marcadores de gravedad. De los factores de riesgo destacamos: prematuridad, edad (menor de 1–6 meses), enfermedad pulmonar crónica (EPC), displasia broncopulmonar (DBP), antecedente de VM neonatal, cardiopatías congénitas, otras enfermedades crónicas (fibrosis quística, neuromusculares, malformaciones, inmunodeficiencias), raza, malnutrición y exposición a tabaco. De las variables clínicas señalamos: apneas, hipoxia (SatO2), infiltrados o atelectasias pulmonares, FR alta, taquicardia, fiebre, rechazo de tomas o vómitos, trabajo respiratorio aumentado, virus implicado (VRS, subtipos, coinfecciones víricas), coinfecciones bacterianas e índices ventilatorios (en pacientes con VM).
Un trabajo ha realizado una revisión sistemática de modelos predictivos de gravedad publicados y los ha tratado de validar en una cohorte de pacientes ingresados con IRA baja por VRS 2. Otra revisión sistemática cualitativa describe la frecuencia de complicaciones extrapulmonares en pacientes con BA59, y 2 estudios evalúan el riesgo de crisis convulsivas y otras encefalopatías en niños ingresados por BA por VRS60,61.
Consistencia entre estudiosAlgunos factores de riesgo se muestran asociados a gravedad en la mayoría de los trabajos analizados, principalmente prematuridad, cardiopatía congénita, enfermedad crónica previa (sobre todo EPC o DBP) y edad menor de 3–6 meses, aunque las diferencias metodológicas y en el análisis originan que las estimaciones de riesgo sean cuantitativamente heterogéneas. Ello se debe a que los trabajos emplean muestras de pacientes diferentes, con distintos riesgos basales (por ejemplo el riesgo de ingreso en UCI entre pacientes hospitalizados varía entre estudios desde un 3–19%) con procedimientos de análisis diferentes (inclusión o no de determinadas variables) y empleando criterios variados en la definición de las variables (por ejemplo distintos puntos de corte para edad o grado de prematuridad). Así, observamos que variables de riesgo como la prematuridad pueden quedar confundidas bajo el peso de otros factores asociados como la EPC o la edad baja al diagnóstico.
De las variables clínicas, las más consistentes son la SatO2, la FR y el trabajo respiratorio. No obstante, la incorporación de muchas de estas variables en protocolos clínicos o como variables clasificadoras de la gravedad, distorsiona la estimación de riesgos y origina variabilidad. La presencia de infiltrados o atelectasias en la Rx de tórax y el rechazo de tomas solo han sido evaluadas en algunos estudios, por lo que no se puede valorar su consistencia.
Estimación de sesgosNo podemos descartar que en algunos trabajos se haya incurrido en sesgos de selección, por la inclusión de pacientes con sibilantes recurrentes o IRA de vías bajas sin criterios claros de BA. Otra cuestión que podría afectar a la validez externa de los resultados es que, en muchos estudios, el criterio de selección de pacientes era la identificación de VRS en las secreciones respiratorias, que ha podido sesgar la inclusión de pacientes. Aunque este posible sesgo ha podido influir en la magnitud de los riesgos observados, no parece que cuestione el papel de los principales factores de riesgo observados.
Ha podido tener una mayor repercusión la falta de control multivariante de importantes covariables en muchos estudios, que haya impedido identificar fenómenos de confusión o interacción. Otro aspecto a tener en cuenta es el hecho de que, por el diseño de los estudios (la mayoría cohortes o casos y controles) no se han podido enmascarar los factores de riesgo a evaluar, por lo que habrán sido considerados en la toma de decisiones (como el ingreso hospitalario, la prolongación de la estancia o el ingreso en UCI) e influido en las estimaciones de riesgo.
Precisión de las estimacionesLos tamaños muestrales de los estudios revisados ofrecen una suficiente potencia estadística y precisión de las estimaciones de riesgo de ingreso en UCI, ingreso hospitalario o prolongación de la estancia. No obstante para algunos factores de riesgo, los intervalos de confianza son extremadamente amplios, en relación a escasos recuentos de eventos encontrados. Por la misma razón, no contamos con estimaciones precisas de riesgo de muerte, ni para factores de riesgo ni para marcadores de gravedad.
Intensidad del efecto o fuerza de la asociaciónUna revisión sistemática antigua buscó modelos predictivos de gravedad publicados2, encontrando 2 modelos predictivos, el de Green (que incluye SatO2 y edad) para ingreso en UCI y el de McConochie (que incluye subtipo de VRS, edad <3 meses, factores de riesgo y prematuridad) para alta puntuación en una escala combinada de gravedad; asimismo, identificó 4 variables con capacidad predictiva independiente de ingreso en UCI (prematuridad y cardiopatía) o de estancia prolongada (edad ≤4 meses y factores de riesgo). Estas variables y modelos predictivos los trataron de validar en una cohorte de pacientes ingresados con IRA baja por VRS, encontrando una limitada capacidad predictiva. El modelo de Green mostró una sensibilidad y especificidad del 98–47%, mientras que el de McConochie una sensibilidad del 77% y especificidad del 76%. Con las variables individuales se obtuvieron peores estimadores de validez.
Otros 4 estudios han estimado la validez de distintas variables o modelos predictivos21,24,39,46,47. Una serie de criterios de riesgo de apnea (edad menor de un mes o <48 semanas postgestacional en pretérminos y/o la observación de apneas antes del ingreso) mostraron una alta sensibilidad (100%) para la aparición de apneas durante el ingreso, aunque con una especificidad del 64%39. Para pacientes atendidos en Urgencias, se ha evaluado en 3 estudios21,24,46,47 la validez de otros tantos modelos predictivos de ingreso hospitalario, 2 de ellos con ajuste multivariante21,46,47. Las variables incluidas en los modelos fueron: edad (<3 o 6 meses) y prematuridad (<34 semanas), como factores de riesgo, y aspecto tóxico, taquipnea (>45 o >70), SatO2 <95%, deshidratación, taquicardia, y presencia de atelectasia en la Rx de tórax, como marcadores de gravedad, con estimadores de riesgo individuales, RR u OR entre 2–4,75. Globalmente los modelos tenían sensibilidades entre el 76–91% y especificidades entre el 60–91% (cocientes de probabilidades positivos entre 2,28–9,56 y negativos entre 0,15–0,26). La traducción a la toma de decisiones de estos indicadores de validez supone que si bien estas variables permiten mejorar nuestras estimaciones subjetivas de gravedad, ninguna de ellas tiene capacidad predictiva suficiente como para conformar criterios estrictos de ingreso.
Para la predicción de ingreso en UCI de pacientes hospitalizados, se ha estimado que los prematuros8,14,25,26,33,40,49,62 tienen un riesgo (RR u OR) entre 1,6–7,5 veces superior. No obstante, de la información disponible no puede extraerse que dicho riesgo sea totalmente independiente de otros factores y que aumente al disminuir la edad gestacional33. También se ha observado un efecto significativo de la prematuridad sobre la estancia hospitalaria25,26,37,38,40,63, con OR ajustadas para ingresos prolongados en torno a 2,5 y diferencias de medias entre 0,15–4 días.
La cardiopatía congénita también constituye un factor de riesgo observado en diversos estudios3,8,10,25,26,28,34, aunque existe una gran variabilidad en las estimaciones de riesgo, tanto para el ingreso en UCI (riesgo entre 2,7–10 veces mayor), como para la estancia hospitalaria prolongada (riesgo entre 4–8 veces mayor), los días de estancia y la necesidad de oxígeno. La información disponible en los estudios revisados no permite diferenciar el riesgo global del de las cardiopatías hemodinámicamente significativas.
Las BA que tienen lugar en los primeros meses de vida presentan también mayor riesgo de ingreso en UCI o estancia hospitalaria prolongada3,8,26,28,29,33,38,40,49,62; sin embargo resulta arriesgado resumir el riesgo asociado (de 1,6–10 veces mayor), ya que los distintos estudios han utilizado puntos de corte de edad diferentes (de 1–6 meses) o calculado el riesgo atribuible por días, semanas o meses. Parece asumible que una edad menor de 6 semanas o 3 meses es un claro factor de riesgo de gravedad.
Otros factores como la presencia de una EPC o displasia broncopulmonar3,8,14,25,35,49 también se asocian a riesgo elevado de ingreso en UCI, necesidad de VM o estancia prolongada (entre 2,3–5 veces mayor). Otras enfermedades crónicas34,35,37,62 (neuromusculares, cromosomopatías, inmunodeficiencias, anomalías congénitas), la raza (india vs otras3, blanca vs otras11), el antecedente de VM neonatal26, la lactancia materna durante menos de 4 meses13 y la coinfección vírica49. En 2 estudios la exposición a tabaco se ha asociado a menor SatO2 y mayor puntuación en escalas clínicas de gravedad12,13.
La evidencia disponible sobre el papel de los marcadores clínicos de gravedad procede sobre todo de estudios en pacientes atendidos en Urgencias, en relación al riesgo de ingreso, y, en menor grado, de estudios con casos hospitalizados en relación a duración de la estancia o escalas clínicas de gravedad. Así, son marcadores de riesgo de ingreso hospitalario, estancia hospitalaria prolongada o puntuaciones clínicas de mayor gravedad: el aspecto tóxico21, la FR elevada21,24, la SatO2 <95%21,24,52, la presencia de atelectasia o infiltrado en la RX de tórax21,52, el trabajo respiratorio46,47, el grado de hidratación46,47, la taquicardia46,47 y la fiebre52. La presencia de estos marcadores incrementan el riesgo de ingreso de forma individual entre 2–4 veces; si bien en algún estudio variables como la presencia de fiebre o hallazgos en la RX de tórax se han visto fuertemente asociadas a la decisión de ingreso. También se ha asociado a ingreso hospitalario la edad del paciente24,46,47,50,51 (<4–6 meses), la exposición a tabaco53, el antecedente de atopia familiar50 y la etiología por VRS53, aunque estas 3 últimas variables pueden mostrar el efecto de otros factores de confusión no controlados. En estudios con pacientes hospitalizados la estancia y mayores puntuaciones en las escalas de gravedad se han asociado a la SatO2 al ingreso, el trabajo respiratorio, los vómitos, el rechazo de tomas, la presencia de infiltrados en la RX de tórax y la fiebre3,5,9,27,37,38.
Los estudios realizados con pacientes de UCI, han mostrado que los casos con factores de riesgo como la prematuridad o la DBP, solo representan un pequeño porcentaje del conjunto de pacientes atendidos en UCI. No obstante, ambos factores se asocian a mayor riesgo de VM44 o estancias prolongadas43,45, fundamentalmente el antecedente de DBP (riesgo 10 veces mayor). Otros indicadores de riesgo a tener en cuenta son la etiología por VRS (probablemente por su asociación con menor edad)41, la colonización bacteriana traqueal19,43 y la presencia de pausas de apnea45, los parámetros ventilatorios15,20 y las Rx de tórax patológicas45. Las estimaciones de riesgo de mortalidad en estos estudios vienen limitadas por el escaso número de exitus encontrados.
Se han documentado frecuencias de complicaciones extrapulmonares en pacientes con BA59, destacando problemas cardiacos: miocarditis (el 35–54% de lactantes ventilados), arritmias-bloqueo cardíaco, taquicardia auricular, supraventricular y ventricular, flutter auricular, fibrilación ventricular y taponamiento cardíaco; neurológicos: apneas centrales (el 16–21% de los ingresos), convulsiones generalizadas y parciales, status epiléptico y letargia; endocrino-metabólicos: hiponatremia (el 33% de ingresados en UCI), aumento de transaminasas (en el 80% de las cardiopatías congénitas y el 46–49% de los lactantes ventilados) y síndrome de Reye. Se ha estimado un riesgo de crisis convulsivas en un intervalo entre el 0,7–1,8%60,61. En pacientes ingresados en UCI el hallazgo de hiponatremia se asocia a riesgo de crisis convulsivas16 y el nivel de transaminasas a mayor gravedad17.
El riesgo de infección bacteriana asociada a formas febriles de BA parece bajo22,56,57, habiéndose estimado que en lactantes de menos de 3 meses con fiebre, tanto el diagnóstico de BA como la identificación de VRS disminuyen el riesgo de encontrar una infección bacteriana asociada, cuando a estos pacientes se les hacía cribado de infección bacteriana.
Finalmente, se han realizado estimaciones de mortalidad asociada a BA en estudios de base poblacional, encontrando diferencias asociadas a la prematuridad y a variables relacionadas con factores socioeconómicos, que carecen de interés clínico54,58.
Grado de relación con la pregunta clínicaPodemos considerar que la evidencia existente es indirecta, debido fundamentalmente a la falta de enmascaramiento en la valoración de los factores de riesgo, la frecuente ausencia de control multivariante y la limitada correlación clínica de algunas medidas de efecto. Si bien existen algunas medidas de efecto que pueden ser consideradas robustas, como la necesidad de VM, otras variables como la decisión de ingreso o la prolongación de la estancia hospitalaria encierran cierto grado de subjetividad y variabilidad, pudiendo no reflejarse en beneficios claros para el paciente.
Validez externa y aplicabilidad de la evidenciaPodemos considerar que los pacientes atendidos en nuestro medio son similares a los incluidos en los estudios publicados. De hecho algunos de ellos han sido realizados en España, en centros de diferente nivel asistencial. De igual manera, la medición de los factores de riesgo y marcadores de gravedad evaluados parecen reproducibles y aplicables en nuestro entorno. No obstante, existen algunas dudas sobre si algunas de las medidas de efecto consideradas (ingreso o estancia hospitalaria) son trasladables de unos sistemas sanitarios a otros o incluso entre centros del mismo sistema.
Balance riesgo-beneficio-costeNo existe información sobre la relación coste-beneficio de la consideración de los factores de riesgo o marcadores de gravedad encontrados.
Estimación del impacto de futuros estudiosConsiderando las limitaciones metodológicas planteadas y, especialmente, la variabilidad en la toma de decisiones entre sistemas o centros sanitarios, parecen necesarios más estudios epidemiológicos en nuestro medio que evalúen los factores pronósticos encontrados con ajuste multivariante, considerando variables robustas de efecto y el potencial beneficio para los pacientes. Interesa especialmente diseñar y validar modelos predictivos que incluyan las principales variables identificadas y evaluar mediante estudios experimentales el impacto de su implantación.
Escalas de valoración de síntomas o gravedad en la BAEn el manejo de los niños con BA, los pacientes pueden ser evaluados en numerosas ocasiones por diferente personal y en entornos asistenciales distintos. Cada evaluador puede dedicar más o menos atención a distintos aspectos del examen clínico y valorar en mayor o menor grado su contribución al estado del paciente. La utilización de herramientas estandarizadas de valoración podría mejorar los cuidados del paciente, al homogeneizar los criterios a emplear en la toma de decisiones diagnósticas o terapéuticas, como la indicación de exploraciones complementarias, el inicio, modificación o retirada de tratamientos, la decisión de ingreso o alta hospitalaria, etc. Para ello necesitamos escalas de valoración de síntomas o signos que sean válidas y reproducibles e, idealmente, que hayan demostrado su impacto en la práctica clínica diaria.
La evidencia sobre la validez y reproducibilidad de escalas de valoración síntomas o gravedad procederá de estudios con la metodología propia de la evaluación de pruebas diagnósticas o reglas de predicción clínica.
Para evaluar la precisión y reproducibilidad deben realizarse mediciones repetidas e independientes de los parámetros a evaluar, en muestras de pacientes representativas, empleando procedimientos y criterios explícitos. La precisión de las escalas se estimará a partir del grado de acuerdo o correlación observados, una vez descontado el debido al azar (índices Kappa, coeficientes de correlación intraclase, etc.).
Para evaluar la validez de una escala se necesita contrastar sus resultados, de forma independiente, con los de un patrón de referencia de gravedad o evolución que sea objetivo y válido. La validez de una escala se estimará a partir de los indicadores de validez (sensibilidad, especificidad, cocientes de probabilidades, etc.) para resultados cualitativos, o del grado de correlación, para resultados cuantitativos. Si no se disponen de patrones de referencia adecuados, deberá valorarse el comportamiento de la escala con el de otros parámetros asociados con gravedad o evolución.
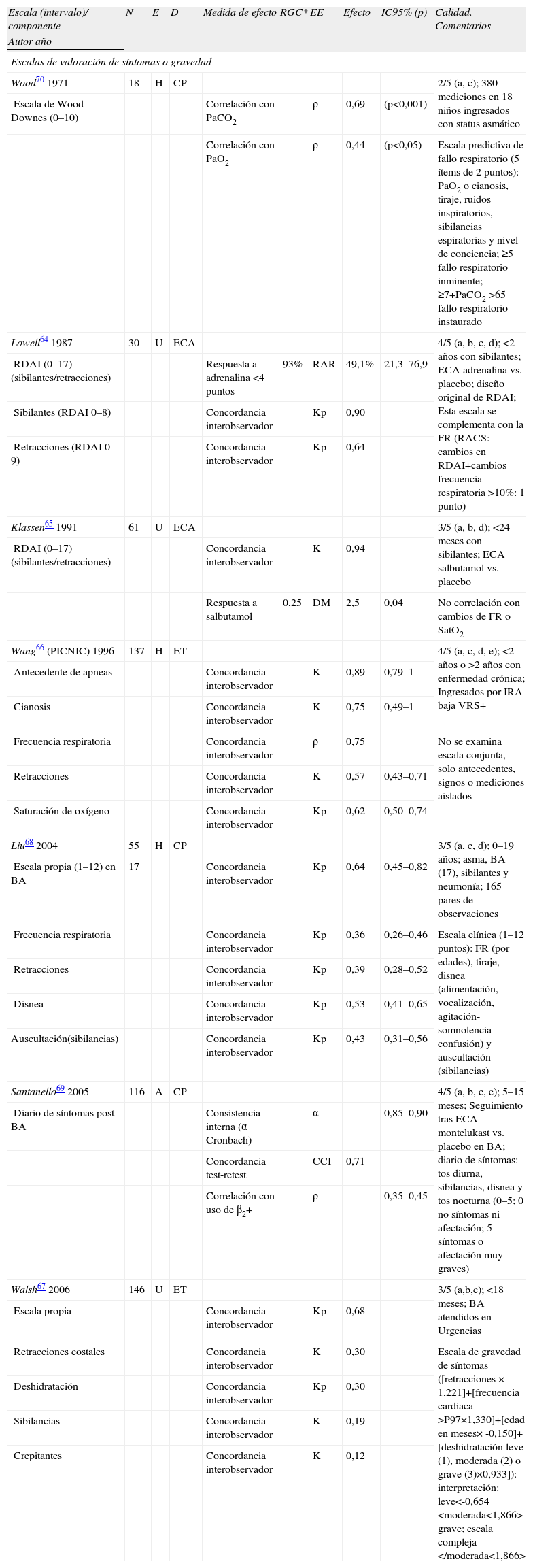
Volumen de la evidenciaEn 6 estudios se analiza la concordancia interobservador o test-retest de diversas escalas de puntuación de síntomas o signos o de sus componentes por separado, en muestras de pacientes con BA, IRA baja por VRS o sibilantes del lactante64–69. En 3 de estos estudios se analiza además la correlación de las escalas con la respuesta a broncodilatadores o la frecuencia de su uso64,65,69. En la tabla 2 se presentan las principales características y resultados de los estudios. La calidad de los estudios queda limitada fundamentalmente por sus escasos tamaños muestrales. Aunque el diseño epidemiológico es variado (ensayos clínicos, estudios de cohortes y transversales), los análisis de concordancia se limitan a mediciones repetidas de carácter transversal.
Tabla simplificada de evidencias sobre escalas de valoración de síntomas o gravedad
| Escala (intervalo)/ componente | N | E | D | Medida de efecto | RGC* | EE | Efecto | IC95% (p) | Calidad. Comentarios |
| Autor año | |||||||||
| Escalas de valoración de síntomas o gravedad | |||||||||
| Wood70 1971 | 18 | H | CP | 2/5 (a, c); 380 mediciones en 18 niños ingresados con status asmático | |||||
| Escala de Wood-Downes (0–10) | Correlación con PaCO2 | ρ | 0,69 | (p<0,001) | |||||
| Correlación con PaO2 | ρ | 0,44 | (p<0,05) | Escala predictiva de fallo respiratorio (5 ítems de 2 puntos): PaO2 o cianosis, tiraje, ruidos inspiratorios, sibilancias espiratorias y nivel de conciencia; ≥5 fallo respiratorio inminente; ≥7+PaCO2 >65 fallo respiratorio instaurado | |||||
| Lowell64 1987 | 30 | U | ECA | 4/5 (a, b, c, d); <2 años con sibilantes; ECA adrenalina vs. placebo; diseño original de RDAI; Esta escala se complementa con la FR (RACS: cambios en RDAI+cambios frecuencia respiratoria >10%: 1 punto) | |||||
| RDAI (0–17) (sibilantes/retracciones) | Respuesta a adrenalina <4 puntos | 93% | RAR | 49,1% | 21,3–76,9 | ||||
| Sibilantes (RDAI 0–8) | Concordancia interobservador | Kp | 0,90 | ||||||
| Retracciones (RDAI 0–9) | Concordancia interobservador | Kp | 0,64 | ||||||
| Klassen65 1991 | 61 | U | ECA | 3/5 (a, b, d); <24 meses con sibilantes; ECA salbutamol vs. placebo | |||||
| RDAI (0–17) (sibilantes/retracciones) | Concordancia interobservador | K | 0,94 | ||||||
| Respuesta a salbutamol | 0,25 | DM | 2,5 | 0,04 | No correlación con cambios de FR o SatO2 | ||||
| Wang66 (PICNIC) 1996 | 137 | H | ET | 4/5 (a, c, d, e); <2 años o >2 años con enfermedad crónica; Ingresados por IRA baja VRS+ | |||||
| Antecedente de apneas | Concordancia interobservador | K | 0,89 | 0,79–1 | |||||
| Cianosis | Concordancia interobservador | K | 0,75 | 0,49–1 | |||||
| Frecuencia respiratoria | Concordancia interobservador | ρ | 0,75 | No se examina escala conjunta, solo antecedentes, signos o mediciones aislados | |||||
| Retracciones | Concordancia interobservador | K | 0,57 | 0,43–0,71 | |||||
| Saturación de oxígeno | Concordancia interobservador | Kp | 0,62 | 0,50–0,74 | |||||
| Liu68 2004 | 55 | H | CP | 3/5 (a, c, d); 0–19 años; asma, BA (17), sibilantes y neumonía; 165 pares de observaciones | |||||
| Escala propia (1–12) en BA | 17 | Concordancia interobservador | Kp | 0,64 | 0,45–0,82 | ||||
| Frecuencia respiratoria | Concordancia interobservador | Kp | 0,36 | 0,26–0,46 | Escala clínica (1–12 puntos): FR (por edades), tiraje, disnea (alimentación, vocalización, agitación-somnolencia-confusión) y auscultación (sibilancias) | ||||
| Retracciones | Concordancia interobservador | Kp | 0,39 | 0,28–0,52 | |||||
| Disnea | Concordancia interobservador | Kp | 0,53 | 0,41–0,65 | |||||
| Auscultación(sibilancias) | Concordancia interobservador | Kp | 0,43 | 0,31–0,56 | |||||
| Santanello69 2005 | 116 | A | CP | 4/5 (a, b, c, e); 5–15 meses; Seguimiento tras ECA montelukast vs. placebo en BA; diario de síntomas: tos diurna, sibilancias, disnea y tos nocturna (0–5; 0 no síntomas ni afectación; 5 síntomas o afectación muy graves) | |||||
| Diario de síntomas post-BA | Consistencia interna (α Cronbach) | α | 0,85–0,90 | ||||||
| Concordancia test-retest | CCI | 0,71 | |||||||
| Correlación con uso de β2+ | ρ | 0,35–0,45 | |||||||
| Walsh67 2006 | 146 | U | ET | 3/5 (a,b,c); <18 meses; BA atendidos en Urgencias | |||||
| Escala propia | Concordancia interobservador | Kp | 0,68 | ||||||
| Retracciones costales | Concordancia interobservador | K | 0,30 | Escala de gravedad de síntomas ([retracciones × 1,221]+[frecuencia cardiaca >P97×1,330]+[edad en meses× -0,150]+[deshidratación leve (1), moderada (2) o grave (3)×0,933]): interpretación: leve<-0,654 | |||||
| Deshidratación | Concordancia interobservador | Kp | 0,30 | ||||||
| Sibilancias | Concordancia interobservador | K | 0,19 | ||||||
| Crepitantes | Concordancia interobservador | K | 0,12 | ||||||
A: ambulatorio; BA: bronquiolitis aguda; CC: casos y controles; CCI: coeficiente de correlación intraclase; CIE: códigos de la clasificación internacional de enfermedades; CP: cohortes; CR: cohortes retrospectivo; E: entorno asistencial; Ec: estudio ecológico; ECA: ensayo clínico aleatorizado; EE: estimador de efecto; EPC: enfermedad pulmonar crónica; ET: estudio transversal; D: diseño epidemiológico; DBP: displasia broncopulmonar; DM: diferencia de medias; DMa: DM ajustada; DP: diferencia de porcentajes; H: hospital; I: cuidados intensivos; IA: incidencia acumulada; IRA: infección respiratoria aguda; K: kappa; Kp: kappa ponderado; LBA: lavado broncoalveolar; MPV: metapneumovirus; N (CE/CC): tamaño muestral (cohorte expuesta o casos / cohorte control o controles); ns: no significativo; P: poblacional; PCR: reacción en cadena de la polimerasa; RDAI: Respiratory Distress Assessment Instrument; RDI: razón de densidades de incidencia; RGC: riesgo grupo control; SG: semanas de gestación; U: servicio de Urgencias; VM: ventilación mecánica; VRS: virus respiratorio sincitial; β: coeficiente de regresión; ρ: coeficiente de correlación.
No hemos encontrado estudios de evaluación de herramientas inicialmente descritas para pacientes con asma, que son frecuentemente empleadas en BA70–72. En el estudio original de la escala de Woods-Downes se evaluó su correlación con parámetros gasométricos de compromiso respiratorio70.
Algunas de estas escalas y otras empleadas en nuestro medio han sido utilizadas como medidas de efecto en estudios sobre factores pronósticos de BA (ver tablas correspondientes)7,9,13,21,27,38,52,57, ofreciendo, algunos de los trabajos, información sobre diferencias de puntuación entre pacientes ingresados y ambulatorios o entre pacientes con estancias cortas o prolongadas21,38,52.
No contamos con estudios que hayan demostrado la eficacia o impacto clínico del uso de estas escalas en pacientes con BA.
Consistencia entre estudiosLos componentes de las escalas varían entre estudios. Los más habituales son la presencia de sibilantes, retracciones torácicas o tiraje; otros componentes habituales son: los signos de disnea, los ruidos inspiratorios, la tos diurna o nocturna, la frecuencia respiratoria, la frecuencia cardíaca, la cianosis, la edad y los signos de deshidratación. Otros síntomas o signos evaluados de forma aislada han sido el antecedente de apneas y la auscultación de crepitantes. Con respecto a variables incorporadas a otras escalas empleadas en nuestro medio, además de las anteriormente mencionadas se han incluido la entrada de aire, el aleteo, la saturación de oxígeno y parámetros de la gasometría7,9,27,38,57.
Las estimaciones de concordancia de los sibilantes o retracciones son algo heterogéneas, lo que podría deberse a la diferencia de criterios en la interpretación de dichas variables. Así, mientras que en la escala Respiratory Distress Assessment Instrument (RDAI) las retracciones se desglosan en un intervalo de 0–9 puntos64,65, en otras escalas adoptan categorías exclusivamente dicotómicas67.
Estimación de sesgosLa mayoría de los trabajos no refieren mecanismos de enmascaramiento en las mediciones repetidas de los parámetros incluidos en las escalas, lo que podría haber influido en los resultados. La inclusión en algunos trabajos de pacientes sin diagnóstico de BA (cuadros de sibilantes recurrentes) o con formas clínicas más graves, puede comprometer la aplicabilidad de los resultados.
Precisión de las estimacionesLa precisión de las estimaciones de concordancia o correlación resulta escasa en relación al reducido tamaño de las muestras en las que se han evaluado.
Intensidad del efecto o fuerza de la asociaciónLa concordancia interobservador que reflejan las escalas evaluadas en conjunto puede catalogarse de «buena» (índices Kappa entre 0,60–0,80).
Analizando por separado los principales componentes de estas escalas, sibilantes y retracciones torácicas, observamos que la concordancia desciende a moderada (índices Kappa entre 0,40–0,60) o incluso baja (índice Kappa entre 0,20–0,40), siendo más alta para los sibilantes64,68 que para las retracciones torácicas, con alguna excepción67. Es posible que la concordancia de estos parámetros varíe en función del nivel de detalle de los criterios de interpretación, aunque las diferencias observadas entre los estudios podrían explicarse por la escasa precisión de sus resultados.
También se han evaluado los siguientes componentes de escalas: signos de disnea68,69 (rechazo de tomas, no vocalización, agitación-somnolencia-confusión), ruidos inspiratorios70, tos diurna o nocturna69, frecuencia respiratoria64–66,68, frecuencia cardiaca67, cianosis70, edad67 y deshidratación67. Otros síntomas o signos evaluados de forma aislada han sido el antecedente de apneas66 y la auscultación de crepitantes67. Todos estos síntomas o signos han mostrado por separado índices de concordancia de moderados a buenos con alguna excepción67.
La escala RDAI, que recoge distintos grados de sibilantes y retracciones, una de las más empleadas en ensayos clínicos, ha reflejado índices de concordancia muy buenos (Kappa 0,90 y 0,94)64,65. No obstante, aunque parece correlacionarse con la respuesta a tratamientos, no necesariamente refleja cambios en otros parámetros de interés clínico como la frecuencia respiratoria o la saturación de oxígeno65. Por ello, dichas variables deberían controlarse de forma independiente o en combinación con las anteriores. Si se analizan los ensayos clínicos que han utilizan esta escala (ver tabla correspondiente), no sorprende encontrar discordancias entre los resultados medidos con la RDAI y los medidos con otros parámetros o eventos de interés clínico (ingresos, complicaciones, etc.).
Las escalas de Liu68 y Walsh67 han presentado concordancias buenas (Kappa 0,64 y 0,68), aunque la de Walsh resulta compleja por requerir cálculos matemáticos. Un diario de síntomas69, diseñado para el seguimiento de pacientes con BA, parece tener una buena consistencia interna y una buena reproducibilidad (correlación test-retest 0,71), pero una moderada correlación con la frecuencia de uso de broncodilatadores o la estimación de días libres de síntomas.
La escala de Wood-Downes70, diseñada inicialmente para predecir el fallo respiratorio en pacientes con status asmático, y que es frecuentemente empleada en su versión original o en versiones adaptadas72, tiene una correlación buena (0,69) con la PaCO2 y moderada con la PaO2 (0,44).
Las puntuaciones de otras escalas empleadas en estudios de factores pronósticos de gravedad (ver tablas correspondientes) varían significativamente entre los pacientes ingresados y ambulatorios y entre los pacientes con estancias cortas o prolongadas21,38,52, aunque los resultados ofrecidos no permiten juzgar su validez. No obstante, la mayoría de las variables incluidas en dichas escalas forman parte de las escalas clásicas.
Grado de relación con la pregunta clínicaPodemos considerar que la evidencia disponible sobre la concordancia de las escalas, síntomas y signos de BA, es de tipo indirecto. Solo una parte de los pacientes incluidos en los estudios realizados representan al conjunto de BA. Por otra parte carecemos de trabajos en los que se haya evaluado la eficacia y el impacto de la utilización de estas escalas.
Validez externa y aplicabilidad de la evidenciaLa inclusión en algunos trabajos de pacientes sin diagnóstico de BA (cuadros de sibilantes recurrentes) o con formas clínicas más graves puede comprometer la aplicabilidad de los resultados a la práctica clínica. Aunque las escalas, síntomas y signos propuestos para la valoración de la gravedad o evolución de los pacientes son relativamente precisos, no tenemos suficiente información sobre su validez y, especialmente, su eficacia y utilidad.
No obstante, parece que es necesario emplear alguna escala de recogida de síntomas o signos en la valoración y seguimiento de los pacientes con BA. Aunque el grado de detalle en la recogida de síntomas o signos (extensión, intensidad y localización de retracciones o sibilantes) podría relacionarse con su precisión, no existe información sobre la mayor eficacia y utilidad clínica de las escalas más complejas. En todo caso, en los pacientes con compromiso respiratorio, estas escalas podrían no reflejar todo su nivel de hipoxia o desaturación.
Balance riesgo-beneficio-costeNo existe información que permita valorar la relación coste-beneficio de la utilización de estas escalas.
Estimación del impacto de futuros estudiosConsiderando la amplia aceptación de algunas de las escalas disponibles, parece necesario evaluar su concordancia, pero además su validez con respecto a parámetros objetivos y su impacto clínico en muestras amplias de pacientes con BA, empleando mecanismos de enmascaramiento en su recogida e interpretación. Los resultados de estos estudios permitirían seleccionar la escala más apropiada para cada entorno asistencial.
Riesgo de asma posbronquiolitisLa información sobre el riesgo de asma postbronquolitis debe idealmente proceder de estudios de cohortes con pacientes que han presentado BA, identificadas con criterios clínicos claros y explícitos, a los que se siga de forma completa y suficiente, para medir la aparición de síntomas relacionados con el asma y se les clasifique con criterios válidos, en función de su frecuencia e intensidad.
Para establecer si la BA es un factor de riesgo independiente de asma o sibilantes recurrentes, se requieren estudios de estudios cohortes amplias de recién nacidos, en los que se valore el riesgo basal y el atribuible a la aparición de una BA. En estos estudios se deberían emplear criterios explícitos y válidos de BA, seguimientos prolongados y completos y medidas de efecto que valoren el riesgo de asma de forma independiente, adecuada y precisa. Puede considerarse también la información de cohortes de pacientes expuestos a BA que se comparen con pacientes no expuestos, en los que se pueda controlar y ajustar la influencia de otras covariables de riesgo de asma.
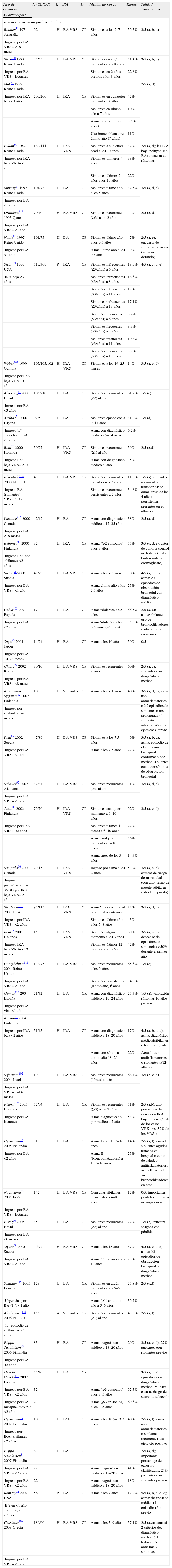
Volumen de la evidenciaTreinta y dos estudios de cohortes prospectivos73–104 y 11 retrospectivos105–115 han estimado la frecuencia de sibilantes recurrentes o asma en pacientes con antecedente de ingreso por BA o IRA baja. Solo en 4 estudios la exposición de riesgo comprendía episodios sin hospitalización92,103,105,115. En la tabla 3 se presentan las principales características y resultados de estos estudios. En la mayoría de los trabajos los pacientes eran niños menores de 1 o 2 años sin criterios de inclusión de riesgo, en uno eran niños prematuros96 y en otro hijos de padres atópicos92. En 20 trabajos las muestras incluían una selección de casos por VRS75–77,80,85,87,91,94,96–102,104,107,108,111,114, y en otros 2 estudios BA por metapneumovirus110 u otros virus88. Solo excepcionalmente se especificó que los ingresos fueron por primeros episodios de sibilantes74,105. Los tamaños muestrales eran la mayoría inferiores a 100 casos, con alguna excepción73,76,83,84,86,91,96,104,107,111; las muestras eran especialmente cortas en las cohortes con largos seguimientos. La calidad metodológica es media-baja, presentando importantes pérdidas en el seguimiento. En 10 trabajos el seguimiento se limita a 1–2 años tras el ingreso por BA o IRA73,75,77,90,96,97,102,104,105,114, en 5 hasta los 3–4 años76,80,91,93,101, en 20 entre los 5–10 años80,82–87,92,94,98,100,101,103,106–111,115, en 6 entre los 10–14 años74,78,79,91,99,103 y en 5 hasta edades posteriores81,88,95,112,113, alcanzando seguimientos hasta los 35 años, aunque de cohortes muy reducidas. Las medidas de efecto más habituales han sido los sibilantes recurrentes y el asma; en ocasiones se detallaba por separado el antecedente de sibilantes en algún momento o formas activas (presencia de episodios en el último año); algunos estudios requerían el diagnóstico médico, mientras que en otros se recurría a criterios operativos a partir de lo declarado por los padres. Algunos trabajos consideraron la tendencia de los sibilantes en distintos momentos de la infancia80,91,101,103.
Tabla simplificada de los trabajos sobre frecuencia de asma posbronquiolitis
| Tipo de Población | N (CE/CC) | E | IRA | D | Medida de riesgo | Riesgo | Calidad. Comentarios |
| Autor/año/país | |||||||
| Frecuencia de asma posbronquiolitis | |||||||
| Rooney94 1971 Australia | 62 | H | BA VRS | CP | Sibilantes a los 2–7 años | 56,5% | 3/5 (a, b, d) |
| Ingreso por BA VRS+ <18 meses | |||||||
| Sims100 1978 Reino Unido | 35/35 | H | BA VRS | CP | Sibilantes en algún momento a los 8 años | 51,4% | 3/5 (a, b, d) |
| Ingreso por BA VRS+ lactantes | Sibilantes en 2 años previos a los 8 años | 22,8% | |||||
| Mok83 1982 Reino Unido | 2/5 (a, d) | ||||||
| Ingreso por IRA baja <1 año | 200/200 | H | IRA | CP | Sibilantes en cualquier momento a 7 años | 47% | |
| Sibilantes en último año a 7 años | 10% | ||||||
| Asma establecido (7 años) | 8,5% | ||||||
| Uso broncodilatadores último año (7 años) | 11% | ||||||
| Pullan91 1982 Reino Unido | 180/111 | H | IRA VRS | CP | Sibilantes a cualquier edad a los 10 años | 42% | 2/5 (a, d); las IRA baja incluyen 109 BA; encuesta de síntomas |
| Ingreso por IRA baja VRS+ <1 año | Sibilantes primeros 4 años | 38% | |||||
| Sibilantes últimos 2 años a los 10 años | 22% | ||||||
| Murray84 1992 Reino Unido | 101/73 | H | BA | CP | Sibilantes último año a los 5 años | 42,5% | 3/5 (a, d, e) |
| Ingreso por BA <1 año | |||||||
| Osundwa114 1993 Qatar | 70/70 | H | BA VRS | CR | Sibilantes recurrentes (⩾3) a los 2 años | 44% | 2/5 (c, d) |
| Ingreso por BA VRS+ <1 año | |||||||
| Noble86 1997 Reino Unido | 101/73 | H | BA | CP | Sibilantes último año a los 9,5 años | 47% | 2/5 (a, e); encuesta de síntomas de asma (asma no definido) |
| Ingreso por BA <1 año | Asma último año a los 9,5 años | 39% | |||||
| Stein103 1999 USA | 519/369 | P | IRA | CP | Sibilantes infrecuentes (≤3/años) a 6 años | 18,9% | 4/5 (a, c, d, e) |
| IRA baja <3 años | Sibilantes infrecuentes (≤3/años) a 8 años | 18,6% | |||||
| Sibilantes infrecuentes (≤3/años) a 11 años | 17% | ||||||
| Sibilantes infrecuentes (≤3/años) a 13 años | 17,1% | ||||||
| Sibilantes frecuentes (>3/años) a 6 años | 8,2% | ||||||
| Sibilantes frecuentes (>3/años) a 8 años | 8,3% | ||||||
| Sibilantes frecuentes (>3/años) a 11 años | 10,3% | ||||||
| Sibilantes frecuentes (>3/años) a 13 años | 8,7% | ||||||
| Weber104 1999 Gambia | 105/105/102 | H | IRA VRS | CP | Sibilantes a los 19–25 meses | 14% | 3/5 (a, c, d) |
| Ingreso por IRA baja VRS+ <1 año | |||||||
| Albernaz73 2000 Brasil | 105/210 | H | BA | CP | Sibilantes recurrentes (≥2) al año | 61,9% | 1/5 (e) |
| Ingreso por BA <3 años | |||||||
| Arribas74 2000 España | 97/52 | H | BA | CP | Sibilantes episódicos a 9–14 años | 41,2% | 1/5 (d) |
| Ingreso 1.er episodio de BA <1 año | Asma con diagnóstico médico a 9–14 años | 6,2% | |||||
| Bont75 2000 Holanda | 50/27 | H | IRA VRS | CP | Sibilantes recurrentes (≥1) al año | 59% | 2/5 (c,d) |
| Ingreso IRA baja VRS+ <13 meses | Asma con diagnóstico médico al año | 35% | |||||
| Ehlenfield108 2000 EE. UU. | 43 | H | BA VRS | CR | Sibilantes recurrentes transitorios a 7 años | 11,6% | 1/5 (a); sibilantes recurrentes transitorios: se curan antes de los 4 años; persistentes: presentes en el último año |
| Ingreso BA (sibilantes) VRS+ 2–18 meses | Sibilantes recurrentes persistentes a 7 años | 34,8% | |||||
| Larouch113 2000 Canadá | 42/42 | H | BA | CR | Asma con diagnóstico médico a 17–35 años | 38% | 2/5 (a, d) |
| Ingreso por BA <18 meses | |||||||
| Reijonen93 2000 Finlandia | 32 | H | IRA | CP | Asma (⩾2 episodios) a los 3 años | 55% | 3/5 (c, d, e); datos de cohorte control no tratada (resto budesonida o cromoglicato) |
| Ingreso IRA con sibilantes <2 años | |||||||
| Sigurs98 2000 Suecia | 47/93 | H | BA VRS | CP | Asma a los 7,5 años | 30% | 4/5 (a, c, d, e); asma: ≥3 episodios de obstrucción bronquial con diagnóstico médico |
| Ingreso por BA VRS+ <1 año | Asma último año a los 7,5 años | 23% | |||||
| Calvo106 2001 España | 170 | H | BA | CR | Asma/sibilantes a ≤5 años | 66,5% | 2/5 (a, e); asma/sibilante: uso de broncodilatadores, corticoides o cromonas |
| Ingreso por BA <2 años | Asma/sibilantes a los 6–9 años (>5 años) | 35,3% | |||||
| Saga95 2001 Japón | 14/24 | H | BA | CP | Asma a los 16 años | 50% | 0/5 |
| Ingreso por BA 10–24 meses | |||||||
| Chung77 2002 Korea | 30/10 | H | BA VRS | CP | Sibilantes recurrentes al año | 60% | 2/5 (a, c); sibilantes con diagnóstico médico |
| Ingreso por BA VRS+ <8 meses | |||||||
| Kotaniemi-Syrjanen82 2002 Finlandia | 100 | H | Sibilantes | CP | Asma a los 7,1 años | 40% | 3/5 (a, d, e); asma: uso antiinflamatorios, o ≥2 episodios de sibilantes o tos prolongada (4 sem) sin infección+test de ejercicio alterado |
| Ingreso por sibilantes 1–23 meses | |||||||
| Pala87 2002 Suecia | 47/89 | H | BA VRS | CP | Sibilantes a los 7,5 años | 46% | 3/5 (a, b, d); asma: episodio de obstrucción bronquial confirmado por médico; sibilantes: cualquier síntoma de obstrucción bronquial |
| Ingreso por BA VRS+ <1 año | Asma a los 7,5 años | 27% | |||||
| Schauer97 2002 Alemania | 42/84 | H | BA VRS | CP | Sibilantes recurrentes (≥3) al año | 31% | 3/5 (a, d, e) |
| Ingreso por BA VRS+ <1 año | |||||||
| Juntti80 2003 Finlandia | 76/76 | H | IRA VRS | CP | Sibilantes cualquier momento a 6–10 años | 62% | 3/5 (a, c, d) |
| Ingreso por IRA VRS+ <2 años | Sibilantes últimos 12 meses a 6–10 años | 22% | |||||
| Asma cualquier momento a 6–10 años | 26% | ||||||
| Asma antes de los 3 años | 14,4% | ||||||
| Sampalis96 2003 Canadá | 2.415 | H | IRA VRS | CP | Ingreso por asma a los 2 años | 5,3% | 3/5 (a, c, d); estudio de riesgo de mortalidad (con alto riesgo de muerte súbita en cohorte expuesta) |
| Ingreso prematuros 33–35 SG por IRA baja VRS+ <1 año | |||||||
| Singleton101 2003 USA | 95/113 | H | IRA VRS | CP | Asma/hiperreactividad bronquial a 2–4 años | 27% | 3/5 (a, d, e) |
| Ingreso por IRA VRS+ <2 años | Sibilantes último año a los 5–8 años | 43% | |||||
| Bont76 2004 Holanda | 140 | H | IRA VRS | CP | Sibilantes algún momento a los 3 años | 60% | 3/5 (a, c, d); descenso de episodios de sibilancias >50% durante el primer año |
| Ingreso IRA baja VRS+ <13 meses | Sibilantes últimos 12 meses a los 3 años | 42% | |||||
| Goetghebuer111 2004 Reino Unido | 134/752 | H | BA VRS | CR | Sibilantes recurrentes a los 6 años | 65,6% | 1/5 (c) |
| Ingreso por BA VRS+ <1 año | Sibilantes persistentes (último año) 6 años | 34,3% | |||||
| Gómez112 2004 España | 71/32 | H | BA | CR | Asma con diagnóstico médico a 19–24 años | 25,3% | 1/5 (a); valoración síntomas 10 años previos |
| Ingreso por BA viral <1 año | |||||||
| Korppi81 2004 Finlandia | |||||||
| Ingreso por IRA baja <2 años | 51/45 | H | IRA | CP | Asma con diagnóstico médico a 18–20 años | 17% | 4/5 (a, b, d, e); asma: diagnóstico médico±sibilantes o tos prolongada. |
| Asma con síntomas último año 18–20 años | 22% | Actual: uso antiinflamatorios o sibilantes+PEF alterado | |||||
| Soferman102 2004 Israel | 19 | H | BA VRS | CP | Sibilantes recurrentes (1/mes) al año | 68,4% | 3/5 (b, c, d) |
| Ingreso por BA VRS+ 2–14 meses | |||||||
| Fjaerli109 2005 Holanda | 57/64 | H | BA | CR | Sibilantes recurrentes (⩾3) a los 7 años | 51% | 2/5 (a,b); alto porcentaje de casos con IRA baja previas (43% de los casos VRS+ vs. 32% de los VRS-) |
| Ingreso por BA lactantes | Asma diagnosticado por médico a 7 años | 54% | |||||
| Hyvarinen78 2005 Finlandia | 81 | H | BA | CP | Asma I a los 13,5–16 años | 14% | 2/5 (a,d); asma I: sibilantes agudos tratados en hospital o centro de salud, o antiinflamatorios; asma II: asma I y/o broncodilatadores en casa |
| Ingreso por BA <2 años | Asma II (broncodilatadores) a 13,5–16 años | 23% | |||||
| Nagayama85 2005 Japón | 142 | H | BA VRS | CP | Consultas sibilantes recurrentes a 4–8 años | 17% | 0/5; importantes pérdidas; 11 casos no ingresaron |
| Ingreso por BA VRS+ lactantes | |||||||
| Pitrez90 2005 Brasil | 45 | H | BA | CP | Sibilantes recurrentes (≥2) al año | 72% | 1/5 (b); muestra sesgada con pérdidas |
| Ingreso por BA <6 meses | |||||||
| Sigurs99 2005 Suecia | 46/92 | H | BA VRS | CP | Asma a los 13 años | 37% | 4/5 (a, c, d, e); asma: ≥3 episodios de obstrucción bronquial con diagnóstico médico |
| Ingreso por BA VRS+ <1 año | Asma último año a los 13 años | 28% | |||||
| Sznajder115 2005 Francia | 128 | U | BA | CR | Sibilantes en algún momento a los 5–6 años | 75,8% | 2/5 (c,d) |
| Urgencias por BA (1.°) <1 año | Asma (≥1) en último año a 5–6 años | 36,7% | |||||
| Al-Shawwa105 2006 EE. UU. | 155 | A | Sibilantes | CR | Sibilantes recurrentes (≥1) al año | 48,3% | 2/5 (a,d) |
| 1.er episodio de sibilancias <2 años | |||||||
| Piippo-Savolainen89 2006 Finlandia | 83 | H | BA | CP | Asma diagnóstico médico a 18–20 años | 29% | 3/5 (a, c, d); 27% pacientes con sibilantes previos |
| Ingreso por BA <2 años | |||||||
| García-García110 2007 España | 55/30 | H | BA | CR | 3/5 (a, c, e); episodios con diagnóstico médico. Muestra escasa, riesgo de sesgo de selección | ||
| Ingreso por BA VRS+ <2 años | 32 | Asma (⩾3 episodios) a los 3–5 años | 62,5% | ||||
| Ingreso por BA metapneumovirus <2 años | 23 | Asma (⩾3 episodios) a los 3–5 años | 69,6% | ||||
| Hyvarinen79 2007 Finlandia | 100 | H | IRA | CP | Asma a los 10,9–13,7 años | 40% | 2/5 (a,d); asma: uso antiinflamatorios, o sibilantes recurrente+test ejercicio positivo |
| Ingreso por IRA+sibilantes <2 años | |||||||
| Piippo-Savolainen88 2007 Finlandia | 83 | H | BA | CP | 2/5 (a, d); importante porcentaje de casos no clasificados; 27% pacientes con sibilantes previos | ||
| Ingreso por BA VRS− <2 años | 22 | Asma diagnóstico médico a 18–20 años | 41% | ||||
| Ingreso por BA VRS+ <2 años | 22 | Asma diagnóstico médico a 18–20 años | 18% | ||||
| Ramsey92 2007 USA | 56 | P | BA | CP | Asma a los 7 años | 17,9% | 5/5 (a, b, c, d, e); asma: diagnóstico médico+1 episodio año previo |
| BA en <1 año con riesgo atópico | |||||||
| Cassimos107 2008 Grecia | 189/60 | H | BA VRS | CR | Asma a los 5–9 años | 57,1% | 2/5 (a,e); asma si 2 criterios de: diagnóstico médico, >1 tratamiento antiasma y síntomas |
| Ingreso por BA VRS+ <1 año | |||||||
A: ambulatorio; BA: bronquiolitis aguda; CC: casos y controles; CCI: coeficiente de correlación intraclase; CIE: códigos de la clasificación internacional de enfermedades; CP: cohortes; CR: cohortes retrospectivo; E: entorno asistencial; Ec: estudio ecológico; ECA: ensayo clínico aleatorizado; EE: estimador de efecto; EPC: enfermedad pulmonar crónica; ET: estudio transversal; D: diseño epidemiológico; DBP: displasia broncopulmonar; DM: diferencia de medias; DMa: DM ajustada; DP: diferencia de porcentajes; H: hospital; I: cuidados intensivos; IA: incidencia acumulada; IRA: infección respiratoria aguda; K: kappa; Kp: kappa ponderado; LBA: lavado broncoalveolar; MPV: metapneumovirus; N (CE/CC): tamaño muestral (cohorte expuesta o casos / cohorte control o controles); ns: no significativo; P: poblacional; PCR: reacción en cadena de la polimerasa; RDAI: Respiratory Distress Assessment Instrument; RDI: razón de densidades de incidencia; RGC: riesgo grupo control; SG: semanas de gestación; U: servicio de Urgencias; VM: ventilación mecánica; VRS: virus respiratorio sincitial; β: coeficiente de regresión; ρ: coeficiente de correlación.
En 33 estudios de cohortes prospectivos73–75,77,78,80–84,86–89,91–93,96–101,103,104,116–123, en 9 de cohortes retrospectivos105–110,112–114 y en 2 de casos y controles111,124, se ha analizado si el ingreso por BA o IRA baja era un factor de riesgo de sibilantes recurrentes o asma, y/o cuales eran los cofactores asociados a dicho riesgo. En la tabla 4 se presentan las principales características y resultados de estos estudios. Las muestras estaban constituidas por pacientes con ingreso por BA o IRA baja, excepcionalmente por pacientes no ingresados92,103,105,118,120,124, que se comparaban con cohortes de niños no expuestos, procedentes de consultorios, registros hospitalarios, escolares o poblacionales. En algunos estudios no existía cohorte no expuesta, analizándose el riesgo en función de otras covariables asociadas78,82,88,89,93,105,106,108,118,121,122. Las principales covariables de riesgo consideradas han sido: antecedentes de sibilantes, dermatitis atópica o rinitis, VRS+, edad mayor de 12 meses, asma o atopia familiar, madre fumadora en el embarazo o en la primera infancia, ingreso hospitalario, prematuridad, sexo masculino y humedad del domicilio. En cuanto a marcadores de riesgo, presentes en el ingreso o en las semanas posteriores al mismo, se han considerado: la proteína catiónica del eosinófilo, la eosinofilia, la IgE total elevada, el prick test a alergenos positivo y ciertas citoquinas. Las características metodológicas de los estudios son similares a las mencionadas anteriormente para los estudios de riesgo de asma, ya que muchos son comunes. No se ha realizado enmascaramiento en la valoración del efecto y, aunque en 20 estudios se ha realizado ajuste multivariante73,81,82,86–88,92,93,97–99,103,106,107,110,111,118,120,121,123, el control ha sido en algunos de ellos incompleto o incorrecto. Las series con seguimientos más prolongados son muy reducidas y con alto riesgo de sesgos de selección o pérdidas. En algunos estudios se ha evaluado la tendencia del riesgo a lo largo de diversos momentos de la infancia80,91,101,103.
Tabla simplificada de los trabajos sobre factores de riesgo de asma posbronquiolitis
| Comparación | N (CE/CC) | E | D | Medida de efecto | RGC* | EE | Efecto | IC95% (p) | Calidad. Comentarios |
| Autor/año | |||||||||
| Factores de riesgo de asma posbronquiolitis | |||||||||
| Sims100 1978 Reino Unido | 35/35 | H | CP | 3/5 (a, b, d); cohorte no expuesta: escolares emparejados por edad, sexo y clase social | |||||
| Ingreso por BA VRS+ lactantes | Sibilantes en algún momento a 8 años | 2,8% | RR | 9 | 2,26–35,91 | ||||
| Función pulmonar; PEF (l/min) | 265 | DM | ‐28 | (p<0,02) | Otros parámetros función pulmonar y test de metacolina alterados | ||||
| Mok83 1982 Reino Unido | 200/200 | H | CP | 2/5 (a, d); cohorte expuesta: ingreso por IRA baja <1 año; cohorte no expuesta: escolares emparejados por edad, sexo y talla | |||||
| Ingreso por IRA baja <1 año | Sibilantes cualquier momento a 7 años | 17% | RR | 2,79 | 1,99–3,92 | ||||
| Sibilantes en último año a 7 años | 1% | RR | 10,50 | 2,49–44,19 | |||||
| Asma establecido (7 años) | 2,5% | RR | 3,40 | 1,28–9,04 | Diagnóstico de asma no definido | ||||
| Uso broncodilatadores último año 7 años | 4% | RR | 2,44 | 1,15–5,18 | Cohorte expuesta: peor función pulmonar y test de ejercicio | ||||
| Pullan91 1982 Reino Unido | 180/111 | H | CP | 2/5 (a, d); ingreso por IRA baja VRS+ <1 año; las IRA baja incluyen 109 BA; | |||||
| Ingreso IRA baja VRS+ <1 año | Sibilantes a cualquier edad a los 10 años | 19% | OR | 2,24 | 1,45–3,45 | ||||
| Sibilantes primeros 4 años | 15% | OR | 2,51 | 1,54–4,09 | Encuesta de síntomas | ||||
| Sibilantes últimos 2 años a los 10 años | 13% | OR | 1,77 | 0,98–3,18 | Importantes diferencias entre cohortes (tabaquismo y hermanos mayores) | ||||
| Medicación antiasmática actual a 10 años | 5% | DP | 0% | ns | |||||
| Test ejercicio caída FEV1 >15% | 5% | DP | 11% | (p<0,05) | Menor riesgo de prick cutáneo positivo en cohortes expuesta | ||||
| Función pulmonar (% PEF para talla) | 111% | DM | -10 | (p<0,005) | |||||
| Murray84 1992 Reino Unido | 101/73 | H | CP | 3/5 (a, d, e); cohorte no expuesta: escolares reclutados a los 5 años de similar edad, raza, área y tabaquismo materno no ingresados por bronquiolitis | |||||
| Ingreso por BA <1 año | Sibilantes último año a los 5 años | 15,1% | RR | 1,78 | 1,26–2,50 | ||||
| Medicación profiláctica último año 5 años | 4,1% | DP | 5,5% | ns | |||||
| Broncodilatadores último año a 5 años | 5,5% | DP | 27,4% | (p<0,0001) | |||||
| Osundwa114 1993 Qatar | 70/70 | H | CR | 2/5 (c, d); cohorte no expuesta: ingresos coetáneos por problema no respiratorios | |||||
| Ingreso por BA VRS+ <1 año | Sibilantes recurrentes (≥3) a 2 años | 12,9% | RR | 3,44 | 1,77–6,69 | ||||
| Noble86 1995 Reino Unido | 101/73 | H | CP | 2/5 (a, e); encuesta de síntomas de asma (asma no definido) | |||||
| Ingreso por BA <1 año | Sibilantes último año a los 9,5 años | 17% | ORa | 3,59 | 1,31–9,81 | ||||
| Asma último año a los 9,5 años | 13% | ORa | 4,43 | 1,63–12 | |||||
| Reijonen122 1997 Finlandia | 100 | H | CP | 3/5 (c, d, e); ingresos por IRA con sibilantes y dificultad respiratoria <2 años; cohortes tratadas con budesonida (34), cromoglicato (34) y control (32) | |||||
| Proteína catiónica eosinófilo >8 | Recurrencia de sibilantes a 16 semanas | 40% | DP | 36% | (p<0,01) | ||||
| Recurrencia de sibilantes a 16 semanas | 40% | Se 41% | Es 87% | ||||||
| Proteína catiónica eosinófilo >16 | Recurrencia de sibilantes a 16 semanas | 45% | DP | 41% | (p<0,01) | Proteína catiónica del eosinófilo al ingreso | |||
| Recurrencia de sibilantes a 16 semanas | 45% | Se 26% | Es 96% | ||||||
| Stein103 1999 EE. UU. | 519/369 | P | CP | 4/5 (a, c d, e) | |||||
| IRA baja por VRS <3 años | Sibilantes infrecuentes (≤3/años) a 6 años | ORa | 3,2 | 2,0–5,0 | Cohortes expuesta y no expuesta proceden de cohorte de Tucson | ||||
| Sibilantes infrecuentes (≤3/años) a 8 años | ORa | 2,5 | 1,5–4,3 | Sibilantes infrecuentes para IRA por otros agentes OR 1,8 (1,1–2,9), o sin virus identificado OR 1,6 (1,1–2,4); no cambia con edad | |||||
| Sibilantes infrecuentes (≤3/años) a 11 años | ORa | 1,7 | 1–2,9 | ||||||
| Sibilantes infrecuentes (≤3/años) a 13 años | ORa | 1,4 | 0,7–2,7 | ||||||
| Sibilantes frecuentes (>3/años) a 6 años | ORa | 4,3 | 2,2–8,7 | ||||||
| Sibilantes frecuentes (>3/años) a 8 años | ORa | 1,9 | 0,9–4,2 | Sibilancias frecuentes para IRA VRS- OR 2 (1,1–3,5), independiente de la edad | |||||
| Sibilantes frecuentes (>3/años) a 11 años | ORa | 2,4 | 1,3–4,6 | No asociación entre IRA baja y posterior status atópico | |||||
| Sibilantes frecuentes (>3/años) a 13 años | ORa | 1,4 | 0,7–2,6 | IRA baja por VRS menor volumen espiratorio forzado a los 11 años | |||||
| Weber104 1999 Gambia | 105/ | H | CP | Sibilantes a los 19–25 meses; casos/100 niños/mes | 0,3 | RDI | 7,33 | 3,10–17,54 | 3/5 (a, c, d); cohorte no expuesta I: emparejados por edad y domicilio de época epidémica; cohorte no expuesta II: época no epidémica |
| Ingreso IRA baja VRS+ <1 año | 105/102 | ||||||||
| Albernaz73 2000 Brasil | 105/210 | H | CP | 1/5 (e); ingresados por BA <3 años; cohorte control poblacional aleatoria (en este grupo factor de riesgo: hermanos <5 años) | |||||
| Ingreso por BA <3 años | Sibilantes recurrentes (≥2) al año | 23,3% | ORa | 4,9 | 2,9–8,3 | ||||
| Arribas74 2000 España | 97/52 | H | CP | 1/5 (d); cohorte no expuesta y sin enfermedad respiratoria o alergia; en expuestos con/sin sibilantes posteriores Test de metacolina+ OR 6,5 (2,3–18,6) | |||||
| Ingreso 1.er episodio BA <1 año | Test metacolina positivo a 9–14 años | 25,9% | OR | 10,6 | 3,8–29,2 | ||||
| Prick test positivo a 9–14 años | 5,7% | OR | 8,0 | 2,3–27,8 | |||||
| Bont75 2000 Holanda | 50/27 | H | CP | 2/5 (c,d); ingreso IRA baja VRS+ <13 meses | |||||
| Interleucina-10 | Número episodio de sibilantes al año | ρ | 0,42 | (p=0,004) | |||||
| Ehlenfield108 2000 USA | 43 | H | CR | 1/5 (a); ingreso BA (sibilantes) VRS+ 2–18 meses; no ajuste multivariante | |||||
| Eosinofilia al ingreso | Sibilantes persistentes a los 7 años | 22% | OR | 4,5 | 1,2–17,2 | Capacidad predictiva de la eosinofilia: Se: 60% (36–80%), Es: 75% (57–87%) | |||
| Larouch113 2000 Canadá | 42/42 | H | CR | 2/5 (a, d); cohorte control: 42 sujetos sin ingreso por bronquiolitis emparejados por edad y sexo | |||||
| Ingreso por BA <18 meses | Asma diagnóstico médico a 17–35 años | 38% | RR | 3,20 | 1,29–7,94 | ||||
| Hiperreactividad bronquial (test de metacolina PC20<8 mg/ml) | 29% | RR | 2,17 | 1,27–3,70 | Revisión de registros hospitalarios | ||||
| FEV1/FVC media (% predicho) | 87 | DM | -7 | (p<0,0001) | |||||
| Nafstad120 2000 Noruega | 3.048 | P | CP | 4/5 (a, c, d, e); cohorte de recién nacidos; asma: diagnóstico médico o síntomas en 12 meses previos; obstrucción bronquial: ≥2 episodios de síntomas o 1 de >1 mes | |||||
| IRA baja <12 meses | Asma a los 4 años | 6,5%* | ORa | 11,6 | 8,3–16,2 | ||||
| Obstrucción bronquial <2 años | Asma a los 4 años | 6,5%* | ORa | 12,9 | 9,1–18,2 | ||||
| Reijonen93 2000 Finlandia | 100 | H | CP | 3/5 (c, d, e); ingresos por IRA con sibilantes y dificultad respiratoria <2 años; cohortes tratadas con budesonida (34), cromoglicato (34) y control (32) | |||||
| Edad > 12 meses | Asma (≥2 episodios) a los 3 años | 20% | ORa | 4,1 | 1,6–10,4 | ||||
| Antecedente de sibilancias | Asma (≥2 episodios) a los 3 años | 5% | ORa | 6,8 | 1,4–34,4 | ||||
| Dermatitis atópica | Asma (≥2 episodios) a los 3 años | 16% | ORa | 3,4 | 1,2–9,4 | Presencia de mascota en el hogar disminuye el riesgo de asma | |||
| Prick test alimentos a los 8 mes | Asma (≥2 episodios) a los 3 años | 7% | ORa | 9,5 | 2,5–36,7 | ||||
| VRS+ | Asma (≥2 episodios) a los 3 años | 41% | ORa | 0,3 | 0,1–0,8 | ||||
| Sigurs98 2000 Suecia | 47/93 | H | CP | 4/5 (a, c, d, e); controles no expuestos: niños del mismo centro de salud, edad y sexo; asma: ≥3 episodios de obstrucción bronquial con diagnóstico médico | |||||
| Ingreso por BA VRS+ <1 año | Asma a los 7,5 años | 3% | ORa | 12,7 | 3,4–47,1 | ||||
| Asma último año a los 7,5 años | 2% | OR | 10,88 | 2,51–47,11 | |||||
| Adler116 2001 EE. UU. | 86/78 | H | CP | Hiperreactividad bronquial (metacolina) a los 12–19 meses | 0/5; tabaquismo parental, asma materno y la exposición a hongos se asocian a menor capacidad residual funcional | ||||
| IRA baja por VRS | – | β | -0,29 | ns | |||||
| Calvo106 2001 España | 170 | H | CR | 2/5 (a, e); ingreso por BA <2 años | |||||
| Asma familiar | Asma/sibilantes a ≤5 años | 66,5%* | ORa | 1,97 | 0,94–4,14 | Capacidad predictiva de la eosinofilia >1% para sibilancias ≤5 años se 46%; Es 73,4%; para sibilancias a los 6–9 años: Se 48,3%; Es 65,4% | |||
| Asma/sibilantes a los 6–9 años | 35,3%* | ORa | 2,06 | 1,01–4,05 | |||||
| Eosinofilia >1% al ingreso | Asma/sibilantes a ≤5 años | 66,5%* | ORa | 2,44 | 1,21–4,94 | ||||
| Asma/sibilantes a los 6–9 años | 35,3%* | ORa | 1,84 | 0,96–3,54 | |||||
| Chung77 2002 Korea | 30 | H | CP | 2/5 (a, c); ingresos por BA VRS+ <8 meses | |||||
| RANTES pg/ml | Sibilantes recurrentes al año | 65 | DM | 68 | (p<0,05) | RANTES y proteína catiónica eosinofílica (ng/ml) al ingreso | |||
| Proteína catiónica del eosinófilo | Sibilantes recurrentes al año | 21 | DM | 34 | (p=0,06) | Análisis expuestos con vs. sin sibilantes | |||
| Kotaniemi-Syrjanen82 2002 Finlandia | 100 | H | CP | 3/5 (a, d, e); ingreso por sibilantes 1–23 meses; | |||||
| Episodios precoces de sibilantes | Asma a los 7,1 años | 40%* | ORa | 4,29 | 1,02–17,99 | Asma: uso antiinflamatorios, o ≥2 episodios de sibilantes o tos prolongada (4 sem) sin infección + test de ejercicio alterado | |||
| Dermatitis atópica | Asma a los 7,1 años | 40%* | ORa | 4,11 | 1,42–11,84 | ||||
| IgE total >60 kU/l | Asma a los 7,1 años | 40%* | ORa | 3,41 | 1,03–11,33 | ||||
| Eosinofilia | Asma a los 7,1 años | 40%* | ORa | 7,02 | 2,26–21,79 | Ajuste solo por edad y sexo | |||
| Etiología VRS | Asma a los 7,1 años | 40%* | ORa | 0,22 | 0,07–0,72 | ||||
| Prick test positivo | Asma a los 7,1 años | 40%* | ORa | 5,22 | 1,79–15,22 | ||||
| Rinitis alérgica | Asma a los 7,1 años | 40%* | ORa | 10,25 | 3,60–29,22 | ||||
| Pala87 2002 Suecia | 47/89 | H | CP | 3/5 (a, b, d); Asma: episodio de obstrucción bronquial confirmado por médico; sibilantes: cualquier síntoma; | |||||
| Ingreso por BA VRS+ <1 año | Asma a los 7,5 años | 1% | ORa | 25,2 | 3,1–206 | ||||
| Sibilantes a los 7,5 años | 1% | ORa | 58 | 7–461 | Cohorte no expuesta poblacional | ||||
| Ploin124 2002 Francia | 80/160 | A | CC | 3/5 (a, c, d); casos: asmáticos activos; controles: reclutados en consultas | |||||
| BA (1.a) <1 año | Asma a los 4–12 años | OR | 5,8 | 3,2–10,7 | |||||
| Schauer97 2002 Alemania | 42/84 | H | CP | 3/5 (a, d, e); cohorte no expuesta: 84 recién nacidos emparejados por nacimiento y sexo | |||||
| Ingreso por BA VRS+ <1 año | Sibilantes recurrentes (≥3) al año | 3,5% | ORa | 8,9 | 1,4–55,9 | ||||
| Madre fumadora en embarazo | Sibilantes recurrentes (≥3) al año | ORa | 6,5 | 1,5–27,2 | |||||
| Cifuentes118 2003 Chile | 138 | U | CP | 2/5 (a, e); BA (1.er episodio de sibilantes) atendidas en Urgencias <2 años; | |||||
| BA VRS+ vs. VRS- | N.° de episodios de sibilantes al año | 2,34 | DM | 1,02 | (p=0,06) | ||||
| Sibilantes recurrentes al año | RRa | 1,41 | 1,03–1,93 | RRa regresión de Cox; no especifica si se analiza tiempo hasta recurrencias | |||||
| BA VRS+ ingreso vs. no ingreso | N.o de episodios de sibilantes al año | 2,07 | DM | 2,11 | (p=0,008) | ||||
| Asma materno | Sibilantes recurrentes al año | RRa | 0,53 | 0,33–0,85 | Asma materno más frecuente en casos VRS+; dudas sobre ajuste; efecto paradójico protector (solo en VRS+) | ||||
| Antecedentes de Rinitis | Sibilantes recurrentes al año | RRa | 1,46 | 0,99–2,15 | |||||
| Juntti80 2003 Finlandia | 76/76 | H | CP | 3/5 (a, c, d); cohorte expuesta: ingreso por IRA VRS+ <2 años; cohorte no expuesta: controles poblacionales por edad y sexo | |||||
| Ingreso por IRA VRS+ <2 años | Sibilantes cualquier momento 6–10 años | 48% | OR | 1,76 | 0,92–3,36 | ||||
| Sibilantes últimos 12 meses a 6–10 años | 24% | OR | 0,93 | 0,44–1,98 | No diferencias en espirometría | ||||
| Asma cualquier momento a 6–10 años | 16% | OR | 1,91 | 0,86–4,24 | |||||
| Asma antes de los 3 años | 1% | OR | 13,44 | 1,45–124 | |||||
| Prick positivo a 6–10 años | 43% | OR | 0,11 | 0,04–0,36 | |||||
| IgE elevado a 6–10 años | 43% | OR | 0,36 | 0,15–0,86 | |||||
| Atopia familiar | 20% | OR | 2,99 | 1,45–6,21 | |||||
| Asma en hermano | 13% | OR | 3,89 | 1,66–9,12 | |||||
| Sampalis96 2003 Canadá | 3/5 (a, c, d); cohorte no expuesta: poblacional emparejada por SG, sexo y residencia | ||||||||
| Ingreso prematuros 33–35 SG por IRA baja VRS+ <1 año | 2.415 / 20.254 | H | CP | Ingreso por asma a los 2 años | 1% | OR | 8 | 6,7–9,6 | |
| Singleton101 2003 EE. UU. | 95/113 | H | CP | 3/5 (a, d, e) | |||||
| Ingreso por IRA VRS+ <2 años | Asma/hiperreactividad bronquiolitis 2–4 años | 9% | RR | 3,09 | 1,57–6,08 | Cohorte expuesta: muestra seleccionada de estudio mayor (dudas de sesgo de selección). Cohorte no expuesta: poblacional por edad y localidad | |||
| Sibilantes último año a los 5–8 años | 36% | DP | 7% | ns | |||||
| Tos productiva a 5–8 años | RR | 1,67 | 1,14–2,44 | No diferencias en asma >5 años | |||||
| Sibilancias con ejercicio a 5–8 años | RR | 4,70 | 1,39–15,9 | ||||||
| Goetghebuer111 2004 Reino Unido | 134/752 | H | CC | 2/5 (a, d): casos ingresados con BA VRS+ con sibilantes posteriores; controles: sin sibilantes posteriores (46) y sangre de cordón de recién nacidos (706) | |||||
| Alelo IL8–251.a | BA con vs. sin sibilantes a los 6 años | OR | 1,86 | 1,1–3,1 | |||||
| BA vs. controles (sangre cordón) | ORa | 2,2 | 0,9–5,7 | ||||||
| Gómez112 2004 España | 71/32 | H | CR | 1/5 (a); ingreso por BA viral <1 año cohorte no expuesta a BA: adultos voluntarios | |||||
| Ingreso por BA viral <1 año | Asma diagnóstico médico a 19–24 años | 6,2% | OR | 5,9 | 1,1–23,47 | ||||
| Tasa de pico espiratorio de flujo ml/s | 7,94 | DM | -0,94 | (p=0,02) | No diferencia en Prick test ni metacolina | ||||
| Korppi81 2004 Finlandia | 51/45 | H | CP | 4/5 (a, b, d, e); cohorte expuesta: ingreso por IRA baja <2 años; cohorte no expuesta: niños emparejados por edad y sexo, de familias no atópicas | |||||
| Ingreso por IRA baja <2 años | Asma diagnóstico médico a 18–20 años | 11% | ORa | 1,40 | 0,36–5,35 | ||||
| Asma síntomas último año 18–20 años | 11% | ORa | 2,09 | 0,58–7,61 | |||||
| Hiperreactividad bronquial (metacolina PD20<4,900) | 32% | ORa | 1,76 | 0,68–4,52 | Asma: diagnóstico médico ± sibilantes o tos prolongada. Asma actual: uso de antiinflamatorios, o bien sibilantes + PEF alterado | ||||
| Función pulmonar alterada | 31% | ORa | 5,27 | 1,60–17,35 | |||||
| Fjaerli109 2005 Holanda | 57/64 | H | CR | 2/5 (a, b); ingresados por BA VRS+ (35) o VRS-(22); cohorte control: 64 escolares, por edad sin ingreso respiratorio 1.er año | |||||
| Ingreso BA lactante | Sibilantes recurrentes (≥3) a los 7 años | 14% | OR | 6,3 | 2,6–15,2 | ||||
| Asma diagnosticado por médico a 7 años | 8% | OR | 14,1 | 4,9–40,3 | Alto porcentaje de casos con IRA baja previas (43% de los casos VRS+ vs. 32% de los VRS-) | ||||
| Tratamiento de asma a 7 años | 8% | OR | 6,4 | 2,2–18,5 | |||||
| Función pulmonar (FVC tras β2) | 1,81 | DM | -0,12 | 0,004–0,22 | Otros parámetros afectados: FEV1 | ||||
| Hyvarinen78 2005 Finlandia | 81 | H | CP | 2/5 (a,d); ingreso por IRA baja (BA o neumonía) <2 años; | |||||
| VRS+ vs. VRS- | Asma II a los 13,5–16 años | 20% | OR | 0,79 | 0,25–2.49 | ||||
| Asma parental | Asma II a los 13,5–16 años | 20% | OR | 1,50 | 0,23–9,44 | Asma I: sibilantes agudos tratados en hospital o centro de salud, o antiinflamatorios; asma II: asma I y/o broncodilatadores en casa | |||
| Sibilantes a los 2 años | Asma II a los 13,5–16 años | 20% | OR | 4,21 | 1,06–16,69 | ||||
| Dermatitis atópica al 0,5–1 años | Asma II a los 13,5–16 años | 20% | OR | 2,66 | 0,86–8,20 | Resultados similares para asma I salvo para sibilantes a los 2 años que no es significativo | |||
| Eosinofilia a los 0,5–1 años | Asma II a los 13,5–16 años | 20% | OR | 11,45 | 1,24–105,49 | ||||
| Rinitis alérgica a los 13,5–16 años | Asma II a los 13,5–16 años | 20% | OR | 16,43 | 62,03–2.917 | ||||
| Sigurs99 2005 Suecia | 46/92 | H | CP | 4/5 (a, c, d, e); controles no expuestos: niños del mismo centro de salud, edad y sexo; asma: ≥3 episodios de obstrucción bronquial con diagnóstico médico | |||||
| Ingreso por BA VRS+ <1 año | Asma a los 13 años | 5,4% | OR | 6,8 | 2,7–17,3 | ||||
| Asma último año a los 13 años | 3,3% | ORa | 10,1 | 3,4–29,8 | |||||
| Al-Shawwa105 2006 EE. UU. | 155 | A | CR | 2/5 (a, d); 1.er episodio de sibilancias <2 años atendidos a nivel ambulatorio; no cohorte no expuesta. | |||||
| Hospitalización | Sibilantes recurrentes (≥1) al año | 22% | OR | 2,84 | 1,24–6,5 | ||||
| VRS negativo | Sibilantes recurrentes (≥1) al año | 47% | OR | 6,28 | 2,84–13,88 | ||||
| Sexo masculino vs. femenino | Sibilantes recurrentes (≥1) al año | 48,3%* | OR | 2,57 | 1,25–5,28 | ||||
| Piippo-Savolainen89 2006 Finlandia | 83 | H | CP | 3/5 (a, c, d); ingresos por BA <2 años | |||||
| Historia familiar de asma | Asma diagnóstico médico a 18–20 años | 29%* | OR | 16,11 | 1,66–156,46 | ||||
| Función pulmonar alterada a 18–20 años | OR | 5,77 | 0,99–33,68 | ||||||
| Sibilancias <1 año | Hiperreactividad bronquial a 18–20 años | OR | 4,32 | 1,15–16,28 | |||||
| Tabaquismo materno 1.a infancia | Asma diagnóstico médico a 18–20 años | OR | 4,1 | 1,2–14,3 | |||||
| Broughton117 2007 Inglaterra | 59 | H | CP | 2/5 (a,e); prematuros <32 SG; cohorte expuesta: 25 casos que tuvieron IRA baja por VRS. Pletismografía al año de edad corregida | |||||
| IRA baja VRS+ | 25 | Resistencia aire al año (kPa/l/s) | 1,84 | DM | 0,75 | (p=0,002) | |||
| Ingreso IRA baja VRS | 10 | Capacidad residual funcional al año | 27,5 | DM | 8,5 | (p=0,003) | |||
| Elphick119 Reino Unido 2007 | H | CP | 1/5 (a); ingreso por BA VRS+ (28) o sibilantes por VRS (9); cohorte no expuesta: selección por fecha de nacimiento, etnia y código postal (77) | ||||||
| Ingreso BA VRS+ <1 año | 28/77 | Uso de β2 inhalado a los 3 años | 6% | OR | 1,7 | 0,4–7,8 | |||
| Uso de corticoides inhalados a 3 años | 4% | OR | 0,9 | 0,09–9,1 | |||||
| Visitas médicas (≥2) a los 3 años | 5% | OR | 2,1 | 0,5–2,1 | Escaso tamaño muestral | ||||
| Ingreso sibilantes VRS+ <1 año | 9/77 | Uso de β2 inhalado a los 3 años | 6% | OR | 8,6 | 1,6–47 | |||
| Uso de corticoides inhalados a 3 años | 4% | OR | 8,7 | 1,4–54 | |||||
| Visitas médicas (≥2) a los 3 años | 5% | OR | 10,8 | 1,9–60 | |||||
| García-García110 2007 España | 55/30 | H | CR | 3/5 (a, c, e); episodios con diagnóstico médico. Muestra escasa, riesgo de sesgo de selección | |||||
| Ingreso BA VRS+ | Asma (≥3 episodios) a los 3–5 años | 13,3%* | ORa | 10,1 | 2,5–40,1 | ||||
| Ingreso BA metapneumovirus | Asma (≥3 episodios) a los 3–5 años | 13,3%* | ORa | 15,9 | 3,6–70,5 | Cohorte control: muestra aleatoria de ingresos por enteritis por rotavirus | |||
| Rinitis alérgica | Asma (≥3 episodios) a los 3–5 años | 13,3%* | ORa | 4,9 | 1,2–19, 9 | ||||
| Prematuridad | Asma (≥3 episodios) a los 3–5 años | 13,3%* | ORa | 0,99 | 0,3–3,8 | ||||
| Hermanos con atopia | Asma (≥3 episodios) a los 3–5 años | 13,3%* | ORa | 2,87 | 0,8–9,7 | ||||
| Tabaquismo materno | Asma (≥3 episodios) a los 3–5 años | 13,3%* | ORa | 1,0 | 0,4–3,3 | ||||
| Piippo-Savolainen88 2007 Finlandia | 83 | H | CP | 2/5 (a, d); ingresos por ba <2 años | |||||
| VRS- vs. VRS+ | Asma diagnóstico médico a 18–20 años | 18% | ORa | 8,34 | 1,18–58,69 | Dudas sobre la adecuación del ajuste | |||
| Piippo-Savolainen121 2007 Finlandia | 83 | H | CP | 3/5 (a, c, d); ingresos por BA <2 años | |||||
| Eosinofilia al ingreso | Asma diagnóstico médico a 18–20 años | 29%* | ORa | 8,34 | 1,18–58,69 | Dudas sobre la adecuación del ajuste; | |||
| Eosinofilia a las 4–6 semanas | Asma diagnóstico médico a 2–3 años | ORa | 2,26 | 1,29–3,95 | 27% pacientes con sibilantes previos | ||||
| Asma diagnóstico médico a 3–4 años | ORa | 2,24 | 1,27–3,95 | No asociación estadística a otras edades | |||||
| Asma diagnóstico médico a 8,5–10 años | ORa | 2,16 | 1,01–4,64 | ||||||
| Ramsey92 2007 EE. UU. | 56 | P | CP | 5/5 (a, b, c, d, e); niños con algún padre atópico; asma: diagnóstico médico +1 episodio año previo; sibilantes recurrentes: 2 episodios año previo | |||||
| BA en <1 año con riesgo atópico | Asma a los 7 años | 8,6% | ORa | 2,77 | 1,23–6,22 | ||||
| Sibilantes recurrentes a los 7 años | ORa | 2,61 | 1,14–5,94 | ||||||
| Simoes123 2007 Multicéntrico (6 países) | 191/230 | H | CP | 2/5 (c, e); prematuros expuestos a palivizumab y que no ingresan por infección VRS y no expuestos; cohortes heterogéneas | |||||
| Palivizumab | Sibilantes recurrentes (≥3) con diagnóstico médico a 2 años | 16% | ORa | 0,43 | 0,23–0,76 | ||||
| Cassimos107 2008 Grecia | 189/60 | H | CR | 2/5 (a,e); ingreso por BA VRS+ <1 año | |||||
| Lactancia materna <3 meses | Asma a los 5–9 años | 57,1%* | ORa | 8,4 | 3,1–22,4 | Asma si 2 criterios de: diagnóstico médico, >1 tratamiento antiasma y síntomas | |||
| Pruebas cutáneas positivas | Asma a los 5–9 años | 57,1%* | ORa | 7,1 | 2,8–18,1 | ||||
| Sexo masculino | Asma a los 5–9 años | 57,1%* | ORa | 5 | 2,2–11,5 | Cohorte no expuesta para estudio espirometría (60) | |||
| Humedad en casa | Asma a los 5–9 años | 57,1%* | ORa | 2,9 | 1,3–6,3 | Los pacientes con asma (108) tuvieron peor función pulmonar (FEV1, FEF50 y PEFR) que los casos sin asma y controles | |||
| Fumadores en casa | Asma a los 5–9 años | 57,1%* | ORa | 4 | 1,8–9,2 | ||||
A: ambulatorio; BA: bronquiolitis aguda; CC: casos y controles; CCI: coeficiente de correlación intraclase; CIE: códigos de la clasificación internacional de enfermedades; CP: cohortes; CR: cohortes retrospectivo; E: entorno asistencial; Ec: estudio ecológico; ECA: ensayo clínico aleatorizado; EE: estimador de efecto; EPC: enfermedad pulmonar crónica; ET: estudio transversal; D: diseño epidemiológico; DBP: displasia broncopulmonar; DM: diferencia de medias; DMa: DM ajustada; DP: diferencia de porcentajes; H: hospital; I: cuidados intensivos; IA: incidencia acumulada; IRA: infección respiratoria aguda; K: kappa; Kp: kappa ponderado; LBA: lavado broncoalveolar; MPV: metapneumovirus; N (CE/CC): tamaño muestral (cohorte expuesta o casos / cohorte control o controles); ns: no significativo; P: poblacional; PCR: reacción en cadena de la polimerasa; RDAI: Respiratory Distress Assessment Instrument; RDI: razón de densidades de incidencia; RGC: riesgo grupo control; SG: semanas de gestación; U: servicio de Urgencias; VM: ventilación mecánica; VRS: virus respiratorio sincitial; β: coeficiente de regresión; ρ: coeficiente de correlación.
Una revisión sistemática del año 2000125 resume los resultados de 4 estudios sobre riesgo de sibilantes recurrentes en pacientes con antecedente de BA por VRS en comparación con niños no expuestos. En 2007, Pérez-Yarza et al126 realizaron una revisión sistemática de 12 estudios sobre riesgo de sibilantes recurrentes y asma asociado al antecedente de infección por VRS, en su mayoría con ingreso, no pudiendo ofrecer medidas agrupadas por la heterogeneidad observada.
Consistencia entre estudiosAunque existe cierta tendencia en las estimaciones de riesgos por edades, se observa una heterogeneidad entre estudios solo parcialmente explicable por las diferencias metodológicas. Los parámetros que más influyen en las diferencias son la edad de seguimiento (a menor edad, mayor riesgo de sibilantes recurrentes), la diferenciación de formas activas o solo antecedente de síntomas (menor riesgo de formas activas) y la consideración de diagnóstico de asma, con o sin confirmación médica (riesgos menores que para sibilantes). Las diferencias relacionadas con la exposición, diagnóstico clínico (BA o IRA bajas) o etiología (VRS u otros) parecen más debidas a su irregular distribución en los estudios revisados, que a un efecto real.
Estimación de sesgosExiste un alto riesgo de sesgos de selección, confusión y clasificación. La inclusión de pacientes con sibilantes previos al episodio de BA o IRA puede sobrevalorar el riesgo asociado a dicha exposición; de hecho, es excepcional que se excluyan esos pacientes. Cuando la selección de pacientes se vincula al hallazgo de VRS, es más probable que se incurra en ese sesgo, ya que aunque dicho virus se identifica con más frecuencia en los casos de BA, su presencia no asegura el diagnóstico. Igualmente, es probable que en las cohortes con seguimiento largo, las muestras de pacientes incluidos tengan un cierto sesgo de selección por asociarse la presencia de síntomas con el contacto con el entorno asistencial y la participación en el estudio.
A pesar de que se ha realizado ajuste multivariante en algunos de los estudios, no se puede garantizar que la existencia de asociación entre BA y asma se deba a un fenómeno de confusión vinculado a un mayor riesgo atópico o a una mayor hiperreactividad bronquial (previa al episodio de BA) en las cohortes expuestas, no adecuadamente controlado en el análisis. En este sentido, al requerir la exposición estudiada el ingreso hospitalario, no podemos distinguir si dicho ingreso expresa la exposición o es una manifestación preliminar del efecto en un paciente previamente predispuesto.
Por último, puede existir un cierto sesgo de clasificación cuando la medida del efecto se basa en la declaración de síntomas por padres o pacientes, o bien, cuando los criterios de definición de asma no son válidos. No obstante, la repercusión de este sesgo podría ser menor ya que, a diferencia de los mencionados anteriormente, afectaría más a la magnitud que a la dirección de los hallazgos, salvo que el error de clasificación fuera diferencial (mayor tendencia a clasificar como asma los síntomas de la cohorte expuesta).
Precisión de las estimacionesSi bien existen estudios con tamaño muestral suficiente y una tendencia clara para establecer con suficiente precisión la asociación entre ingreso por BA o IRA baja y sibilantes recurrentes en la primera infancia, la información sobre el riesgo de asma en la adolescencia o edad adulta está basada en estudios con pequeño tamaño muestral, lo que podría originar cierta imprecisión en las estimaciones de riesgo.
Intensidad del efecto o fuerza de la asociaciónLa frecuencia de sibilantes recurrentes a 1–2 años de un ingreso por BA o IRA de vías bajas varía entre el 14–72% (mediana 44%). A los 3–4 años del 27–70% (mediana 57%). De los 5–10 años de 8–76% (mediana 34%); con formas activas del 8–47% (mediana 23%). De los 10–15 años del 6–42% (mediana 22%); para formas activas el intervalo es similar (mediana 17%). Por encima de los 15 años del 17–50% (mediana 27%); para formas activas la mediana es del 22%. Las medianas para las estimaciones de frecuencias correspondientes a casos con VRS solo son discretamente superiores (medianas un 4% superiores), mientras que para las estimaciones basadas en diagnóstico de asma resultan globalmente un 10% inferiores a las de sibilantes recurrentes (medianas del 29 y 39%); para ambos parámetros la relación se invierte al aumentar la edad: a mayor edad mayores son las cifras asociadas a casos de VRS y diagnóstico de asma. La frecuencia observada en las BA es mayor que la de las IRA bajas en general (17% superior), aunque esta diferencia parece debida al predominio de cohortes de BA en los estudios con seguimiento más corto. La gran heterogeneidad existente impide realizar estimaciones agrupadas de las distintas edades y medidas de efecto, no obstante, puede considerarse que la frecuencia es más alta en los primeros años de vida, reduciéndose al aumentar la edad.
El ingreso por BA o IRA baja parece ser un factor de riesgo de sibilantes recurrentes en la primera infancia. Los estudios con seguimiento a 1–2 años del ingreso73,80,97,114 encuentran riesgos significativos (RR u OR) entre 3,4–13,4. Entre los 3–4 años101,120 el riesgo se mantiene en cifras entre 3–11,6. Entre los 5–10 años83,84,86,91,92,103,124, encontramos un menor riesgo, no siempre significativo80,91,101 entre 0,9–5,8; no obstante, en 3 trabajos87,98,109 se han observado cifras de OR mucho más altas (entre 10–25,2), aunque existen dudas sobre la validez del riesgo de asma en las cohortes no expuestas (sorprendentemente bajas). En un amplio estudio de cohortes con ajuste multivariante, se ha observado que el riesgo significativo existente hasta los 6 años (OR entre 3,2–4,3) descendía a los 13 años (OR 1,4), dejando de ser significativo103. No obstante algún otro trabajo ha encontrado riesgos significativos a esta edad99. A edades posteriores encontramos cifras similares, con resultados significativos en 2 trabajos sin ajuste multivariante112,113 y no significativos en otro con ajuste81. En algunos de estos estudios, incluso en ausencia de asociación entre el antecedente de BA o IRA baja y el asma, los pacientes expuestos tenían una mayor hiperreactividad bronquial o peores parámetros de función pulmonar74,81,91,100,109,113.
De las covariables relacionadas se ha encontrado asociación entre sibilantes recurrentes o asma y la proteína catiónica del eosinófilo77,122, la eosinofilia78,82,106,108,121, la edad >12 meses93, la dermatitis atópica82,93, la rinitis alérgica78,82, el prick test positivo82,93,107, la IgE elevada82, el asma familiar106,118, ciertas citoquinas75,77,89, madre fumadora en el embarazo o primera infancia o fumadores en el domicilio89,97,107, el ingreso hospitalario105,118, el sexo masculino105,107, y una lactancia materna <3 meses107. Las medidas de riesgo encontradas para cada variable son heterogéneas y su magnitud no permite establecer una predicción del riesgo de asma en pacientes concretos. De hecho las estimaciones de validez predictiva encontradas para la eosinofilia106,108 y para la proteína catiónica del eosinófilo122 resultan poco útiles.
El hallazgo de VRS en BA o IRA baja se ha asociado a menor riesgo de asma82,88,93,105, aunque en un estudio con seguimiento de un año se encontró la asociación inversa118. Esta asociación puede ser el resultado de algún sesgo de selección por tener lugar los casos con VRS en niños más pequeños, y los debidos a otros virus en niños más mayores, entre los que es más frecuente que se incluyan los episodios de broncoespasmo en pacientes predispuestos. Se ha documentado en BA por metapneumovirus un riesgo similar o superior al observado en las BA debidas a otros virus110.
Una revisión sistemática del año 2000125, de calidad media, resume los resultados de 4 estudios incluidos en este documento, encontrando que el antecedente de BA por VRS en el primer año de vida se asociaba a sibilantes recurrentes (≥3) hasta los 5 años de vida (OR 5,5; 2,4–12,6), pero no de los 5–10 años (OR 2,4; 0,7–8,4). En la revisión sistemática de Pérez-Yarza et al126, sobre 12 estudios, se observó un amplio intervalo de riesgos de sibilantes recurrentes o asma, no agrupables, y una clara disminución del mismo a mayor edad de seguimiento.
En la cohorte de recién nacidos de Tucson, Martínez et al127 encontraron que el 40,8% de los niños con sibilantes antes de los 3 años persistían a los 6 años. No obstante, en este estudio no se estimó el riesgo asociado a episodios de IRA baja o BA.
Grado de relación con la pregunta clínicaLa evidencia disponible puede ser considerada indirecta fundamentalmente por las limitaciones del factor de exposición considerado (ingreso por BA o IRA baja), que no permite diferenciar el riesgo preexistente (que puede favorecer el ingreso) del atribuible al episodio infeccioso (formas graves de la enfermedad), aunque se recurra a ajuste multivariante. Asimismo, resulta complejo valorar la importancia clínica de las medidas de efecto consideradas, por la valoración subjetiva de los síntomas, la ausencia de medición del grado de afectación de los pacientes y el empleo de criterios poco definidos o heterogéneos de asma.
Validez externa y aplicabilidad de la evidenciaExisten dudas sobre la representatividad de las muestras de pacientes incluidos en los estudios y su aplicabilidad al conjunto de BA, por haber muchos trabajos que recogen distintas IRA de vías bajas (incluyendo neumonías y bronquitis) o infecciones por VRS (sin perfil clínico definido), en ocasiones con sibilantes previos. Por otra parte, no está claro si la evidencia disponible es aplicable a las BA atendidas en el medio extrahospitalario.
Balance coste-beneficio-riesgoNo existe información aplicable a nuestro medio sobre el impacto del riesgo de asma en los pacientes con BA. En un estudio119 se ha evaluado la morbilidad posterior a un ingreso por IRA baja por VRS, fundamentalmente consultas e ingresos por episodios de sibilantes.
Estimación del impacto de futuros estudiosPara establecer la magnitud del riesgo de sibilantes recurrentes o asma asociado a la BA, serían necesarios estudios de cohortes de recién nacidos suficientemente numerosas, en los que se valorara el riesgo basal y el atribuible a la aparición de una BA. En estos estudios se deberían emplear criterios explícitos y válidos de BA, seguimientos prolongados y completos y medidas de efecto que valoren el riesgo de asma de forma apropiada y precisa.
FinanciaciónFinanciado con una beca de la Fundación-Hospital Torrevieja (código de protocolo: BECA0001).
Conflictos de interesesTodos los autores implicados en la elaboración de este documento han realizado una declaración explícita de los conflictos de intereses por escrito. No constan conflictos de intereses que puedan influir en el contenido de este documento. No obstante, algunos autores (JFS, JMEB y SLLA) han declarado su participación en ponencias, congresos y proyectos patrocinados por distintas empresas de la industria farmacéutica relacionadas con el tema tratado (ALK-Abello, GSK y MSD).
AgradecimientosA María García-Puente Sánchez del Hospital de Torrevieja de Alicante y a Beatriz Muñoz Martín del Complejo Asistencial de Zamora por su labor como documentalistas.
Jesús M. Andrés de Llano, Servicio de Pediatría, Complejo Asistencial de Palencia, Palencia
María Aparicio Rodrigo, Centro de Salud Entrevías, Área 1 de Atención Primaria, SERMAS, Madrid
Ana Fe Bajo Delgado, Servicio de Pediatría, Hospital Virgen Concha Zamora
Albert Balaguer, Servicio de Pediatría, Hospital General de Catalunya, Universitat Internacional de Catalunya, Barcelona
Antonio Bonillo, Servicio de Pediatría, Hospital de Torrecárdenas, Almería
José Cristóbal Buñuel Álvarez, Centro de Salud, ABS Girona-4, ICS, Gerona
Andrés Canut Blasco, Sección Microbiología, Hospital Santiago Apóstol, Osakidetza-Servicio Vasco de Salud, Vitoria
José María Eiros Bouza, Servicio de Microbiología, Hospital Clínico Universitario de Valladolid, Facultad de Medicina de Valladolid, Valladolid
Jordi Fàbrega Sabaté, Servicio de Pediatría, Hospital Universitari Germans Trias i Pujol, Badalona
José Elviro Fernández Alonso, Servicio de Pediatría, Complejo Asistencial de Palencia, Palencia
Mercedes Fernández Rodríguez, Centro de Salud EAP Potes, SERMAS, Madrid
Santiago Lapeña López de Armentia, Servicio de Pediatría, Complejo Asistencial de León, León
Javier López Ávila, Centro de Salud San Bernardo Oeste, Salamanca
Cristina Molinos Norniella, Servicio de Pediatría, Hospital de Cabueñes, Gijón
Gloria Orejón de Luna, Centro de Salud General Ricardos, Área 11 de Atención Primaria, SERMAS, Madrid
Svetlana Todorcevic, Servicio de Pediatría, Hospital Materno Infantil de Gran Canaria, Las Palmas de Gran Canaria
Documentalistas: María García-Puente Sánchez, Hospital de Torrevieja, Alicante y Beatriz Muñoz Martín, Complejo Asistencial, Zamora
Avalado por la Asociación Española de Pediatría (AEP), Asociación Española de Pediatría de Atención Primaria (AEPap), Sociedad Española de Pediatría Extrahospitalaria y Atención Primaria (SEPEAP), Sociedad Española de Urgencias Pediátricas (SEUP), Sociedad Española de Infectología Pediátrica (SEIP), Sociedad Española de Neumología Pediátrica (SENP), Sociedad Española de Inmunología Clínica y Alergia Pediátrica (SEICAP), Sociedad Española de Cuidados Intensivos Pediátricos (SECIP), Sociedad Española de Neonatología (SEN) y Sociedad Española de Cardiología Pediátrica (SECPCC).