La fortificación de la leche materna (LM) es una práctica habitual para alcanzar los aportes necesarios para el crecimiento y desarrollo del recién nacido prematuro. Sin embargo, puede aumentar su osmolalidad. Según la Academia Americana de Pediatría, se recomienda no superar 450 mOsm/kg (aproximadamente 400 mOsm/l) en la alimentación del lactante, aunque el límite de la seguridad se estima entre 400-600 mOsm/kg.
El objetivo de este estudio es determinar la osmolalidad de la LM donada (LMD) descongelada y fortificada.
MétodoSe analizó la LMD de 6 madres sanas, sin fortificar y con 4 pautas de fortificación, realizando mediciones por triplicado de las muestras a tiempo 0, 4, 9 y 24 h tras su preparación. Entre mediciones se almacenó refrigerada (2-8°C). Los grupos de estudio fueron: 1) A: LMD no fortificada; 2) B: LMD con adición de vitaminas; 3) C: con adición de fortificante; 4) D: con adición de módulo proteico a dosis baja, y 5) E: con adición de módulo proteico a dosis alta. Las determinaciones de osmolalidad se realizaron un osmómetro crioscópico. El análisis de datos se realizó con R software (v.3.5.1).
ResultadosSe analizaron un total de 30 muestras (360 mediciones). La osmolalidad de la LMD a t = 0h fue 301 mOsm/kg (DE 5,2) y aumentó ligeramente con el tiempo a 308,11 mOsm/kg (DE 5,21) después de 24 h (t = 24h), manteniéndose en los límites de seguridad. La adición de vitaminas no aumentó la osmolalidad de manera significativa (grupo B). La adición de fortificante (C) y módulo de proteínas con dosis baja (D) o dosis alta (E) produjo un aumento de osmolalidad basal que se incrementó en el tiempo de manera estadísticamente significativa (p=0,007) pero sin diferencias entre los tipos C, D y E. Hubo diferencias entre la osmolalidad en t=0 con la fortificación según la ficha técnica del fabricante (339 mOsm/l) y los hallazgos en nuestro laboratorio (432,33 mOsm/l).
ConclusiónLos valores de osmolalidad hallados en las muestras de LMD descongelada son similares a los de otros estudios. La fortificación de la LMD y su conservación refrigerada entre 2-8°C durante 24h aumenta la osmolalidad, pero manteniéndose dentro de los límites de seguridad.
The fortification of maternal milk (MM) is a standard practice in order to achieve the requirements needed for the growth and development of the premature newborn. However, its osmolality could increase. According to the American Paediatrics Academy, it is recommended not to exceed 450 mOsm/kg (approximately 400 mOsm/L) in the diet of the infant, even though the safety limit is estimated to be between 400 and 600 mOsm/kg.
The aim of this study is to determine the osmolality of thawed and fortified donated MM (DMM).
MethodAn analysis was performed on DMM of 6 healthy mothers, without fortifying, and with 4 levels of fortification. Measurement of the samples was carried out in triplicate at 0, 4, 9, and 24hours after their preparation. They were stored refrigerated (2-8°C) between measurements. The study groups were: (A) Non-fortified DMM; (B) DMM with vitamins added; (C) with the addition of a fortifier; (D) with the addition of a low-dose protein formula; and (E) with the addition of a high-dose protein formula. The osmolality determinations were carried out using a freezing-point osmometer. The data analysis was performed using R software (v.3.5.1).
ResultsA total of 30 samples were analysed with 360 measurements. The osmolality of the DMM at t=0h was 301 mOsm/kg (SD 5.2) and slightly increased with time to 308.11 mOsm/kg (SD 5.21) after 24hours (t=24h), being maintained within the safety limits. The addition of vitamins (Group B) did not significantly increase the osmolality. The addition of a fortifier (C) and a low dose (D) or high dose (E) protein formula produced an increase in the baseline osmolality that increased statistically significantly in time (P=.007), but with no differences between the C, D, and E types. There were differences between the osmolality at t=0 with the fortification according to the manufacturer's data sheet (339 mOsm/l) and the findings in our laboratory (432.33 mOsm/l).
ConclusionThe osmolality values found in the thawed DMM samples were similar to those of other studies. The fortification of the DMM samples and their storage refrigerated at 2-8°C for 24h increased the osmolality, but keeping them within the safety limits.
La lactancia materna es el patrón de oro de alimentación de los recién nacidos prematuros (RNPT) por sus beneficios sobre la salud a corto y largo plazo. En caso de no disponer de lactancia materna propia, la LM donada (LMD) obtenida a partir de bancos de leche materna es considerada la mejor alternativa1. Sin embargo, en muchas ocasiones no es suficiente para cubrir sus necesidades nutricionales1-3. Para optimizar los aportes nutricionales en este grupo de población con la finalidad de mejorar su crecimiento y desarrollo, se han diseñado fortificantes para la leche materna (LM) que aportan energía, proteínas, minerales y vitaminas. La mayoría son preparados multicomponentes derivados de leche bovina, aunque también se han comercializado fortificantes a partir de LMD y algunos módulos aportan únicamente un componente4. Es práctica habitual en las unidades de Neonatología el uso de estos preparados, bien con una estrategia estándar o una individualizada, que ajusta los fortificantes en función del análisis de la leche o de la determinación del BUN. Estudios iniciales comparando este manejo nutricional en los RNPT con la alimentación con LM mostraban una mejor evolución de parámetros antropométricos, mejores resultados de balance nitrogenado y cifras de BUN, albúmina sérica, proteínas totales y prealbúmina, y normalización de los índices bioquímicos de estado mineral óseo5,6. Sin embargo, una revisión reciente únicamente encuentra diferencias antropométricas durante el ingreso hospitalario, pero no otros beneficios, complicaciones o efectos secundarios relevantes5. No obstante, la fortificación de la LM no está exenta de inconvenientes, ya que la manipulación de la leche disminuye la absorción de grasas y aumenta la osmolalidad. Osmolaridad y osmolalidad son 2términos que se usan para expresar la concentración de solutos totales u osmoles de una solución. En general, la osmolalidad mide la concentración de osmoles de soluto por kilogramo de solvente, expresado como mOsm/kg y la osmolaridad la concentración de osmoles de soluto por litro de solvente expresado en mOsm/l. Dado que el volumen de la solución cambia con la cantidad de soluto añadido, así como con los cambios de temperatura y presión, la osmolaridad es difícil de determinar. En cambio, la cantidad de solvente permanece constante independientemente de la temperatura y presión, siendo la osmolalidad más fácil de evaluar y se usa más comúnmente, siendo actualmente la medida estándar de concentración7.
La relación entre osmolalidades altas en la alimentación y riesgo de problemas gastrointestinales y enterocolitis necrosante (ECN) es un motivo de preocupación7. Para disminuir el riesgo, la Academia Americana de Pediatría (AAP) recomienda no superar la osmolalidad de 450 mOsm/kg (aproximadamente, 400 mOsm/l)8 en la alimentación del lactante. La evidencia científica de esta recomendación es escasa y discutible, ya que parece que la relevancia clínica no va más allá del enlentecimiento de la velocidad de vaciamiento gástrico7. Osmolalidades> 700 mOsm/kg en preparados terapéuticos o contrastes radiológicos sí se han relacionado con aumento ECN9, por lo que el límite de seguridad teórico se considera entre 400 y 600 mOsm/kg, pero no hay evidencia que respalde esta afirmación10.
Es práctica habitual en las unidades de Neonatología utilizar LMD pasteurizada y congelada. Está documentado que estos procesos afectan a la osmolalidad de la LM. Mientras que la pasteurización la disminuye, la congelación la aumenta, aunque no de manera significativa6. En la literatura encontramos datos contradictorios referentes a la cinética del cambio en la osmolalidad de una muestra de LM fortificada. Los estudios más recientes relacionan el aumento con la sobrecarga de solutos que se produce inmediatamente tras la adición del fortificante11,12, mientras que con el paso del tiempo el aumento de la osmolalidad no es tan significativo.
En nuestra unidad neonatal la práctica habitual de alimentación del RNPT es con LM o LMD cuando no disponemos de LM propia, y con fortificación estándar con un fortificante multicomponente y la adición, de forma individualizada, de módulo de proteína, si se requiere. Es también protocolo de la unidad suplementar con un polivitamínico a aquellos pacientes que no reciben fortificante de la leche materna.
No hemos encontrado en la literatura estudios que evalúen los aumentos en la osmolalidad que supone la adición en la LMD de los componentes utilizados en nuestra unidad.
Por este motivo, hemos diseñado este estudio para analizar los cambios en la osmolalidad de la LMD tras adición de un fortificante multicomponente de LM a base de proteína bovina y de un módulo de proteína, así como un suplemento polivitamínico. Con el fin de ajustarnos a la práctica clínica habitual, se ha estudiado el cambio de la osmolalidad a lo largo del tiempo.
MétodoDiseño del estudioEstudio prospectivo llevado a cabo en los Servicios de Neonatología y Farmacia del Hospital Universitario y Politécnico La Fe de Valencia, desde mayo del 2018 hasta febrero del 2019. Se analizó la osmolalidad de LMD donada al Banco de Leche Materna de la Comunidad Valenciana (BLMCV), que no cumplía los requisitos establecidos por el protocolo del banco de leche necesarios para su administración a pacientes, pero cuyas donantes han firmado el consentimiento para su utilización en investigación.
Análisis de los componentes de la leche materna donadaEl análisis de macronutrientes (grasa, proteína y lactosa) de la leche ha sido realizado con el analizador Miris HMA© (Miris Holding AB, Uppsala, Suecia) mediante la técnica de espectroscopia por infrarrojos, los resultados se muestran en la tabla 1. Las muestras son descongeladas y calentadas a 40°C y homogenizadas (1,5 s por 1ml de muestra) con un homogeneizador de ultrasonidos (VCX 130; Sonics & Material, Newtown, CT, EE. UU.) previo al análisis. Siguiendo el protocolo de la unidad, se ha realizado una única medición y si el valor no estaba en el rango habitual, esta se ha repetido.
Composición y osmolalidad de las 6 leches materna donadas
| Componente | Leche | |||||
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | |
| Proteínas (g/100 ml) | 2,1 | 1 | 0,5 | 1,8 | 0,9 | 0,8 |
| Grasas (g/100 ml) | 5,2 | 2,6 | 1,6 | 2,4 | 3,5 | 2,7 |
| Lactosa (g/100 ml) | 6,9 | 7,5 | 7,9 | 6,9 | 7,7 | 7,7 |
| Energía (Kcal/100 ml) | 85 | 59 | 49 | 59 | 67 | 60 |
| Osmolalidad (mOsm/kg)a | 310 ± 3,2 | 303 ± 2,6 | 300 ± 1,5 | 295 ± 1,5 | 298 ± 0,6 | 301 ± 1,2 |
La fortificación se ha realizado siguiendo el protocolo de la unidad y las recomendaciones de la casa comercial. Se ha utilizado el fortificante PreNAN FM85© (Nestlé Infant Nutrition, Vevey, Suiza), el suplemento proteico Resource© Instant Protein (Nestlé Health Science, Vevey, Suiza) e Hidropolivit© (Grupo Menarini, Badalona, España) como suplemento polivitamínico (composiciones en tablas 2 y 3).
Composición de fortificante de leche materna y suplemento de proteínas utilizado
| PreNAN FM 85© (por 100 g) | Resource Instant Protein© (por 100 g) | |
|---|---|---|
| Proteínas | 35,5 g | 90,3 g |
| Hidratos de carbono | 32,4 g | 0,2 g (lactosa) |
| Grasas | 18,1 g | 1 g |
| Na | 0,9 g | 15 mg |
| K | 1,2 g | 15 mg |
| Ca | 1,9 g | 1,4 g |
| P | 1,1 g | 0,74 g |
| Mg | 0,1 g | |
| Cl | 0,8 g | |
| I | 0,4 mg | |
| Zn | 23,5 mg | |
| Cu | 1,3 mg | |
| Fe | 45 mg | |
| Se | 93μg | |
| Energía | 435 Kcal | 371 Kcal |
| Osmolaridad | 339 mOsm/la |
Contenido en vitaminas de los compuestos utilizados
| Hidropolivit© | PreNAN FM 85© | ||
|---|---|---|---|
| Componente | 1 ml=28 gotas | 4 gotas | 1 g |
| Retinol (vit. A) | 1.500 UI | 214 UI | 297 UI |
| Rivoflavina (vit. B2) | 2 mg | 0,3 mg | 0,05 mg |
| Nicotinamida (vit. PP) | 12,5 mg | 1,8 mg | |
| Piridoxina (vit. B6) | 1,6 mg | 0,2 mg | 0,03 mg |
| Biotina (vit. H) | 0,125 mg | 0,018 mg | 0,001 mg |
| Ácido ascórbico (vit. C) | 50 mg | 7,14 mg | 5 mg |
| Colecalciferol | 600 UI | 85 UI | 36 UI |
| Acetato DL-A-tocoferilo (vit. E) | 10 mg | 1,4 mg | 1 mg |
Fuente: Menarini y Nestlé Infant Nutrition.
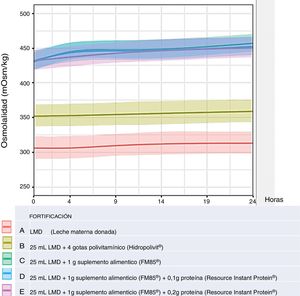
Cada una de las muestras se analizó sin aditivo (fortificación tipo A: LMD sin fortificar) y con 4 tipos diferentes de fortificación: fortificación tipo B: adición a 25ml de LMD 4 gotas de polivitamínico Hidropolivit©; fortificación tipo C: adición a 25ml de LMD de 1g de PreNAN FM85©; fortificación tipo D: adición a 25ml de LMD de 1g de PreNAN FM85© y 0,1g de Resource© Instant Protein y fortificación tipo E: adición a 25ml de LMD de 1g de PreNAN FM85© y 0,2g de Resource© Instant Protein.
La LMD fue conservada congelada a –20°C desde su extracción hasta su utilización y descongelada a temperatura ambiente previo a la preparación.
La adición de la fortificación se hizo de manera escalonada, agitando el preparado con un vórtice (Vortamix, Argos Technologies, South Scottsdale Court, EE. UU.) hasta conseguir la homogenización de la preparación.
Osmómetro y medición de la osmolalidadLa medición de la osmolalidad se realizó con el osmómetro Fiske 210 (Advanced Instruments Inc., Norwood, Massachusetts, EE. UU.), que determina la concentración de soluciones midiendo el punto de congelación. Utiliza termistores de alta precisión para medir la temperatura de la muestra, controlar el nivel de sobreenfriamiento e inducir congelación, además de medir el punto de congelación de la muestra, midiendo diferencias de±1 mOsm/kg de H2O13. En general, los osmómetros de punto de congelación son los utilizados por la industria y son el estándar en laboratorios de química clínica e investigación farmacéutica. Las mediciones son rápidas, precisas y es la técnica más ampliamente referenciada para la medición de la osmolalidad6.
El instrumento se calibró con 20μL de la solución de referencia Accuref 290 (Advanced Instruments Inc., Norwood, Massachusetts, EE. UU.). Todas las muestras se prepararon en volúmenes de 25ml y los datos se convirtieron por 100ml de LM. Para asegurar una extracción de alícuotas representativa de LM, se homogeneizaron las muestras (volumen de 25ml) durante 30 s utilizando un agitador tipo vórtice (Vortamix, Argos Technologies, South Scottsdale Court, EE. UU.). El nivel de osmolalidad se determinó en LM nativa y con las diferentes fortificaciones, realizando mediciones por triplicado de las muestras a tiempo 0 (inmediatamente tras la adición), 4, 9 y 24h. Entre mediciones, la leche se almacenó refrigerada entre 2-8°C y se atemperó justo antes para realizar la medición. Se utilizó para cada medición 20μL de muestra y los resultados se expresaron como osmolalidad total en mOsm/kg.
Análisis estadísticoEl análisis estadístico de los datos se realizó con R software (v.3.5.1) y paquetes clicR (v.0.4.22) e lme4 (v.1.1-18-1) (The Freesoftware Foundation, Boston, USA). Los datos se resumieron utilizando la media (desviación típica) y mediana (1.er y 3.er cuartil) en el caso de las variables numéricas y la frecuencia absoluta (%) en el caso de variables cualitativas. Para ver la evolución de la osmolalidad de cada alícuota en el tiempo según el tipo de fortificación se ajustó un modelo de regresión lineal mixto, introduciendo cada leche como factor aleatorio y aplicando una interacción entre fortificación y tiempo. Se tuvo en cuenta la composición de las distintas muestras de LMD y la cantidad de grasa, proteína y lactosa se añadieron como variables de confusión. Para ver la evolución de la leche según su composición se ajustó un modelo de regresión lineal utilizando cada leche como factor aleatorio.
ResultadosSe analizó un total de 30 muestras de LMD de 6 madres sanas, sin fortificar y con 4 pautas de fortificación. Se analizaron en 4 tiempos distintos por triplicado, resultando un total de 360 determinaciones. La osmolalidad expresada como media ± DE de la LMD a t=0h (n=18) fue 301 ± 5,2 mOsm/kg), que coincide con lo publicado en la literatura4,6,14. La osmolalidad de la LMD (fortificación tipo A) conservada refrigerada entre 2 y 8°C aumenta ligeramente con el tiempo, hasta alcanzar a t=24h una media ± DE de 308,11 ± 5,21 mOsm/kg (p=0,021), manteniéndose en los límites de seguridad para su administración a RNPT. La adición de vitaminas (fortificación tipo B) no aumentó la osmolalidad de manera clínicamente significativa con respecto a la LMD sin fortificar, alcanzando una osmolalidad de 347,33 ± 19,22 y un aumento en el tiempo hasta 354,11 ± 19,12 mOsm/kg a las 24h, sin diferencia estadística al aumento del tipo A (p=0,971). La adición de PreNAN FM85© módulo de proteínas sí supuso un aumento de osmolalidad basal que además se incrementó más en el tiempo de manera estadísticamente significativa (p <0,001, 0,007 y 0,007 para C, D y E, respectivamente) pero sin diferencias entre los tipos C, D y E. Véanse los resultados en la tabla 4 y figura 1.
Media ± desviación estándar de osmolalidad (mOsm/kg) en cada tipo de fortificación y medida en distintos tiempos
| Tiempo (H)Tipo | 0 | 4 | 9 | 24 | p valor (cada fortificación consigo misma en el tiempo) | p valor (cada fortificación con respecto a fortificación A) |
|---|---|---|---|---|---|---|
| A (n=6)LMD | 301,44 ± 5,20 | 301,56 ± 5,63 | 304,89 ± 4,96 | 308,11 ± 5,21 | 0,021 | No aplica |
| B (n=6)LMD + Hidropolivit© | 347,33 ± 19,22 | 348,17 ± 21,44 | 349,67 ± 19,58 | 354,11 ± 19,12 | <0,001 | 0,971 |
| C (n=6)LMD + FM85© | 432,33 ± 14,49 | 446,94 ± 11,56 | 449,94 ± 10,67 | 459,18 ± 11,18 | 0,01 | <0,001 |
| D (n=6)LMD + FM8,© + ReIP© (0,1 g proteína) | 433,94 ± 13,53 | 445,22 ± 8,64 | 447,89 ± 8,24 | 454,28 ± 9,74 | 0,02 | 0,007 |
| E (n=6)LMD + FM85© + ReIP© (0,2 g proteína) | 435 ± 13,98 | 440,28 ± 11,45 | 445,72 ± 11,17 | 453,22 ± 8,15 | 0,038 | 0,007 |
LMD: Leche materna donada; ReIP: Resource Instant Protein©.
En el caso de la fortificación con PreNAN FM85© (tipo C) siguiendo las recomendaciones del fabricante, la osmolalidad obtenida a t=0 fue 432,33 mOsm/kg (14,49), distinta de la que consta en ficha técnica del fabricante (osmolaridad=339 mOsm/l, que equivaldría a 381 mOsm/kg), pero se halla dentro de los límites considerados seguros.
DiscusiónLos elevados requerimientos nutricionales de los RNPT no se alcanzan con la LM exclusivamente, por lo que es recomendable su fortificación. Pero esta práctica se ha relacionado con aumento de la intolerancia digestiva y de reflujo gastroesofágico15. La asociación con enfermedad más grave como la ECN es controvertida y no hay evidencia clara al respecto. La ECN es una enfermedad multifactorial y se ha hipotetizado que los fortificantes de LM, por aumentar la osmolalidad en la luz intestinal, podrían contribuir a su desarrollo11. Aunque parece haber cada vez más evidencia en contra de esta hipótesis, hay que ser cautos a la hora de elegir el tipo de fortificante para no exponer a nuestros pacientes a un riesgo de momento no descartado7. Los primeros estudios de osmolalidad de LM fortificada mostraban cifras preocupantes superiores a 450 mOsm/kg considerados seguros por la AAP. Hoy en día, con la aparición de nuevos preparados y nuevas estrategias de fortificación que en ocasiones combinan varios preparados, nos encontramos ante una falta de información referente al cambio en la osmolalidad que se induce en la LM y la LMD de banco, que además sufre un procesado que también modifica su osmolalidad.
Recientemente, una encuesta realizada en varias unidades neonatales europeas de nivel iii y otra a nivel nacional revelaban gran variabilidad en las prácticas de manipulación de la LM, incluida la fortificación16,17. Las diferencias en estructura, dotación de personal, disponibilidad de LMD y productos para fortificar disponibles implican que cada unidad debe protocolizar el uso de LM y LMD y la fortificación, orientándolo a la mayor efectividad y seguridad.
La práctica habitual en nuestra unidad de tercer nivel consiste en fomentar intensamente la alimentación con LM propia a todos los RNPT con muy bajo peso al nacer y también disponemos de LMD proporcionada por el BLMCV, para los casos en los que LM propia no esté disponible o no alcance a cubrir las necesidades. La LMD ha sido previamente pasteurizada según el protocolo del BLMCV (pasteurización Holder, 62,5°C durante 30 min) y se conserva congelada hasta su administración. Así mismo, utilizamos una estrategia de fortificación estándar inicialmente con un fortificante multicomponente de manera rutinaria, ajustando en casos seleccionados el aporte de proteínas con la adición de un módulo de proteínas de una manera más individualizada en función del análisis del metabolismo proteico o del análisis nutricional de la LM o LMD. La fortificación individualizada es recomendable en prematuros que no alcanzan el ritmo de crecimiento esperado, sobre todo aquellos que se alimentan con LMD, dada la variabilidad en la composición de esta18. El análisis de macronutrientes se realiza con por espectroscopia por infrarrojos, con una utilidad demostrada por nuestro grupo en un trabajo anterior19. Kreissl et al. documentan un incremento de la osmolaridad de la leche de 297 mOsm/L a 436 mOsm/L con la adición de un fortificante a base de proteína bovina, y un incremento adicional de 23,5 mOsm/l por cada 0,5g de suplemento proteico6. En este trabajo se utilizaban cantidades de proteínas que excedían en mucho las recomendaciones sobre los aportes a los RNPT publicadas por la ESPGHAN2. No hemos encontrado en la literatura datos sobre esta nueva formulación de fortificante de LM multicomponente PreNAN FM85©, combinado con leche de banco, que ha sufrido proceso de pasteurización y congelación.
Tras el análisis de nuestras muestras, podemos afirmar que en nuestra práctica clínica habitual el máximo nivel de fortificación utilizado, aunque supera los 450 mOsm/kg, considerados como límite seguro por AAP, con un máximo de 459,18 mOsm/kg8,18 no rebasa en ningún caso los 600 mOsm/kg, estando dentro de la zona que se cree segura para la alimentación de los RNPT10.
En nuestros resultados parece existir una tendencia a la disminución de la osmolalidad con el aumento del módulo de proteínas. El aporte es +0,1 o +0,2g de proteínas por 25ml de LMD, que en cómputo total de las proteínas de la muestra no es significativo y de hecho no hay diferencias estadísticamente significativas entre los distintos tipos de fortificación C, D y E. Este hecho está en consonancia con los resultados de otros trabajos que promedian el aumento de la osmolalidad de 1g de proteína hidrolizada, igual que la que contiene el fortificante utilizado en nuestro estudio, en 38 mOsm/kg20, lo que supondría diferencias entre nuestros tipos C, D y E de 3,8 mOsm/kg, lo cual resulta clínicamente no significativo y explicaría que estadísticamente tampoco lo sea.
En cuanto a la adición del polivitamínico, siempre que la ingesta enteral sea con aportes completos, con tomas de volumen superior a unos 20ml, es una práctica segura que disminuye manipulación sin constituir un riesgo de intolerancia gástrica secundaria al aumento de la osmolalidad. Estos datos coinciden con otras publicaciones21,22. En casos de tomas de volumen inferior se podría contemplar la administración de la cantidad diaria repartida en mayor número de dosis para disminuir la osmolalidad en cada administración. Siempre que la LM o LMD esté fortificada con PreNAN FM85©, y los aportes superen los 100ml/kg al día, no precisa polivitamínico, ya que las cantidades recomendadas se alcanzan con el fortificante y es conveniente evitar la combinación de distintos productos.
Referente a la cinética del cambio inducido en la osmolalidad, nuestros resultados coinciden con lo publicado por otros autores11,12, objetivándose un aumento de la osmolalidad inmediatamente tras la preparación (el 86% del aumento total) siendo su conservación refrigerada 24h responsable del 14% del aumento total. La adición del fortificante es responsable de la mayor parte del aumento de la osmolalidad por suponer un incremento en la carga de solutos, en cuanto a la degradación de los componentes de la leche o los fortificantes a lo largo del tiempo, principalmente por el efecto de la amilasa de la LM liberando sustancias con poder osmolar (mono o disacáridos), es un proceso mucho más lento y que contribuye de manera menos importante en el aumento de la osmolalidad y es responsable del aumento que tiene la preparación a lo largo del tiempo11. Este dato apoya la decisión de contar, en un servicio de Unidad de Cuidados Intensivos Neonatales, con de una zona destinada a la preparación de la alimentación de prematuros que confiera seguridad y evite la contaminación. Incluso, aunque lo ideal sería la preparación de la alimentación inmediatamente antes de su administración, se podría considerar la preparación la alimentación para 24h en un único acto al día, por la misma persona, con la dedicación del tiempo necesario para minimizar errores, evitar contaminación, etc. y esto no supondría un menoscabo en la seguridad del paciente, en cuanto a osmolalidad se refiere.
ConclusionesLos valores de osmolalidad hallados en las muestras de LMD descongelada son similares a los publicados en otros estudios. Los aumentos de osmolalidad por la conservación de la LMD descongelada refrigerada entre 2-8°C se encuentran dentro de los límites aceptados como seguros, por lo que la preparación de la alimentación de estos recién nacidos en una Unidad de Cuidados Intensivos Neonatales puede realizarse una vez al día y conservarse refrigerada sin que ello resulte en un aumento de osmolalidad peligroso para su administración. El aumento de osmolalidad que supone la adición de un polivitamínico a la LMD no fortificada con otros aditivos no supera el límite considerado seguro para la alimentación del RNPT.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Queremos agradecer a Amparo Ramón y Antonia Gazquez, por su contribución en la obtención y análisis nutricional de las muestras de LMD, y a Antonio J. Cañada Martínez por el apoyo en el análisis estadístico.
Presentación previa: abstract oral presentado en el XXVII Congreso de Neonatología y Medicina Perinatal, Madrid, del 2 al 4 de octubre del 2019.