Los pacientes críticos frecuentemente presentan inestabilidad hemodinámica que puede verse empeorada por la administración de algunos fármacos. El omeprazol es un fármaco muy empleado en la profilaxis de la hemorragia digestiva en estos pacientes, pero se desconocen sus efectos cardiovasculares. El objetivo fue estudiar los cambios hemodinámicos producidos por la administración de omeprazol por vía intravenosa en niños críticos y analizar si existen diferencias entre 2 dosis diferentes de omeprazol.
Material y métodosSe realizó un estudio prospectivo observacional aleatorizado, que incluyó niños críticos entre un mes y 14 años de edad, que precisaban profilaxis de hemorragia digestiva. La muestra aleatoria fue de 37 pacientes de los cuales, 19 recibieron omeprazol por vía intravenosa 0,5mg/kg cada 12 h y 18 omeprazol por vía intravenosa 1mg/kg cada 12 h. La dosis correspondiente se administró en 20 min mediante bomba de infusión continua. Se recogieron la frecuencia cardiaca, presión arterial sistólica, media y diastólica, presión venosa central y el electrocardiograma basal, a los 15, 30, 60 y 120min de la infusión.
ResultadosLa edad media fue de 27,7±33,3 meses. Todos los pacientes recibieron dopamina y 14, adrenalina. No se produjeron modificaciones significativas en ninguna de las variables estudiadas. Ningún paciente precisó modificación del tratamiento inotrópico. No se objetivaron diferencias entre las 2 dosis de omeprazol.
ConclusionesEl omeprazol por vía intravenosa es un fármaco hemodinámicamente seguro en niños críticos, a cualquiera de las 2 dosis utilizadas.
Critical patients usually have hemodynamic disturbances which may become worse by the administration of some drugs. Omeprazole is a drug used in the prophylaxis of the gastrointestinal bleeding in these patients, but its cardiovascular effects are unknown. The objective was to study the hemodynamic changes produced by intravenous omeprazole in critically ill children and to find out if there are differences between two different doses of omeprazole.
Material and methodsA randomized prospective observational study was performed on 37 critically ill children aged from 1 month to 14 years of age who required prophylaxis for gastrointestinal bleeding. Of these, 19 received intravenous omeprazole 0.5mg/kg every 12hours, and 18 received intravenous omeprazole 1mg/kg every 12hours. Intravenous omeprazole was administered in 20minutes by continuous infusion pump. Heart rate, systolic, diastolic and mean arterial blood pressure, central venous pressure and ECG were recorded at baseline, and at 15, 30, 60 and 120minutes of the infusion.
ResultsThere were no significant changes in the electrocardiogram, heart rate, blood pressure and central venous pressure. No patients required inotropic therapy modification. There were no differences between the two doses of omeprazole.
ConclusionsIntravenous omeprazole administration of 0.5mg/kg and 1mg/kg is a hemodynamically safe drug in critically ill children.
Los pacientes críticos presentan un riesgo aumentado de hemorragia digestiva debida a lesión aguda de la mucosa gástrica (LAMG)1–3. La LAMG está producida generalmente por una suma de factores, que incluyen la presencia de ácido gástrico, la disminución del flujo sanguíneo y la alteración de la barrera de moco y bicarbonato4,5. El riesgo de hemorragia digestiva (HD) es mayor cuanto mayor es la gravedad del paciente y mayor número de factores de riesgo estén presentes6.
Los bloqueantes H2 y los inhibidores de la bomba ATPasa son los fármacos más utilizados para la profilaxis de la HD en los pacientes críticos adultos y niños7–9. Los antiácidos y el sucralfato son utilizados con menor frecuencia9.
Múltiples estudios han comparado la eficacia y los efectos secundarios de los fármacos utilizados para la profilaxis de la HD en el paciente crítico7,10,11. Ya que la eficacia de los bloqueantes H2 y los inhibidores de la ATPasa es similar, la decisión de utilizar uno u otro tipo de fármaco podría ser tomada de acuerdo con su perfil de seguridad.
Los pacientes críticos frecuentemente presentan inestabilidad hemodinámica, que puede verse empeorada por la administración de algunos fármacos. La administración de bloqueantes H2 puede producir hipotensión, sobre todo si su administración es rápida12. No existen estudios que hayan analizado los efectos cardiovasculares de los inhibidores de la bomba de protones (IBP) en este tipo de pacientes.
El objetivo de este trabajo fue estudiar los cambios hemodinámicos producidos por la administración de omeprazol por vía intravenosa en niños críticos y analizar si existen diferencias entre 2 dosis diferentes de omeprazol.
Pacientes y métodosSe realizó un estudio prospectivo observacional en el que se incluyó a los niños entre un mes y 14 años de edad ingresados en la unidad de cuidados intensivos pediátricos (UCIP) que precisaban profilaxis de HD. El protocolo fue aceptado por el comité ético del hospital y los pacientes fueron incluidos en el estudio tras obtenerse el consentimiento informado escrito de los padres o tutores. Los pacientes fueron distribuidos de forma aleatorizada mediante la utilización de una tabla de aleatorización en uno de los 2 grupos terapéuticos. El grupo A incluyó a 19 pacientes, a los que se administró omeprazol por vía intravenosa, 0,5mg/kg cada 12h (dosis máxima 40mg/dosis). El grupo B incluyó a 18 pacientes, a los que se administró omeprazol por vía intravenosa 1mg/kg cada 12h (dosis máxima 40mg/dosis).
En todos los casos, la infusión del omeprazol se preparó diluyendo el vial de 40mg de omeprazol en 100ml de suero fisiológico. La dosis se administró en 20min mediante bomba de infusión continua para evitar efectos debidos a la forma de infundir el fármaco.
La repercusión hemodinámica del omeprazol se realizó analizando la evolución de las variables de frecuencia cardiaca, presión arterial sistólica, media y diastólica, presión venosa central y registro del electrocardiograma de forma basal, y a los 15, 30, 60 y 120min de la infusión. La frecuencia cardiaca se monitorizó mediante electrocardiograma continuo y la presión venosa central y presión arterial, mediante monitorización invasiva. Se realizó un análisis comparativo entre las 2 dosis de omeprazol. El análisis estadístico se realizó mediante un modelo ANOVA de medidas repetidas. Se consideró significativa una p<0,05.
ResultadosSe estudió a 37 niños, 14 niñas y 23 niños. La edad media±DE fue de 27,7±33,3 meses (rango 1-84 meses). El 97,2% ingresó en la UCIP en el postoperatorio de cirugía cardiaca. Los 37 pacientes recibieron tratamiento con dopamina (dosis media 7,3±2,9 μg/kg/min; rango 5-10 μg/kg/min) y 14 con adrenalina (dosis media 0,22±0,15 μg/kg/min; rango 0,09-0,5 μg/kg/min).
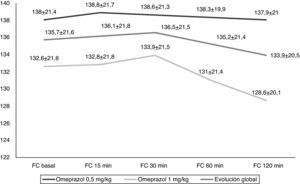
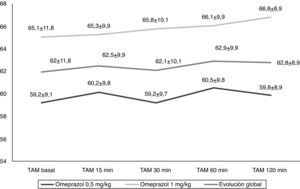
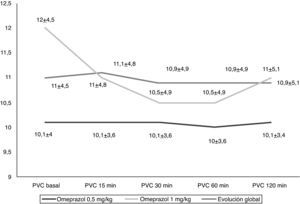
Tras la administración de omeprazol no se produjeron modificaciones significativas en el electrocardiograma, la frecuencia cardiaca (fig. 1), la presión arterial (fig. 2) ni de la presión venosa central (fig. 3) en los 120min de evolución de forma global ni al analizar las 2 dosis de omeprazol por separado (tabla 1).
Evolución de la frecuencia cardiaca global y según la dosis de omeprazol. No existieron cambios significativos en la evolución global (p=0,234). No existieron diferencias significativas entre las 2 dosis empleadas (p=0,59). FC basal: frecuencia cardiaca basal; FC 15min: frecuencia cardiaca 15 min; FC 30min: frecuencia cardiaca 30min; FC 60min: frecuencia cardiaca 60 min; FC 120min: frecuencia cardiaca 120min.
Evolución de la presión arterial global y según la dosis de omeprazol. No existieron cambios significativos de forma global (p=0,89). No existieron diferencias significativas entre las 2 dosis empleadas (p=0,66). PAM basal: presión arterial media basal; PAM 15min: presión arterial media 15 min; PAM 30min: presión arterial media 30 min; PAM 60min: presión arterial media 60min; PAM 120min: presión arterial media 120min.
Evolución de la presión venosa central global y según la dosis de omeprazol. No existieron cambios significativos de forma global (p=0,35). No existieron diferencias significativas entre las dos dosis empleadas (p=0,25). PVC basal: presión venosa central basal; PVC 15min: presión venosa central 15 min; PVC 30min: presión venosa central 30 min; PVC 60min: presión venosa central 60min; PVC 120min: presión venosa central 120min.
Evolución variables hemodinámicas y dosis de omeprazol
| Omeprazol 0,5mg/kg/dosis | Omeprazol 1mg/kg/dosis | |
| FC basal | 138±21,4 (102-190) | 132,6±21,6 (85-193) |
| PAS basal | 84±12,8 (55-127) | 88±14,6 (58-120) |
| PAD basal | 48±8,2 (32-75) | 53±8,9 (34-83) |
| PAM basal | 59±9,1 (40-98) | 66±11,8 (33-97) |
| PVC basal | 10±4 (3-22) | 12±4,5 (4-24) |
| FC 15min | 138,8±21,7 (96-191) | 132,8±21,8 (86-193) |
| PAS 15min | 84±12,8 (54-116) | 87±14,2 (70-121) |
| PAD 15min | 47±7,9 (30-64) | 53±55,8 (36-66) |
| PAM 15min | 59±9,7 (39-87) | 65±9,9 (43-84) |
| PVC 15min | 10±3,6 (5-22) | 11±4,8 (4-24) |
| FC 30min | 138,6±21,3 (100-189) | 133,9±21,5 (84-194) |
| PAS 30min | 84±13,2(57-121) | 88±14,7 (62-125) |
| PAD 30min | 46±7,9 (31-66) | 53±8,8 (36-73) |
| PAM 30min | 58±9,7 (40-90) | 64±10,1 (44-86) |
| PVC 30min | 9±3,6 (4-22) | 10±4,9 (5-24) |
| FC 60min | 138,3±19,9 (103-187) | 131±21,4 (80-194) |
| PAS 60min | 85±13,3 (63-118) | 88±13,8 (70-110) |
| PAD 60min | 46±7,9 (34-67) | 53±7,6 (39-70) |
| PAM 60min | 60±9,7 (43-85) | 64±9,9 (47-84) |
| PVC 60min | 10±3,6 (2-21) | 10±4,9 (4-24) |
| FC 120min | 137,9±21 (96-188) | 128,6±20,1 (88-195) |
| PAS 120min | 84±12,3 (58-115) | 90±13,8 (72-137) |
| PAD 120min | 46±7,1 (34-66) | 52±8,8 (41-75) |
| PAM 120min | 60±8,9 (43-87) | 66±8,9 (50-82) |
| PVC 120min | 9±7,4 (2-23) | 11±5,1 (3-22) |
FC: frecuencia cardiaca; PAD: presión arterial diastólica; PAM: presión arterial media; PAS: presión arterial sistólica; PVC: presión venosa central; min: minutos.
Los datos se presentan como media±desviación estándar (rango).
Ninguno de los pacientes precisó modificación del tratamiento inotrópico como consecuencia de la administración del omeprazol.
DiscusiónLos IBP como el omeprazol son compuestos benzoimidazólicos que inhiben de forma selectiva e irreversible la ATPasa intercambiadora de K+/H+ mediante la formación de puentes disulfuro entre el fármaco y los residuos de cisteína de la subunidad alfa de la ATPasa. El omeprazol se administra en forma de prodroga que requiere un medio ácido para su activación. La inhibición de la bomba de protones depende no solo del pH del medio, sino también de la concentración de omeprazol.
La bomba ATPasa intercambiadora de K+/H+ situada a nivel gástrico es responsable de la absorción de K+ y la secreción de H+ activa en contra del gradiente electroquímico. La función principal es la acidificación del contenido gástrico13,14.
Sin embargo, estudios experimentales realizados en ratas han permitido, mediante técnicas de reacción en cadena de la polimerasa, inmunocitoquímica y Western blot, aislar la ATPasa K+/H+ en los miocitos de este roedor15. Otros estudios han demostrado también su expresión en cobayas, en el músculo liso de los vasos de animales de experimentación16 y en el músculo de la vía aérea de humanos17.
Algunos estudios experimentales han analizado los efectos hemodinámicos de los inhibidores de la bomba ATPasa. Estudios realizados en cobayas y ratas han demostrado la sensibilidad de la bomba de protones cardiaca al omeprazol18,19.
Yenisehirli et al.20 valoraron el efecto de algunos de los IBP, como el omeprazol, sobre el músculo liso auricular de ratas, encontrando que los IBP tenían un efecto inotrópico positivo, cronotrópico negativo y antiarritmogénico. Sin embargo, la concentración requerida para lograr estos efectos era muy superior a la que se necesitaba para inhibir la ATPasa gástrica, probablemente porque su expresión a nivel cardiaco es mucho menor que a nivel gástrico y porque el pH del medio es relativamente básico.
Parece que la ATPasa K+/H+ desempeña cierto papel en las propiedades fisiológicas del músculo cardiaco, pudiendo intervenir en procesos patológicos como el fallo cardiaco.
A nivel vascular, el omeprazol ha demostrado de forma experimental capacidad para inducir relajación del anillo aórtico en ratas21 y de arterias aisladas humanas previamente contraídas por agentes agonistas22. Esta enzima ayuda a mantener el gradiente de K+ y el pH intracelular en las células de la pared muscular de los vasos22. Los efectos producidos a este nivel son debidos a la regulación del calcio intracelular más que a la inhibición de ATPasa K+/H+ y, al igual que ocurre a nivel cardiaco, requieren dosis muy superiores a las necesarias para suprimir la secreción ácida gástrica22.
Al contrario de los efectos observados a nivel experimental, nuestro estudio no mostró variaciones significativas sobre la frecuencia cardiaca, la presión arterial, la presión venosa central o el electrocardiograma. Estos datos son similares a los publicados por otros autores sobre ratas anestesiadas23. Las diferencias entre los estudios in vivo y los estudios in vitro pueden ser debidas a que in vivo la concentración plasmática del omeprazol disminuye rápidamente por el efecto de la distribución del compartimento vascular al periférico, la unión a proteínas, el metabolismo y la excreción23, y la pequeña concentración activa que queda no es suficiente para provocar efectos cardiovasculares.
Nuestro estudio no encontró diferencias entre las 2 dosis utilizadas, por lo que ambas son igualmente seguras desde el punto de vista cardiovascular.
Concluimos que el omeprazol, a cualquiera de las 2 dosis utilizadas, es un fármaco hemodinámicamente seguro en niños críticos. Esta puede ser una ventaja sobre los fármacos bloqueantes H2, como la ranitidina, en los niños críticamente enfermos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.