Estudiar la nutrición parenteral (NP) pediátrica en 2008 en un hospital terciario. Conocer su adecuación con las guías de práctica clínica actuales.
Material y métodosEstudio longitudinal, descriptivo y retrospectivo de las historias clínicas de pacientes menores de 16 años (excluidos los ingresados en las unidades neonatales) que recibieron NP en 2008. Recogimos datos demográficos y datos de la NP: indicación, composición en el primer día, lípidos, aminoácidos, micronutrientes, tipo de mezcla, estandarización, adición de medicamentos, duración, acceso venoso, causa de interrupción y complicaciones.
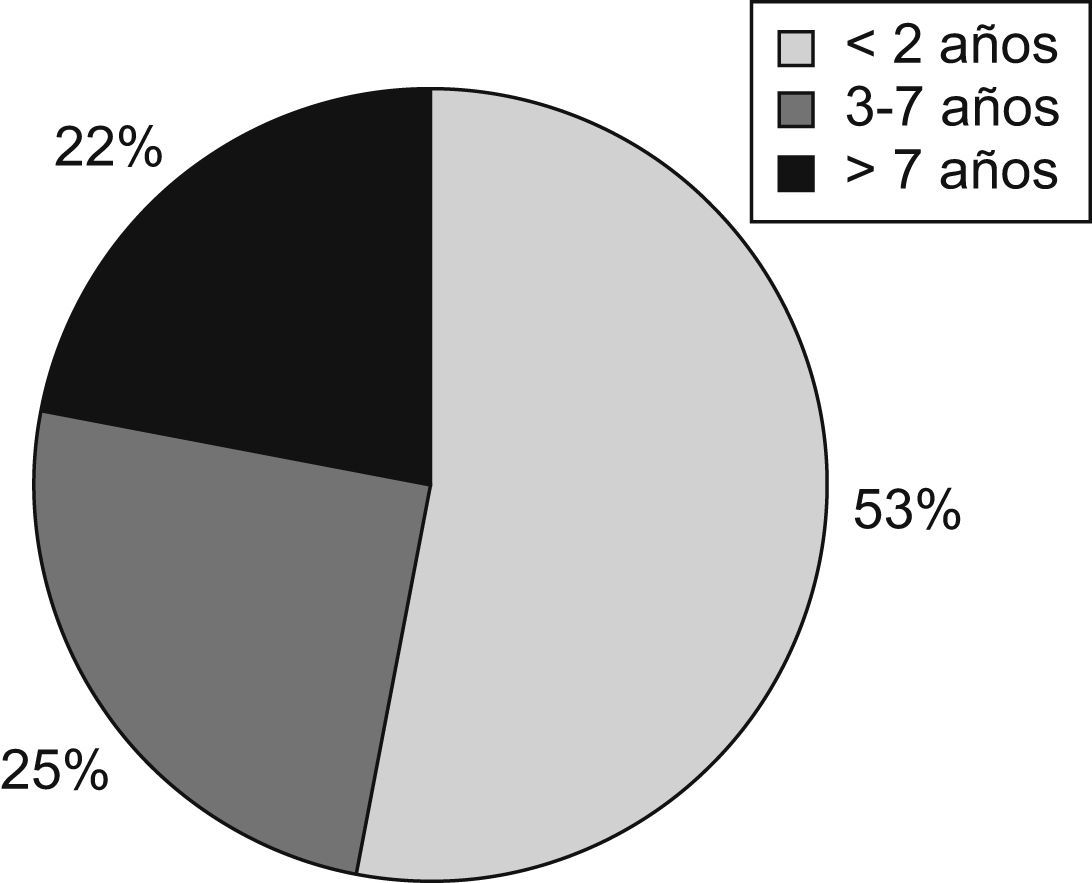
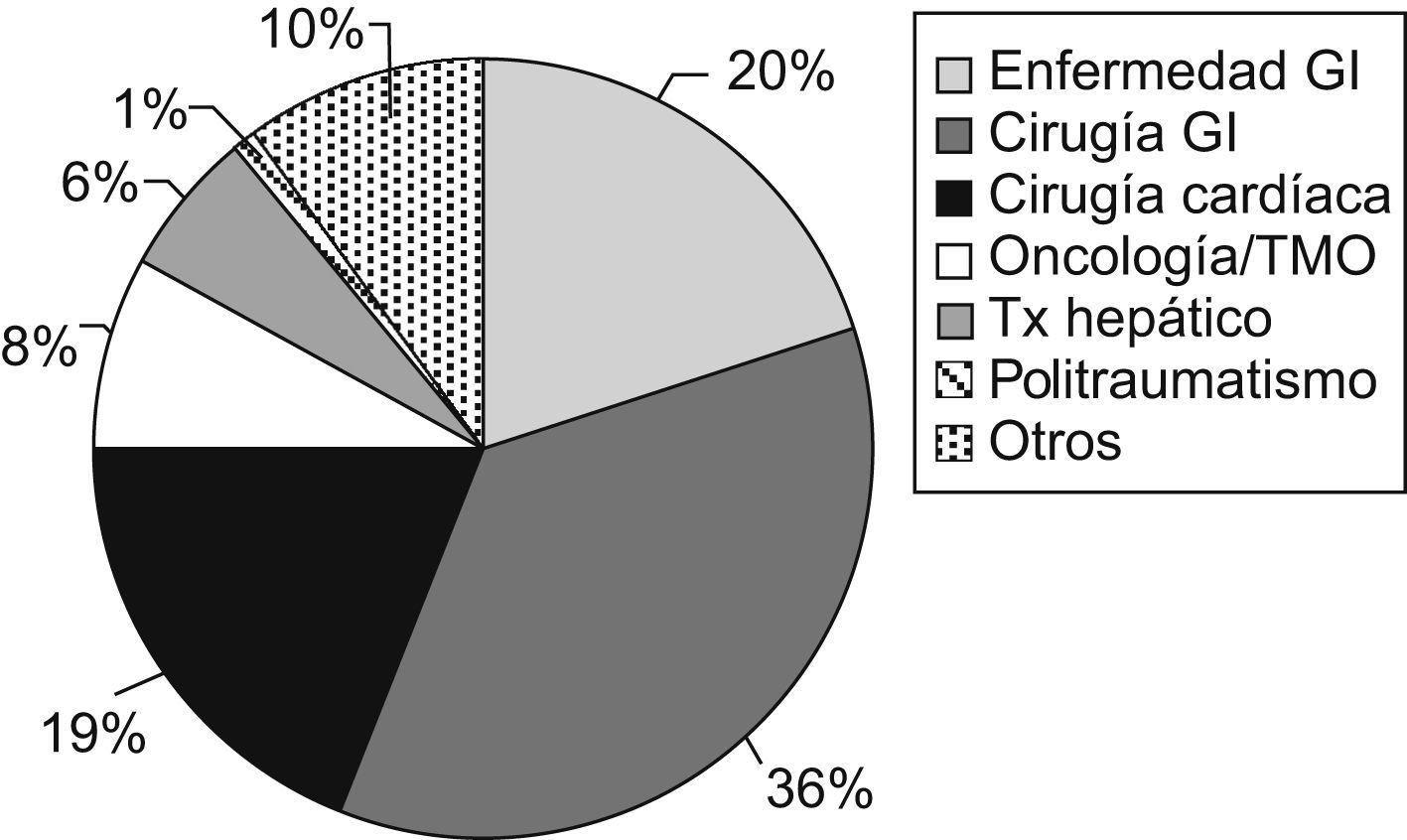
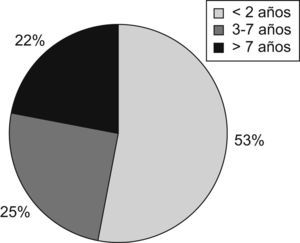
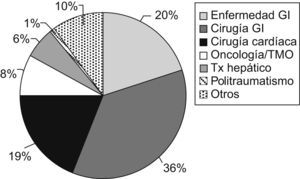
ResultadosRecibieron NP 120 niños: 63 menores de 2 años, 30 preescolares y 27 mayores de 7 años. Constituyeron el 1,6% de los niños hospitalizados en ese período. Las indicaciones más frecuentes fueron cirugía gastrointestinal (35,5%) y enfermedades gastrointestinales (19,8%). La composición media del primer día fue de 63,1±21,3kcal/kg/día, volumen de 76,6±28,4ml/kg/día, hidratos de carbono de 9,6±3,2g/kg/día, aminoácidos de 2,1±0,6g/kg/día y lípidos de 1,9±1g/kg/día. La duración media fue de 10,5±9,8días. Los accesos venosos más frecuentes fueron la vena yugular (34,7%) y la vena femoral (26,5%). La causa principal de interrupción fue la tolerancia oral, seguida de NP domiciliaria. El 27,3% tuvo complicaciones asociadas a la NP.
ConclusionesLa mitad de las NP se prescribió en lactantes, y la principal indicación fue la cirugía gastrointestinal. Todas las mezclas fueron ternarias con micronutrientes todos los días. La mayoría se estandarizó parcialmente, lo que ayuda a disminuir los errores en la prescripción y preparación.
To describe the characteristics of inpatient parenteral nutrition during 2008 in a tertiary level paediatric hospital. To compare this practice with recent standards.
Material and methodsLongitudinal, descriptive, and retrospective study of patients under 16 years receiving parenteral nutrition in 2008. Demographic data as well as data of the nutritional support were recorded.
ResultsA total of 120 children received parenteral nutrition, of whom 63 were under 2 years, 30 between 3 and 7 years, and 27 older than 7 years. They accounted for 1.6% of all the inpatients during that period. Most frequent indication was gastrointestinal surgery (35.5%), followed by non-surgical gastrointestinal diseases (19.8%). The average composition in the first day of parenteral nutrition was: 63.1kcal/kg (SD: 21.3); volume, 76.6ml/kg (SD: 28.4); carbohydrates 9.6g/kg/d (SD: 3.2); amino acids 2.1g/kg/d (SD: 0.6), and lipids 1.9g/kg/d (SD: 1). The mean duration of parenteral support was 10.5 days (SD: 9.8). Internal jugular vein (34.7%) and femoral vein were the most common intravenous access. The main reason to discontinue parenteral nutrition was transition to oral/enteral feedings. The complication rate was 27.3%.
ConclusionsThere is an interest in evaluating standard practice in parenteral nutrition in order to develop improvement strategies. Infants and toddlers are the principal candidates for parenteral nutrition. Standardisation is one way to decrease errors in its preparation and prescription.
Desde la primera descripción del empleo de la administración de nutrientes por una vía venosa a un niño en el año 1968 hasta la actualidad, la nutrición parenteral (NP) se ha convertido en una herramienta terapéutica de uso generalizado en pacientes pediátricos desnutridos o con riesgo de estarlo, incapaces de cubrir sus necesidades nutricionales por la vía digestiva1,2.
Dos cuestiones, sin embargo, merecen especial atención. Por una parte, la escasez de estudios que muestren la eficacia de esa intervención3,4. Por otra parte, la cortedad de descripciones de su empleo en el paciente pediátrico no neonatal5. Los años 1970, 1980 y comienzos de 1990 significaron un auge considerable en el empleo de la NP en pediatría, que se vio acompañado de un desarrollo considerable tanto de las soluciones de nutrientes como de la propia técnica. Desde la década de 1990 hemos asistido a un gran impulso en la utilización de la nutrición enteral (NE) en el paciente hospitalizado, de tal manera que en situaciones clínicas en las que previamente se empleaba NP ahora se utiliza habitualmente la NE (prematuridad, paciente crítico, paciente posquirúrgico, etc.). Este comienzo del siglo pone en su justa medida el empleo de ambas técnicas de soporte nutricional. Jeejeebhoy, en un artículo crucial, señala que la NP es tan efectiva como la NE cuando existe riesgo de desnutrición y no se tolera la NE o existe un fracaso intestinal6. La Sociedad Europea para la Nutrición Clínica y el Metabolismo (ESPEN) y la Sociedad Europea de Gastroenterología, Hepatología y Nutrición Pediátricas (ESPGHAN) en 20057 y Sociedad Española de Nutrición Parenteral y Enteral (SENPE)-Sociedad Española de Farmacia Hospitalaria (SEFH)-Sociedad Española de Gastroenterología, Hepatología y Nutrición Pediátrica (SEGHNP)8 en 2007 publicaron 2 documentos guía que pretenden racionalizar el empleo de la NP en el paciente pediátrico.
Tuvimos ocasión de realizar un estudio similar al ahora presentado en los años 1994 y 20025. Nuestro interés radica en conocer las características de la NP hospitalaria en 2008, después de la publicación de los documentos anteriormente citados.
Pacientes, material y métodosEl estudio, longitudinal, descriptivo y retrospectivo, estudia las características de todas las NP prescritas en pacientes menores de 16 años durante el año 2008, excluyendo las unidades de neonatología. El estudio se desarrolló en un hospital terciario con 133 camas pediátricas, incluyendo 16 camas de Cuidados Intensivos-Reanimación Posquirúrgica.
La población se estratificó en 3 grupos de edad: lactantes (<2 años), niños pequeños (3 a 7 años) y niños mayores (>7 años). Se recogieron, además de los datos demográficos, los referidos a la indicación de la NP: composición, tipo de acceso venoso, duración y motivo de retirada, así como las complicaciones.
La prescripción en nuestro centro permite 3 posibilidades: NP individualizada (prescripción de todos los componentes por kg de peso y día); NP estandarizada (soluciones prediseñadas que cubren los requerimientos de todos los nutrientes), y NP parcialmente estandarizadas (aporte individualizado de macronutrientes y normalizado por litro de solución, de electrolitos y minerales). Se valoró también, como medida de la adecuación de la indicación, el porcentaje de NP que se utilizó por un período inferior a 5 días. Con respecto a las complicaciones asociadas a la NP, se recogieron sólo 2 tipos de complicaciones: las infecciones asociadas a catéter y la afectación hepática. Se consideró infección asociada a catéter en presencia de fiebre superior a 38,5°C y cultivo positivo de sangre extraída a través de la luz del catéter con/sin hemocultivo periférico positivo. Se consideró alteración hepática relacionada con la NP a aquélla en la que la bilirrubina conjugada fuese mayor de 2,0g/dl o la gammaglutamil transpeptidasa (GGT), la glutámico-oxálico transaminasa (GOT) (AST) o la glutámico-pirúvico transaminasa (GPT) (ALT) tuviesen valores superiores al doble de los valores normales de nuestro laboratorio en 2 determinaciones consecutivas y en ausencia de alteraciones hepáticas previas.
Aspectos estadísticos: las variables cuantitativas se presentan como media y desviación estándar (DE), y las variables cualitativas se presentan como porcentajes. Para la comparación de variables continuas se utilizó la t de Student, y el test de la X2 se utilizó para la comparación de las variables discontinuas. Un valor de p<0,05 se consideró como significación estadística.
ResultadosDurante el año 2008 recibieron NP 121 niños (fig. 1). El número de bolsas preparadas durante este período fue de 1.270. El 1,6% de los pacientes ingresados en el hospital durante ese año recibió NP (frente al 1,3% en 2002 y al 1% en 1994). La indicación más frecuente fue la cirugía gastrointestinal (35,5%), seguida de las enfermedades digestivas no quirúrgicas (19,8%) y de la cirugía cardíaca (19%) (fig. 2). Fue excepcional el empleo de NP periféricas (2,5%). El acceso venoso empleado con más frecuencia fue la vena yugular interna (35%), seguida de la vena femoral (26,5%), mientras que los catéteres tunelizados se emplearon en un 20% y los reservorios subcutáneos en un 7,5%. Los catéteres venosos centrales de abordaje periférico sólo se utilizaron en un 5% de los pacientes.
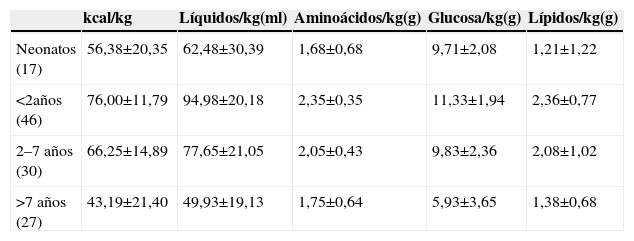
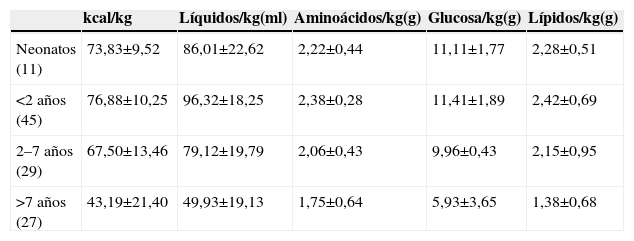
En la tabla 1 se muestra la composición media de la NP el primer día de prescripción estratificada de acuerdo con las edades en el momento de inicio. En la tabla 2 el análisis excluyó a los pacientes cardiópatas que no recibieron lípidos en el primer día de NP por la restricción importante de fluidos. Consideramos que esta variable limitaba esencialmente la posibilidad de administrar calorías y nutrientes. Pudieron utilizarse mezclas estandarizadas no comerciales en un 11,6% de los pacientes, soluciones individualizadas en el 41% y mezclas parcialmente estandarizadas en el resto (48%). Todos los pacientes recibieron mezclas unitarias de nutrientes, que fueron ternarias en el 88% de los casos. Excepto en las mezclas estandarizadas (utilizadas sólo en niños mayores de 7 años), siempre se utilizaron soluciones de aminoácidos pediátricos y emulsiones lipídicas ricas en aceite de oliva. El protocolo del hospital contempla la adición diaria de vitaminas (Soluvit® y Vitalipid®, Lab Fresenius Kabi, Barcelona, España) y oligoelementos (Peditrace®, Baxter, España) así como el empleo de fosfatos orgánicos (glicerofosfato). En el 10% de las mezclas se modificó el aporte de oligoelementos y vitaminas por la presencia de afectación hepática (fundamentalmente colestasis), y en el 3,3% por insuficiencia renal oligoanúrica.
Composición de la nutrición parenteral en su primer día de prescripción, disgregada por edades
| kcal/kg | Líquidos/kg(ml) | Aminoácidos/kg(g) | Glucosa/kg(g) | Lípidos/kg(g) | |
| Neonatos (17) | 56,38±20,35 | 62,48±30,39 | 1,68±0,68 | 9,71±2,08 | 1,21±1,22 |
| <2años (46) | 76,00±11,79 | 94,98±20,18 | 2,35±0,35 | 11,33±1,94 | 2,36±0,77 |
| 2–7 años (30) | 66,25±14,89 | 77,65±21,05 | 2,05±0,43 | 9,83±2,36 | 2,08±1,02 |
| >7 años (27) | 43,19±21,40 | 49,93±19,13 | 1,75±0,64 | 5,93±3,65 | 1,38±0,68 |
El grupo de edad <2 años se subdividió en neonatos (<28 días) y el resto (entre y 24 meses). Los valores se expresan en unidades por kilo y día.
Misma tabla anterior cuando se eliminaron del análisis los cardiópatas que no recibieron lípidos en su primer día de nutrición parenteral a causa de la restricción de volumen
| kcal/kg | Líquidos/kg(ml) | Aminoácidos/kg(g) | Glucosa/kg(g) | Lípidos/kg(g) | |
| Neonatos (11) | 73,83±9,52 | 86,01±22,62 | 2,22±0,44 | 11,11±1,77 | 2,28±0,51 |
| <2 años (45) | 76,88±10,25 | 96,32±18,25 | 2,38±0,28 | 11,41±1,89 | 2,42±0,69 |
| 2–7 años (29) | 67,50±13,46 | 79,12±19,79 | 2,06±0,43 | 9,96±0,43 | 2,15±0,95 |
| >7 años (27) | 43,19±21,40 | 49,93±19,13 | 1,75±0,64 | 5,93±3,65 | 1,38±0,68 |
La adición de heparina (1UI/ml) fue excepcional y se reservó para mezclas sin lípidos y con ritmos de infusión inferiores a 5ml/h. Las razones para no emplear de forma habitual heparina en las soluciones de NP son 2: la falta de evidencia científica sobre su utilidad y el riesgo de precipitación cuando se emplea en combinación con calcio y lípidos9. Sin embargo, en aquellos cardiópatas con una importante restricción hídrica —y, por tanto, con flujos de infusión muy bajos— y sin lípidos administramos habitualmente heparina por el riesgo elevado de trombosis vascular. Sólo en una ocasión se añadió insulina rápida a la bolsa de la NP para el control de la hiperglucemia.
La duración media de la NP fue de 10,5 días (DE: 9,7), similar a lo recogido en 2002 (11 días), pero significativamente inferior a lo ocurrido en 1994 (15,2 días, p<0,05). Diecisiete pacientes recibieron NP por un período inferior a 5 días, 6 de ellos por tratarse de pacientes con NP a domicilio y otros 2 pacientes fallecieron antes de los 5 días, por lo que la tasa de mala indicación fue inferior al 8%.
El motivo de retirada fue el paso a alimentación oral/enteral en el 75% de las ocasiones.
Las características del estudio sólo permitieron recoger la incidencia de bacteriemias/sepsis relacionadas con el catéter (en 20 ocasiones, el 16,5% de los pacientes), en su mayoría por Staphylococcus epidermidis o similares (65%), seguidos de gérmenes gramnegativos y hongos. La hepatopatía relacionada con la NP ocurrió en el 7% de los pacientes.
DiscusiónLos pacientes pediátricos son especialmente sensibles a las restricciones de energía y nutrientes, lo que los convierte en pacientes de riesgo nutricional, en especial en las primeras etapas de la vida. Se considera, por tanto, que la NP está indicada en aquellos niños desnutridos o con riesgo de desnutrición que no son capaces de recibir un soporte nutricional adecuado por vía enteral por un período superior a 5 días7,8. Una revisión Cochrane reciente concluye, sin embargo, que existe poca evidencia para apoyar o refutar la necesidad de proporcionar soporte nutricional durante la primera semana de estancia en UCI pediátricas10.
La mayoría de recomendaciones que se proporcionan en las guías citadas se basan en evidencias científicas de baja calidad, generalmente series de casos o recomendaciones de expertos. Aun conociendo las dificultades que entraña realizar estudios controlados en nutrición clínica, se hace preciso un esfuerzo encaminado a dotar de mayor fuerza científica a lo que constituye nuestra práctica clínica habitual. Este esfuerzo incluye también encontrar herramientas adecuadas de valoración nutricional en determinados contextos, por ejemplo, el paciente pediátrico gravemente enfermo11.
Se considera que la prescripción y la elaboración individualizada son el mejor método de empleo de la NP en pediatría, ya que ofrece las ventajas de un mejor control bioquímico y nutricional. Ésta es la pauta seguida en la mayoría de los hospitales europeos, también en los españoles12,13. Sin embargo, para que sea óptima, la NP debe prescribirse de forma adecuada y requiere médicos conocedores de la NP. Los datos de una encuesta realizada en hospitales españoles en 2002 muestra la gran variabilidad que existe tanto en prescripción como en elaboración12, aunque es cierto que su realización fue anterior a la publicación de las guías citadas. Lapillone et al14, en una encuesta realizada en unidades neonatales francesas, encontraron que aunque la mayoría de los médicos conocían los objetivos nutricionales, tanto el momento de introducción de los nutrientes como el ritmo de progresión distaban mucho de las recomendaciones.
Los datos epidemiológicos de nuestra serie son similares a las de otras publicadas en la literatura médica, principalmente en lo referente a las enfermedades de base y los accesos vasculares. La indicación de NP en el postoperatorio de la cirugía cardíaca sólo se realizó cuando no pudo establecerse una NE pospilórica eficiente (imposibilidad de acceso enteral, desnutrición grave previa a la cirugía, bajo gasto sistémico, intolerancia a la NE, fundamentalmente).
En los datos recogidos de nuestra práctica habitual en 2008, los aportes iniciales de energía y macronutrientes se aproximan a las recomendaciones de las guías, excepto para el caso de las calorías en el grupo de los neonatos. Es preciso recordar nuevamente que sólo se revisaron los neonatos fuera de las unidades neonatales, en nuestro estudio, recién nacidos con una cardiopatía congénita grave a los que se les realizó una corrección quirúrgica precoz. Los aportes de hidratos de carbono en ese primer día de infusión fueron superiores a lo recomendado en la guía de ESPEN-ESPGHAN en la línea de alcanzar en el menor tiempo posible los requerimientos totales de nutrientes. El diseño del estudio no permite, sin embargo, conocer el ritmo de progresión de los aportes. Los aportes de aminoácidos y lípidos en ese día estuvieron, para todos los grupos de edad, dentro de las recomendaciones.
Aunque, como se señalaba anteriormente, la individualización permite un ajuste fino de los aportes, conlleva un aumento en la carga de trabajo y un mayor riesgo de errores en la elaboración. El empleo de soluciones estandarizadas o parcialmente estandarizadas junto con las individualizadas permite aprovechar las ventajas de ambos sistemas15. En esta línea de trabajo —maximizar recursos, minimizar riesgos— se encuadran el empleo de mezclas ternarias y el hecho de no adicionar heparina o carnitina16. Sin embargo, desde el punto de vista de que la NP debe imitar en la medida de lo posible a la alimentación habitual, el aporte de vitaminas y oligoelementos se realizó a diario, y se ajustaron los aportes en caso de colestasis o de insuficiencia renal17–19.
No es posible, en un sistema público de salud como el nuestro, conocer con precisión el coste de la NP en pediatría. Este precio depende de muchos factores, por ejemplo, del número de bolsas elaboradas diariamente y, por tanto, de la posibilidad de utilizar envases enteros. Como término medio, el precio de los elementos utilizados en la elaboración de una bolsa de NP es de 22€ (25g de aminoácidos: 6,4€; 175g de glucosa: 2,2€; 20g de lípidos: 2,45€; 12mEq de magnesio: 0,35€; 10mEq de calcio: 0,6€; 10mEq de potasio: 0,2€; 10mEq de sodio: 0,2€; 10mmol de glicerofosfato: 0,87€; Peditrace®: 1,63€; vitaminas —Soluvit® y Vitalipid® —: 3,47€, y bolsa multicapas: 2,68€). No se han podido computar los datos correspondientes a gastos de personal, instalaciones, mantenimiento, etc.
A pesar del uso creciente de la NE no hemos observado disminución en el número de NP elaboradas durante estos últimos 15 años, ni en los valores absolutos ni en el porcentaje de pacientes hospitalizados que precisan NP. Incluso se aprecia una discreta tendencia a un mayor uso. Por el contrario, la incidencia de complicaciones o se ha estabilizado —número de complicaciones infecciosas— o incluso ha disminuido (complicaciones hepáticas) (datos no publicados).
¿Es útil conocer las características de uso de la NP hospitalaria? Para el propio centro, sin duda. Se consiguen razones para implementar la técnica: disminución del número de NP mal indicadas y mejoría del porcentaje de complicaciones. Para los demás, a falta de datos publicados, es una forma de establecer comparaciones. Para todos, diseñar estudios con la fortaleza suficiente para mejorar nuestra práctica clínica habitual.
Con vistas al futuro, la prescripción electrónica de las NP desde las plantas de hospitalización, la implementación de protocolos de prescripción y elaboración o la implicación directa del farmacéutico en las plantas como refuerzo del trabajo de la Unidad de Nutrición Clínica pueden ayudar a mejorar la detección y el seguimiento de pacientes susceptibles de cuidados nutricionales específicos20.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.