Una baja adherencia al tratamiento antirretroviral (TARV) es la causa más frecuente de fracaso terapéutico tanto en niños como en adultos que viven con el VIH, siendo especialmente importante durante la adolescencia. En consecuencia, cualquier análisis de la efectividad del TARV deberá considerarse incompleto si no incluye una evaluación de la adherencia. El objetivo de este estudio es evaluar la utilidad de un programa de valoración de la adherencia al TARV en una población de pacientes pediátricos infectados por el VIH.
Pacientes y métodosSe trata de un estudio observacional y transversal, dentro del «Programa de educación sanitaria para la optimización de la adherencia en pacientes pediátricos con VIH», que forma parte del proyecto «No estoy solo». La adherencia se estudió simultáneamente mediante una combinación de diferentes métodos: entrevista personal, evolución de la carga viral y del recuento de linfocitos TCD4+, determinación de concentraciones plasmáticas de fármacos y registros de dispensación de farmacia.
ResultadosSe incluyó un total de 20 pacientes (50% mujeres, edad mediana: 14,5 años). Se obtuvo un porcentaje de adherencia completa informada por el propio paciente o cuidador del 90% (IC 95%: 70-97,2%); sin embargo, el porcentaje medio de adherencia según los registros de dispensación fue significativamente inferior (83,3%; DE=32,88). La media de principios activos/día y de medicamentos/día fue de 3,5 (DE=0,83) y 5,5 (DE=2,72), respectivamente. Hubo una relación inversa entre el n.° de medicamentos/día y las puntuaciones de adherencia (F=13,8; p=0,002). Ninguno de los métodos de evaluación se relacionó de manera estadísticamente significativa con la adherencia, presentando la determinación de concentraciones plasmáticas una tendencia a la significación.
ConclusionesLa adherencia global al TARV fue elevada y se vio favorecida por el uso de pautas posológicas sencillas. La adherencia informada por el paciente y/o el cuidador sobreestimó la verdadera adherencia al TARV. Recomendamos la utilización simultánea de diversos métodos de valoración de la adherencia en los niños y adolescentes que viven con el VIH.
Poor adherence to antiretroviral treatment (ART) is the commonest cause of treatment failure in children and adults living with HIV, and this is especially important during adolescence. Therefore, any analysis of ART effectiveness in children should include an evaluation of adherence to ART. The aim of this study is to assess the usefulness of an ART adherence monitoring program in an HIV-infected paediatric population.
Patients and methodsAn observational and cross-sectional study was performed, within the framework of the “Health Education Program for Optimising Adherence in Paediatric Patients with HIV”, which is part of the “I am not alone” project. Adherence was assessed simultaneously by different methods: personal interview, therapeutic drug monitoring, pharmacy dispensing records and evolution of viral load and T CD4+ lymphocyte count.
ResultsTwenty patients were included (50% female, median age 14.5 years). Percentage of self-reported full adherence was 90% (95% CI: 70-97.2%); however, the median adherence percentage according to pharmacy dispensing records was significantly lower (83.3%, SD=32.88). The average of drugs and dosage forms per day were 3.5 (SD=0.83) and 5.5 (SD=2.72), respectively. There was an inverse relationship between the number of dosage forms per day and adherence scores (F=13.8; P=.002). No single method was statistically related to adherence, although therapeutic drug monitoring showed a trend towards significance.
ConclusionsGlobal adherence to ART was high and was easier with simpler regimens. Self-reported adherence overestimated real adherence to ART in our cohort. The simultaneous use of different methods to assess adherence is recommended in HIV-infected children.
La introducción de la terapia antirretroviral de gran actividad (TARGA) ha supuesto una importante reducción de la mortalidad y morbilidad de los pacientes con infección por el virus de la inmunodeficiencia humana (VIH). Su efectividad se supone óptima cuando la relación entre la dosis administrada y la dosis pautada – es decir, la adherencia-, es superior al 95%1, aunque estudios más recientes indican que, con regímenes basados en inhibidores de la transcriptasa inversa no análogos de nucleósidos (ITINAN) y/o inhibidores de la proteasa (IP) potenciados, se podrían alcanzar los objetivos terapéuticos con menores niveles de adherencia, especialmente en pacientes con viremias previamente indetectables2–4.
Una mala adherencia al tratamiento antirretroviral (TARV) es la primera causa de fracaso terapéutico en niños5 y en adultos6–8en las fases iniciales de la enfermedad, por delante del desarrollo de cepas del virus resistentes 9. Los estudios realizados en pacientes pediátricos indican que la adherencia al TARV es un factor predictivo del impacto terapéutico10. Asimismo se ha puesto en evidencia que, a menudo, la adherencia es subóptima11,12. Debe tenerse en cuenta, además, que estos fracasos terapéuticos constituyen un problema de ineficiencia del sistema de salud pública ya que reducen la efectividad clínica de una medicación que resulta muy costosa (6.000 euros por paciente/año)13.Por todo ello, es necesaria la instauración de programas de atención global al paciente, tanto para evaluar la efectividad del TARV, como para elaborar estrategias de actuación dirigidas a optimizar los resultados. La evaluación de la adherencia al TARV se puede realizar mediante métodos directos e indirectos, cuyo uso simultáneo minimiza las limitaciones e incrementa la exactitud.
El objetivo principal del presente estudio es evaluar la utilidad de un programa de valoración de la adherencia al tratamiento antirretroviral en una población de pacientes pediátricos con VIH adquirido por transmisión vertical. Los objetivos secundarios son detectar las características del tratamiento, paciente o cuidador que puedan repercutir en la adherencia; correlacionar el grado de adherencia de cada paciente con los resultados clínicos y analíticos; y detectar posibles discrepancias entre los diferentes métodos de evaluación.
Pacientes y métodosEn el contexto del «Programa de educación sanitaria para la optimización de la adherencia en pacientes pediátricos con VIH», que forma parte del proyecto «No estoy solo», del Hospital Universitari Vall d’Hebron, se realizó un primer estudio observacional y transversal. Se incluyeron los primeros 20 pacientes menores de 18 años y que acudieron consecutivamente a control a la Unitat de Patologia Infecciosa i Immunodeficiències de Pediatria del centro entre marzo de 2008 y mayo de 2009. El proyecto fue aprobado por el Comité Ético del centro (PR(AMI)140/2008).
En todos ellos se evaluó, como parte de su visita rutinaria, la adherencia al TARV mediante los diferentes métodos, tanto indirectos (evaluación de la adherencia mediante encuesta) como directos (concentraciones plasmáticas de ARV, recuento de CD4+ y carga viral y dispensación de ARV en farmacia). Los datos sobre los tratamientos y características demográficas se recogieron aparte. Los métodos que se utilizaron fueron los siguientes:
- 1.
Evaluación de la adherencia informada: se determinó mediante un formulario (Anexo 1) que cumplimentaron los pacientes o cuidadores, previo consentimiento informado, junto con una enfermera entrenada para esta actividad. Las entrevistas las respondió el cuidador cuando éste era el responsable de la administración de la medicación. Se definió adherencia completa a la toma de todas las dosis en los 3 días previos a la entrevista (por ser el periodo de tiempo utilizado más habitualmente en este tipo de evaluaciones) y adherencia no completa a la falta de alguna de ellas. Además, en el mismo momento, los pacientes o cuidadores autoevaluaron su grado de adherencia mediante una escala analógica del 1 al 10 (de peor a mejor).
- 2.
Determinación de concentraciones plasmáticas de antirretrovirales: se analizaron los niveles plasmáticos de IP y de ITINAN, siguiendo las recomendaciones de las guías existentes13. Se clasificaron en 3 categorías, dependiendo de que las concentraciones plasmáticas estuviesen dentro del rango terapéutico (terapéuticas), fuesen inferiores (infraterapéuticas) o superiores (supraterapéuticas). Se utilizaron como guía los márgenes terapéuticos considerados de referencia en adultos, recogidos en www.hivpharmacology.com, utilizados también en población pediátrica en el estudio de Nso-Roca et al14 Todas las muestras analizadas se extrajeron el día de la visita, en ayunas y antes de la toma de la siguiente dosis de medicación. La determinación de concentraciones plasmáticas de ARV se estudió mediante cromatografía líquida de alta eficacia en fase reversa y detector de ultravioleta en el Laboratorio de Farmacología y Toxicología del Servicio de Bioquímica y Genética Molecular del Centro de Diagnóstico Biomédico del Hospital Clínico de Barcelona.
- 3.
Evolución de la carga viral: la medición del HIV RNA viral (en copias/ml) se clasificó según fuera detectable (si ≥ 50) o indetectable (si<50). Para detectar el RNA del VIH-1 se utilizaron los métodos NASBA a tiempo real (Easy Mag y Nuclisens Easy Q, de BioMerieux).
- 4.
Evolución del recuento de linfocitos CD4+: El estudio de inmunofenotipo linfocitario se realizó con métodos de citometría de flujo con cultivos de anticuerpos monoclonales (Becton-Dickinson-Facscalibur). Se compararon los valores de linfocitos CD4+ (en porcentaje si el paciente era menor de 6 años, o en valor absoluto/mm3, si el paciente era mayor) obtenidos el día de la visita con los de la visita realizada 3 meses antes. Se consideró que la cifra de linfocitos CD4+ era: estable (si la variación era ≤ 5% o ≤ 100 células/mm3), en descenso (si disminuía más del 5% o más de 100 células/mm3) o en aumento (si aumentaba más del 5% o más de 100 células/mm3).
- 5.
Registro de dispensaciones de farmacia: la frecuencia de dispensaciones (entrega de medicación al paciente en el servicio de farmacia) establecida en nuestro centro es de 3 meses. Se revisaron los registros de dispensación de farmacia de un período de 6 meses (desde 3 meses antes hasta 3 meses después de la entrevista). Se calculó el porcentaje de dosis perdidas (calculando la proporción entre las dosis dispensadas y las prescritas para comprobar si el paciente había recogido medicación suficiente para el periodo entre una y otra visita) y el porcentaje de adherencia (100 - porcentaje de dosis perdidas). Se registraron los principios activos y los medicamentos, definidos como cada unidad de comprimido, cápsula o dosis de jarabe que recibió cada paciente.
La relación entre 2 variables continuas se estudió a través de la prueba de la t de Student-Fisher o por regresión lineal. La relación entre una variable continua y una categórica se estudió a través del ANOVA. Al tratarse de una muestra de pequeño tamaño, se comprobó la significación estadística con la prueba no paramétrica U de Mann Whitney. Para el cálculo de intervalos de confianza de las proporciones se utilizó el método de Wilson. Para el análisis se dispuso del software SPSS para Windows versión 15.0.
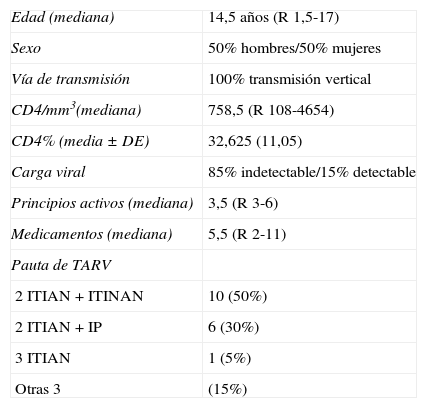
ResultadosSe incluyó un total de 20 pacientes, que representan la mitad de los pacientes que son atendidos en la unidad, como muestra inicial para este estudio. La mediana de edad de los pacientes incluidos fue de 14,5 años (rango: 1,5 a 17 años), siendo el 90% (n=18) mayor de 12 años, y no se observaron diferencias de género. Todos los pacientes habían contraído la infección por transmisión vertical. La tabla 1 recoge las principales características demográficas, clínicas, analíticas y pautas terapéuticas de los pacientes el día de la entrevista.
Resumen de las principales características demográficas, clínicas y analíticas de los pacientes y pautas terapéuticas
| Edad (mediana) | 14,5 años (R 1,5-17) |
| Sexo | 50% hombres/50% mujeres |
| Vía de transmisión | 100% transmisión vertical |
| CD4/mm3(mediana) | 758,5 (R 108-4654) |
| CD4% (media ± DE) | 32,625 (11,05) |
| Carga viral | 85% indetectable/15% detectable |
| Principios activos (mediana) | 3,5 (R 3-6) |
| Medicamentos (mediana) | 5,5 (R 2-11) |
| Pauta de TARV | |
| 2 ITIAN+ITINAN | 10 (50%) |
| 2 ITIAN+IP | 6 (30%) |
| 3 ITIAN | 1 (5%) |
| Otras 3 | (15%) |
DE: desviación estándar; IP: inhibidores de la proteasa; ITIAN: inhibidores de la transcriptasa inversa análogos de nucleósidos/nucleótidos; ITINAN: inhibidores de la transcriptasa inversa no análogos de nucleósidos; R: rango.
La mediana de principios activos al día fue 3,5 (rango de 3 a 6 principios activos al día): 13 pacientes (65%) recibían 3, 5 pacientes (25%) recibían 4 y los 2 pacientes restantes recibían 5 y 6 principios activos al día, respectivamente.La mediana de medicamentos al día que recibía cada paciente era de 5,5 (2-12). El 80% (N=13) de los pacientes recibía 5 o más medicamentos al día. Todos los pacientes recibían su medicación en forma de cápsulas o comprimidos, excepto uno, que la recibía en forma de suspensión oral.
Respecto a la evaluación de la adherencia informada a través del cuestionario y la entrevista personal, el porcentaje de adherencia completa fue del 90% (IC 95%: 70-97,2%). Sólo 2 pacientes (10%) informaron haber omitido alguna dosis en los últimos 3 días (adherencia no completa). Doce de las entrevistas se realizaron al paciente y 8 al cuidador. La puntuación media de adherencia global fue de 8,9 (DE=1,2). Las puntuaciones propuestas por los cuidadores (9,8; DE=0,5) fueron un 14% superiores a las referidas por los pacientes (8,4; DE=1,3); (diferencia de medias=1,4; IC 95%: 0,4-2,4; p=0,01).
Los 2 pacientes que refirieron adherencia no completa eran mayores de 15 años. Debido a que la población de estudio incluía un rango de edades muy amplio con una distribución asimétrica, no se pudo establecer una relación entre la edad y la adherencia. No se observaron diferencias en las puntuaciones de adherencia en función del sexo (p=0,7).
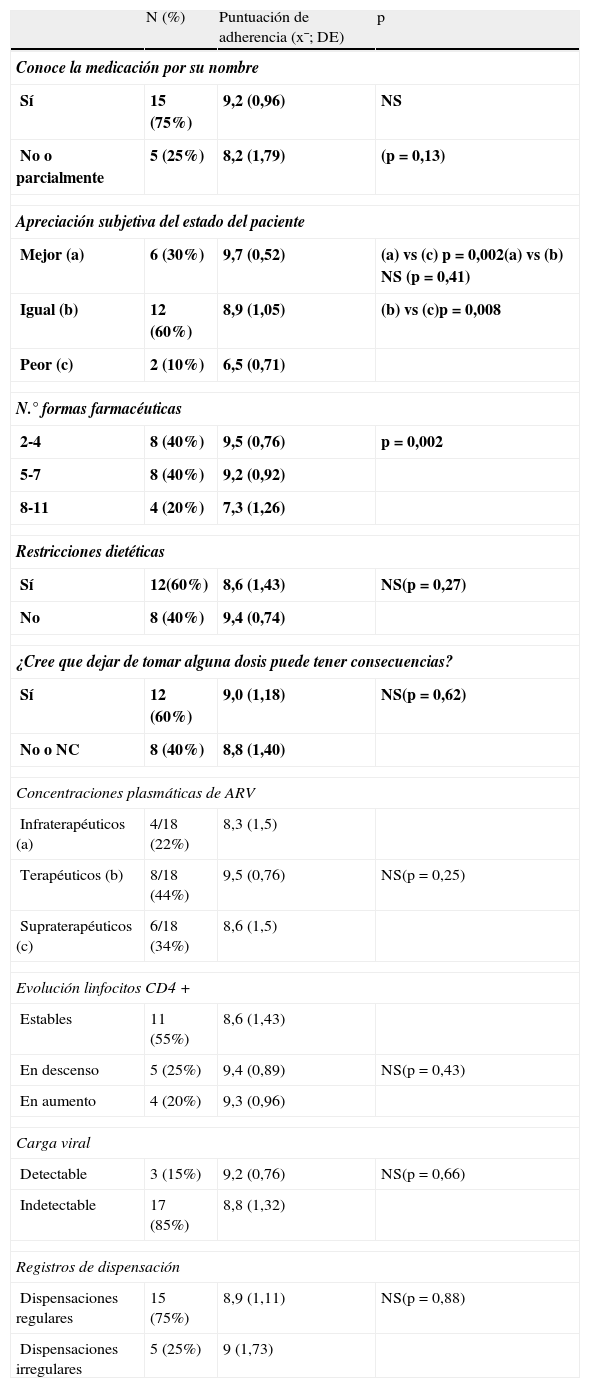
La tabla 2 recoge las características recogidas en la entrevista, la determinación de concentraciones plasmáticas y marcadores analíticos y su relación con la puntuación de la adherencia (informada del 1 al 10). A medida que aumentaba el número de medicamentos al día, las puntuaciones de adherencia disminuían, de forma estadísticamente significativa (F=13,8; p=0,002). Por cada medicamento/día que recibía el paciente, la puntuación de adherencia disminuía 0,3 puntos sobre 10. Los regímenes posológicos de los 2 pacientes que refirieron adherencia no completa consistían en pautas que incluían 9 medicamentos/día y 11 medicamentos/día, respectivamente.
Puntuación de adherencia al tratamiento antirretroviral según métodos indirectos y directos
| N (%) | Puntuación de adherencia (x¯; DE) | p | |
| Conoce la medicación por su nombre | |||
| Sí | 15 (75%) | 9,2 (0,96) | NS |
| No o parcialmente | 5 (25%) | 8,2 (1,79) | (p=0,13) |
| Apreciación subjetiva del estado del paciente | |||
| Mejor (a) | 6 (30%) | 9,7 (0,52) | (a) vs (c) p=0,002(a) vs (b) NS (p=0,41) |
| Igual (b) | 12 (60%) | 8,9 (1,05) | (b) vs (c)p=0,008 |
| Peor (c) | 2 (10%) | 6,5 (0,71) | |
| N.° formas farmacéuticas | |||
| 2-4 | 8 (40%) | 9,5 (0,76) | p=0,002 |
| 5-7 | 8 (40%) | 9,2 (0,92) | |
| 8-11 | 4 (20%) | 7,3 (1,26) | |
| Restricciones dietéticas | |||
| Sí | 12(60%) | 8,6 (1,43) | NS(p=0,27) |
| No | 8 (40%) | 9,4 (0,74) | |
| ¿Cree que dejar de tomar alguna dosis puede tener consecuencias? | |||
| Sí | 12 (60%) | 9,0 (1,18) | NS(p=0,62) |
| No o NC | 8 (40%) | 8,8 (1,40) | |
| Concentraciones plasmáticas de ARV | |||
| Infraterapéuticos (a) | 4/18 (22%) | 8,3 (1,5) | |
| Terapéuticos (b) | 8/18 (44%) | 9,5 (0,76) | NS(p=0,25) |
| Supraterapéuticos (c) | 6/18 (34%) | 8,6 (1,5) | |
| Evolución linfocitos CD4+ | |||
| Estables | 11 (55%) | 8,6 (1,43) | |
| En descenso | 5 (25%) | 9,4 (0,89) | NS(p=0,43) |
| En aumento | 4 (20%) | 9,3 (0,96) | |
| Carga viral | |||
| Detectable | 3 (15%) | 9,2 (0,76) | NS(p=0,66) |
| Indetectable | 17 (85%) | 8,8 (1,32) | |
| Registros de dispensación | |||
| Dispensaciones regulares | 15 (75%) | 8,9 (1,11) | NS(p=0,88) |
| Dispensaciones irregulares | 5 (25%) | 9 (1,73) | |
NC: no sabe; NS: no estadísticamente significativo.
Puntuación de adherencia: 1-10 (de peor a mejor). En negrita, los datos correspondientes a la evaluación mediante métodos indirectos; en normal, evaluados mediante métodos directos.
En el 60% (N=12) de los tratamientos estudiados era necesario realizar restricciones dietéticas, que se seguían correctamente en el 66,6% (N=8) de los casos. En ningún caso se refirieron dificultades a la hora de tomar/administrar la medicación debido a las características organolépticas de los medicamentos (sabor, tamaño de los comprimidos, etc.). Además, aquellos pacientes o cuidadores que informaron apreciar un mejor o igual estado de salud subjetivo respecto a la visita anterior presentaron puntuaciones de adherencia superiores que aquellos que decían encontrarse peor (p=0,002; y p=0,008, respectivamente; tabla 2).
El 20% (N=4) de los pacientes o cuidadores afirmaron haber omitido alguna dosis alguna vez en caso de que el paciente no se encontrase bien. Al 70% (N=14) de los pacientes/cuidadores no les preocupaba el hecho de tener que tomar/administrar la medicación fuera de su domicilio frente al 25% (N=5) que sí, por dificultades para el transporte y conservación. Uno de ellos no quiso contestar a esta pregunta. Sólo 2 pacientes refirieron tener que tomar alguna dosis fuera del hogar de forma habitual.
Cuando se evaluaron los resultados de la monitorización de las concentraciones plasmáticas de los diferentes antirretrovirales, se observó que el tratamiento de 19 de los 20 pacientes estudiados era susceptible de ser monitorizado (o sea, que incluía ITINAN o IP). De estos se obtuvieron concentraciones plasmáticas de 18 de ellos. Del total de estos 18 pacientes, el 56% (N=10) se encontraron fuera del rango terapéutico y el 44% (N=8) restante presentaron concentraciones terapéuticas. De los 2 pacientes que refirieron una adherencia no completa, uno presentó concentraciones plasmáticas infraterapéuticas, mientras que el otro presentó valores supraterapéuticos. Al estudiar la relación entre las puntuaciones de adherencia y las concentraciones plasmáticas (tabla 2), se observó que las puntuaciones de los pacientes con concentraciones infra o supraterapéuticas eran más bajas que las de los pacientes con valores terapéuticos, aunque la diferencia no fue estadísticamente significativa (p=0,25).
Sólo 3 pacientes (15%) presentaron cargas virales detectables, que oscilaron entre 900 y 9.800 copias/ml. Todos ellos refirieron haber tomado todas las dosis de antirretrovirales en los últimos 3 días y presentaban puntuaciones de adherencia de 8,5, 9 y 10, respectivamente. No se pudo relacionar el hecho de presentar cargas virales indetectables con una buena adherencia (p=0,66), o viceversa.
La tabla 2 recoge también los resultados de la evolución de los linfocitos T CD4+ desde la última visita y su relación con la puntuación media de adherencia. No se pudo demostrar de forma estadísticamente significativa que a mayor puntuación de adherencia informada se produjera una mejor evolución de linfocitos T CD4+ ya que, de hecho, los pacientes que se encontraban en descenso fueron los que presentaron una mayor media en la puntuación de adherencia. Dos de los 3 pacientes con carga viral detectable presentaron un descenso del valor de linfocitos T CD4+ respecto a la última visita, mientras que el tercer paciente mantuvo unos valores estables.
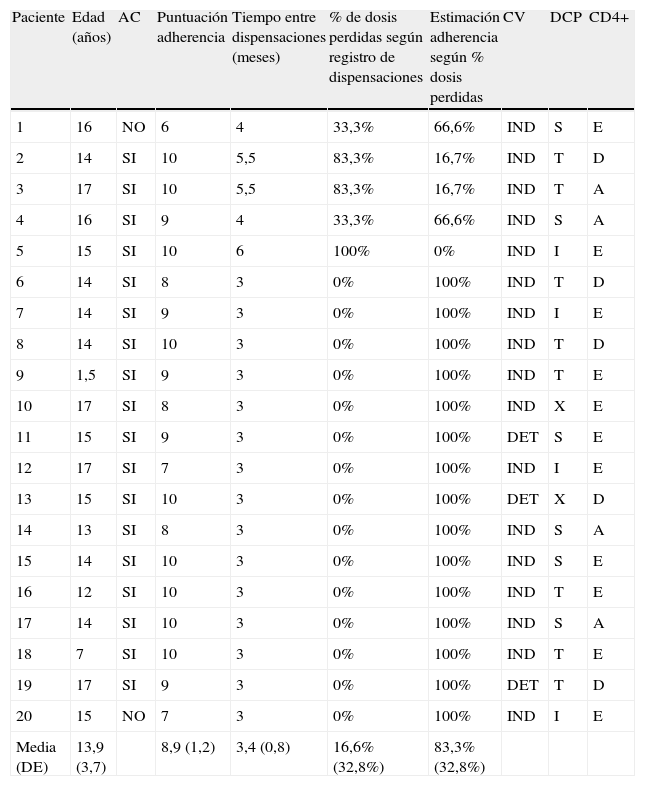
El porcentaje de adherencia medio según los registros de dispensación fue de 83,3% (DE=32,8). Según el registro de dispensación de farmacia, 5 pacientes deberían presentar un porcentaje de adherencia inferior al 80%. El resto de pacientes presentó un 100% de adherencia. Este porcentaje fue inferior al obtenido mediante las entrevistas (75 vs. 90%; p=0,41). En la tabla 3 se comparan los datos de adherencia obtenidos en la entrevista con los obtenidos mediante la revisión del registro de dispensación de farmacia.
Correlación de la adherencia al TARV según métodos indirectos y registro de dispensación de la farmacia
| Paciente | Edad (años) | AC | Puntuación adherencia | Tiempo entre dispensaciones (meses) | % de dosis perdidas según registro de dispensaciones | Estimación adherencia según % dosis perdidas | CV | DCP | CD4+ |
| 1 | 16 | NO | 6 | 4 | 33,3% | 66,6% | IND | S | E |
| 2 | 14 | SI | 10 | 5,5 | 83,3% | 16,7% | IND | T | D |
| 3 | 17 | SI | 10 | 5,5 | 83,3% | 16,7% | IND | T | A |
| 4 | 16 | SI | 9 | 4 | 33,3% | 66,6% | IND | S | A |
| 5 | 15 | SI | 10 | 6 | 100% | 0% | IND | I | E |
| 6 | 14 | SI | 8 | 3 | 0% | 100% | IND | T | D |
| 7 | 14 | SI | 9 | 3 | 0% | 100% | IND | I | E |
| 8 | 14 | SI | 10 | 3 | 0% | 100% | IND | T | D |
| 9 | 1,5 | SI | 9 | 3 | 0% | 100% | IND | T | E |
| 10 | 17 | SI | 8 | 3 | 0% | 100% | IND | X | E |
| 11 | 15 | SI | 9 | 3 | 0% | 100% | DET | S | E |
| 12 | 17 | SI | 7 | 3 | 0% | 100% | IND | I | E |
| 13 | 15 | SI | 10 | 3 | 0% | 100% | DET | X | D |
| 14 | 13 | SI | 8 | 3 | 0% | 100% | IND | S | A |
| 15 | 14 | SI | 10 | 3 | 0% | 100% | IND | S | E |
| 16 | 12 | SI | 10 | 3 | 0% | 100% | IND | T | E |
| 17 | 14 | SI | 10 | 3 | 0% | 100% | IND | S | A |
| 18 | 7 | SI | 10 | 3 | 0% | 100% | IND | T | E |
| 19 | 17 | SI | 9 | 3 | 0% | 100% | DET | T | D |
| 20 | 15 | NO | 7 | 3 | 0% | 100% | IND | I | E |
| Media (DE) | 13,9 (3,7) | 8,9 (1,2) | 3,4 (0,8) | 16,6% (32,8%) | 83,3% (32,8%) |
A: aumento de > 5% o > 100/mm3 CD4+; AC: adherencia completa; CV: carga viral; D: descenso de > 5% o > 100/mm3 CD4+; DCP: determinación de concentraciones plasmáticas; DE: desviación estándar; DET: detectable; E: estables; I: infraterapéuticas; IND: indetectable; S: supraterapéuticas; T: terapéutica.
En el programa de atención multidisciplinario al niño y adolescente que vive con el VIH que se lleva a cabo en nuestro centro, «No estoy solo», un punto que reviste especial interés es el seguimiento y mejoría de la adherencia al TARV de estos pacientes por considerarse un punto clave en el control de su enfermedad. Así, se ha utilizado una valoración desde múltiples enfoques para detectar los potenciales puntos a mejorar y en este sentido se ha desarrollado el presente estudio.
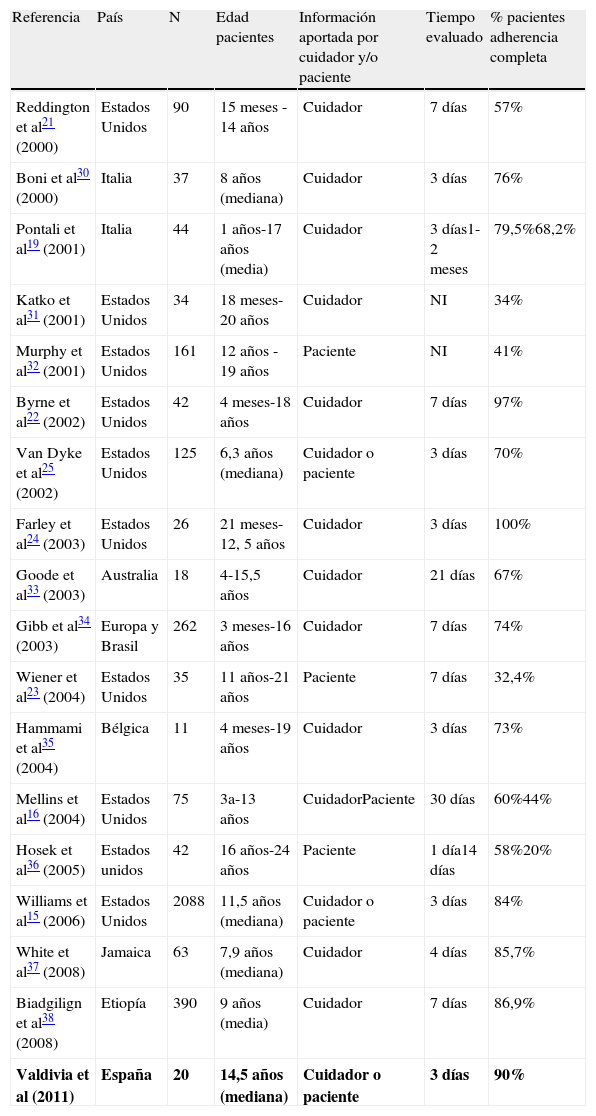
En cuanto a la evaluación mediante cuestionario y entrevista, el porcentaje de adherencia completo obtenido en el presente estudio (90%) es similar al obtenido en la mayoría de estudios que utilizaron la adherencia «autoinformada» en los 3 días previos a la entrevista. Sin embargo, cuando el período de valoración es mayor, en general las cifras de adherencia completa tienden a ser más bajas. La tabla 4 compara los principales trabajos que han utilizado este método. Es posible que la inclusión de esta encuesta en un programa de educación sanitaria explique, en parte, el elevado porcentaje de adherencia completa obtenido en nuestros pacientes, ya que el hecho de realizar un seguimiento más estrecho y la determinación periódica de la adherencia pueden haber contribuido a aumentar la motivación de los pacientes/cuidadores15. Sin embargo, la falta de datos anteriores a la implantación del programa impide sacar conclusiones a este respecto.
Evaluación de la adherencia al tratamiento antirretroviral según la literatura médica
| Referencia | País | N | Edad pacientes | Información aportada por cuidador y/o paciente | Tiempo evaluado | % pacientes adherencia completa |
| Reddington et al21 (2000) | Estados Unidos | 90 | 15 meses -14 años | Cuidador | 7 días | 57% |
| Boni et al30 (2000) | Italia | 37 | 8 años (mediana) | Cuidador | 3 días | 76% |
| Pontali et al19 (2001) | Italia | 44 | 1 años-17 años (media) | Cuidador | 3 días1-2 meses | 79,5%68,2% |
| Katko et al31 (2001) | Estados Unidos | 34 | 18 meses-20 años | Cuidador | NI | 34% |
| Murphy et al32 (2001) | Estados Unidos | 161 | 12 años -19 años | Paciente | NI | 41% |
| Byrne et al22 (2002) | Estados Unidos | 42 | 4 meses-18 años | Cuidador | 7 días | 97% |
| Van Dyke et al25 (2002) | Estados Unidos | 125 | 6,3 años (mediana) | Cuidador o paciente | 3 días | 70% |
| Farley et al24 (2003) | Estados Unidos | 26 | 21 meses-12, 5 años | Cuidador | 3 días | 100% |
| Goode et al33 (2003) | Australia | 18 | 4-15,5 años | Cuidador | 21 días | 67% |
| Gibb et al34 (2003) | Europa y Brasil | 262 | 3 meses-16 años | Cuidador | 7 días | 74% |
| Wiener et al23 (2004) | Estados Unidos | 35 | 11 años-21 años | Paciente | 7 días | 32,4% |
| Hammami et al35 (2004) | Bélgica | 11 | 4 meses-19 años | Cuidador | 3 días | 73% |
| Mellins et al16 (2004) | Estados Unidos | 75 | 3a-13 años | CuidadorPaciente | 30 días | 60%44% |
| Hosek et al36 (2005) | Estados unidos | 42 | 16 años-24 años | Paciente | 1 día14 días | 58%20% |
| Williams et al15 (2006) | Estados Unidos | 2088 | 11,5 años (mediana) | Cuidador o paciente | 3 días | 84% |
| White et al37 (2008) | Jamaica | 63 | 7,9 años (mediana) | Cuidador | 4 días | 85,7% |
| Biadgilign et al38 (2008) | Etiopía | 390 | 9 años (media) | Cuidador | 7 días | 86,9% |
| Valdivia et al (2011) | España | 20 | 14,5 años (mediana) | Cuidador o paciente | 3 días | 90% |
NI: no indicado.
Basada y actualizada de Simoni JM, Montgomery A, Martin E, New M, Demas PA, Rana S. Adherence to antiretroviral therapy for pediatric HIV infection: a qualitative systematic review with recommendations for research and clinical management. Pediatrics. 2007;119:1371-1383.
El hecho de que las puntuaciones realizadas por los cuidadores fuesen superiores a las de los pacientes puede deberse a que realmente los cuidadores controlen el tratamiento de forma más rigurosa, o a que tiendan a sobrestimar la adherencia, en comparación con los propios pacientes, fenómeno observado en otros estudios16–18. Además, no debe olvidarse que se trata de valoraciones subjetivas por lo que su valoración debe ser cuidadosa. El principal factor asociado a una mayor adherencia según el cuestionario y la entrevista fue la administración del TARV en pautas posológicas sencillas, que incluían menos medicamentos (< 6 medicaciones/día) y menos restricciones dietéticas, hecho reflejado también por otros estudios11,15,19. Del mismo modo, el hecho de que aquellos pacientes/cuidadores con mejor adherencia mostrasen una tendencia a conocer mejor los fármacos que formaban parte del tratamiento y la importancia de una buena adherencia pone de manifiesto la necesidad de la tarea educativa del personal sanitario hacia los pacientes para conseguir el máximo rendimiento de la medicación y prevenir resistencias.
Un punto importante a tener en cuenta es que la gran mayoría de nuestros pacientes son adolescentes (hecho que refleja la realidad del paciente infectado por transmisión vertical en nuestro medio hoy en día), ya que se ha relacionado esta etapa de la vida con una menor adherencia al TARV. Así, en un estudio realizado con 2.088 pacientes de 3 a 18 años se observó que se producía un aumento significativo de la odds ratio (1,10 [1,1-1,2]; p<0,001) con 10% de un aumento de posibilidades de no adherencia por cada año que aumenta la edad15. En la adolescencia el riesgo de abandono es más elevado, incluso en pacientes que previamente han sido buenos cumplidores. Los problemas que presentan los adolescentes a la hora de adaptar los complejos regímenes posológicos son similares a los de los adultos, pero con los inconvenientes añadidos de disponer de menos autonomía, movilidad y privacidad. Además, problemas en el entorno social/familiar, baja autoestima, toxicomanías, cambios hormonales y metabólicos -que hacen más prevalente la aparición de toxicidad-, y el hecho de encontrarse en un estado avanzado de la infección por VIH, pueden conducir al abandono del tratamiento13,20. Por todo ello consideramos que se trata de una población sobre la que volcar todos nuestros esfuerzos en la mejoría de la adherencia al TARV.
A pesar de la buena correlación demostrada entre una buena adherencia «autoinformada» y la efectividad antirretroviral21–25, deben tenerse presente una serie de limitaciones de este método como la tendencia a sobrestimar la adherencia o el reflejo solamente de un corto período de tiempo, pudiendo no detectar períodos de mala adherencia. Por todo ello es necesario utilizarla conjuntamente con otros métodos.
La determinación de concentraciones plasmáticas como método de control de la adherencia es un método directo, objetivo y fiable, pero no exento de inconvenientes. Los más destacados son: variabilidad individual (alteraciones en la absorción, interacciones medicamentosas, etc.), elevado coste y, por último, el no garantizar la continuidad del tratamiento (mejoría del cumplimiento previo a los controles analíticos)13. En nuestro trabajo, los pacientes con concentraciones plasmáticas en el rango terapéutico tendían a presentar puntuaciones de adherencia más elevadas, lo que concuerda con los datos del estudio de Nso-Roca et al.14 en el que se observó que las concentraciones plasmáticas infraterapéuticas, acompañadas de cifras bajas de linfocitos T CD4+, se presentan con mayor frecuencia en pacientes con baja adherencia.
Nuestro trabajo no permite sacar conclusiones acerca de la relación entre la adherencia y carga viral, posiblemente en relación con el bajo número de pacientes, sin embargo esta asociación ha sido demostrada por otros autores15,21,25.
En cuanto a los registros de dispensación, las discrepancias detectadas al compararlos con los resultados de las entrevistas permite incrementar la exactitud de las mediciones de la adherencia. Por ejemplo, pacientes que no recogieron su medicación en 4, 5 o 6 meses, se autoasignaron puntuaciones de adherencia muy elevadas, cuando difícilmente podrían haber cumplido el tratamiento por falta de medicación. Sin embargo, no se puede descartar que el paciente dispusiera de medicación de dispensaciones anteriores o que la hubiese compartido con algún miembro enfermo de la familia (fenómeno observado, ya que el paciente suele compartir diagnóstico con sus progenitores o hermanos).
Nuestro estudio presenta algunas limitaciones. En primer lugar, el pequeño tamaño de la muestra se justifica por tratarse de un estudio realizado con el objetivo de detectar los principales puntos a incidir. En segundo lugar, la recogida retrospectiva de los datos puede haber supuesto alguna pérdida, hecho minimizado al realizarse por los mismos responsables del programa. Finalmente, no se utilizó un cuestionario validado, ya que no existen cuestionarios dirigidos específicamente a la población pediátrica. A pesar de que se dispone de cuestionarios validados para la población adulta en nuestro país como el SMAQ y el SERAD26,27, y que algunos autores sugieren utilizar la adaptación del SMAQ para la población pediátrica28, se decidió adaptar los cuestionarios de GESIDA29 por ser de fácil realización tanto por parte del personal sanitario como del paciente y/o cuidador.
En conclusión, la adherencia al TARV en los pacientes acogidos en nuestro programa, fue elevada y favorecida por pautas posológicas sencillas. El riesgo de abandono se incrementó en la adolescencia, por lo que consideramos que se debe intensificar el seguimiento en estos pacientes. Los pacientes con mejor adherencia tendieron a presentar concentraciones plasmáticas en el rango terapéutico con más frecuencia, lo que refuerza la idea de la utilidad de este método. Del mismo modo, los registros de dispensación del TARV en farmacia permitieron detectar discrepancias con los métodos de autoevaluación de la adherencia. Todo ello nos lleva a reforzar la idea de que a la hora de valorar la adherencia al TARV en el paciente pediátrico y adolescente que vive con el VIH, la combinación de diferentes métodos incrementa su utilidad. En este sentido, consideramos necesario que toda unidad encargada del cuidado de niños y adolescentes que viven con el VIH, incluya en el manejo de los mismos un seguimiento de la adherencia al TARV que incluya: cuestionarios de adherencia sencillos y adaptados a la edad del paciente, un seguimiento estrecho de su evolución inmunovirológica y de las concentraciones plasmáticas de los diferentes fármacos antirretrovirales que reciben, así como un control de la dispensación en farmacia de la medicación. Opinamos que dicha evaluación debería realizarse de forma semestral en todos estos pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A los pacientes y sus familiares por haber hecho posible la realización de este trabajo, a la enfermera Ana Álvarez Roig por haber colaborado activamente en este proyecto, a los Dr. Bruno Montoro y Juan Carlos Suárez del Servicio de Farmacia del Hospital Universitari Vall d’Hebron por su revisión crítica del documento y a la Dra. Rosa López-Galera del Servicio de Bioquímica y Genética Molecular del Centro de Diagnóstico Biomédico del Hospital Clínico de Barcelona por la determinación de las concentraciones plasmáticas de los antiretrovirales.