Introducción
La gastroenteritis aguda (GEA) es uno de los principales motivos de consulta en pediatría y en todo el mundo representa una de las primeras causas de mortalidad infantil (2 millones de muertes/año)1. Si bien en los últimos años la rehidratación oral ha pasado a ser pilar fundamental del tratamiento2-8, un número no despreciable de pacientes sigue ingresando en un hospital y generando una carga asistencial importante y un coste económico y social. En el mundo desarrollado, la GEA ha sido definida como una Ambulatory Care Sensitive Condition (ACSC), es decir, como uno de los códigos de diagnóstico de alta hospitalaria que pretende servir de medida de hospitalizaciones que se consideran potencialmente evitables9,10.
En el Baix Empordà, el 100 % de la atención primaria está reformada y existe una estrecha relación entre hospital y atención primaria: historia clínica informatizada común y accesible desde los dos niveles, los mismos pediatras de primaria realizan asistencia en urgencias hospitalarias, sesiones y protocolos comunes, etc. A pesar de ello, las GEA siguen representando un importante porcentaje de los ingresos hospitalarios.
Los objetivos de nuestro estudio fueron evaluar la carga asistencial y los costes generados por los pacientes ingresados por GEA en nuestro centro y evaluar la práctica clínica en cuanto al tratamiento de estos pacientes (pautas de rehidratación, uso de antibióticos, solicitud de exploraciones complementarias, etc.).
Material y métodos
Estudio prospectivo de los pacientes con edades comprendidas entre 1 mes y 14 años que ingresaron en nuestro hospital entre el 1 de junio de 2003 y el 1 de junio de 2004 por diarrea y/o vómitos (con o sin fiebre). Los pacientes visitados en urgencias que no ingresaron en la planta de Pediatría no fueron incluidos en el estudio. La decisión de ingreso y la pauta terapéutica inicial fueron decididas por el pediatra de guardia. La selección de los pacientes se realizó manualmente, revisando, una vez ingresado en planta, el motivo del ingreso según el informe de urgencias. Se excluyeron aquellos pacientes en los que se halló un diagnóstico diferente a gastroenteritis que pudiera explicar la clínica de vómitos o diarrea (p. ej., infección de orina, traumatismo craneoencefálico, etc.).
Se recogió información sobre síntomas previos al ingreso y durante la hospitalización, tratamiento recibido antes, durante y después de su ingreso, exploraciones complementarias solicitadas, así como consultas realizadas en área básica de salud (ABS), urgencias u hospitalizaciones previas.
En los pacientes con diarrea se solicitó coprocultivo en medios selectivos (en nuestro hospital se realiza de forma sistemática para Salmonella sp. y Shigella sp.) y determinación de rotavirus por enzima inmunoanálisis (EIA).
Los costes se determinaron a partir de un estudio previo realizado en la entidad para el mismo período. Se utilizó la metodología propuesta por el Grupo de trabajo sobre el consumo de recursos de la Unión Catalana de Hospitales11. Se incluyen los costes de personal, compras, servicios externos y amortizaciones.
Se calculó el coste medio de cada uno de los episodios de actividad de las diferentes líneas de actividad (hospitalización, consultas externas, urgencias, hospital de día, cirugía mayor ambulatoria, diálisis ambulatoria, rehabilitación ambulatoria y atención primaria). Igualmente, se calculó el coste medio de una exploración radiológica y de una determinación de laboratorio El consumo de farmacia durante los episodios fue imputado directamente a cada paciente.
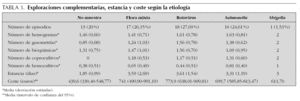
Para el cálculo del coste de cada episodio de gastroenteritis se contabilizaron los días de estancia hospitalaria y su consumo de farmacia, las visitas de urgencias y atención primaria relacionadas y las pruebas complementarias realizadas valoradas a los precios expresados en la tabla 1.
Se confeccionó una base de datos creada para el estudio en Microsoft Access 97 y para el análisis estadístico se utilizó el programa SPSS versión 13.0 para Windows. El análisis estadístico es descriptivo para las diferentes variables utilizadas. Para éste se agruparon los episodios en cuatro grupos: pacientes sin muestra para estudio microbiológico, pacientes con coprocultivo positivo para algún enteropatógeno (gastroenteritis bacteriana), pacientes con determinación positiva para rotavirus (gastroenteritis viral) y pacientes en los que en el coprocultivo se halló flora mixta y la determinación de rotavirus fue negativa. Para la comparación de las variables cuantitativas se empleó el estadístico t de Student, análisis de la varianza y test de Kruskal-Wallis. El nivel de significación estadística fue p < 0,05. Para las comparaciones múltiples se utilizó el test de U de Mann-Whitney y la significación estadística se ajustó con la técnica de Bonferroni.
El estudio fue aprobado por el comité de investigación del hospital. No se consideró necesario solicitar el consentimiento informado de los tutores, dado que se trataba de un estudio observacional.
Resultados
Según el censo de 2003, la población de 0-14 años en el Baix Empordà era de 16.231 habitantes. Durante el período de estudio hubo 393 ingresos de pacientes entre 1 mes y 14 años de edad (24,2 ingresos/1.000 hab./año), 65 de los cuales (16,6 %) fueron diagnosticados de GEA (62 pacientes, 3 pacientes, 2 ingresos). El 52,3 % eran varones. La distribución de edades (media 42 meses, rango 2 meses a 13,8 años, mediana de 16 meses) queda reflejada en la tabla 2. De los 62 pacientes ingresados por GEA, 6 procedían de fuera de la comarca del Baix Empordà. En ningún caso se trataba de diarrea nosocomial.
En la tabla 3 queda reflejada la distribución de los pacientes según la etiología del cuadro. Destaca que en el 20 % de los casos no se realizó estudio microbiológico de las heces y en el 26,15 % no se identificó ningún patógeno.
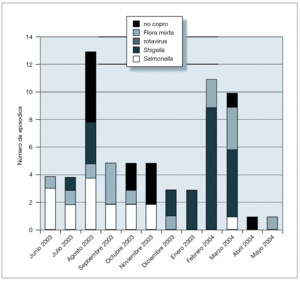
La distribución estacional de los ingresos fue diferente según la época del año, con dos picos claramente diferenciados, uno durante el mes de agosto y el otro en febrero-marzo (fig. 1).
Figura 1. Estacionalidad y etiología de las gastroenteritis.
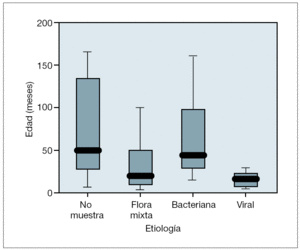
La distribución etaria de los pacientes según la etiología de los episodios de GEA queda recogida en la figura 2, con diferencias estadísticamente significativas (p < 0,001). Los pacientes con infección bacteriana tuvieron edades significativamente superiores que los afectados de gastroenteritis por rotavirus (p < 0,005). Los pacientes en los que no se efectuó estudio de heces fueron de más edad que a los que se les realizó (p = 0,026).
Figura 2. Edades según estudio microbiológico de heces.
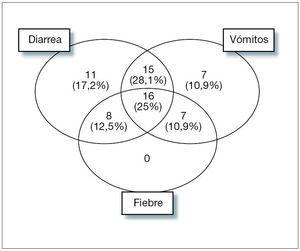
La combinación de síntomas en el momento del ingreso queda reflejada en la figura 3. Cinco de los pacientes presentaban deshidratación grave (> 9 %) y 12 moderada (entre 3 y 9 %). El 78,1 % de los pacientes incluidos en el estudio presentó diarrea, el 70,3 %, vómitos y el 48,4 %, fiebre. Dos pacientes (3,1 %) refirieron cefalea como clínica de presentación.
Figura 3. Clínica al ingreso.
Durante el ingreso se pautó sueroterapia intravenosa en 58 de los episodios (89,2 %), 26 pacientes recibieron antitérmicos, 13 pacientes (20 %) recibieron antibióticos parenterales y 8 continuaron con tratamiento antibiótico oral al alta. En 9 pacientes se pautó leche sin lactosa durante el ingreso y/o al alta.
De los 13 pacientes que recibieron tratamiento antibiótico en 5 se aisló Salmonella sp. en el coprocultivo, en 1 Shigella sp., en 2 se identificaron rotavirus por EIA y en 5 no se identificó patógeno. En los 2 pacientes en que se detectó rotavirus en el estudio microbiológico se suspendió el tratamiento antibiótico. Las 2 pacientes en que se mantuvo tratamiento antibiótico a pesar del cultivo negativo fue debido a patología concomitante a la gastroenteritis: neutropenia grave en un caso que persistió durante más de un mes y en el otro caso se trataba de una paciente con un retraso pondoestatural grave, metabolopatía en estudio, inmunodeficiencia y retraso mental.
Sólo 5 de los 16 pacientes con infección por Salmonella recibieron antibioticoterapia y en todos ellos se inició el tratamiento antes de tener el resultado del coprocultivo. Todos los pacientes que recibieron antibióticos presentaron fiebre (superior a 39 °C en 3 de los 5 pacientes) y más de 10 deposiciones al día, algunas con sangre.
Se solicitó un total de 66 estudios de heces (en 13 episodios no se solicitó y en 14 episodios se cursaron 2 muestras). El 63,6 % de las muestras resultó positivo, y se halló un patógeno en el 68,6 % de los episodios. Se cursaron además 38 hemocultivos (7 contaminados y el resto negativos), 99 bioquímicas sanguíneas, 81 gasometrías, 41 sedimentos de orina, 5 pruebas de coagulación, 2 punciones lumbares, 10 radiografías y 4 ecografías. Las exploraciones solicitadas según el resultado del estudio microbiológico de heces se detallan en la tabla 3.
Estos 62 pacientes generaron un total de 59 visitas en el ABS y 94 visitas en urgencias del hospital, además de los 65 ingresos hospitalarios.
La estancia hospitalaria global fue de 206 días. La estancia media fue de 3,1 días: 21 de los episodios (32,3 %) con estancias menores a 48 h y tan sólo 3 (4,6 %) tuvieron una hospitalización igual o superior a 7 días.
La estancia a tenor del patógeno queda reflejada en la tabla 3.
El coste médico directo total generado por estos 62 pacientes fue de 44.254,74 € (media 710,46 €/paciente; IC 95 %: 616,37-804,56 €) siendo el 82,9 % del coste generado por la estancia hospitalaria. Los costes generados en cada episodio según la etiología de la GEA quedan reflejados en la tabla 3. No hubo diferencias estadisticamente significativas entre los costes generados por los pacientes según el resultado del estudio microbiólogico de la heces (p = 0,059). El coste generado por los pacientes en los que no se realizó estudio microbiológico de heces (media 439,60 euros, desviación estándar [DE]: 180,69 €) fue significativamente inferior al generado por los pacientes a los cuales se les solicitó estudio de heces (media 737,20 €; DE: 180,68 €) (p < 0,05), explicado por la menor estancia de dichos pacientes (p < 0,001).
Discusión
Las GEA representan en nuestro hospital una de las primeras causas de hospitalización en el servicio de Pediatría (16,6 % de los ingresos). Se detectaron dos claros picos estacionales: uno en febrero-marzo, debido a la epidemia de rotavirus, y otro en agosto, debido a un incremento en los casos de salmonelosis, y asimismo, a un aumento de la población infantil en nuestra área debido a la importante afluencia de turismo familiar. La carga asistencial generada por estos episodios se suma así a la ya intensa carga en ambos períodos: pico invernal de infecciones respiratorias/bronquiolitis en enero-febrero y época estival con un incremento de la población del Baix Empordà que puede llegar a multiplicar por cinco la población habitual. Esta sobrecarga concreta supone un verdadero reto para la planificación de los recursos sanitarios.
El tratamiento clínico de nuestros pacientes difirió considerablemente del recomendado en las últimas pautas que preconizan la rehidratación oral en el caso de deshidratación leve o moderada y reservan la vía intravenosa sólo para los casos de deshidratación grave2-8. A pesar de que sólo 17 de nuestros pacientes (26,1 %) presentaban deshidrataciones superiores al 3 %, el 89,2 % recibió sueroterapia intravenosa. Este hecho podría justificarse por diferentes razones: el 70,3 % de los pacientes presentaba vómitos, el 13,9 % de los pacientes tenía menos de 6 meses de edad, el 60 % de los pacientes había consultado en al menos una ocasión previa por el cuadro de GEA y el 20 % de los pacientes llevaba cinco o más días de evolución clínica sin mejoría. Todos estos factores favorecen que el médico que atiende a estos pacientes se incline por instaurar sueroterapia a pesar de las recomendaciones actuales para el tratamiento de las GEA en términos generales.
Según dichas recomendaciones actuales, la solicitud de exploraciones complementarias estaría raramente indicada en pacientes con GEA. Sin embargo, dado que se trata de pacientes ingresados y el 89 % recibió sueroterapia, hay cierto acuerdo en que si se instaura perfusión intravenosa es conveniente disponer de valores de urea e iones para adecuar el tratamiento de estos pacientes6,7.
La proporción de pacientes con estudio de heces en que se identificó algún microorganismo (35/51 = 68,6 %) fue superior al publicado en otras series a pesar de que no se hizo estudio para Campylobacter sp., astrovirus, calicivirus ni adenovirus, que se estiman en diferentes estudios y que representan entre el 4 y el 20 % de las GEA en niños hospitalizados12,13. En la mayoría de los pacientes en que no se cursó estudio microbiológico de heces (8/11) la clínica que justificó el ingreso fueron los vómitos.
A diferencia de otros estudios13, el cálculo del coste se realizó, no a partir de los importes facturados a los pacientes, mutuas o servicio de salud, sino a partir de la estimación del coste real que supone la asistencia a dichos pacientes en nuestro centro, y es a nuestro juicio un valor mucho más ajustado al valor real.
El menor coste generado por los pacientes en los que no se solicitó estudio microbiológico de heces se debe a la menor estancia hospitalaria de tales pacientes, y no parece depender ni de la edad de los pacientes ni de la etiología de la GEA.
No debemos olvidar que los costes médicos directos representan sólo una parte de los costes reales generados por estos pacientes. Al gasto sanitario hay que sumar el coste de la pérdida de horas de trabajo por parte de los padres, los desplazamientos para las visitas médicas, la pérdida de días de escolarización, etc.
El pequeño tamaño muestral puede haber impedido el hallar diferencias estadísticamente significativas en cuanto a costes según la etiología. A pesar de que se ha utilizado la metodología propuesta por el Grupo de Trabajo sobre el Consumo de Recursos de la Unión Catalana de Hospitales11, los costes pueden no ser totalmente extrapolables a otros entornos.
En conclusión, podemos decir que a pesar de que la GEA se considera una causa de ingreso hospitalario potencialmente evitable, representa en nuestro entorno una de las principales causas de ingreso en la población pediátrica. En nuestra serie, si sólo hubieran ingresado los pacientes con deshidrataciones moderadas o graves, los pacientes menores de 3 meses, aquellos con patología de base o con vómitos intensos, el número de ingresos por GEA se habría reducido en un 30 % aproximadamente. En nuestro estudio no nos es posible valorar el coste evitable, dado que no podemos asumir que los pacientes que no ingresan no generan nuevos costes (visitas a urgencias, visitas en ABS o incluso empeoramiento clínico con necesidad de ingreso posterior).
Correspondencia: Dra. E. Parada Ricart.
Avda. Catalunya 42, 2.º2.ª 17230 Palamós. Girona. España.
Correo electrónico: esterparada@yahoo.es
Recibido en enero de 2006.
Aceptado para su publicación en septiembre de 2007.