Introducción
El empiema pleural es una complicación frecuente de la neumonía en los niños1. Su origen es multifactorial; en su desarrollo influyen tanto características del huésped como del agente etiológico2-4. El retraso en el diagnóstico de neumonía aumenta 2,9 veces el riesgo de desarrollar empiema en niños menores de 5 años5. El reconocimiento precoz de los signos de neumonía podría reducir la frecuencia de esta complicación.
En Uruguay, desde la inclusión de la vacuna anti-Haemophilus influenzae tipo b en el esquema obligatorio de vacunación, Streptococcus pneumoniae es la causa más frecuente de neumonía adquirida en la comunidad, y por lo tanto de empiema paraneumónico, en niños. Staphylococcus aureus es una causa poco frecuente6,7.
En el Hospital Pediátrico del Centro Hospitalario Pereira Rossell (HP-CHPR), hospital público de referencia nacional, el empiema paraneumónico es una causa importante de hospitalización7.
En el año 1997 se creó una unidad médico-quirúrgica para la asistencia integral de todos los niños hospitalizados con esta patología, en la que se aplican pautas de diagnóstico y tratamiento8. Esto ha permitido un uso más racional de los recursos humanos y materiales. Entre el 1 de enero de 2000 y el 1 de octubre de 2005 se hospitalizaron en esta unidad 800 pacientes con empiema paraneumónico, observándose un aumento en el número de casos en los últimos 2 años.
La toracotomía no está exenta de riesgos y complicaciones. Además de los inherentes al acto quirúrgico-anestésico, una proporción importante de estos niños requiere cuidados intensivos en el postoperatorio inmediato, presentan mayor morbilidad y una estancia hospitalaria que continúa siendo prolongada.
En la evolución del empiema paraneumónico se distinguen 3 etapas: exudativa, fibrinopurulenta y organizada. En la etapa exudativa, el líquido es escaso, sin tabiques, pudiendo ser evacuado fácilmente mediante toracocentesis y drenaje de tórax. En la etapa organizada, una corteza fibrosa restringe la movilidad y expansión pulmonar por lo que es necesario realizar toracotomía para decorticación y en muchos casos neumonectomías parciales atípicas9-14. En la etapa fibrinopurulenta, el derrame es espeso y se forman tabiques o septos de fibrina (empiema loculado). En esta etapa el tratamiento es controvertido; existen dudas respecto a qué tipo de procedimiento de drenaje se debe realizar y en qué momento. El drenaje de tórax es generalmente insuficiente ya que se bloquea frecuentemente y, si no se produce rápidamente la resolución, es probable que la tabicación requiera toracotomía y decorticación. Algunos autores recomiendan realizar este procedimiento en forma precoz13-18. En cambio otros utilizan la instilación de fibrinolíticos intrapleurales y la videotoracoscopia como forma de prevenir la cirugía más agresiva y disminuir la morbimortalidad asociada con la toracotomía15,16,19-21.
Desde la primera descripción de la instilación pleural de fibrinolíticos por Trillett y Sherry en 1949 hasta el momento actual, se han comunicado pocos estudios comparando la eficacia de esta técnica con la cirugía convencional y la videotoracoscopia con resultados controvertidos22. Los ensayos clínicos controlados en niños son escasos, con un número de pacientes inadecuado y poder estadístico insuficiente para demostrar un beneficio de este tratamiento y poder recomendarlo en indicaciones precisas23. Recientemente se ha publicado un ensayo clínico controlado, multicéntrico, que concluye que la administración de estreptoquinasa intrapleural comparada con placebo no mejora la mortalidad, la tasa de cirugía en los primeros 3 meses de evolución o la duración de la estancia hospitalaria en adultos con empiema24. Sin embargo, y a pesar de la calidad de esta evidencia, los resultados de este estudio no son aplicables a nuestra población. Los adultos con empiema tienen etiologías diferentes a las de los niños, presentan mayor comorbilidad y una tasa más elevada de mortalidad. Por otra parte, en este estudio la estreptoquinasa se utilizó como tratamiento coadyuvante de la antibioterapia y del drenaje de tórax, no como una alternativa terapéutica en el empiema complicado.
A comienzos del año 2005, se decidió poner en práctica en la unidad médico-quirúrgica un protocolo de instilación intrapleural de estreptoquinasa para el tratamiento de los niños con empiema paraneumónico complicado como alternativa del tratamiento quirúrgico.
El objetivo del estudio es describir los resultados de la instilación de estreptoquinasa intrapleural en niños hospitalizados con empiema paraneumónico complicado y compararlos con los resultados de la toracotomía precoz.
Pacientes y métodos
Se incluyeron niños con empiema paraneumónico complicado, hospitalizados en la unidad médico-quirúrgica del HP-CHPR en el período 1 de enero de 2004 a 1 de octubre de 2005.
El diagnóstico de empiema se confirmó mediante toracocentesis al obtener pus u observar bacterias en el examen directo o por la presencia de dos o más de los siguientes criterios en el análisis citoquímico: pH < 7,10; LDH > 1.000 UI/l; glucosa < 0,40 mg/dl; leucocitos > 10.000/μl (90 % polimorfonucleares)8,25.
Todos los pacientes recibieron el mismo tratamiento convencional: colocación de drenaje de tórax bajo anestesia general y antibioterapia intravenosa según protocolo de la unidad8,26.
Se definió empiema complicado cuando una vez colocado el drenaje de tórax el paciente presentó fiebre (temperatura ≥ 38 °C axilar) durante más de 48 h, mal estado general o disfunción del tubo de drenaje y la ecografía de tórax mostró la presencia de derrame complejo, tabicado.
Los pacientes se dividieron en dos cohortes:
Cohorte histórica: los niños hospitalizados con empiema complicado entre el 1 de enero y el 31 de diciembre de 2004 que recibieron tratamiento convencional con toracotomía antes de los 8 días de colocado el drenaje de tórax.
Cohorte prospectiva: los niños hospitalizados entre el 1 de enero y el 1 de octubre de 2005 que recibieron tratamiento con estreptoquinasa intrapleural, antes de los 8 días de colocado el drenaje de tórax. Los pacientes recibieron durante 3 días una dosis diaria de 100.000 UI (< 1 año) o 200.000 UI (> 1 año) diluidas en 40 ml de solución salina isotónica, a través del tubo de drenaje de tórax, con clampeo posterior del mismo durante 4 h y cambios de posición. Se realizó control con ecografía de tórax a las 12 h de la última dosis y de persistir derrame tabicado se prolongó el tratamiento por 2 días más. Previo al tratamiento con fibrinolíticos todos los pacientes fueron evaluados con coagulación sanguínea y hemograma. Los criterios de exclusión para la realización de estreptoquinasa fueron: postoperatorio inmediato (primeras 48 h), fístula broncopleural, sangrado activo, malformaciones arteriovenosas o aneurismáticas, tumores intracraneanos conocidos, accidentes cerebrovasculares o endocarditis sospechada o diagnosticada.
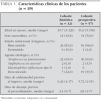
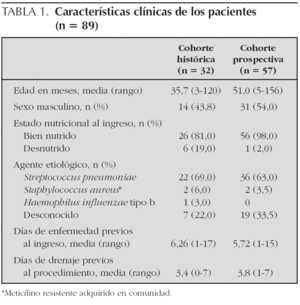
Se compararon las siguientes características clínicas: edad, sexo, estado nutricional al ingreso, duración de la enfermedad previa al ingreso (definida por la presencia de fiebre y/o fatiga mantenidas), duración del drenaje de tórax previo al procedimiento, etiología y comorbilidad.
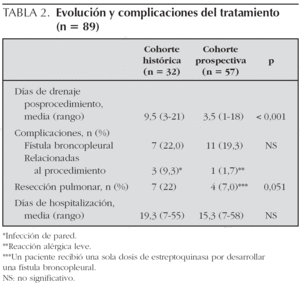
La evolución y complicaciones del tratamiento se valoraron a través de las siguientes variables: duración del drenaje posprocedimiento, complicaciones, reingresos, duración de la estancia hospitalaria y muerte.
El protocolo de investigación fue aprobado por el Comité de Ética del HP-CHPR. Se solicitó consentimiento informado y escrito a todos los pacientes que recibieron tratamiento con estreptoquinasa intrapleural.
Análisis estadístico
Se compararon ambos grupos (cohorte histórica-cohorte prospectiva) en cuanto a sexo, edad, estado nutricional al ingreso y días de enfermedad previo al ingreso. Se realizó comparación de medias con el test no paramétrico U de Mann-Whitney para las variables continuas (días de drenaje pretubo y postubo, días de drenaje total, días de internación). Para comparar las variables discretas (complicaciones, reingresos y resección pulmonar) se utilizó el test de chi cuadrado de Pearson. Los datos se procesaron con SPSS versión 10.0.
Resultados
Se incluyeron en el estudio 89 niños hospitalizados con empiema paraneumónico; 32 en la cohorte histórica (toracotomía) y 57 en la cohorte prospectiva (estreptoquinasa).
La mayoría fueron menores de 5 años, previamente sanos, con buen estado nutricional al ingreso. El agente causal se identificó en 71 % de los pacientes; S. pneumoniae sensible a penicilina fue la etiología más frecuente. La media de la duración de la enfermedad previa al ingreso fue superior a 5 días. No se observaron diferencias significativas en las variables analizadas excepto para el estado nutricional que fue mejor en el grupo tratado con estreptoquinasa (tabla 1).
En la tabla 2 se comparan la evolución y complicaciones de los niños con empiema paraneumónico complicado tratados con toracotomía precoz y con estreptoquinasa intrapleural. Si bien la estancia hospitalaria fue similar en ambos grupos, la duración del drenaje de tórax después de la instilación de estreptoquinasa intrapleural fue significativamente menor que tras la toracotomía (p < 0,001). En el grupo tratado con toracotomía una proporción significativamente mayor de pacientes requirió neumonectomía parcial atípica (p = 0,051).
En el grupo tratado con estreptoquinasa 4 pacientes requirieron toracotomía con neumonectomía parcial; uno de ellos fue una niña de 7 años con empiema neumocócico, que tras la primera dosis de estreptoquinasa intrapleural presentó una fístula broncopleural que obligó a suspender dicho tratamiento.
Ninguno de los pacientes incluidos en el estudio falleció.
No se observaron diferencias significativas en la frecuencia de complicaciones ni en el número de reingresos entre ambos grupos.
Uno de los pacientes tratado con estreptoquinasa intrapleural presentó erupción cutánea leve como reacción adversa a la bupivacaína, que no contraindicó el tratamiento.
Discusión
Los resultados de este estudio confirman que la instilación intrapleural de estreptoquinasa es una alternativa válida para el tratamiento de niños con empiema paraneumónico complicado (empiema loculado).
El estudio realizado no corresponde a un ensayo clínico. Los primeros 10 pacientes en los que se realizó instilación intrapleural de estreptoquinasa de acuerdo al protocolo descrito, evolucionaron favorablemente sin requerir toracotomía. Se decidió entonces continuar la experiencia y comparar los resultados obtenidos con una cohorte histórica que había recibido tratamiento convencional. Los resultados que se muestran en este trabajo corresponden a los primeros 9 meses de la puesta en práctica de la técnica. No se calculó el tamaño de la muestra; todos los pacientes que cumplían los criterios de inclusión fueron captados.
A pesar de las limitaciones relacionadas con la falta de aleatorización, los pacientes incluidos en ambas cohortes fueron similares en edad, sexo, etiología de la neumonía, días de enfermedad previo al ingreso y días de drenaje pleural previo al procedimiento, condiciones que pueden influir en la evolución de la enfermedad.
La instilación intrapleural de estreptoquinasa disminuyó la necesidad de toracotomía y los días de permanencia de drenaje de tórax después del procedimiento. El principal beneficio observado fue evitar la toracotomía y por lo tanto los riesgos inherentes al procedimiento anestésico quirúrgico.
Otros autores han comunicado beneficios similares con la instilación intrapleural de fibrinolíticos en el tratamiento del empiema y los derrames paraneumónicos complicados en niños. Sin embargo, la mayoría de las comunicaciones previas corresponden a descripciones de series de casos, utilizan urocinasa y alteplasa y no comparan la administración de fibrinolíticos con otras intervenciones27-30.
Barbato A et al31 mediante un diseño similar al utilizado en nuestro trabajo observaron que la instilación intrapleural de urocinasa en niños con empiema paraneumónico no aumentó el riesgo de neumotórax y disminuyó la estancia hospitalaria. Es posible que al aumentar el período de observación y el número de pacientes tratados con estreptoquinasa en la unidad médico-quirúrgica del HP-CHPR, se puedan demostrar beneficios similares sobre la incidencia de complicaciones y la duración de la estancia hospitalaria.
Se destaca como ventajas adicionales del procedimiento su sencillez, que permite su realización por personal no especializado previamente entrenado, en la sala general, no requiere cuidados especiales y no interfiere con la actividad del niño ni con su alimentación.
En esta experiencia no se observaron reacciones adversas graves; el procedimiento fue bien tolerado por todos los pacientes, sin aumento de la morbilidad. Éste constituye un hallazgo importante ya que se ha referido menor incidencia de reacciones adversas con urocinasa y con el activador del plasminógeno alteplasa. En los diferentes trabajos publicados no se han detectado diferencias en la eficacia y seguridad de estos fármacos para esta nueva indicación32. Las principales reacciones adversas comunicadas son molestias, dolor leve y tos durante la instilación. La utilización de estreptoquinasa más purificada ha disminuido la incidencia de reacciones alérgicas.
En el mes de junio se diseñó un dispositivo (G.G.F.) que facilita la administración del fármaco evitando el clampeo del drenaje durante el tiempo de su permanencia en la cavidad pleural.
Como complemento de este estudio se estimaron los costes del procedimiento implementado y se compararon con los de la toracotomía. El tratamiento con estreptoquinasa intrapleural tiene un coste de 100 dólares americanos por paciente mientras que el coste de un paciente tratado con toracotomía es de 1.000 dólares americanos.
Los beneficios demostrados en esta primera etapa seguirán siendo evaluados con un protocolo de seguimiento, incluyendo la evolución a largo plazo. Wells et al32 utilizando urocinasa y alteplasa observaron la resolución completa o casi completa de la consolidación parenquimatosa y de la opacidad pleural un mes después del alta en la mayoría de los niños que pudieron ser seguidos radiológicamente.
Son necesarios futuros estudios para definir con mayor precisión las indicaciones, momento de administración y dosis. En la próxima etapa se intentará definir criterios que permitan un diagnóstico más precoz de empiema complicado con el objetivo de realizar instilación de estreptoquinasa en forma más temprana33,34. El aspecto ecogénico de los derrames paraneumónicos constituye un auxiliar diagnóstico de importancia. La presencia de tabicaciones múltiples y complejas orienta al diagnóstico de empiema complicado y podría utilizarse como criterio para indicar estreptoquinasa intrapleural35.
Agradecimientos
A la Prof. Agda. Dra. Stella Gutiérrez por su apoyo y contribución durante la preparación del proyecto inicial de este estudio.
Correspondencia: Dr. G. Giachetto Larraz.
Centro Hospitalario Pereira Rossell. Hospital Pediátrico.
Bvar. Artigas, 1550, piso 3. 11600 Montevideo. Uruguay.
Correo electrónico: ggiachet@adinet.com.uy
Recibido en junio de 2006.
Aceptado para su publicación en marzo de 2007.