En la actualidad, el mayor uso de aciclovir, por vía intravenosa u oral, para tratar infecciones de la familia Herpesviridae, conlleva un aumento del número de efectos adversos descritos. La neurotoxicidad y nefrotoxicidad son los efectos secundarios más graves que se han comunicado. La monitorización de la función renal es fundamental para detectar estos casos, pues cursa como insuficiencia renal no oligúrica. Por ello, el uso ambulatorio y oral del fármaco puede dar lugar a una infraestimación del número de casos totales.
Presentamos los casos de 2 pacientes que por su patología de base (herpes genital y encefalitis viral) precisaron aciclovir intravenoso, y que durante su estancia hospitalaria desarrollaron insuficiencia renal aguda no oligúrica, que cedió al suspender la administración del fármaco.
The increasing use of oral or IV acyclovir to treat infections caused by herpesviridae family involves a rise in the number of observed adverse effects. Neuro- and nephrotoxicity are most serious observed and reported secondary effects. The monitoring of renal function is essential to detect these cases since it develops as a non-oliguric renal failure. Because of this, the outpatient and oral use of the drug can result in an underestimation of the number of cases reported.
We report two patients with genital herpes and viral encephalitis that required IV acyclovir. Both inpatients developed an acute renal failure that resolved after the drug was withdrawn.
El aciclovir es un fármaco de primera elección, tanto por vía oral como parenteral, para combatir infecciones producidas por la familia Herpesviridae1,2. Los efectos secundarios más frecuentes son intolerancia gastrointestinal para la administración oral y flebitis en la administración intravenosa. Sin embargo, se han descrito complicaciones neurológicas y nefrotóxicas al administrar el fármaco3–5. El mecanismo por el cual se produce daño renal es incierto, y se postula como causa su baja solubilidad y las altas concentraciones en las que se haya en el túbulo renal3. El objetivo de este manuscrito es ilustrar mediante dos casos clínicos el potencial efecto nefrotóxico del aciclovir.
OBSERVACIÓN CLÍNICASe presentan los casos de 2 pacientes, separados poco en el tiempo, que por su patología precisaron aciclovir intravenoso, y que durante su enfermedad presentaron insuficiencia renal aguda no oligúrica.
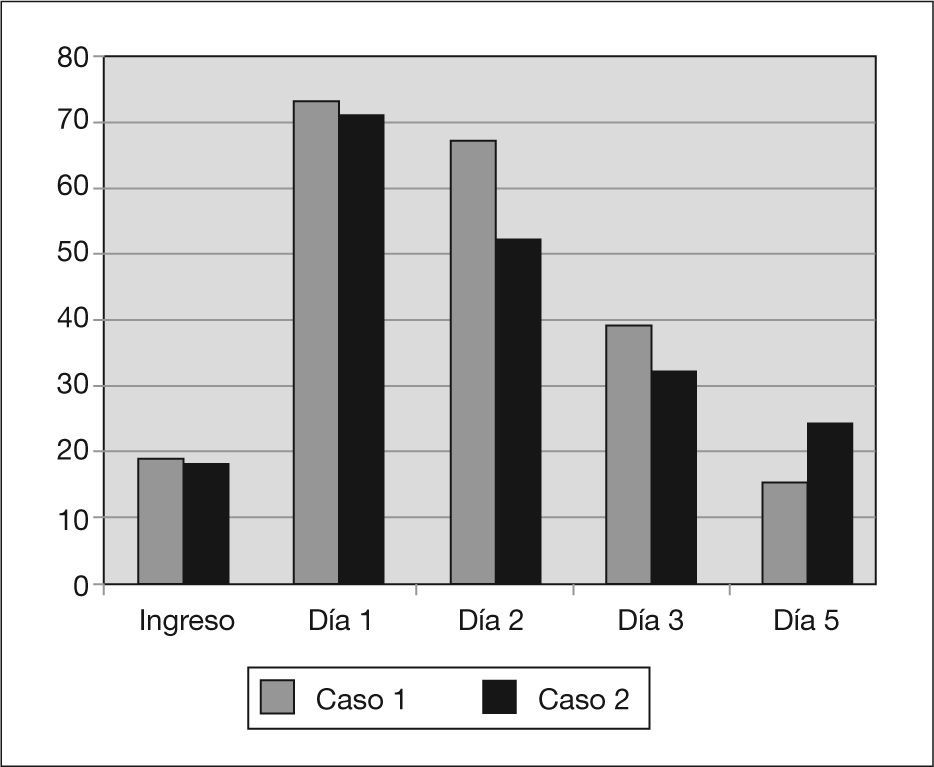
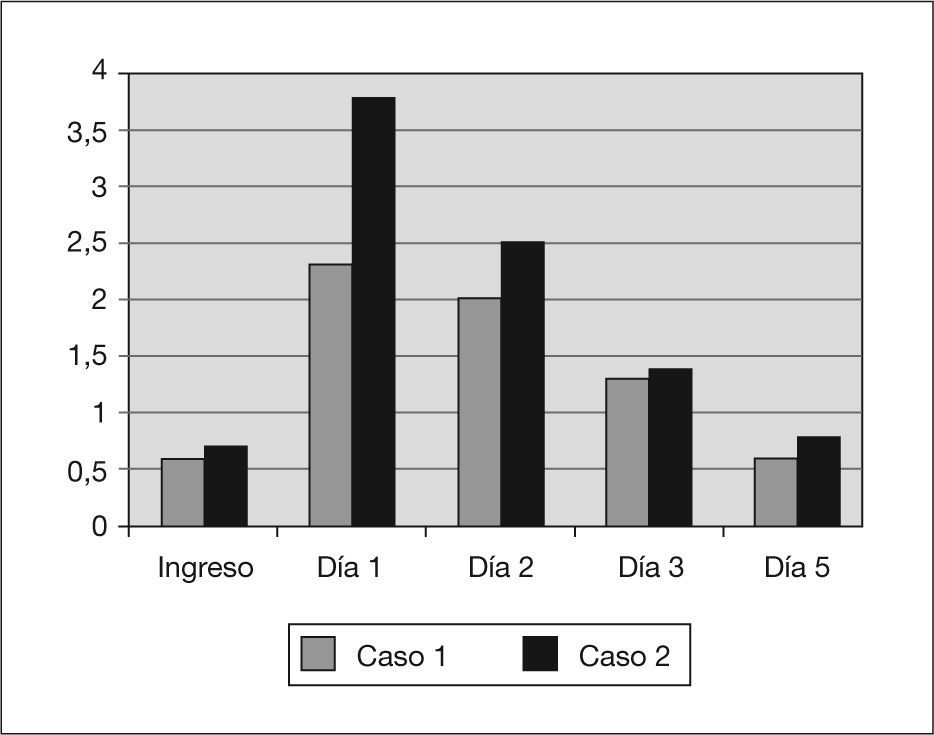
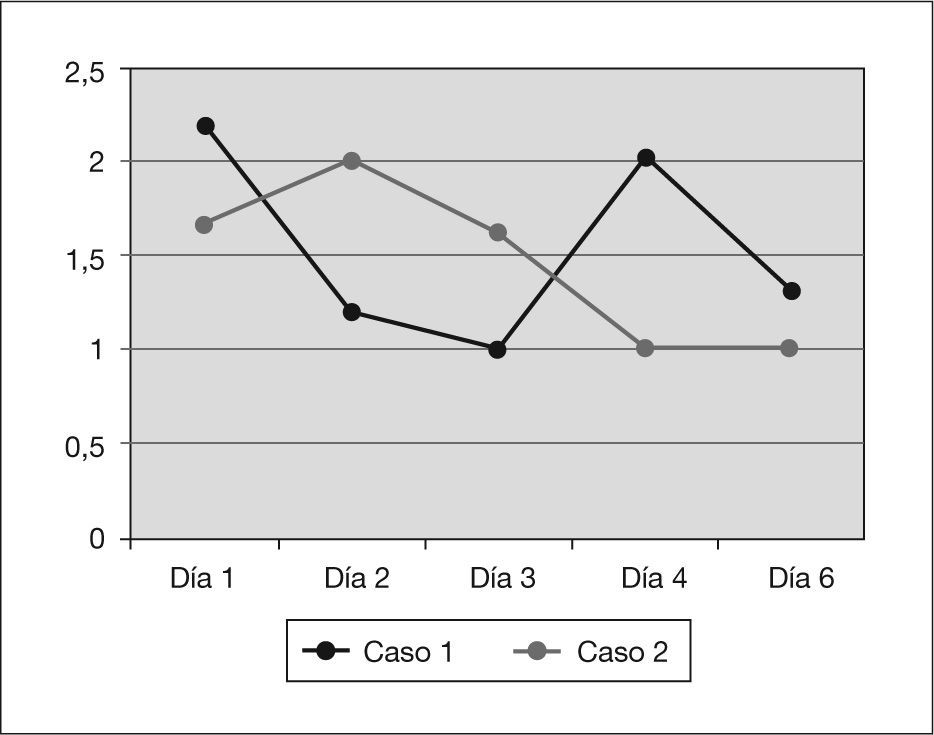
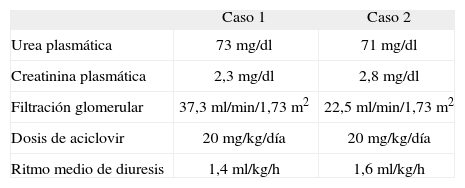
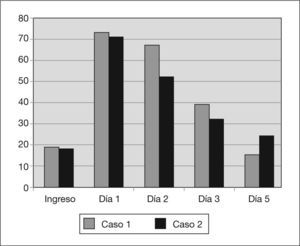
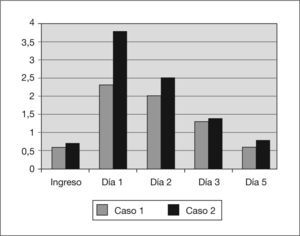
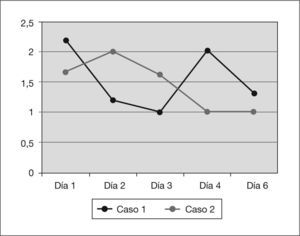
En la tabla 1 y en las figuras. 1 a 3 se muestran los datos analíticos evolutivos y de la diuresis de los 2 pacientes.
Datos analíticos al diagnóstico de la insuficiencia renal aguda
| Caso 1 | Caso 2 | |
| Urea plasmática | 73mg/dl | 71mg/dl |
| Creatinina plasmática | 2,3mg/dl | 2,8mg/dl |
| Filtración glomerular | 37,3ml/min/1,73m2 | 22,5ml/min/1,73m2 |
| Dosis de aciclovir | 20mg/kg/día | 20mg/kg/día |
| Ritmo medio de diuresis | 1,4ml/kg/h | 1,6ml/kg/h |
Niña de 12 años de edad, de origen magrebí, que llevaba en España desde hacía 2 semanas antes de su ingreso. No tenía antecedentes de enfermedades nefrourológicas en la familia. Ingresa en nuestro centro por fiebre acompañada de tos y dificultad respiratoria. A la exploración física destaca la presencia de lesiones vesiculares en vulva y labios menores compatibles con infección herpética.
Se diagnostica neumonía con derrame pleural y herpes genital, por lo que se inicia el tratamiento con fluidoterapia según las necesidades basales (ritmo: 80ml/h), cefotaxima intravenosa para el proceso respiratorio (100mg/kg) y aciclovir intravenoso para el proceso genital (60mg/kg/ día).
Las pruebas de laboratorio realizadas, antes del inicio del tratamiento, muestran los siguientes resultados: leucocitosis con neutrofilia, urea 18mg/dl, creatinina 0,7mg/dl, iones normales, proteína C reactiva (PCR) 4mg/dl. En la radiografía de tórax se observa una imagen de condensación en el hemitórax derecho con derrame pleural asociado; la prueba IDR de Mantoux fue positiva. Se diagnostica de neumonía tuberculosa y herpes genital; al cuarto día de su ingreso se comienza el tratamiento antituberculoso (triple terapia).
Al sexto día se detecta una elevación de las cifras de urea y creatinina (73 y 2,3mg/dl, respectivamente), sin oliguria y con cifras de presión arterial de 90/60mmHg. El estudio analítico aporta los siguientes resultados: sistemático de orina con pH 5,5; densidad 1.010; excreción urinaria 66mEq/l; índice de insuficiencia renal 3,5; excreción fraccionada de sodio 2,52 %; filtración glomerular 37,3ml/min/1,73m2. Se diagnostica de insuficiencia renal de origen parenquimatoso y se procede a la suspensión del aciclovir intravenoso y al inicio de un tratamiento conservador de la insuficiencia renal aguda. La función renal se normaliza a los 5 días de la suspensión del fármaco.
Caso 2Niña de 12 años de edad ingresada en nuestro centro por fiebre, cefalea y vómitos de 48h de evolución, que se acompañan de rigidez nucal. No refiere antecedentes familiares de enfermedad renal en la familia. Los exámenes complementarios muestran leucocitosis con neutrofilia; PCR 2,36mg/dl, punción lumbar con pleocitosis, normoglucorraquia e hiperproteinorraquia. Debido al estado general de la paciente y los datos de laboratorio, se decide iniciar tratamiento con cefotaxima intravenosa (dosis de 150mg/kg/día) hasta la llegada de cultivos. En los siguientes días se aprecia un empeoramiento progresivo con alteraciones del comportamiento y vómitos incoercibles, motivo por el que se aumenta la fluidoterapia (100ml/h) y se asocia aciclovir intravenoso al tratamiento con dosis de 60mg/kg/día que se infunde en una hora. Al quinto día de iniciar este tratamiento presenta elevación de las cifras de urea y creatinina (71 y 3,8mg/dl, respectivamente) sin oliguria y con discreta hipertensión sistólica (130/71mmHg). El análisis urinario y sanguíneo muestra los siguientes resultados: sistemático de orina pH 5, densidad 1.005; excreción urinaria de sodio 114mEq/l; índice de insuficiencia renal 7; excreción fraccionada de sodio 5 %; filtración glomerular 22,5ml/ min/1,73m2. La ecografía renal es normal. Los datos muestran una insuficiencia renal de origen parenquimatoso, por lo que se suspende el tratamiento con aciclovir y se inicia tratamiento conservador de la insuficiencia renal aguda, con lo que se normaliza la función renal al cabo de 5 días.
En ambos casos, dado el carácter autolimitado del proceso con el tratamiento conservador tras la suspensión del aciclovir, no se requirió biopsia renal.
DISCUSIÓNEl aciclovir es actualmente el agente farmacológico de elección para el tratamiento, de infecciones cuyo origen es la familia Herpesviridae1,2. Su uso se ha extendido tanto a pacientes inmunocompetentes con sospecha de enfermedad grave por virus del herpes (encefalitis herpética, herpes genital)3,4,6 como en pacientes inmunocomprometidos (con trasplante renal, sida, etc.) que reciben este medicamento como quimioprofilaxis7.
Se han descrito efectos secundarios que van desde los más frecuentes y menos graves, como intolerancia gastrointestinal (administración oral) y flebitis (administración parenteral), hasta otros menos frecuentes pero potencialmente más graves, como neurotoxicidad4 y nefrotoxicidad3–5,8.
La incidencia de insuficiencia renal en pacientes que toman aciclovir se estima, según distintas series, en torno al 19%3,9. El uso cada vez más extendido de este fármaco hace posible la descripción con mayor frecuencia de efectos secundarios potencialmente graves5 como la nefrotoxicidad, de las 2 pacientes que presentamos, en un breve espacio de tiempo.
En ambos casos la insuficiencia renal fue no oligúrica, se detectó al quinto día de haber iniciado el tratamiento con aciclovir intravenoso, y revirtió con la retirada del fármaco y el tratamiento conservador. Estos datos se superponen a los encontrados en la bibliografía actual en los cuales los pacientes recuperan la función renal basal en el plazo de 5 o 7 días3–5.
El mecanismo patogénico por el que se produce el fallo renal actualmente es incierto. El aciclovir es excretado por la orina mediante mecanismos de filtración glomerular y secreción tubular, y hasta en un 60 % se encuentra en su forma intacta en el túbulo renal3,8. La teoría más aceptada es que, debido a la baja solubilidad del aciclovir y las elevadas concentraciones en las que se halla en el túbulo renal, produce una precipitación de éste y, secundariamente, una obstrucción del flujo tubular3,8. La demostración de cristales en la zona luminar del túbulo mediante luz polarizada9, la presencia de proteinuria tubular10 y no hallar lesión en los glomérulos cuando se practica una biopsia, son algunas de las razones que apoyan esta teoría11–13.
La vía de administración del aciclovir no parece ser un factor de riesgo para desarrollar insuficiencia renal, pues se han descrito casos tanto con la administración oral como intravenosa5,7. En los casos presentados, el fármaco se suministró por vía intravenosa, de forma lenta y asegurando una hidratación adecuada. Se ha descrito una correlación positiva entre la administración en bolo del fármaco y la probabilidad de presentar insuficiencia renal9–11. En los casos en los que la situación basal obligue a una restricción hídrica del paciente, es necesaria una monitorización más estrecha para controlar la nefrotoxicidad de la medicación. Las pacientes en el momento de la detección de la insuficiencia renal tenían un aporte de líquidos adecuado a su peso y dirigido a un equilibrio hídrico neutro dada la situación basal (neumonía con derrame, meningoencefalitis).
La administración conjunta de aciclovir con otros fármacos con potencial nefrotóxico es otro factor que se postula para el desarrollo de la insuficiencia renal aguda3,7,10.
No debe olvidarse que debido a que la insuficiencia renal es no oligúrica, en ocasiones puede pasar inadvertida, especialmente en aquellos pacientes a los que se administra el aciclovir de forma ambulatoria, infraestimándose los casos de nefrotoxicidad existentes.
Finalmente, el objetivo de nuestra comunicación es poner de manifiesto un efecto que, aunque raro, quizá esté infraestimado debido a su presentación clínica. Hay que remarcar que aquellos pacientes a los que se suministre aciclovir, por vía intravensa u oral, deben ser monitorizados desde el punto de vista renal (parámetros de la función glomerular y tubular) para evitar y/o tratar con prontitud los efectos nefrotóxicos.
Es recomendable asegurar una buena hidratación y evitar en lo posible la administración conjunta de fármacos que puedan potenciar el efecto nefrotóxico del aciclovir.
Presentado en el XXXII Congreso de Nefrología Pediátrica. Oviedo, 1-4 de noviembre de 2006.
- Inicio
- Todos los contenidos
- Publique su artículo
- Acerca de la revista
- Métricas