En el momento actual existe una situación de indefinición con respecto a cuándo, cómo y de qué forma debe introducirse el gluten en la dieta del lactante. Durante años ha prevalecido la recomendación del Comité de Nutrición de la ESPGHAN de evitar tanto la introducción precoz, antes de los 4 meses, como la tardía, después de los 7 meses, y de introducir el gluten gradualmente mientras el lactante recibe leche materna; se pretendía con ello reducir el riesgo de enfermedad celiaca, diabetes y alergia al gluten. Sin embargo, 2 estudios independientes publicados en octubre de 2014 en The New England Journal of Medicine llegan a la conclusión de que la edad de introducción del gluten no modifica el riesgo de desarrollar la enfermedad celiaca y que la lactancia materna a cualquier edad tampoco confiere protección.
Por otra parte, según la evidencia científica disponible, en general, se recomienda la introducción de otros alimentos en la dieta distintos de la leche materna o de fórmula alrededor de los 6 meses de edad, ya que la introducción antes de los 4 meses se asociaría a un riesgo aumentado de enfermedades autoinmunes y alergia alimentaria, y retrasarla más allá de los 7 meses no tendría efecto protector.
En este contexto, un grupo de expertos ha considerado pertinente elaborar un documento de consenso basado en las evidencias científicas actuales y establecer unas recomendaciones generales para la introducción del gluten en la práctica clínica diaria.
At present there is a degree of uncertainty regarding when, how and in what form gluten should be introduced into the infant diet. For years the recommendations of the ESPGHAN Committee on Nutrition have prevailed, which include avoiding early introduction, before 4 months, and late, after 7 months, and gradually introducing gluten into the diet while the infant is being breastfed, with the aim of reducing the risk of celiac disease, diabetes and gluten allergy. However, 2 independent studies published in The New England Journal of Medicine in October 2014 reached the conclusion that the age of introduction of gluten does not modify the risk of developing celiac disease, and that breastfeeding at any age does not confer protection against celiac disease development.
On the other hand, according to available scientific evidence, the introduction of foods other than breast milk or formula into the infants diet is generally recommended around 6 months of age, since the introduction before 4 months could be associated with an increased risk of food allergy and autoimmune diseases, and delaying it beyond 7 months would not have a protective effect.
In this context, a group of experts has considered it appropriate to produce a consensus document based on the current scientific evidence and present general recommendations for daily clinical practice on the introduction of gluten into the diet.
Desde hace más de 20 años la ESPGHAN ha realizado, a través de su Comité de Nutrición (CN-ESPGHAN), recomendaciones referentes a la edad de introducción del gluten en la dieta del lactante1,2 con el objetivo de prevenir el desarrollo de la enfermedad celiaca (EC) y reducir el riesgo de diabetes mellitus tipo 1 (DM 1) y de alergia al trigo2,3.
Sin embargo, estudios recientes de alto grado de evidencia han demostrado que la edad de introducción del gluten no influye en el desarrollo de EC en población con riesgo genético4,5, poniendo en entredicho las recomendaciones actuales de la ESPGHAN2, de la European Food Safety Authority6 y las más recientes de la American Academy of Pediatrics; estas últimas, recomendando la introducción de la alimentación complementaria (AC) alrededor de los 6 meses de edad, sin hacer mención especial al gluten7.
Ante la situación de confusión actual, un grupo de expertos en EC y en nutrición pediátrica han elaborado un documento de consenso basado en las evidencias científicas actuales, estableciendo unas recomendaciones para la práctica clínica diaria.
Aspectos generales de la introducción de la alimentación complementariaLas recomendaciones de la ESPGHAN, la European Food Safety Authority y la American Academy of Pediatrics respecto a la introducción de la AC tienen en cuenta, además de las necesidades nutricionales, la posibilidad de influir en el desarrollo de ciertas enfermedades2,6,7.
Prevención de la alergiaNo hay datos científicos que apoyen recomendaciones diferentes en la introducción de la AC basadas en el riesgo del lactante de padecer alergia (familiar de primer grado con historia comprobada de alergia)8–11.
La introducción de la AC después de los 6 meses no tiene efecto protector sobre la aparición de alergia alimentaria12. Por el contrario, si se realiza antes de los 4 meses se asocia a un riesgo aumentado de desarrollar dermatitis atópica.
Tampoco se ha demostrado un riesgo aumentado de desarrollar alergia alimentaria cuando los alimentos potencialmente más alergizantes se incluyen en la dieta después de los 4 meses de edad10.
Con independencia del momento de introducción, tras incorporar un nuevo alimento, parece prudente recomendar una exposición regular (por ejemplo, varias veces a la semana) para mantener la tolerancia oral. También se ha observado que la inclusión de una mayor diversidad de alimentos en el primer año se asocia a un riesgo disminuido de padecer asma, alergia alimentaria o sensibilización a alimentos13.
Desarrollo de obesidadUna ingesta proteica elevada, especialmente de origen animal y en los 2 primeros años de vida, se asocia a un riesgo aumentado de padecer obesidad más tarde14,15.No hay evidencia sobre cuándo introducir la AC para disminuir el riesgo de obesidad16.
Desarrollo de diabetes mellitus tipo 1Se ha encontrado un riesgo aumentado de desarrollar DM 1 cuando la AC se introduce antes de los 4 meses o después de los 617. Sin embargo, no se ha demostrado un mayor riesgo asociado a un factor dietético específico18.
En resumen, de acuerdo con la evidencia científica, la introducción de la AC antes de los 4 meses se asocia a un riesgo aumentado de enfermedad, mientras que la introducción después de los 7 meses no tiene efecto protector, manteniéndose, pues, vigente el consejo de introducir la AC alrededor de los 6 meses.
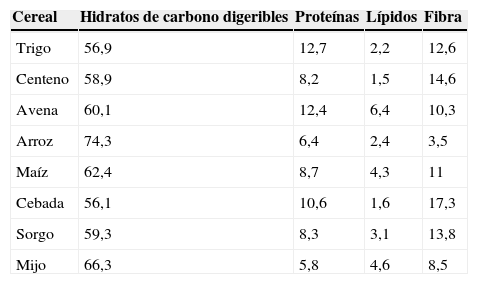
Valor nutricional de los cerealesLos cereales, uno de los pilares de la alimentación humana, representan la principal fuente de hidratos de carbono (HC) y fibra de la dieta, siendo los más utilizados: trigo, arroz, maíz, centeno, cebada, avena, mijo y sorgo19. Contienen aproximadamente un 70-78% de HC, 6-13% de proteínas y 1-6% de grasas (tabla 1)19,20.
Composición de los cereales
| Cereal | Hidratos de carbono digeribles | Proteínas | Lípidos | Fibra |
|---|---|---|---|---|
| Trigo | 56,9 | 12,7 | 2,2 | 12,6 |
| Centeno | 58,9 | 8,2 | 1,5 | 14,6 |
| Avena | 60,1 | 12,4 | 6,4 | 10,3 |
| Arroz | 74,3 | 6,4 | 2,4 | 3,5 |
| Maíz | 62,4 | 8,7 | 4,3 | 11 |
| Cebada | 56,1 | 10,6 | 1,6 | 17,3 |
| Sorgo | 59,3 | 8,3 | 3,1 | 13,8 |
| Mijo | 66,3 | 5,8 | 4,6 | 8,5 |
Composición aproximada de los cereales (g/100g de porción comestible).
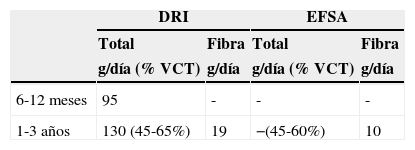
El almidón es el principal HC de los cereales, que además contienen otros polisacáridos no digeribles, componentes de la fibra dietética. Los HC deben suponer entre el 45-65% del valor calórico total de la dieta del lactante (tabla 2)21,22.
Requerimientos dietéticos de los hidratos de carbono
| DRI | EFSA | |||
|---|---|---|---|---|
| Total | Fibra | Total | Fibra | |
| g/día (% VCT) | g/día | g/día (% VCT) | g/día | |
| 6-12 meses | 95 | - | - | - |
| 1-3 años | 130 (45-65%) | 19 | −(45-60%) | 10 |
DRI: dietary reference intakes («ingesta dietética de referencia»); EFSA: European Food Safety Authority; VCT: valor calórico total.
Aunque los cereales contienen todos los aminoácidos, presentan deficiencias relativas de algunos de ellos, lo que les confiere un bajo valor biológico, debiendo ser complementados con otras proteínas. El contenido proteico varía según el tipo de cereal, siendo mayor el del trigo y la avena, y menor el del arroz y el maíz19.
Los cereales son una importante fuente de vitaminas del grupo B (niacina y tiamina)23, de pequeñas cantidades de elementos traza (hierro y selenio) y de minerales (fósforo, potasio, magnesio y calcio).
El gluten en los cerealesEl gluten es, por su naturaleza cohesiva y viscoelástica, especialmente relevante en los procesos de panificación24. Contiene cientos de proteínas ricas en glutamina y prolina, llamándose por ello prolaminas25; estas son digeridas solo parcialmente por las proteasas humanas, aspecto relevante en la patogenia de la EC.
Las prolaminas del trigo (gliadinas), del centeno (secalinas) y de la cebada (hordeínas) se relacionan con la EC, siendo controvertido el papel de las prolaminas de la avena (aveninas). No obstante, en general se consideran cereales con gluten: trigo, cebada, centeno y avena. El gluten representa el 80% de las proteínas, variando la proporción de prolaminas, siendo esta muy superior en el trigo en comparación con la de otros cereales.
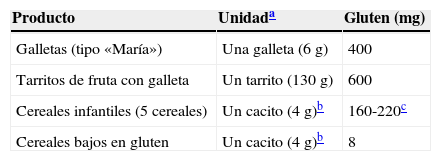
Clásicamente, los cereales son el primer alimento que se añade tras la leche a la dieta del lactante2. En la tabla 3 se muestra el contenido en gluten de los alimentos utilizados más comúnmente en el inicio de la AC.
No existen razones nutricionales que justifiquen el consumo de un cereal concreto. Generalmente, se recomienda iniciar la AC con cereales sin gluten por tener menor capacidad antigénica. El consumo de un cereal u otro viene determinado por razones culturales: en Europa y los países occidentales se consume preferentemente trigo, en América, maíz, y en los países orientales, arroz.
Recomendaciones del Comité de Nutrición de la European Society for Paediatric Gastroenterology, Hepatology and NutritionEn 1982 el CN-ESPGHAN1, siguiendo unas recomendaciones de 1969, hizo la siguiente advertencia general: «el gluten no debería ser introducido en la dieta de los lactantes antes de los 4 meses de edad e incluso podía ser aconsejable posponerlo hasta los 6 meses». Estas recomendaciones estaban basadas en que posiblemente la sensibilización al gluten podía ser inducida más fácilmente en el lactante pequeño, especialmente en los alimentados artificialmente.
Estas normas estuvieron vigentes hasta el año 2008, en que el CN-ESPGHAN2 las actualizó basándose en:
- •
Una revisión sistemática y metaanálisis que mostraba que el riesgo de desarrollar EC se reducía significativamente en los lactantes que recibían lactancia materna (LM) en el momento de la introducción del gluten comparados con los que no recibían LM, y que la mayor duración de la LM se asociaba con menor riesgo de EC. Sin embargo, no quedaba demostrado si la LM proporcionaba una protección permanente frente a la EC o solo retrasaba la edad de aparición26.
- •
La llamada «epidemia sueca» de EC: entre los años 1984 y 1996 se detectó un brusco incremento en la incidencia de EC en niños<2 años coincidiendo con cambios en la introducción del gluten: a partir de los 6 meses e introducción súbita de grandes cantidades de trigo. Así, a los 6-8 meses de edad, el consumo de trigo aumentó de 10 a 26g/día (equivalente a un incremento de 0,9 a 2,7g de gluten/día). A finales de los noventa, tras adelantar de nuevo la introducción del gluten al cuarto mes y reducir≥30% el consumo de trigo, se observó una caída significativa del número de casos de EC en este grupo de edad27.
- •
Un estudio prospectivo (Norris et al.) que demostró, en niños con un familiar de primer grado con DM 1 o con HLA de riesgo (DR3 o DR4), que la introducción muy precoz de gluten (<3 meses), o tardía (>7 meses), incrementaba el riesgo de EC28.
Con base en estos estudios el CN-ESPGHAN aconsejó: «es prudente evitar la introducción precoz (<4 meses) y tardía (>7 meses) del gluten, e introducirlo gradualmente mientras el lactante recibe LM, ya que así se puede reducir el riesgo de EC, DM 1 y alergia al gluten»2. Esta recomendación fue corroborada por la European Food Safety Authority6 y por una revisión sistemática sobre alimentación del lactante y prevención de EC3, si bien se precisaba que eran necesarios más estudios para clarificar cuestiones aún no resueltas. De hecho, el Comité de Nutrición y el de Toxicología del Reino Unido29 puntualizaron que no había suficiente evidencia científica para hacer recomendaciones específicas sobre la introducción del gluten en la alimentación del lactante; efectivamente, estudios suecos recientes demuestran que a pesar de no haber cambiado las últimas normas de introducción del gluten, el número de casos de EC volvió a aumentar a finales de los noventa, observándose desde entonces, y hasta el momento actual, una incidencia acumulada semejante a la de los años ochenta, años de la epidemia30,31.
En resumen, las actuales recomendaciones del CN-ESPGHAN referidas a cuándo –de los 4 a los 7 meses–, cómo –incremento progresivo partiendo de pequeñas cantidades– y en qué circunstancias –mientras el lactante recibe LM– se debe introducir el gluten parece que no serían suficientes para la prevención primaria de la EC.
Introducción del gluten y riesgo de enfermedad celiacaLa hipótesis de una ventana entre los 4 y los 7 meses durante la cual la introducción de pequeñas cantidades de gluten mientras el niño aún recibe LM podría proteger del desarrollo de EC a los niños de riesgo3,27,30–33 ha sido abordada recientemente por 2 estudios publicados en The New England Journal of Medicine4,5. Además, un editorial incluido en la misma edición destaca la relevancia de los hallazgos reportados34.
En el estudio PreventCD (www.preventcd.com), prospectivo, se seleccionaron bebés con riesgo de EC (familiar de primer grado con EC y al menos un HLA de riesgo: DQ2 y/o DQ8)4. Estos fueron separados, de forma aleatoria (a ciegas), en 2 grupos, recibiendo, a partir de las 16 semanas de vida, diariamente durante 8 semanas o 200mg de gluten (conteniendo 100mg de gluten inmunogénico), grupo 1, o placebo (2g de lactosa), grupo 2, recomendándose la LM durante todo este periodo. A partir de las 24 semanas se aumentaba la cantidad de gluten utilizando productos habituales en la alimentación infantil (cereales o galletas), siguiendo un protocolo preestablecido: entre los 6-7 meses, 250mg de gluten al día; entre los 7-8 meses, 500mg; a los 8-9 meses, 1.000mg, a los 9-10 meses, 1.500mg, y consumo libre a partir de los 11 meses. Novecientos noventa y cuatro niños cumplieron este protocolo, que incluía seguimiento clínico: signos o síntomas indicativos de EC35, detección de anticuerpos antitransglutaminasa, control del crecimiento y de la dieta (LM y consumo de gluten). Cuando todos los niños alcanzaron los 3 años se abrieron los códigos, analizando los 2 grupos por separado. La frecuencia de EC en la cohorte a los 3 años (incidencia acumulada) fue del 5,2%, no observándose diferencias entre el grupo 1 y el grupo 2. Tampoco se encontró relación entre el desarrollo de EC y la duración de la LM (exclusiva o mixta) ni con el mantenimiento de la LM durante la introducción del gluten. Sin embargo, sí se vio que los lactantes DQ2 homocigotos (DR3-DQ2/DR3-DQ2 o DR3-DQ2/DR7-DQ2) tenían un riesgo significativamente mayor de desarrollar EC antes de los 3 años que los lactantes con haplotipos de menos riesgo.
Por otra parte, a los 3 años la frecuencia de EC en niñas doblaba la frecuencia en niños: 7,2 frente a 3,4%. Así mismo, se detectó una mayor incidencia acumulada estadísticamente significativa de EC en las niñas que introdujeron el gluten a las16 semanas comparada con la de aquellas que lo introdujeron a las 24, diferencia no observada en los niños.
Los autores concluyen que «la introducción de pequeñas cantidades de gluten entre las 16 y las 24 semanas de vida no redujo el riesgo de EC».
En la misma edición de The New England Journal of Medicine se publica el estudio multicéntrico CELIPREV, en el que recién nacidos con riesgo de EC (al menos un familiar de primer grado con EC) fueron seleccionados y aleatorizados: un grupo inició la ingesta de gluten a los 6 meses (pasta, sémola y galletas), grupo 1, y el otro, a partir de los 12, grupo 25. La cantidad de gluten ingerida por los lactantes fue libre. Durante el primer año de vida se recopiló información sobre infecciones intestinales y la dieta (contenido de gluten diario), y a los 15 meses se realizó el genotipado HLA (excluyéndose los DQ2-DQ8 negativos), determinándose anticuerpos antigliadina y antitransglutaminasa a los 2, 3, 5, 8 y 10 años en los 553 niños finalmente incluidos. A los 2 años, los niños del grupo 1 habían desarrollado la EC en un porcentaje significativamente más alto (12 vs. 5%) que los del grupo 2. A los 5 y los 10 años las diferencias entre los 2 grupos no fueron estadísticamente significativas. A los 10 años, el 25,8% de los niños homocigotos DQ2/DQ2 habían desarrollado EC frente al 15,8% de los que poseían fenotipos de menor riesgo. La LM no se asoció con el desarrollo de EC. Aunque los autores plantean que retrasar el inicio de la EC podría tener algún beneficio, no hay evidencia para apoyar esta premisa.
Los autores concluyen que «ni la introducción tardía de gluten ni la LM modificaron el riesgo de EC entre los niños de riesgo, aunque la introducción tardía del gluten se asoció con un retraso en la aparición de la enfermedad».
Conclusiones de ambos estudios- •
La edad de introducción del gluten no modifica el riesgo de desarrollar la EC, por lo que ninguno de los 2 estudios apoya la hipótesis de una ventana de edad que propicie el desarrollo de tolerancia al gluten. La introducción a partir de los 12 meses podría retrasar el inicio de la EC.
- •
El fenotipo genético es el factor más determinante de riesgo de desarrollar EC en edades tempranas, especialmente para los homocigotos DQ2/DQ2.
- •
La LM no protege frente al desarrollo de EC.
La introducción de la AC a partir de los 4 meses de edad no se relaciona con el desarrollo de alergia alimentaria ni de DM 1, aunque si es hiperproteica puede favorecer el desarrollo de obesidad.
La introducción de los cereales se justifica por sus propiedades nutricionales, basándose la elección del cereal en las costumbres de la población.
No hay evidencias de que sean necesarias recomendaciones diferentes o específicas para la introducción de la AC en los lactantes con riesgo de alergia o de EC.
La duración de la LM exclusiva y el momento de la introducción de la AC no se relacionan con la aparición ni de EC ni de alergia alimentaria.
La introducción de pequeñas cantidades de gluten en edades tempranas no reduce el riesgo de EC en niños con riesgo genético. Retrasar la introducción del gluten tampoco modifica el riesgo de EC en lactantes con predisposición genética, aunque la introducción tardía podría retrasar la edad de aparición de la enfermedad.
Ante la falta de estudios recientes, se acepta el mayor riesgo de autoinmunidad asociado a la introducción del gluten antes de los 4 meses de edad en población con predisposición genética. Por otra parte, los datos del estudio PreventCD en niñas de alto riesgo genético para la EC recomiendan cautela con la introducción del gluten en esta subpoblación antes de los 6 meses de edad.
A día de hoy, no existe ninguna recomendación de sociedades científicas sobre la cantidad concreta de gluten a introducir. En Suecia los lactantes consumían en los años anteriores a la epidemia 0,9g de gluten/día, durante la epidemia, 2,5-2,7g/día, y aproximadamente 2g/día en los años posteriores. En países con menor prevalencia de EC como Dinamarca, en esa época (1987) el consumo era aproximadamente de 0,2g/día a los 6-8 meses, y de 1,8g a los 9-12 meses. No obstante, estos datos son una estimación basada en las ventas de cereales infantiles en los años correspondientes y en las recomendaciones nutricionales de la época, y no en encuestas dietéticas de consumo real. Por otra parte, el estudio PreventCD demuestra que el consumo de solo 200mg de gluten puede inducir respuesta inmunológica.
Tampoco se ha observado que la introducción del gluten mientras se mantiene la LM proteja del desarrollo de EC.
Una variedad más amplia de alimentos en la diversificación en el primer año de vida puede tener un efecto protector en el desarrollo de enfermedades alérgicas.
En resumen, si bien los estudios recientemente publicados no apoyan las recomendaciones actuales del CN-ESPGHAN en cuanto a la introducción del gluten en la dieta del lactante, tampoco las invalidan. Tampoco aportan evidencias que permitan establecer nuevas recomendaciones. Desconocemos la edad idónea de introducción del gluten en la alimentación del lactante y la forma más adecuada de administrarlo tanto en población general como en población de riesgo.
Recomendaciones del grupo de expertosAunque en el momento actual no hay suficiente evidencia científica, basándose en los conocimientos actuales (estudios de requerimientos de nutrientes y estudios de impacto de alimentación temprana y prevención de enfermedades) el grupo de expertos llegó a un consenso sobre los siguientes aspectos, tanto para población general como para población de riesgo:
- 1.
La LM es siempre recomendable, independientemente de su efecto sobre el desarrollo de EC.
- 2.
Se recomienda introducir la AC preferentemente mientras se mantiene la LM.
- 3.
Se desaconseja la introducción del gluten antes de los 4 meses de edad.
- 4.
Se recomienda introducir el gluten en torno a los 6 meses de edad:
- a.
Parece una opción razonable su introducción entre los 5-6 meses.
- b.
Si por cualquier motivo se inicia la alimentación complementaria de forma precoz, eventualmente podría considerarse introducirlo a partir de los 4 meses, aunque a esa edad se podrían utilizar otros cereales, como maíz o arroz, no relacionados con la EC.
- c.
En caso de retraso en la introducción de la AC podría demorarse la inclusión del gluten sin que ello suponga un riesgo adicional para el paciente con respecto al posible desarrollo de EC.
- a.
- 5.
Introducir el gluten en pequeñas cantidades: puede iniciarse con 1-2 cacitos de cereales o una galleta al día, o cantidades equivalentes de gluten (tabla 3).
- 6.
Una vez introducido, aumentar su consumo de forma gradual en función de las necesidades nutricionales (aporte calórico) y la tolerancia del lactante.
Este trabajo no ha sido financiado.
Conflicto de interesesNo hay conflicto de intereses.