Sr. Editor:
La neumatosis intestinal se define como la presencia de aire en el espesor de la pared intestinal 1,2. Es un hallazgo relativamente frecuente durante el período neonatal, con relación a enterocolitis necrosante, pero extraordinariamente raro en edad pediátrica 2. Su etiología es desconocida, aunque se han descrito casos en relación con trasplante de órganos sólidos y médula ósea, tratamiento inmunosupresor y corticoideo, isquemia, inflamación y obstrucción intestinal, etc. 3. Recientemente se han descrito casos de neumatosis en relación con trasplantes de órganos torácicos en niños 2, aunque esta asociación es menos frecuente que en adultos.
Se presenta el caso de una niña de 13 años portadora de trasplante cardíaco ortotópico secundario a miocardiopatía dilatada idiopática que presenta, a los 45 días postrasplante, un episodio de distensión abdominal grave, sin dolor, alteración del ritmo intestinal ni otra sintomatología asociada.
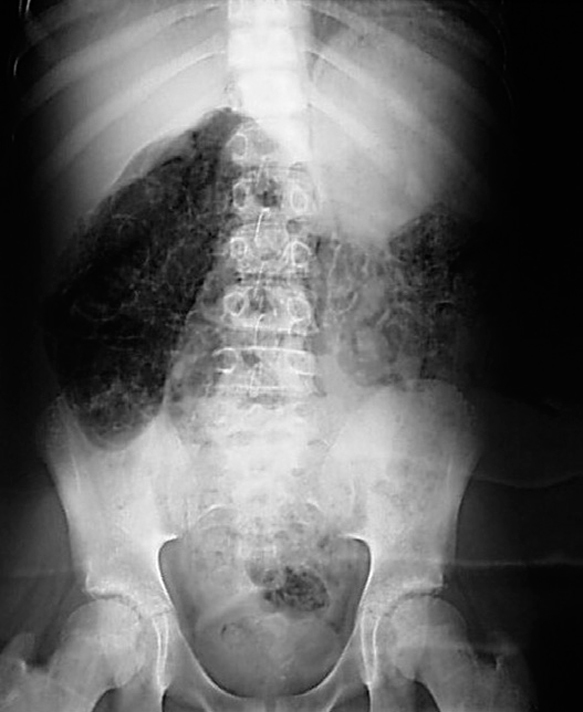
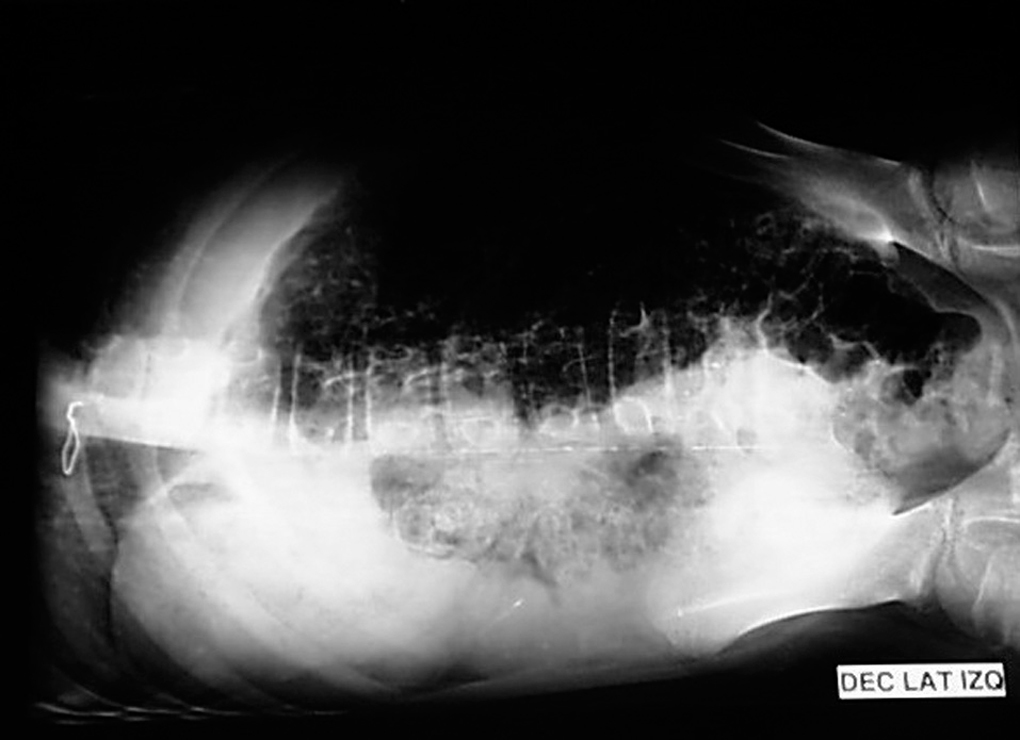
Se realizó radiografía simple de abdomen, objetivando patrón radiolucente en el espesor de la pared intestinal con imágenes microvesiculares quísticas difusas, sin presencia de aire ectópico (figs. 1 y 2). Se confirmó el diagnóstico mediante realización de TC abdominal, realizando coprocultivos y determinación de rotavirus en heces, así como antigenemia a citomegalovirus, con resultados negativos. El estudio se completó con biopsia intestinal que resultó normal.
Figura 1. Radiografía simple de abdomen en la que se observa una imagen compatible con neumatosis intestinal.
Figura 2. Imagen en decúbito lateral compatible con neumatosis intestinal.
En el momento del episodio, recibía tratamiento inmunosupresor con tacrolimus (concentraciones plasmáticas: > 10 ng/ml), azatioprina y metilprednisolona (0,6 mg/kg/día en dosis única diaria).
La paciente había presentado 2 episodios de rechazo, el primero a los 8 días postrasplante (grado IIIa), que fue tratado con corticoterapia intravenosa, y el segundo 10 días antes del episodio de neumatosis, para el que recibió tratamiento con corticoides intravenosos y anticuerpos antilinfocitos policlonales de caballo (ATGAM).
Se administró oxigenoterapia mediante gafas nasales con disminución progresiva de la distensión abdominal hasta normalizarse en 3-4 días, y persistencia de las anomalías radiológicas hasta 4 meses más tarde, coincidiendo con la disminución paulatina de la corticoterapia (hasta 0,1 mg/kg/día) y el control de la infección por citomegalovirus (antigenemia positiva a los 2 meses postrasplante y tratamiento con ganciclovir).
La neumatosis intestinal es una entidad clínico-radiológica cuyo comportamiento, tratamiento y pronóstico difiere según la edad de presentación. Así, en el período neonatal es mucho más común en relación con enterocolitis necrosante y estos pacientes presentan mayor mortalidad, riesgo de perforación y complicaciones secundarias 4.
Los factores de riesgo asociados en el período neonatal son: prematuridad, bajo peso al nacimiento o elevado aporte alimenticio de forma precoz. Mientras que en edades posteriores son: menor edad 2, tratamiento mantenido con esteroides, por la atrofia del tejido linfoide y disección de pared intestinal que producen; se ha descrito que dosis de prednisona superiores a 0,5 mg/kg/día aumentan el riesgo de desarrollar neumatosis intestinal en pacientes trasplantados 2, infecciones por rotavirus, Clostridium difficile y citomegalovirus por su contribución a la disminución de la integridad de la pared intestinal 2,5,6, trasplante de órganos sólidos 7 y de médula ósea.
La forma de presentación más habitual en ambas edades consiste en: distensión y/o dolor abdominal, vómitos, diarrea con o sin sangre, y el paciente puede encontrarse asintomático inicialmente, sobre todo en edad pediátrica 2,8.
Una vez establecida la sospecha clínica, la confirmación diagnóstica es radiológica 1 (radiografía simple y/o TC) y se recomienda la realización de radiografía abdominal en todo paciente portador de trasplante con sintomatología digestiva 2, teniendo en cuenta que el patrón radiológico puede pasar inadvertido en fases iniciales.
Respecto al tratamiento y evolución, hay que destacar que, debido a que la mayoría de la experiencia publicada sobre neumatosis intestinal deriva de su presentación en neonatos, se ha considerado habitualmente como un proceso de mal pronóstico 9 que precisa de atención quirúrgica inmediata y medidas agresivas 6. Por el contrario, en la edad pediátrica, el tratamiento conservador con reposo intestinal, antibioterapia sistémica y oxigenoterapia, suele ser suficientes para la resolución del cuadro, junto con un adecuado tratamiento de la enfermedad de base 2,8,10. En estos pacientes se considera la presencia de gas en el sistema venoso portal y/o la acidosis signos de peor pronóstico; estas son de las pocas indicaciones establecidas para el tratamiento quirúrgico agresivo desde el inicio del cuadro 9.
Por todo esto, podemos concluir que ante todo niño trasplantado, con tratamiento inmunosupresor u otros factores de riesgo asociados, debemos estar alerta ante la posibilidad de desarrollar neumatosis intestinal, y realizar las exploraciones complementarias adecuadas ante la mínima sintomatología digestiva, y teniendo en cuenta que en la mayoría de las ocasiones el tratamiento conservador es suficiente para la buena evolución de los paciente en edad pediátrica.
Correspondencia: Dra. C. Iglesias Fernández.
Antonio Acuña, 25. 2.º C. 28009 Madrid. España.
Correo electrónico: cristinaif@hotmail.com