El objetivo de este estudio es conocer las características epidemiológicas, clínicas y analíticas de la primoinfección por el virus de Epstein-Barr (VEB) en niños sin diagnóstico previo de ninguna enfermedad inmune y su relación con la forma de presentación clínica.
Pacientes y métodosEstudio retrospectivo de pacientes entre 0 y 15 años con IgM sérica frente a la cápside viral del VEB positiva o indeterminada, durante un período de 22 meses. Se analizaron datos epidemiológicos, clínicos y de laboratorio y se compararon según tuvieran una clínica típica (síndrome mononucleósico) o no típica.
ResultadosSe incluyeron 103 niños. La mediana de la edad fue de 7 años (3-12,5 años). El 63% de los pacientes presentaron clínica típica o síndrome mononucleósico y el 37% una clínica no típica. La edad fue significativamente menor en el grupo de clínica no típica (p=0,03) y recibieron menos tratamiento antibiótico (p=0,015). En los parámetros analíticos no hubo diferencias estadísticamente significativas excepto en la PCR, discretamente más elevada en el grupo de clínica típica (p=0,04). El 33% de los pacientes tuvieron anticuerpos heterófilos positivos. El 20% tuvieron una IgM frente a la cápside viral indeterminada, la mayoría con clínica oligosintomática o atípica. El 21% tuvieron IgM positivas para otros virus y 3 de ellos fueron posibles falsos positivos para el VEB.
ConclusionesEn nuestra población, la primoinfección por VEB es frecuente en niños de menor edad, y en ellos predominan las formas oligosintomáticas. El porcentaje de anticuerpos heterófilos positivos ha sido muy bajo en nuestra muestra. Los casos con IgM frente a la cápside viral indeterminada son más frecuentes en el grupo de clínica no típica. Es común detectar coinfección con otros virus.
The aim of this study is to assess epidemiological, clinical and laboratory characteristics of primary infection by Epstein-Barr virus (EBV) in children without previous diagnosis of any immune disease and its relationship with clinical presentation.
Patients and methodsA retrospective study was conducted on all children from 0 to 15 years with IgM against viral capsid of EBV positive or indeterminate during a 22 month period. Epidemiological, clinical and laboratory data were analysed and compared between typical (mononucleosis syndrome) and non-typical clinical symptoms.
ResultsThe study included a total of 103 children, with a median age of 7 years (3-12.5 years). Almost two-thirds (63%) of patients had typical clinical signs, with a mononucleosis syndrome, and 37% had a non-typical presentation. The non-typical clinical group had a lower age (P=.03) and took less antibiotic than the typical clinical group (P=.015). From laboratory studies, there were no differences between the groups, except in RCP, which was higher in typical clinical group (P=.04). Heterophile antibodies were positive in 33% of patients. An indeterminate IgM against viral capsid was present in 20% of the patients, and most of them had an oligosymptomatic or atypical presentation. An IgM positive for other viruses was found in 21%, and 3 of them were suspicious of false positive for EBV.
ConclusionsIn the studied population, a primary infection due to EBV is common in younger ages, and they have usually an oligosymptomatic clinical presentation. A very low percentage of positive heterophile antibodies were found. Cases with indeterminate IgM against viral capsid are more frequent in the non-typical clinical group. Co-infection with other viruses is common.
La primoinfección por el virus de Epstein-Barr (VEB) suele producir un síndrome mononucleósico completo: fiebre, astenia, adenopatías, faringoamigdalitis exudativa, hepatoesplenomegalia y exantema tras la administración de penicilina. Pero en ocasiones puede cursar de forma oligosintomática o con síntomas atípicos, siendo en estos casos más difícil su diagnóstico. En los pacientes de menor edad la primoinfección suele ser asintomática u oligosintomática y es en los adolescentes donde la primoinfección cursa con el síndrome mononucleósico completo.
La edad a la que ocurre la primoinfección por el VEB varía según factores culturales y socioeconómicos. En países en vías de desarrollo y zonas rurales la mayoría de los niños han adquirido la infección por VEB entre los 3 y los 6 años de edad. En cambio, en zonas urbanas y en países desarrollados la primoinfección ocurre en edades más tardías y es más frecuente que produzca más síntomas o un síndrome mononucleósico1–3.
El diagnóstico de la mononucleosis infecciosa se basa en las manifestaciones clínicas, apoyadas en los hallazgos analíticos típicos (leucocitosis con linfomonocitosis, linfocitos atípicos y aumento de enzimas hepáticas). La presencia de anticuerpos heterófilos es muy específica pero poco sensible, y su producción aumenta con la edad4–6. Las formas oligosintomáticas de la primoinfección por VEB se suelen confirmar con métodos serológicos.
La serología específica de anticuerpos virales IgG e IgM frente a los complejos antigénicos de la cápside viral (VCA), el antígeno precoz y el antígeno nuclear del VEB son la prueba de elección para determinar la infección aguda en un huésped inmunocompetente y monitorizar la progresión de la infección a lo largo del tiempo5–7. Las nuevas técnicas de diagnóstico molecular, como la detección de ADN por reacción en cadena de la polimerasa, podrían ayudarnos en la interpretación de algunos perfiles serológicos dudosos, aunque aún conocemos pocos datos, especialmente en individuos sanos y en población infantil, y harán falta más estudios para estandarizar los niveles de carga viral8–10. No se utilizan en el diagnóstico de mononucleosis en pacientes inmunocompetentes11.
La seroprevalencia y las edades a las que se produce la primoinfección por el VEB en la población española han sido poco estudiadas. Uno de los estudios realizados en España por Pariente et al. muestra un pico entre los 2 y los 4 años y otro entre los 14 y los 18 años12.
La mayoría de los estudios publicados incluyen pacientes con síntomas de mononucleosis infecciosa y hospitalizados13–15, por lo que conocemos pocos datos sobre otras formas clínicas de primoinfección en niños sin diagnóstico previo de enfermedades inmunes.
El objetivo de nuestro trabajo es conocer las características epidemiológicas, clínicas y analíticas de la primoinfección por VEB en los niños sanos de nuestro Departamento de Salud y evaluar su relación con el tipo de clínica presentada durante la primoinfección.
Pacientes y métodosDiseño y ámbito del estudioSe estudiaron retrospectivamente todos los niños de 0 a 15 años con serología positiva para VEB, solicitada desde Atención Primaria, Urgencias Hospitalarias u Hospitalización.
Población y criterios de selecciónSe incluyeron los pacientes cuyos sueros presentaban una IgM frente a la VCA del VEB positiva o indeterminada, en un período de 22 meses (desde septiembre de 2012 a junio de 2014). La inclusión de los casos se realizó desde el laboratorio de Microbiología, que centraliza la atención sanitaria de 204.623 habitantes del Departamento Xátiva-Ontinyent en la provincia de Valencia (censo de 2013), de los cuales 30.636 son menores de 15 años.
Se definió como «caso» todo paciente con serología IgM VCA del VEB positiva o indeterminada mediante la técnica de quimioluminiscencia Liaison® (Diasorin, Italia). Se incluyeron las serologías con IgM VCA indeterminada ya que, al tratarse de una técnica cuantitativa, pertenecen a un rango en que no son claramente negativas y podría tratarse de una fase precoz de la primoinfección. Se excluyeron los pacientes cuyos sueros tenían IgM VCA negativa, tenían una edad mayor o igual a 16 años o aquellos en los que al revisar la historia clínica presentaban alguna enfermedad crónica de base o recibían tratamiento inmunosupresor o corticoides.
Fuente de datosSe realizó la recogida de datos epidemiológicos, clínicos y analíticos a partir de la historia clínica electrónica, según el protocolo establecido por nuestro centro para el acceso a los datos y su confidencialidad. El estudio fue aprobado por el Comité de Investigación Clínica de nuestro departamento.
Variables estudiadasSe recopilaron las siguientes características epidemiológicas: sexo, edad y mes del año de la primoinfección. También se recogieron datos sobre la necesidad de ingreso y la administración de antibiótico. En cuanto a las manifestaciones clínicas, se recogió la presencia de fiebre, amigdalitis exudativa, exantema, esplenomegalia en la palpación abdominal, adenopatías (mayores de 1cm), astenia y la variable «otros síntomas», que incluía vómitos, diarrea, dolor abdominal, ictericia, hepatomegalia a la palpación, mialgias y edema palpebral. Según estas variables, los pacientes se dividieron en 2 grupos. En el grupo con clínica típica (síndrome mononucleósico) se incluyeron aquellos pacientes con al menos 2 de los siguientes síntomas: fiebre, faringoamigdalitis, adenopatías y astenia. En el grupo de clínica no típica se incluyeron el resto de los pacientes, es decir, aquellos con menos de 2 síntomas de los referidos (oligosintomáticos) y pacientes con síntomas atípicos o diferentes a los que forman parte del síndrome mononucleósico.
En cuanto a los datos analíticos, se incluyeron los valores de leucocitos y plaquetas. Se recogieron además las cifras de GOT y GPT, considerando hipertransaminasemia la elevación de uno de los 2 parámetros 2 veces por encima del valor normal de referencia de nuestro laboratorio (30UI/ml), la cifra de la proteína C reactiva (PCR) y si se habían detectado anticuerpos heterófilos (test rápido de aglutinación de partículas de látex en porta Monogen®; Biokit, Barcelona). Por último, se recogieron datos de coinfección con otros virus en aquellos casos en que se habían solicitado otras serologías.
Análisis estadísticoSe analizaron los datos mediante el programa estadístico informático de SPSS® 21.0. Se realizó un análisis descriptivo de los mismos y el análisis comparativo entre el grupo con clínica típica y el grupo con clínica no típica. Los resultados para las variables cuantitativas fueron expresados como medianas y valores de primer y tercer cuartil. Por otra parte, las variables cualitativas fueron presentadas como frecuencias y proporciones.
Las variables cualitativas fueron comparadas entre ambos grupos mediante el test de Fisher, mientras que las variables cuantitativas (que no seguían una distribución normal) lo fueron con el test de Kruskal-Wallis. Se ha considerado una diferencia estadísticamente significativa cuando el valor de p del test es menor o igual a 0,05.
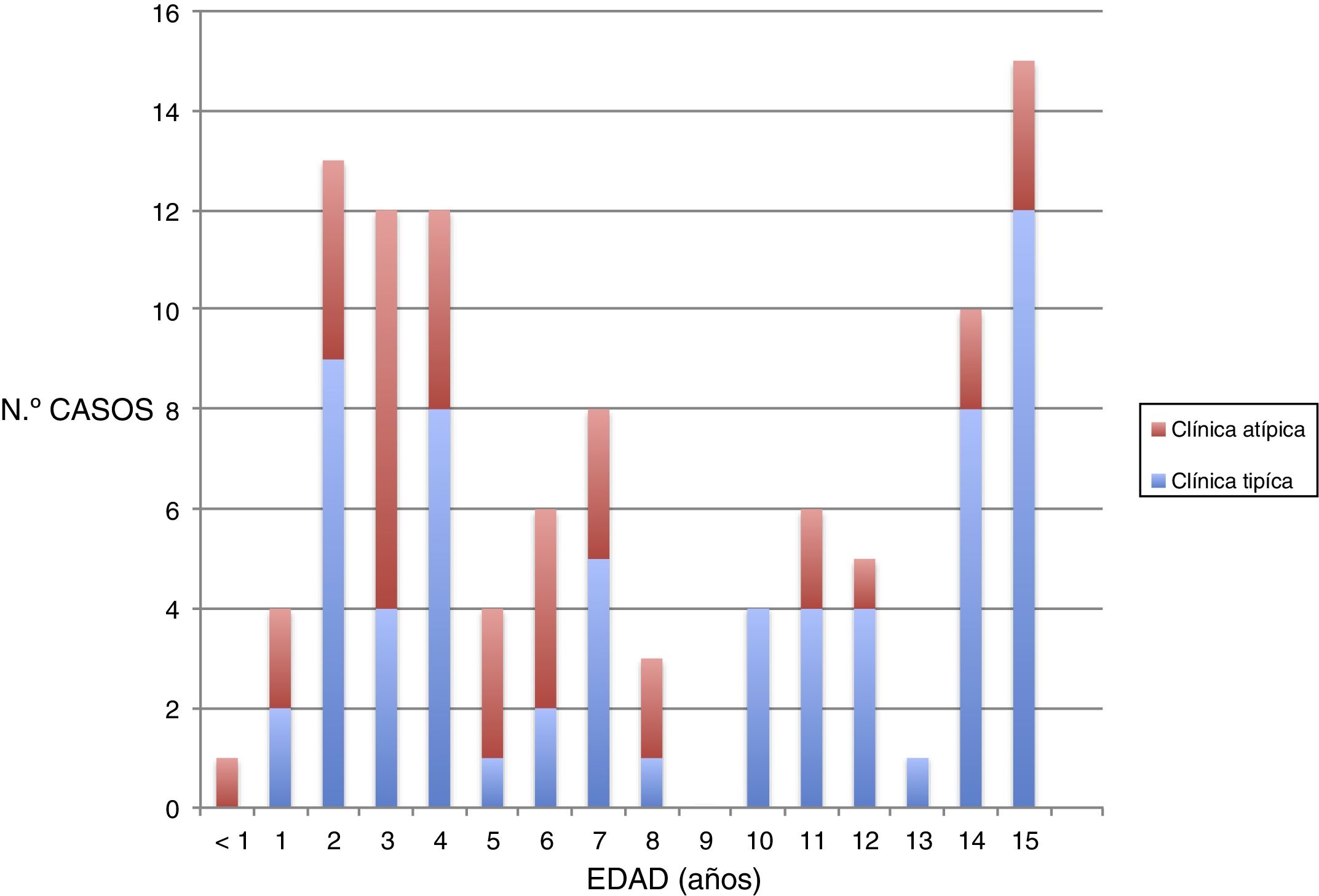
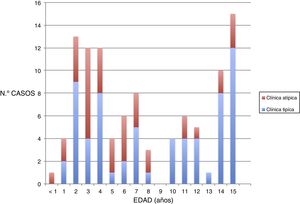
ResultadosAnálisis descriptivoSe obtuvo una muestra de 103 niños. Un 47% fueron varones y un 56%, mujeres. La mediana de la edad fue de 7 años (3-12,5). En cuanto a la distribución por edades, observamos 3 picos de mayor incidencia: a los 2-4 años, a los 7 años y en la adolescencia (14-15 años) (fig. 1).
El 62% de nuestros pacientes presentaron la primoinfección en los meses de otoño e invierno (septiembre-febrero).
En todos los casos se había solicitado la confirmación serológica por sospecha clínica de una primoinfección. Entre los diagnósticos de sospecha por los que se solicitó la serología, los más frecuentes fueron mononucleosis infecciosa (22%), adenitis (18%) y amigdalitis (11%). La serología se solicitó sobre todo desde el ambiente hospitalario (un 44% desde el Servicio de Urgencias Hospitalarias y un 34% desde la sala de hospitalización de Pediatría y el Hospital de Día de Pediatría). El 22% restante se solicitó desde Atención Primaria.
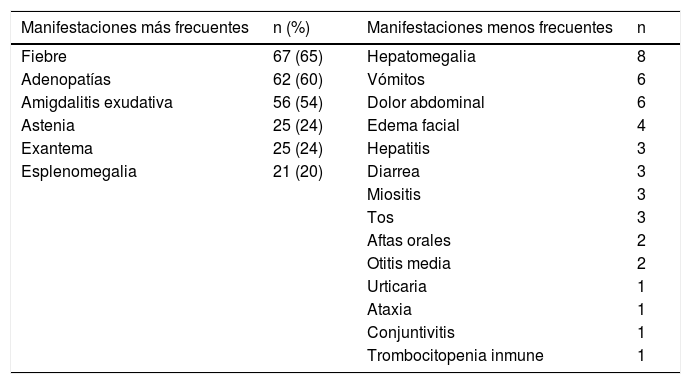
Las manifestaciones clínicas recogidas en la historia clínica se muestran en la tabla 1.
Características clínicas de la muestra (n=103)
| Manifestaciones más frecuentes | n (%) | Manifestaciones menos frecuentes | n |
|---|---|---|---|
| Fiebre | 67 (65) | Hepatomegalia | 8 |
| Adenopatías | 62 (60) | Vómitos | 6 |
| Amigdalitis exudativa | 56 (54) | Dolor abdominal | 6 |
| Astenia | 25 (24) | Edema facial | 4 |
| Exantema | 25 (24) | Hepatitis | 3 |
| Esplenomegalia | 21 (20) | Diarrea | 3 |
| Miositis | 3 | ||
| Tos | 3 | ||
| Aftas orales | 2 | ||
| Otitis media | 2 | ||
| Urticaria | 1 | ||
| Ataxia | 1 | ||
| Conjuntivitis | 1 | ||
| Trombocitopenia inmune | 1 |
Se clasificó a los pacientes según el tipo de clínica. El 63% (65 casos) presentaron una clínica típica o síndrome mononucleósico y el 37% (38 casos) una clínica no típica.
El 49% (50 casos) recibieron tratamiento antibiótico (penicilinas y derivados) en algún momento de la evolución; apareció exantema en 19 de los 50 casos (38%), mientras que solo apareció en 6 de los 53 casos (11%) que no fueron tratados con antibiótico (p=0,002).
Precisaron ingreso el 17% de los pacientes (18 casos), sin diferencias significativas en cuanto al tipo de clínica. Los principales motivos de ingreso fueron la afectación del estado general, la duración de la clínica, alteraciones analíticas (trombocitopenia, leucopenia) y la presencia de manifestaciones atípicas como miositis o ataxia.
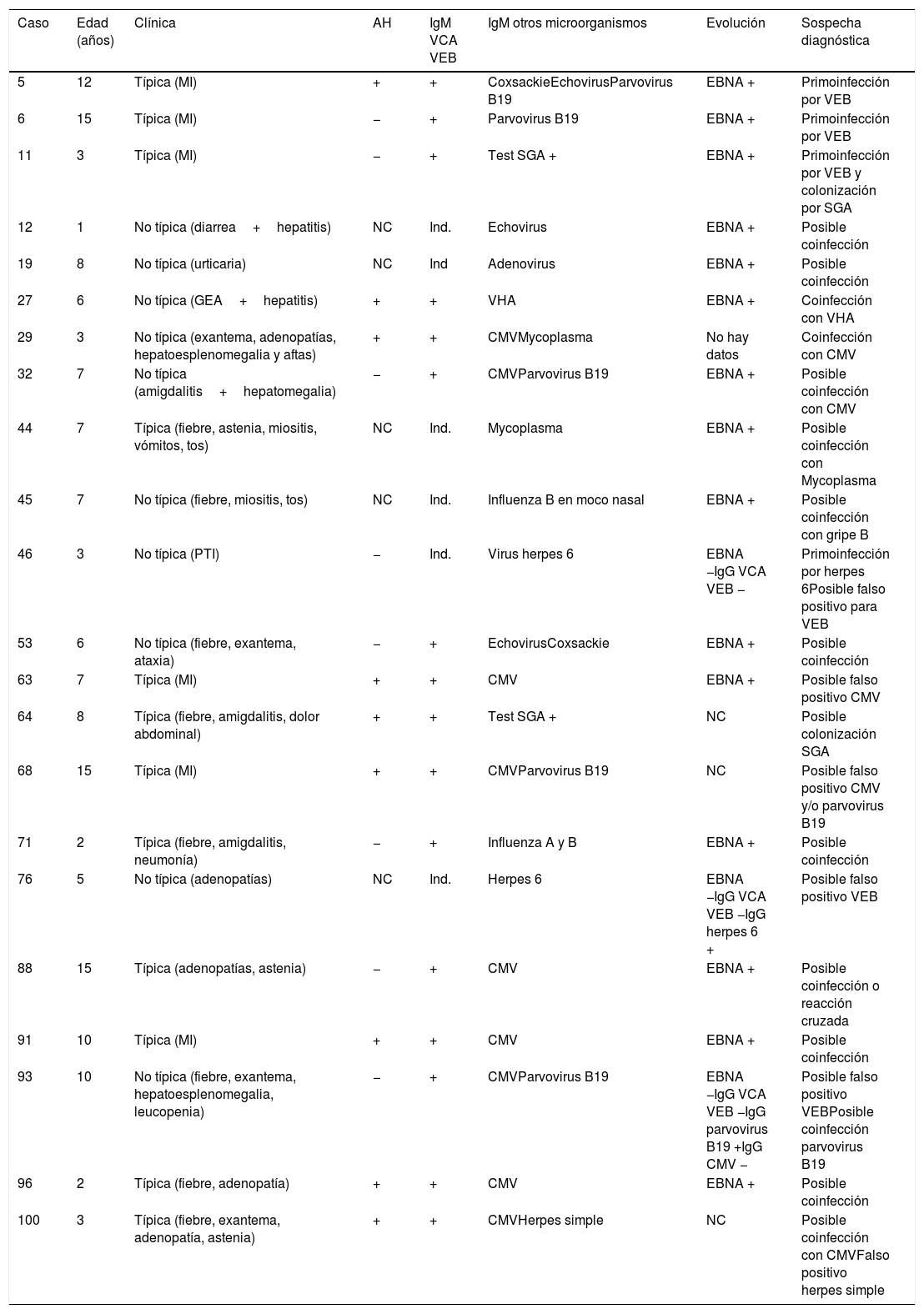
En 22 pacientes (21%) en que se habían solicitado otras serologías se encontraron IgM positivas para otros virus. Incluso en algunos pacientes se observaron más de un virus u otros microorganismos. Los más frecuentes fueron citomegalovirus (CMV) y parvovirus B19. En ninguno se solicitó la detección de ADN para otros virus. En la tabla 2 se recogen la clínica y las características serológicas de estos pacientes, así como datos de su evolución en aquellos casos en que se han podido obtener.
Pacientes con serología positiva para otros agentes infecciosos
| Caso | Edad (años) | Clínica | AH | IgM VCA VEB | IgM otros microorganismos | Evolución | Sospecha diagnóstica |
|---|---|---|---|---|---|---|---|
| 5 | 12 | Típica (MI) | + | + | CoxsackieEchovirusParvovirus B19 | EBNA + | Primoinfección por VEB |
| 6 | 15 | Típica (MI) | − | + | Parvovirus B19 | EBNA + | Primoinfección por VEB |
| 11 | 3 | Típica (MI) | − | + | Test SGA + | EBNA + | Primoinfección por VEB y colonización por SGA |
| 12 | 1 | No típica (diarrea+hepatitis) | NC | Ind. | Echovirus | EBNA + | Posible coinfección |
| 19 | 8 | No típica (urticaria) | NC | Ind | Adenovirus | EBNA + | Posible coinfección |
| 27 | 6 | No típica (GEA+hepatitis) | + | + | VHA | EBNA + | Coinfección con VHA |
| 29 | 3 | No típica (exantema, adenopatías, hepatoesplenomegalia y aftas) | + | + | CMVMycoplasma | No hay datos | Coinfección con CMV |
| 32 | 7 | No típica (amigdalitis+hepatomegalia) | − | + | CMVParvovirus B19 | EBNA + | Posible coinfección con CMV |
| 44 | 7 | Típica (fiebre, astenia, miositis, vómitos, tos) | NC | Ind. | Mycoplasma | EBNA + | Posible coinfección con Mycoplasma |
| 45 | 7 | No típica (fiebre, miositis, tos) | NC | Ind. | Influenza B en moco nasal | EBNA + | Posible coinfección con gripe B |
| 46 | 3 | No típica (PTI) | − | Ind. | Virus herpes 6 | EBNA −IgG VCA VEB − | Primoinfección por herpes 6Posible falso positivo para VEB |
| 53 | 6 | No típica (fiebre, exantema, ataxia) | − | + | EchovirusCoxsackie | EBNA + | Posible coinfección |
| 63 | 7 | Típica (MI) | + | + | CMV | EBNA + | Posible falso positivo CMV |
| 64 | 8 | Típica (fiebre, amigdalitis, dolor abdominal) | + | + | Test SGA + | NC | Posible colonización SGA |
| 68 | 15 | Típica (MI) | + | + | CMVParvovirus B19 | NC | Posible falso positivo CMV y/o parvovirus B19 |
| 71 | 2 | Típica (fiebre, amigdalitis, neumonía) | − | + | Influenza A y B | EBNA + | Posible coinfección |
| 76 | 5 | No típica (adenopatías) | NC | Ind. | Herpes 6 | EBNA −IgG VCA VEB −IgG herpes 6 + | Posible falso positivo VEB |
| 88 | 15 | Típica (adenopatías, astenia) | − | + | CMV | EBNA + | Posible coinfección o reacción cruzada |
| 91 | 10 | Típica (MI) | + | + | CMV | EBNA + | Posible coinfección |
| 93 | 10 | No típica (fiebre, exantema, hepatoesplenomegalia, leucopenia) | − | + | CMVParvovirus B19 | EBNA −IgG VCA VEB −IgG parvovirus B19 +IgG CMV − | Posible falso positivo VEBPosible coinfección parvovirus B19 |
| 96 | 2 | Típica (fiebre, adenopatía) | + | + | CMV | EBNA + | Posible coinfección |
| 100 | 3 | Típica (fiebre, exantema, adenopatía, astenia) | + | + | CMVHerpes simple | NC | Posible coinfección con CMVFalso positivo herpes simple |
AH: anticuerpos heterófilos; CMV: citomegalovirus; EBNA: IgG frente al antígeno nuclear del virus de Epstein Barr; GEA: gastroenteritis aguda; IgG VCA VEB: IgG frente a la cápside viral del virus de Epstein-Barr; IgM VCA VEB: IgM frente a la cápside viral del virus de Epstein-Barr; Ind.: indeterminado; MI: mononucleosis infecciosa; NC: no consta; PTI: púrpura trombocitopénica idiopática; SGA: Streptococcus pyogenes grupo A; VEB: virus de Epstein-Barr.
En cuanto a los parámetros analíticos (tabla 4), un paciente tuvo leucopenia (<2×109/L) y otro trombocitopenia grave (2×109/L). Este último se diagnosticó de púrpura trombocitopénica idiopática y presentó coinfección por el virus herpes simple tipo 6. Recibió tratamiento con inmunoglobulinas intravenosas. El valor máximo de la PCR fue de 121,5mg/L, sin evidencia de sobreinfección bacteriana mediante cultivos.
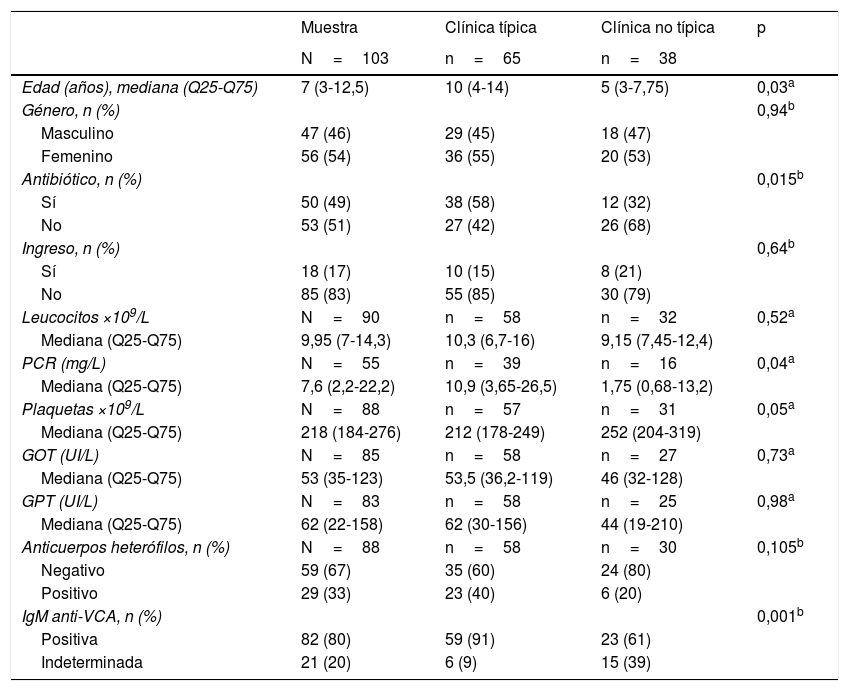
Características clínicas y analíticas según el tipo de clínica en la primoinfección
| Muestra | Clínica típica | Clínica no típica | p | |
|---|---|---|---|---|
| N=103 | n=65 | n=38 | ||
| Edad (años), mediana (Q25-Q75) | 7 (3-12,5) | 10 (4-14) | 5 (3-7,75) | 0,03a |
| Género, n (%) | 0,94b | |||
| Masculino | 47 (46) | 29 (45) | 18 (47) | |
| Femenino | 56 (54) | 36 (55) | 20 (53) | |
| Antibiótico, n (%) | 0,015b | |||
| Sí | 50 (49) | 38 (58) | 12 (32) | |
| No | 53 (51) | 27 (42) | 26 (68) | |
| Ingreso, n (%) | 0,64b | |||
| Sí | 18 (17) | 10 (15) | 8 (21) | |
| No | 85 (83) | 55 (85) | 30 (79) | |
| Leucocitos ×109/L | N=90 | n=58 | n=32 | 0,52a |
| Mediana (Q25-Q75) | 9,95 (7-14,3) | 10,3 (6,7-16) | 9,15 (7,45-12,4) | |
| PCR (mg/L) | N=55 | n=39 | n=16 | 0,04a |
| Mediana (Q25-Q75) | 7,6 (2,2-22,2) | 10,9 (3,65-26,5) | 1,75 (0,68-13,2) | |
| Plaquetas ×109/L | N=88 | n=57 | n=31 | 0,05a |
| Mediana (Q25-Q75) | 218 (184-276) | 212 (178-249) | 252 (204-319) | |
| GOT (UI/L) | N=85 | n=58 | n=27 | 0,73a |
| Mediana (Q25-Q75) | 53 (35-123) | 53,5 (36,2-119) | 46 (32-128) | |
| GPT (UI/L) | N=83 | n=58 | n=25 | 0,98a |
| Mediana (Q25-Q75) | 62 (22-158) | 62 (30-156) | 44 (19-210) | |
| Anticuerpos heterófilos, n (%) | N=88 | n=58 | n=30 | 0,105b |
| Negativo | 59 (67) | 35 (60) | 24 (80) | |
| Positivo | 29 (33) | 23 (40) | 6 (20) | |
| IgM anti-VCA, n (%) | 0,001b | |||
| Positiva | 82 (80) | 59 (91) | 23 (61) | |
| Indeterminada | 21 (20) | 6 (9) | 15 (39) |
PCR: proteína C reactiva; IgM anti-VCA: IgM frente a la cápside viral.
Presentaron hipertransaminasemia el 51% de los pacientes (42 casos), con un valor máximo de GOT de 2.236UI/ml y un valor máximo de GPT de 3.347UI/ml. Únicamente 3 de estos pacientes tuvieron síntomas de hepatitis aguda (ictericia, vómitos, dolor abdominal), observándose en 2 de ellos coinfección con Echovirus (caso 12) y hepatitis A (caso 27).
En 88 niños se solicitaron en el momento del diagnóstico los anticuerpos heterófilos, que fueron positivos en 29 casos (33%).
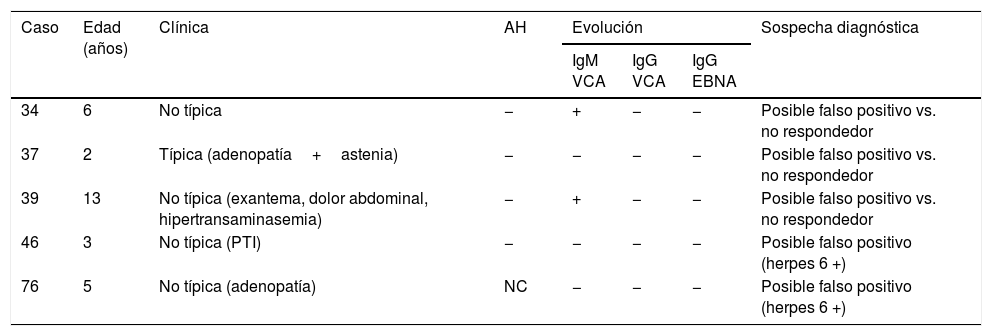
En lo referente a la serología, un 20% de los pacientes (21 casos) tuvo una IgM indeterminada en el momento de la primoinfección. De ellos, 7 pertenecían al grupo de clínica típica, pero solo 2 pacientes tuvieron un cuadro de mononucleosis infecciosa; el resto fueron oligosintomáticos (2 síntomas). Los otros 14 se clasificaron en el grupo de clínica no típica, 7 tuvieron manifestaciones atípicas (hepatitis, urticaria, aftas, miositis y trombocitopenia) y los otros 7 fueron oligosintomáticos (un síntoma). En 5 casos no se detectaron anticuerpos heterófilos y las IgG VCA VEB y los anticuerpos IgG del antígeno nuclear del VEB fueron negativos en controles posteriores (tabla 3).
Pacientes con IgM frente a la cápside viral indeterminada en el momento de la primoinfección y ausencia de seroconversión posterior
| Caso | Edad (años) | Clínica | AH | Evolución | Sospecha diagnóstica | ||
|---|---|---|---|---|---|---|---|
| IgM VCA | IgG VCA | IgG EBNA | |||||
| 34 | 6 | No típica | − | + | − | − | Posible falso positivo vs. no respondedor |
| 37 | 2 | Típica (adenopatía+astenia) | − | − | − | − | Posible falso positivo vs. no respondedor |
| 39 | 13 | No típica (exantema, dolor abdominal, hipertransaminasemia) | − | + | − | − | Posible falso positivo vs. no respondedor |
| 46 | 3 | No típica (PTI) | − | − | − | − | Posible falso positivo (herpes 6 +) |
| 76 | 5 | No típica (adenopatía) | NC | − | − | − | Posible falso positivo (herpes 6 +) |
AH: anticuerpos heterófilos; IgG EBNA: IgG frente al antígeno nuclear del virus de Epstein-Barr; IgG VCA: IgG frente a la cápside viral del virus de Epstein-Barr; IgM VCA: IgM frente a la cápside viral del virus de Epstein-Barr; NC: no constan; PTI: púrpura trombocitopénica idiopática.
Se analizaron las variables según el tipo de clínica. En el grupo de clínica no típica la edad de los pacientes fue menor (p=0,03) (fig. 1).
En el grupo de clínica típica los pacientes recibieron más tratamiento antibiótico (p=0,015). La PCR estaba discretamente más elevada en este grupo (p=0,04), sin diferencias estadísticamente significativas en el resto de los parámetros analíticos. La IgM VCA positiva al diagnóstico fue más frecuente en el grupo con clínica típica y la IgM VCA indeterminada, en el grupo de clínica no típica (p=0,001) (tabla 4).
DiscusiónEn nuestros pacientes observamos 2 picos de incidencia de primoinfección por VEB antes de la adolescencia: entre los 2-4 años y a los 7 años. Tradicionalmente en la literatura se describe un mayor número de casos en la adolescencia2. En nuestra muestra hasta un 64% de los pacientes diagnosticados serológicamente de primoinfección por VEB fueron menores de 10 años, probablemente debido a que en niños de mayor edad se trata de un cuadro clínico más florido y en muchas ocasiones se realiza un diagnóstico clínico y no se solicita confirmación analítica como en nuestro estudio14–16.
A pesar de una mayor prevalencia de niños menores, en nuestro estudio predomina la clínica típica (65 casos). Dentro del grupo de los pacientes con clínica típica, 13 niños presentaban solo 2 síntomas y 52 niños, más de 2 síntomas. No obstante, en muchos casos el tercer síntoma pertenecía a la variable «otros síntomas», donde se incluyen manifestaciones clínicas que no forman parte estrictamente del síndrome mononucleósico. Esta forma de clasificar la clínica puede haber sobreestimado la presencia de clínica típica en nuestra muestra.
Las manifestaciones clínicas más frecuentes en el momento de la primoinfección por VEB fueron fiebre, adenopatías cervicales y amigdalitis exudativa, al igual que en la mayoría de las series publicadas3,13–15,17, pero con unos porcentajes diferentes. Probablemente estas diferencias sean debidas a que nuestros casos no son exclusivamente niños hospitalizados, a diferencia de la mayoría de los estudios referidos.
Nos parece interesante que en un 22% se detectara coinfección con otros virus. En algunos de estos casos es difícil interpretar el agente etiológico solo por las manifestaciones clínicas. Al revisar la evolución de estos niños, hemos interpretado que los casos en los que se ha solicitado un control y se han obtenido IgG del antígeno nuclear VEB positivos han podido tratarse de coinfecciones además de haber tenido una primoinfección por el VEB, aunque no podemos asegurarlo con los datos de que disponemos. Los casos con clínica típica y con presencia de anticuerpos heterófilos podrían ser coinfecciones con más seguridad. Existen pocas referencias sobre coinfecciones con otros virus, aunque sí que se han publicado casos de serologías doblemente positivas para VEB y CMV13,18. Se han descrito 2 casos de trombocitopenia grave con coinfección por herpes simple tipo 6 y CMV18,19, al igual que nuestro paciente 46.
Los casos 46, 76 y 93 se han interpretado como posibles falsos positivos para el VEB, aunque no podemos confirmarlo, pues no se obtuvo en el momento de la primoinfección determinación de DNA del VEB y algunas personas pueden no generar respuesta serológica tras la primoinfección.
Los casos con IgM anti-VCA indeterminada son también de difícil interpretación, sobre todo cuando no se asocian con una clínica típica. De los pacientes en los que hemos obtenido datos de su evolución posterior, 5 no han realizado seroconversión (tabla 3). Los casos 46 y 76 tuvieron IgM positiva para otros virus herpes (tipo 6), con lo que teniendo en cuenta la clínica y que los anticuerpos heterófilos fueron negativos, interpretamos que fueron más probablemente falsos positivos para el VEB. En cambio, en los casos 34 y 39, la IgM VCA fue posteriormente positiva, y no disponemos de otros datos de coinfección, por lo que no podemos saber si han sido falsos positivos para el VEB o niños que no han generado memoria frente al virus. Ninguno presentó complicaciones clínicas ni ningún dato que hiciera sospechar una inmunodeficiencia de base en ese momento, aunque el paciente 39 había tenido el antecedente de una leucemia linfoblástica 6 años antes, actualmente en remisión y sin tratamiento. Es importante no descartar el diagnóstico de primoinfección ante una IgM indeterminada, ya que podría tratarse de una fase precoz de la infección. Además, es interesante en los casos de IgM VCA indeterminada descartar coinfección por otros virus herpes y realizar un control posterior para ver la evolución serológica.
El porcentaje de anticuerpos heterófilos positivos (33%) ha sido más bajo en ambas formas de presentación clínica respecto a lo descrito en la literatura. Autores como Sumaya y Ench encuentran una prevalencia de anticuerpos heterófilos de hasta un 83% en niños mayores de 4 años; en cambio, esta cifra disminuye a 50% en niños de 2 y 3 años de edad4,6. Otros autores europeos describen una prevalencia algo menor (42%), además de encontrar que son frecuentemente negativos en la fase precoz y en la fase tardía de la primoinfección20. Revisiones posteriores, en cambio, refieren una positividad del 25-50% en niños menores de 12 años21, más acorde con la prevalencia en nuestra serie. No todas las técnicas para detectar los anticuerpos heterófilos tienen la misma sensibilidad y especificidad22. El test utilizado en nuestro laboratorio tiene una sensibilidad del 76% y una especificidad del 98% según el fabricante (Monolatex Biokit). La baja producción de anticuerpos heterófilos en nuestros pacientes podría deberse a que un 64% de ellos eran menores de 10 años. Otra posible explicación es que se hubieran solicitado en una fase precoz de la primoinfección, o en una fase tardía, sobre todo en el caso del 22% de las serologías que se solicitaron desde Atención Primaria. Otros autores españoles también encuentran una prevalencia baja (32%) de anticuerpos heterófilos en mayores de 4 años, sin encontrar una explicación razonable13.
Los pacientes con formas oligosintomáticas suelen ser de menor edad, tal y como se describe en la literatura1–3. En el resto de las características epidemiológicas y analíticas no hemos encontrado diferencias importantes en ambos grupos, aunque en algunas variables el tamaño muestral era pequeño. No hemos encontrado estudios descriptivos sobre las diferentes formas clínicas de primoinfección. La mayoría de los estudios se han realizado en pacientes ingresados y con clínica de mononucleosis infecciosa13,14,17.
Nuestro estudio posee las limitaciones propias de un análisis retrospectivo, sin disponer de datos del seguimiento, que podrían ayudar a la interpretación de algunos casos. Somos conscientes del posible sesgo, al no poder incluir a toda la población con primoinfección por VEB, ya que solo incluimos a los que han presentado algún síntoma y se les ha solicitado confirmación serológica. Además, en el grupo de clínica no típica se incluyen pacientes que potencialmente pueden tener un comportamiento distinto. Por un lado, pacientes oligosintomáticos, generalmente de menor edad y en los que es esperable un comportamiento benigno de la infección. Por otro lado, pacientes con manifestaciones atípicas, en los que no podemos descartar que esta forma de presentación se deba a algún trastorno en su respuesta inmune. A pesar de ello, ninguno de los pacientes con manifestaciones atípicas presentó ninguna complicación y el cuadro evolucionó favorablemente.
Por otra parte, hemos conseguido excluir el sesgo que se obtendría si la muestra fuera solo de pacientes hospitalizados y hemos analizado formas oligosintomáticas y atípicas.
ConclusionesEs común en nuestra población que la primoinfección por VEB afecte a niños de menor edad, predominando en ellos las formas oligosintomáticas. El porcentaje de anticuerpos heterófilos positivos ha sido muy bajo en nuestra muestra en ambas formas de presentación clínica, con tendencia a ser más frecuentes en las formas típicas. Los casos con IgM anti-VCA indeterminada son más frecuentes en el grupo de clínica no típica, tanto en casos oligosintomáticos como en aquellos con manifestaciones atípicas.
Es habitual detectar coinfección con otros virus, sobre todo CMV y parvovirus B19; en estos casos es recomendable descartar que se trate de un falso positivo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
62 Congreso extraordinario de la AEP, Madrid, junio de 2014. Comunicación formato póster: «Evolución serológica de la primoinfección por VEB en niños sanos». XXXI Reunión de la Sociedad Valenciana de Pediatría, junio de 2015. Comunicación oral: «Primoinfección sintomática por el VEB: más frecuente de lo que parece».