En 1965 Lilly y Stillwell fueron los primeros en citar el término probiótico1 para describir cualquier sustancia u organismo que contribuyera a mantener el equilibrio intestinal en los animales. Según estos autores, serían sustancias segregadas por un microorganismo las que estimulan el crecimiento de otro. Posteriormente, en 1989, Fuller2 los consideró como un suplemento alimentario microbiano vivo que beneficia al huésped animal con una mejoría del balance microbiano intestinal. Como tantas del léxico científico, la palabra probiótico deriva del griego "pro-vida", es decir "a favor de la vida", en oposición al término antibiótico puesto a la luz previamente y que significa "contra la vida". Anteriormente, en 1908, el premio Nobel ruso Iliá Mechnikov sugirió que la ingesta de yogur con lactobacilos disminuía el número de bacterias que producen toxinas en el intestino y contribuía a la longevidad de los campesinos búlgaros. La definición actual más completa, siguiendo a Teitelbaum y Walker3, sería la de una preparación o producto que contiene microorganismos viables definidos, en cantidad suficiente para alterar la microflora (por implantación o colonización) en el intestino ejerciendo efectos beneficiosos en el huésped.
Los criterios para que los microorganismos sean considerados como probióticos, siguiendo a Teitelbaum, se podrían enunciar como:
Ser de origen humano.
No ser patogénicos por naturaleza.
Ser resistentes a la destrucción por procedimientos tecnológicos.
Ser resistentes a la destrucción por las secreciones gástricas y por la bilis.
Poder adherirse al epitelio intestinal.
Ser capaces de colonizar el tracto gastrointestinal, incluso por cortos períodos.
Producir sustancias antimicrobianas.
Modular las respuestas inmunitarias.
Ejercer una influencia en algunas actividades metabólicas humanas, como la asimilación del colesterol, producción de vitaminas, etc.
Las cepas más comúnmente usadas como probióticos son:
1. L. acidophilus, L. bulgaricus, L. reuterii, L. plantarum, L. casei GG (LGG).
Se seleccionó originalmente LGG por su resistencia a los jugos gástricos y a la digestión biliar, así como por su capacidad de colonizar el colon humano. No posee plásmidos, así que tiene una resistencia estable ante los antibióticos. Produce solamente ácido láctico (no el isómero D). En su membrana expresa factores adhesivos que permiten su interacción con los enterocitos humanos. L. acidophilus también se puede unir a enterocitos de una forma independiente del calcio. Se cree que la adhesión tiene lugar mediante un componente proteínico extracelular. Además, inhibe otras bacterias anaeróbicas in vitro, como Clostridium, bacteroides, bifidobacterias, pseudomonas, estafilococos, estreptococos y enterobacterias. También inhibe bacterias francamente patogénicas, como Yersinia enterocolitica, Bacillus cereus, Escherichia coli, Listeria monocytogenes y Salmonella. Estos efectos duran tan sólo mientras se consumen; en un estudio se demostró que en un 67% de voluntarios desaparecieron de las heces en 7 días.
2. Bifidobacterias como Bifidobacterium breve, B. lonmgum, B. infantis, B. animalis. Constituyen el grupo más importante de bacterias sacarolíticas del intestino grueso, hasta un 25% en el colon del adulto, y hasta un 95% del recién nacido con leche materna. No forman aminas alifáticas, derivados sulfurosos ni nitritos, producen vitaminas, sobre todo del grupo B, así como enzimas digestivas; su metabolismo produce ácidos grasos de cadena corta (AGCC), como acetato y lactato, que disminuyen el pH intestinal con efectos antibacterianos. Además, estos AGCC son un combustible excelente para el colonocito, e intervienen en el metabolismo hepático. Un 30% de B. bifidum ingeridos se pueden recuperar en las heces3.
3. Streptococcus salivarius spp. Thermophilus, usados normalmente en la obtención, junto con L. bulgaricus de los yogures de consumo diario. También se usan L. casei, L. paracasei y L. rhamnosus.
4. El hongo Saccharomyces boulardii, con efectos probióticos probados y muy usado en España (Ultralevura®), se ha demostrado que inhibe el crecimiento de bacterias patógenas tanto in vitro como in vivo; la temperatura óptima para su desarrollo es de 37 ºC y se ha demostrado que es resistente a la digestión por los jugos gástricos y biliares alcanzando indemne el colon; por tratarse de un hongo y no de una bacteria, no se ve afectado por el uso concomitante de antibióticos. Una vez retirada su administración es rápidamente eliminado. El uso en recién nacidos con procesos que originen una malnutrición ha de ser prudente. En el 2000 publicamos un caso de fungemia por S. cerevisiae, en dos recién nacidos, uno de ellos tratado con Saccharomyces4.
5. Otro probiótico sería el kefir, que no ha encontrado padrino que estudie y demuestre sus efectos beneficiosos. Considerado como un regalo que hizo Mahoma a los primeros conversos del Cáucaso, sólo se ha podido demostrar que inhibe el crecimiento de Salmonella.
Mecanismos de acción
1. Uno de los mecanismos de acción es la inducción de un pH ácido por debajo de 4:
- En parte por la producción de AGCC, como acetatos, butiratos, etc. Estos AGCC pueden llegar a unas concentraciones que impidan el crecimiento de gérmenes. El pH ácido favorece el crecimiento de las bacterias tolerantes del ácido.
Algunos prebióticos, como los lactobacilos, generan peróxido de hidrógeno, que reduce el pH luminal y el potencial redox, y produce bactericinas que inhiben el crecimiento de las bacterias patógenas y, en ocasiones, mediante la presión baja de oxígeno favorecen el crecimiento de anaerobios.
Otros actúan produciendo gran cantidad de ácido láctico5, como L. salivarius, que ha demostrado su utilidad en el tratamiento de la infección por Helicobacter pylori y en la reducción de la inflamación de la mucosa gástrica.
2. Restablecimiento de la flora normal tras una gastroenteritis aguda, que disminuye la permeabilidad intestinal y potencia el efecto barrera inmunológico6,7.
3. Los lactobacilos y bifidobacterias promueven la maduración del intestino y su integridad, y son antagónicos de patógenos y contribuyen a la modulación de la inmunidad intestinal8. La administración continuada de L. casei induce a una menor proliferación de bacterias aeróbicas gramnegativas, con mayor recuperación de lactobacilos en heces9.
4. Disminuyen la intolerancia a la lactosa10 e incrementan la actividad lactásica intestinal, con la mejora del trofismo del intestino11,12.
5. Ejercen influencia en la transferencia de plásmidos y en el establecimiento de transconjugados en el intestino13.
6. Poseen la capacidad de adherirse a enterocitos y colonocitos y afectan a la composición del ecosistema intestinal, incrementando el efecto barrera no dependiente del sistema inmunológico. En ocasiones compiten con diversos patógenos en su adhesión al epitelio por medio de ciertos determinantes adhesivos14.
7. Los probióticos ejercen un efecto competitivo con otras bacterias, ocupando sus lugares de nidación e inhibiendo el crecimiento de especies de enteropatógenos.
8. Acortan el tiempo de excreción de rotavirus, según demostró Guarino et al15 en 100 niños afectados por rotavirus.
9. Poseen la capacidad de aumentar la expresión de las mucinas ileocolónicas MUC2 y MUC3, coadyuvando al recubrimiento del intestino de una capa de moco, mecanismo inespecífico, pero muy eficaz de la lucha antibacteriana.
10. Los lactobacilos y las bifidobacterias pueden segregar antibióticos naturales con amplio espectro de actividad, como las lactocinas, las helveticinas, las curvacinas, las nicinas y las bifidocinas. De esta forma acortan la duración de la diarrea, pero en estudios recientes se ha demostrado que para ser realmente efectivos primero han de haber colonizado16, por lo que sus efectos no se notarán hasta 2-3 días después de su administración.
11. Pueden competir con nutrientes de la flora intestinal patógena.
12. Dificultan la traslocación bacteriana, por lo que podrán ser útiles en pacientes que reciben alimentación parenteral.
13. Acción en el sistema inmunitario. El sistema inmunitario consiste en diferentes órganos, linfáticos, intestino, bazo, médula ósea, etc., así como en diferentes tipos celulares. Las interacciones antigénicas entre esas células inducen a una respuesta celular inmunitaria mediada por células activadas y a una respuesta humoral mediada por anticuerpos. Las interacciones celulares están aumentadas por moléculas "de adhesión" y las células activadas liberan diferentes citocinas. Estas complejas interacciones celulares conducen a la respuesta inmunitaria sistémica. Si el antígeno penetra por vía oral, se obtiene sobre todo una respuesta inmunitaria secretora mediada por la inmunoglobulina (Ig) A secretora (IgA S). La determinación del número de células B o T, la determinación cualitativa o cuantitativa de las citocinas, el nivel de anticuerpos o el estudio de la función celular, tal como la actividad fagocítica, son usadas para evaluar el estado de la respuesta inmunitaria17. Las bacterias probióticas productoras de ácido láctico y, en general, todas las probióticas, tienen unos mecanismos de acción que pueden influir y modular todas esas respuestas inmunitarias, en parte mediadas por el tejido linfoide asociado al intestino (gut associated lymphoid tissue [GALT]).
Con el empleo de probióticos se ha demostrado:
Por parte de los linfocitos, la producción de gama interferón gamma (IFN)
Por parte de los macrófagos peritoneales, la producción de IFN-α.
Se ha podido demostrar un estímulo de las células T helper (Th) 1, productoras de citocinas y causantes de la inmunidad celular. Pueden modificar las relaciones entre las Th1 y las Th2 y así influir en el pronóstico y la evolución de las alergias.
El marcaje del sistema inmunitario mediante patrones de reconocimiento innatos de la superficie celular o también a través de la activación directa de las células linfoideas. En algunas ocasiones estas acciones son suficientes para modular las respuestas inmunitarias in vivo tanto en el ámbito local como sistémico18.
El estímulo de la inmunidad secretora, con el aumento de la producción de IgA S mediante interacciones complejas entre los diferentes constituyentes del ecosistema intestinal, como la microflora, las células epiteliales y las células inmunes. Mediante diferentes mecanismos los probióticos envían señales que activan estas células inmunes. Este aumento de la IgA S es interesante en la defensa contra infecciones de cualquier etiología; sabemos que la IgA S es un dímero que se une al antígeno e impide su interacción con la célula epitelial.
Perdigon et al17 demostraron que ciertas bacterias productoras de ácido láctico eran capaces de inducir una inmunidad secretora específica, mientras que otras aumentaban la respuesta inflamatoria inmune del intestino. La administración oral de esas bacterias (L. casei, L. delbrueckii spp., L. bulgaricus, L. acidophilus, L. plantarum, L. rhamnosus, Lactococcus lactis y Streptococcus salivarius spp. thermophilus) inducía a un aumento de las celulas B IgA+, además de inducir a la IgA a interaccionar con las células M de las placas de Peyer. En otras ocasiones también podían estimular las células IgM+.
También demostró un aumento de los linfocitos CD4, lo que indica aún más una interacción con las placas de Peyer y un incremento de la migración de las células T y B.
Este incremento de la IgA S en los primeros meses de vida es particularmente interesante, ya que en esta época de la vida la IgA S está baja y los anticuerpos específicos contra la mayoría de virus y bacterias no existen19,20, aunque sí que se posee la capacidad para producirlos.
Con un adecuado conocimiento de la microflora intestinal normal, y de las complejas interacciones de estas bacterias productoras de ácido láctico, se puede afinar el estudio y la selección de una cepa determinada de probióticos con propiedades inmunoestimulantes, y como vectores de vacunas orales21, en parte por su carácter de antígenos bacterianos.
Mediante estos efectos relacionados con los probióticos22 que estimulan los mecanismos protectores del sistema inmunitario, especialmente en trabajos realizados con Bifidobacterium lactis HN019, se ha reducido la gravedad de la diarrea producida por E. coli y rotavirus. También otros probióticos contribuyen a la curación tras gastroenteritis agudas virales en niños y lactantes23.
La modulación de la inmunidad basada en la producción de ácido láctico y en el estímulo de la inmunidad se ha estudiado con B. adolescentis y Bacteroides thetaiotaomicron en ratas gnotobióticas; B. adolescentis es una bacteria grampositiva productora de ácido láctico al que se le atribuyen propiedades probióticas; B. thetaiotaomicron es un bastón gramnegativo autóctono del intestino del hombre y de la rata. En el trabajo de Scharek et al24 se realizó un seguimiento de la colonización del intestino mediante contajes bacterianos en las heces. Para valorar los efectos en la inmunidad de B. adolescentis, estos autores dosificaron en suero los anticuerpos IgG e IgA contra ambas especies bacterianas. También se valoró la reacción inmune intestinal con la medición de la IgA específica en heces de las ratas. Se pudo comprobar que B. adolescentis inducía una reacción mucosa inmune, mientras que B. thetaiotaomicron agredía la mucosa, así como el sistema inmunitario. Posteriormente B. adolescentis fue capaz de suprimir la reacción inmune sistémica y mucosa contra el autóctono B. thetaiotaomicron.
14. El mecanismo de acción de los probióticos también se ha estudiado en niños afectados del virus de la inmunodeficiencia humana (VIH), que aquejan de frecuentes episodios de diarrea y malabsorción25. Con la administración de Lactobacillus plantarum 299v se consiguió colonizar el intestino de niños con VIH y desencadenar una respuesta sistémica inmunitaria.
15. También se ha demostrado su acción en la protección contra candidiasis orales sujetas a inmunodeficiencias graves, pero usando lactobacilos acidófilos y L. casei inactivados mediante tratamiento térmico, lo cual induce a pensar26 que el mecanismo de acción está en parte vinculado a componentes antigénicos no desnaturalizados por el calor.
16. Mecanismo de acción sobre la alergia. Matzusaki et al han demostrado una mejoría de la evolución y predisposición alérgica tras la administración de L. casei cepa Shirota en ratones BALBC/c preinyectados con ovoalbúmina intraperitonealmente, comparado con un grupo control no suplementado con L. casei27-29. Así consiguió inhibir la producción de IgE. Otros autores30 han podido comprobar esta inhibición. Este efecto puede tener interesantes repercusiones en el tratamiento de la alergia.
Este mecanismo se puede entender mejor al observar la figura 1. Las células T CD4 activadas originan las Th1 y las Th2. Las Th1 son las predominantes en el individuo sano, y las Th2 son las que predominan en el alérgico. En parte hay un equilibrio entre ambas, de modo que cuando aumentan las Th1, disminuyen las Th2, y viceversa. Las Th1 inducen la producción de IFN-γ, interleucina (IL) 2, 3, factor estimulantes de granulocitos macrófagos, es decir las Th1 son las causantes de mantener la inmunidad celular. Las Th2 inducen la formación de IL-4, IL-13, IL-5; esta última favorece la diferenciación de los eosinófilos, es decir las Th2 son la causa de la producción de IgE, o sea las causantes de la alergia; así podemos entender en parte el aumento de los procesos alérgicos que estamos viviendo en la actualidad. El exceso de higiene y el excesivo uso de antibióticos inducen a una baja producción de Th1, y por ello se dispara la producción de Th2, lo que conlleva cifras más altas de IgE con aumento de los procesos alérgicos. Antes de la era antibiótica, junto con las peores condiciones higiénicas, la cifra de Th1 superaba generalmente la cifra de Th2, lo que justificaba la baja incidencia de alergia en el pasado. Por ello una solución es la que propone Matsuzaki y los otros autores citados: administrar "suciedad limpia", bacterias inofensivas, engañosas como son los probióticos, como L. casei, para inducir un aumento de las Th1 en detrimento de las Th2 (fig. 2). Otro modo de inducir menor producción de IgE sería la administración de LGG que producen el transforming growth factor beta 2, que bloquea la formación de IgE. En nuestra unidad hemos conseguido la reducción del tiempo de evolución de la alergia en una serie de lactantes afectados de alergia a las proteínas de la leche de vaca con la administración de L. reuterii, comparados con otros lactantes alérgicos a las mismas proteínas con semejantes niveles de partida de anticuerpos IgE específicos contra las proteínas de leche de vaca.
Figura 1. Activación de CD4 en T helper (Th) 1 y Th2. IFN: interferón; IL: interleucina; Ig: inmunoglobulina; GM-CSF: factor estimulante de colonias de granulocitos macrófagos.
Figura 2. Aumento de producción de T helper (Th) 1 inducida por la administración de Lactobacillus casei; bloqueo de la formación de inmunoglobulina (Ig) E por la acción del transforming growth factor beta 2 (TGF-β2).
17. Mecanismos de acción en el metabolismo del colesterol. Se ha citado que el pueblo massai de África consume grandes cantidades de carne, sangre y leche, y presenta una baja incidencia de enfermedad cardiovascular, a pesar de esta dieta aterogénica. La ingesta de leche en estos pueblos se acompaña de la ingesta de prebióticos, lo que podría justificar la baja incidencia de enfermedad cardiovascular. Estudios en ratas y humanos han demostrado que cuando se toma grandes cantidades de yogur o leche con probióticos (bifidobacterias) los niveles de colesterol y de las lipoproteínas de baja densidad descienden hasta un 31%.
Uno de los mecanismos propuestos que puede influir en el descenso del colesterol al ingerir probióticos es la disminución de la actividad de la betahidroximetil glutaril-CoA hepática.
También propician el aumento de ácidos biliares en heces, lo que indica que inducen una conversión aumentada de colesterol a ácidos biliares, segundo mecanismo que justifica el descenso de colesterol.
Un tercer mecanismo estaría mediado por el estímulo en la formación de AGCC propionatos y butiratos que inducen en el intestino grueso. Estos ácidos grasos se absorben y pasan a la sangre. El acetato aumenta los niveles de colesterol en sangre y disminuye los valores de ácidos grasos, mientras que el propionato aumenta los niveles de glucosa en sangre y disminuye la respuesta hipercolesterolémica del acetato.
Un último mecanismo por el que pueden descender los niveles de colesterol es por la rápida hidrólisis de ácidos biliares que inducen, lo que conduce a una conversión más rápida de colesterol a ácidos biliares y a un mayor descenso de los niveles de colesterol.
18. Mecanismos de acción sobre la prevención del cáncer. Hay estudios que han demostrado una relación inversa entre la aparición de cáncer de mama en Francia y los Países Bajos con el consumo de probióticos. En pacientes de bajo riesgo se ha hallado un mayor número de lactobacillus y Eubacterium aerofaciens en heces.
El cáncer de colon se presenta como etapa final de una serie de episodios en parte dirigidos géneticamente. Morfológicamente los cambios tempranos se inician como una hiperproliferación de células en el interior de las criptas del colon llamadas "criptas aberrantes", consideradas como estructuras preneoplásicas. Un pequeño número de ellas evolucionarán a pólipos y posteriormente a tumores. Se ha podido demostrar que con la administración de leche fermentada se ha conseguido una reducción de hasta el 50% del número de criptas aberrantes en ratones tratados con sustancias oncogénicas.
Por otra parte, en 1998, Reddy describió la disminución de marcadores tumorales de proliferación celular en ratas (el índice de etiquetaje colónico, la actividad de la ornitindescarboxilasa y la actividad oncogénica del ras-p21) a las que se administró B. longum.
Los mecanismos por los que se ejerce esta acción antioncogénica no están claros. Se ha especulado con que los lactobacilos se pueden unir a compuestos mutagénicos. Otra teoría sería la de que las "malas bacterias" pueden convertir los procarcinógenos en carcinógenos mediante varias enzimas, acción que por competición inhibirían las "buenas bacterias" y se formarían menos subproductos nocivos. Así se ha demostrado que el LGG disminuye la betaglucoronidasa fecal, la nitrorreductasa y la colilglicina hidrolasa, todos ellos agentes procancerígenos. L. casei cepa shirota tiene efectos poderosos antitumorales y antimetastásicos en células tumorales trasplantables de roedores por un mecanismo vinculado a la supresión de la carcinogénesis inducida químicamente31. Igualmente L. casei es un poderoso estimulante de la granulopoyesis en el bazo y la médula ósea, según los trabajos realizados en ratones irradiados. Esa misma cepa por un mecanismo de modificación de las respuestas inmunitarias humorales y celulares impide el desarrollo de la artritis colágena de tipo II32. También se ha especulado con que los probióticos desactivan los carcinógenos impidiendo las modificaciones que ejercen en el ácido desoxirribonucleico.
Otra teoría sería la de que los thiol, subproductos del metabolismo de las proteínas originados por las proteasas bacterianas, desactivan varios mutágenos colónicos.
Muchos de estos trabajos se han realizado en animales y se debería comprobar si algo semejante sucede en humanos.
19. Efectos en la diabetes mellitus. La administración oral de L. casei a un modelo de diabetes mellitus inducida en ratones inhibió el desarrollo de diabetes mellitus y reguló la respuesta inmune33. En trabajos posteriores, en los que se administró este lactobacilo a ratones afectados de una diabetes no dependiente de insulina, se consiguió reducir los niveles de glucosa en sangre, además de modificar la respuesta inmunológica34.
Mecanismos para aumentar la seguridad de alimentos conLactobacillus casei
La mayoría de los probióticos es estable durante períodos limitados almacenados en frío y seco. Muchos de ellos son polvos congelados secos con bacterias "dormidas" y su disponibilidad depende de:
Tipo de presentación: tabletas, cápsulas, polvo.
Tipo de envasado: a granel, tamaño de paquetes.
De que forma se han mantenido almacenados: en refrigeración o en depósitos corrientes.
Cuando los probióticos experimentan la acción de la humedad, el oxígeno o el calor, las células microbianas se dañan irreversiblemente. Los productos probióticos en forma líquida son de reducida estabilidad; en cambio, en polvo, ya sean servidos como tabletas o como cápsulas, pueden disolverse en alimentos o líquidos previamente a su ingesta, así se consigue una estabilidad muy superior y se puede administrar a niños o lactantes. La microencapsulación ha significado un progreso enorme y una supervivencia mayor en su paso mediante secreciones gástricas y biliares.
En la seguridad de su uso se ha de tener en cuenta las eventualidades de las infecciones sistémicas, las alteraciones del metabolismo o la transferencia de genes. Los inmunodeficientes han de ser precavidos con su uso, ya que algunas especies de lactobacilos, estreptococos y enterococos contienen patógenos oportunistas potenciales.
La seguridad en el uso de alimentos con L. casei, se ha incrementado con la reafirmación de la resistencia contra bacteriófagos que pueden infectar y alterar la fermentación de alimentos por L. casei. Se ha conseguido una clonación y expresión del fago opresor, y se ha obtenido la cepa L. casei EM 40: cl. Este lactobacilo tiene el gen opresor A2 incorporado al genoma35, resistente al fago A2 y, por lo tanto, capaz de fermentar la leche independientemente de la presencia del mencionado fago.
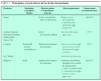
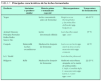
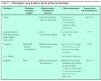
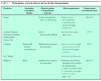
Según la última resolución del Scientific Committee on Food (Report of the Scientific Committee on Food on the Revision of Essential Requirements of Infant Formulae and Follow-on Formulae [SCF/CS/NUT/IF/65 Final]. European Commission, 18 de mayo de 2003), se ha aprobado la adición de probióticos a las leches de continuación, siempre que se haya evaluado su beneficio y seguridad mediante estudios clínicos controlados y a doble ciego. La ESPGHAN, en comunicados más recientes36,37, aprueba su uso en leches de continuación, pero no en las de inicio. El uso por debajo de los 6 meses sólo debe administrarse en condiciones muy específicas. La Agencia Francesa de Seguridad de los Alimentos se adhiere a estas pautas de prudencia (tablas 1-3)
Nota final
Como hemos visto, hay un sinfín de ventajas que los probióticos pueden inducir en el organismo. Por ello, muchos se han incorporado a productos lácteos de consumo corriente (L. acidophilus, Bifidocaterium spp., L. casei, S. salivarius spp. termophilus). Las cepas de probióticos que se utilizan, como dice Baker et al38, no siempre pertenecen al mismo ecosistema del que los recibe y probablemente no tienen el mismo impacto en el propio ecosistema que las bacterias autóctonas. Algunos probióticos administrados ejercen sin duda efectos específicos en el intestino, influyen en la producción de moco del intestino y reducen la permeabilidad o incrementan la inmunidad local o sistémica. Sin embargo, se desconoce todavía cómo funcionan estas acciones específicas y cómo las controla el huésped; por ello la selección de los probióticos que se debe usar es discutible. Aunque los lactobacilos y bifidobacterias generalmente se detectan en las heces de niños que reciben leches suplementadas, se han descrito grandes diferencias en la recuperación fecal de esos probióticos administrados a varios niños en similares condiciones, a la misma dosis y a las mismas horas. Por otra parte, todos los trabajos realizados en humanos se basan en probióticos aislados en heces; sin duda, lo que sucede en tramos superiores del colon, o en el ciego o íleon, puede ser bien diferente.
Por otra parte, en algunos de estos productos lácteos a los que se ha incorporado probióticos, como ya hemos mencionado, la viabilidad es escasa39. Para valorar bien la viabilidad de estas bacterias probióticas hay que ser rigurosos con la metodología usada en la enumeración de estas bacterias. Además, la viabilidad puede mejorarse con la selección adecuada de cepas resistentes a ácidos y bilis, uso de contenedores de oxígeno impermeables, fermentación en dos etapas, microencapsulación, incorporación de micronutrientes --como péptidos y aminoácidos-- y por sonicación de las bacterias del yogur.
La investigación sobre los mecanismos de acción de los probióticos, las repercusiones de su uso en la inmunidad, el intestino, la alergia, los efectos favorables nutricionales, sin duda, sigue y deberá seguir en el futuro. Probablemente sea la asignatura pendiente de gastroenterólogos, alergólogos, inmunólogos, nutricionistas, así como de la industria de productos lácteos.