Las recomendaciones incluidas en este documento forman parte de una revisión actualizada de la asistencia respiratoria en el recién nacido. Están estructuradas en 12 módulos, y en este trabajo se presentan los primeros tres módulos. El contenido de cada módulo es el resultado del consenso de los miembros del Grupo Respiratorio y Surfactante de la Sociedad Española de Neonatología. Representan una síntesis de los trabajos publicados y de la experiencia clínica de cada uno de los miembros del grupo. Cada módulo se acompaña de un resumen de la evidencia científica con cuatro grados de recomendaciones.
The recommendations included in this document will be part a series of updated reviews of the literature on respiratory support in the newborn infant. These recommendations are structured into twelve modules, with the first three modules being developed in this work. Each module it is the result of a consensus process amongst all members of the Surfactant and Respiratory Group of the Spanish Society of Neonatology. They represent a summary of the published papers on each specific topic and of the clinical experience of each one of the members of the group. Each module includes a summary of the scientific evidence available, graded into four levels of recommendations.
Hace ya 6 años se publicó en Anales Españoles de Pediatría las primeras recomendaciones sobre ventiloterapia neonatal convencional1. Desde entonces, muchas cosas han cambiado, sobre todo en los dispositivos y estrategias empleados en la asistencia respiratoria neonatal. Los principales avances se refieren, por una parte, a las nuevas modalidades de ventilación asistida y a la introducción de la ventilación no invasiva y, por otra, a la integración de monitores de función pulmonar en los respiradores neonatales. También ha cambiado la patología pulmonar tributaria de beneficiarse de la asistencia respiratoria. Así, el amplio uso de corticoides prenatales en la amenaza del parto prematuro ha disminuido la incidencia y la gravedad del síndrome de la dificultad respiratoria (SDR). Además, el síndrome de aspiración meconial (SAM) grave es hoy en día excepcional, al mejorar el manejo perinatal.
MétodosEl actual Grupo Respiratorio y Surfactante (RespiSurf) de la Sociedad Española de Neonatología (SEN) decidió revisar las anteriores recomendaciones publicadas en el año 2001, y estructurarlas en 12 módulos (tabla 1). Cada módulo fue desarrollado por uno o dos miembros del grupo, y posteriormente consensuado por el resto de miembros. Dos miembros del grupo (F. Castillo y A. Valls) actuaron de editores, para homogeneizar el formato y reducir su extensión. En esta primera entrega se desarrollan los primeros tres módulos.
Estructura de los módulos de las recomendaciones en la asistencia respiratoria en el recién nacido
|
Cada módulo resulta del consenso entre los miembros, y representa un resumen de lo publicado sobre el tema desde la publicación de las anteriores recomendaciones, así como de la experiencia clínica de todos los miembros del grupo. Al final de cada módulo se incluye un breve resumen de la mejor evidencia científica disponible sobre el tema en la base de datos de la Colaboración Cochrane neonatal o en la literatura médica, así como unas recomendaciones basadas en estas evidencias.
Módulo 1: monitorización del recién nacido con asistencia respiratoriaObjetivos de la monitorización en la asistencia respiratoria- 1.
Mantener unos gases arteriales dentro de un rango aceptado como normal, para evitar la presencia de hipoxia o daño por hiperoxia, y facilitar la regulación del equilibrio ácido-base.
- 2.
Minimizar el daño pulmonar evitando volutrauma y barotrauma, utilizando parámetros ventilatorios adecuados y volúmenes corrientes en rango fisiológico.
- 3.
Monitorizar la evolución de la enfermedad pulmonar mediante la observación de los parámetros de función pulmonar durante la asistencia respiratoria.
- 4.
Favorecer el bienestar del neonato y su adaptación al respirador, y disminuir el distrés, mediante el estudio de las gráficas de presión flujo y volumen del ventilador y la regulación de sus parámetros.
- 5.
Facilitar la recuperación de la enfermedad pulmonar, mediante la instauración de una capacidad residual funcional óptima y la utilización de volúmenes pulmonares adecuados para evitar atelectasias o sobredistensión pulmonar.
Una valoración clínica cuidadosa del paciente sometido a asistencia respiratoria no debe ser descuidada nunca. Debemos valorar el color del niño, la presencia de confort o agitación, la ventilación pulmonar mediante visualización de los movimientos de la caja torácica, su sincronización con los ciclos del ventilador y la auscultación de ambos campos pulmonares en busca de asimetría o dificultad en el flujo aéreo. Los datos obtenidos de la exploración clínica deben valorarse conjuntamente con la radiografía de tórax, los resultados de gases sanguíneos y los parámetros de función pulmonar que nos proporciona el ventilador. Además, debemos vigilar el correcto funcionamiento del ventilador, la disposición de las tubuladuras, el sistema de calentamiento de gases y ausencia de condensación.
Objetivos gasométricosLos objetivos gasométricos en asistencia respiratoria deben compatibilizar una adecuada respiración celular con unos parámetros que no dañen en exceso el pulmón. En el pretérmino, estos parámetros podrían ser: PaO2 50-60mmHg, SatO2 88-92 % y PaCO2 50–55mmHg. En el neonato a término los objetivos podrían ser: PaO2 50–70mmHg, SatO2 92–95 % y PaCO2 45–55 mmHg1. Estos valores son orientativos, debiendo tener en cuenta la enfermedad de base, la cronicidad y otros parámetros. Puede haber diferencias entre la pO2 preductal y posductal en hipertensión pulmonar con ductus permeable. La oximetría de pulso es eficaz para detectar los episodios de hipoxemia, pero no es un método exacto para valorar situaciones de hiperoxia. El rango de medida utilizable es entre el 80 y el 95 %. Fuera de estos valores es difícil conocer el grado de oxigenación arterial2,3.
Monitorización de la ventilación, invasiva y no invasivaDurante la asistencia respiratoria es necesario monitorizar la oxigenación (pO2, saturación de oxígeno de la hemoglobina [SaO2]), ventilación pulmonar (pCO2) y el equilibrio ácido-base en neonatos con enfermedad pulmonar. La monitorización puede ser continua o esporádica, invasiva o no invasiva. La ideal es la monitorización continua y no invasiva, pero no es posible en todas las situaciones o con la precisión deseada. Es habitual obtener una gasometría de catéter o por punción arterial como patrón de referencia. También son útiles las gasometrías venosas y capilares, menos agresivas pero de menor precisión que la punción arterial. La información que ofrecen debe interpretarse sabiendo el lugar de su extracción.
La medida de los gases sanguíneos se puede conseguir de forma no invasiva mediante electrodos transcutáneos que miden conjuntamente la pO2 y pCO2 a través de la superficie cutánea. Dicha medida se realiza por difusión de los gases a través de la piel. Para ello se precisa conseguir la dilatación de la red capilar subyacente al electrodo mediante la aplicación cuidadosa de calor que evite quemaduras. La medida de pO2 y pCO2 transcutáneo es muy útil como sistema de control continuo, cuando se pueden producir rápidas variaciones en los gases sanguíneos, durante la enfermedad pulmonar aguda o en el tratamiento con ventilación de alta frecuencia.
La medición del CO2 espirado (capnografía) puede detectar situaciones de hipoventilación o hiperventilación, y es también útil para valorar la extubación accidental o la situación anormal del tubo endotraqueal durante la intubación.
La monitorización continua de los parámetros del respirador, la visualización simultánea de los trazados de presión, flujo y volumen tidal (Vt), así como las curvas de presión-volumen y flujo-volumen, son de gran utilidad para ajustar los parámetros ventilatorios. Su análisis permite detectar precozmente situaciones potencialmente dañinas para el pulmón, como la sobredistensión pulmonar, la presión positiva al final de la espiración (PEEP) insuficiente o la sobredistensión y atrapamiento excesivo de aire en el pulmón.
Los valores de función pulmonar, como el Vt, la resistencia y la distensibilidad, son útiles para valorar la situación de la enfermedad pulmonar y la respuesta al tratamiento.
Las gráficas de tendencias del Vt, el volumen minuto y la FiO2 aportan una idea de la evolución de la enfermedad pulmonar y de las necesidades de tratamiento.
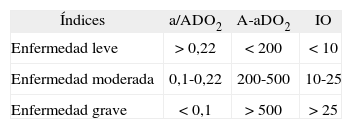
Índices de oxigenación y ventilaciónSon útiles para evaluar la gravedad de la enfermedad respiratoria. Tienen en cuenta la oxigenación arterial y la cantidad de oxígeno o la intensidad de la asistencia respiratoria empleada4. Los más utilizados se representan en la tabla 2.
Índices de oxigenación y ventilación
| Índices | a/ADO2 | A-aDO2 | IO |
| Enfermedad leve | > 0,22 | < 200 | < 10 |
| Enfermedad moderada | 0,1-0,22 | 200-500 | 10-25 |
| Enfermedad grave | < 0,1 | > 500 | > 25 |
a/ADO2: fracción alveolo-arterial de oxígeno; A-aDO2: diferencia alveolo-arterial de oxígeno; IO: índice de oxigenación.
- –
Cociente arterial-alveolar de O2 (a/ADO2 = PaO2/ [713 × FiO2] – [PaCO2/0,8]) y la diferencia alveolo-arterial de O2 (A – aDO2 = [713 × FiO2] – [PaCO2/0,8] – PaO2). Son útiles para comparar la gravedad del paciente en ventilación espontánea, ya que no tienen en cuenta los parámetros de asistencia respiratoria.
- –
Índice de oxigenación (IO = MAP × FiO2 × 100/PaO2): fácil de calcular y útil para valorar la oxigenación y la gravedad de un paciente durante la asistencia respiratoria. Este índice es aceptado para indicar otros tratamientos (óxido nítrico, oxigenación por membrana extracorpórea [ECMO]) y establecer el riesgo de mortalidad.
Actualmente disponemos de sistemas de medida de la función pulmonar sin interrumpir la ventilación, acoplados a los respiradores neonatales, que pueden ser de gran ayuda para decidir los ajustes de los parámetros del ventilador, y entender mejor la fisiología ventilatoria del neonato con enfermedad respiratoria.
Los valores numéricos, trazados y gráficas útiles durante la asistencia respiratoria:
Valores numéricos- –
Medidos: FiO2, tiempo inspiratorio, presión inspiratoria pico (PIP), PEEP. Importantes para valorar los fallos en el ventilador. Indican la diferencia entre los valores seleccionados y los reales.
Calculados: Vt, volumen minuto, presión media en la vía media (MAP), distensibilidad, resistencia y sobredistensión. Son básicos para seleccionar los parámetros de la asistencia respiratoria.
Trazados gráficosProporcionan información de la adecuación de los parámetros del ventilador.
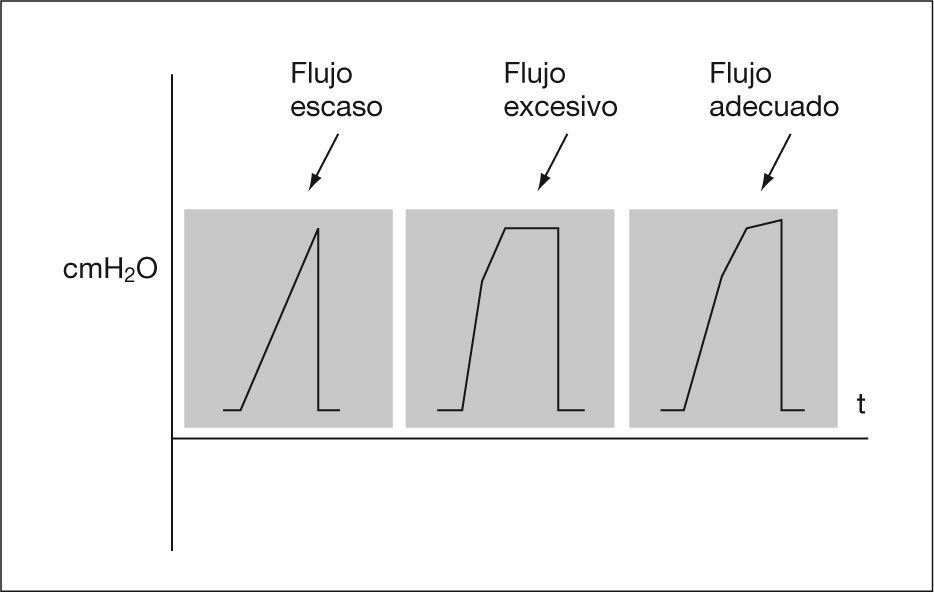
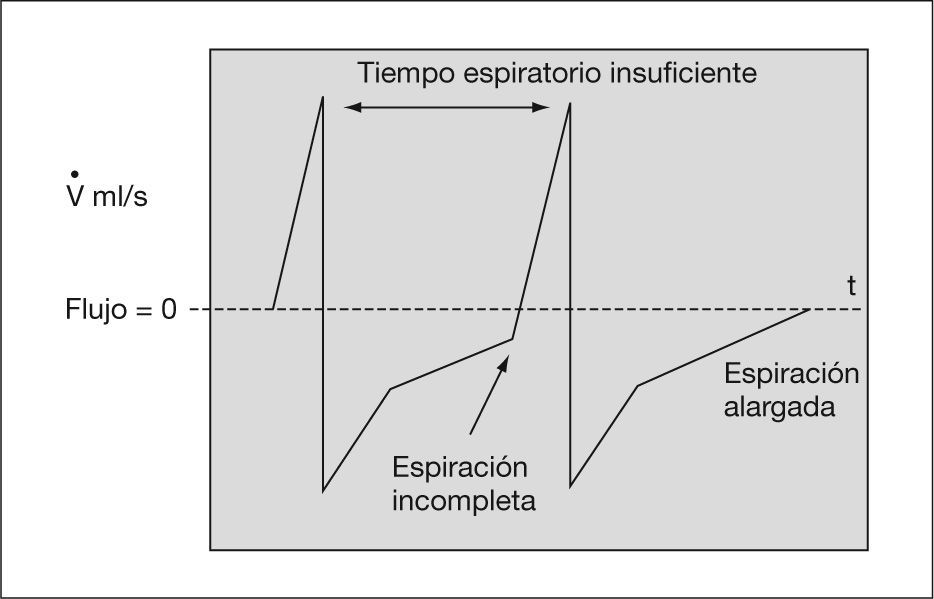
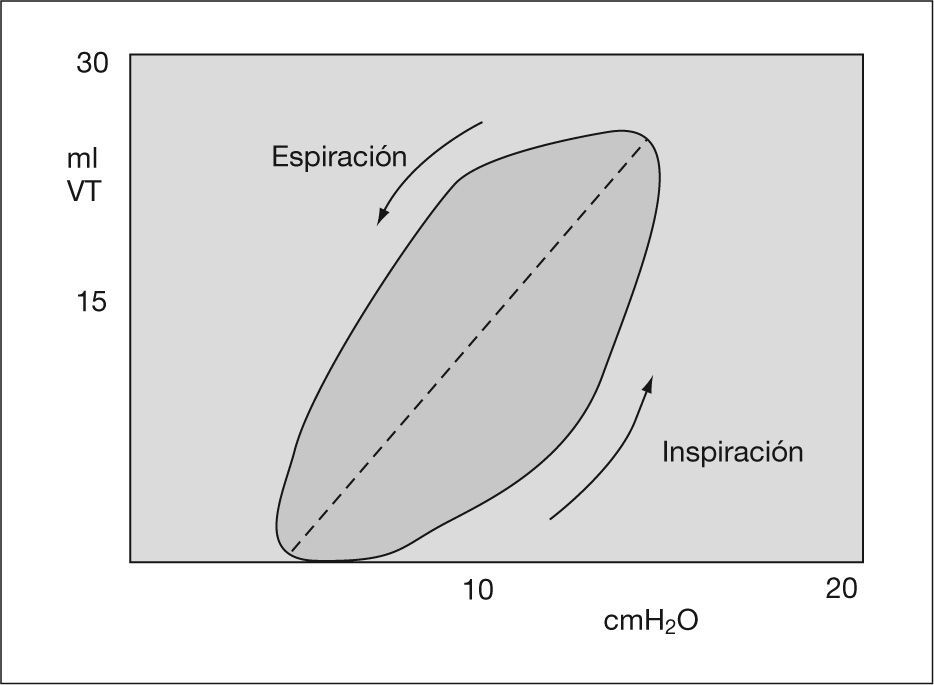
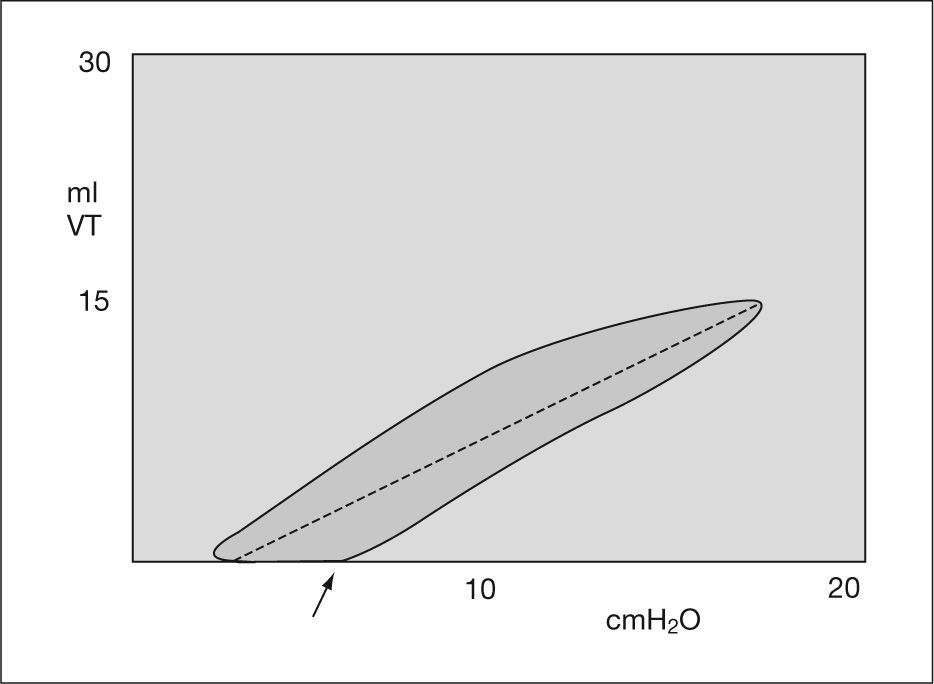
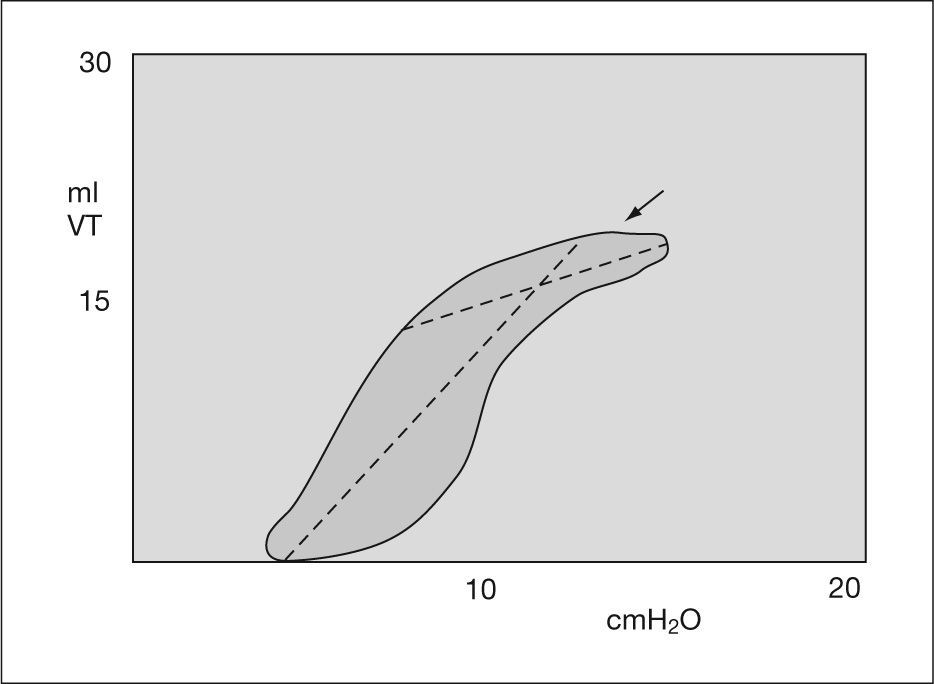
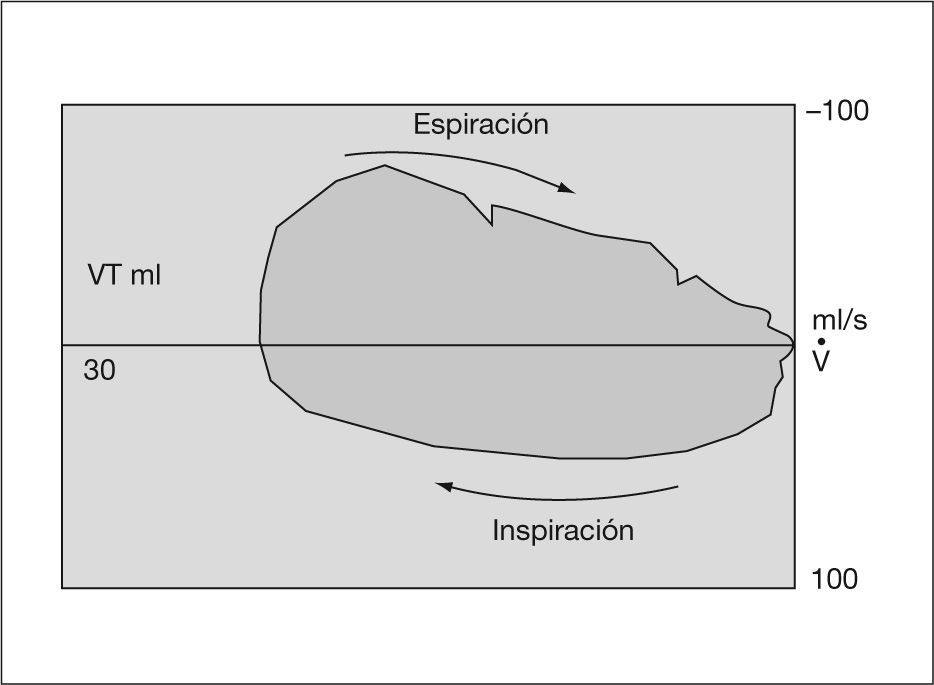
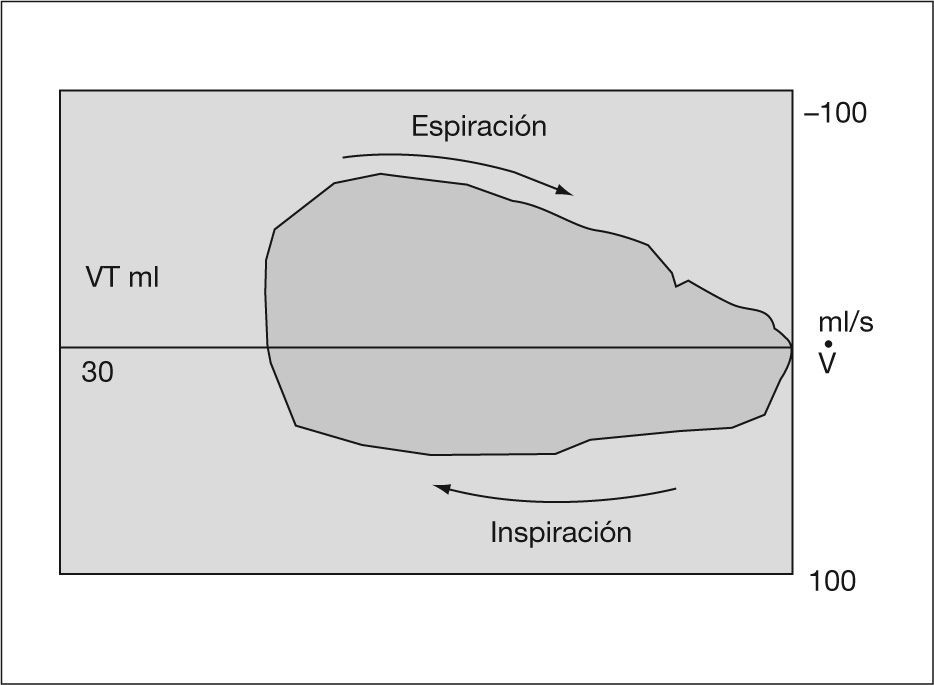
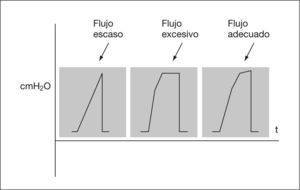
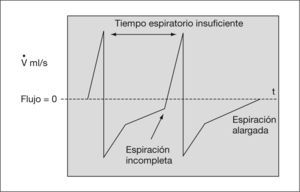
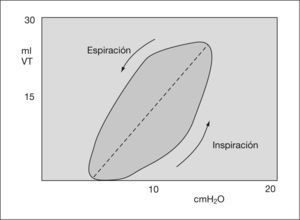
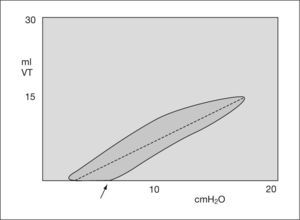
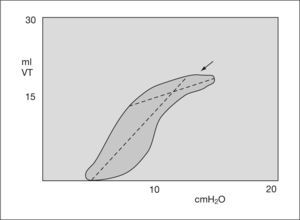
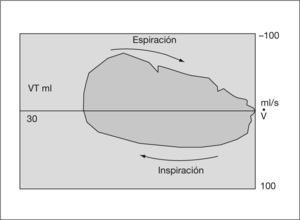
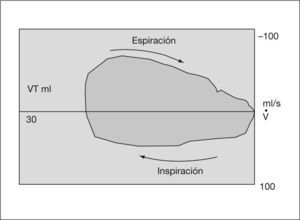
Gráficas de presiónDe presión-volumen y de flujo-volumen (fig. 3). Gráfica de presión-volumen corriente. Cálculo de distensibilidad y sobredistensión (figs. 4 y 5). Gráfica de volumen/flujo. Valoración de las resistencias (figs. 6 y 7).
Trazado de tendenciasValoran la interacción de los parámetros de función pulmonar y las modificaciones realizadas en el ventilador durante períodos de tiempo largos, así como la evolución de la enfermedad pulmonar y la respuesta a otras medidas terapéuticas.
Resumen de la evidenciaSi bien la medición continua de la función mecánica pulmonar no se relaciona de modo directo con una menor mortalidad, optimiza el manejo del ventilador y disminuye el número de determinaciones gasométricas. Además, simplifica la adecuación de los parámetros de asistencia respiratoria a las características del pulmón neonatal5,6.
RecomendacionesSe recomienda que a todo neonato que precise asistencia respiratoria se le monitoricen de modo continuo las constantes vitales y la SaO2. Además, es conveniente emplear respiradores neonatales que dispongan de un sistema incorporado de monitorización y visión de la función mecánica pulmonar.
Módulo 2: oxigenoterapiaLa meta de la oxigenoterapia es conseguir una adecuada entrega de oxígeno a los tejidos sin crear toxicidad. El oxígeno se transporta en la sangre en combinación química con la hemoglobina y disuelto, en solución física. La mayor parte del oxígeno esta unido a hemoglobina, dependiendo el grado de unión de la presión parcial de éste (PaO2) y se describe con la curva de disociación del oxígeno. Cuando la PaO2 es de 100mmHg, la hemoglobina está saturada al 97 %. A medida que desciende la PaO2, la disminución en la SaO2 se hace más rápida. Presiones de oxígeno por debajo de 40mmHg originan un rápido descenso de la SaO2. Presiones de oxígeno superiores a 100mmHg sólo aportan un mínimo aumento en la capacidad transportadora de oxígeno7.
La PaO2 en sangre fetal es entre un cuarto y un quinto de la del adulto. Sin embargo, tiene una mayor capacidad de transporte y afinidad para el oxígeno por la presencia de hemoglobina fetal. Esta mayor afinidad permite una mayor captación de oxígeno en la placenta. La teórica desventaja de la menor liberación del oxígeno a los tejidos es compensada por el hecho de que la curva de saturación de hemoglobina fetal tiene una mayor pendiente, por lo que pequeños descensos de la PaO2 ocasionan mayores descensos de la saturación de oxígeno y, por tanto, entrega de oxígeno.
Tradicionalmente, la reanimación se realizaba con el 100 % de oxígeno, pero en recién nacidos a término (RNAT) se ha comprobado que aumenta la mortalidad 8, lo que también puede ser de riesgo en recién nacidos prematuros (RNPRM) ya que produce una reducción del 20 % del flujo cerebral9. Debe recordarse que durante los primeros 5min de vida, la SaO2 aumenta muy lentamente desde valores del 50–60 al 90 %10. La pulsioximetría ayuda a evitar los picos de hiperoxia y, además, mide adecuadamente la frecuencia cardíaca, es un buen marcador de la eficacia de la reanimación y puede ayudar a guiar la administración de O210. Estudios en RNAT que precisaron reanimación sugieren una más rápida recuperación si se emplea aire en lugar de O211, un menor estrés oxidativo12, sin que se observaran diferencias en el seguimiento a largo plazo13.
Después del período neonatal inmediato, hay datos que sugieren que la SaO2 en RNPRM que reciben oxigenoterapia debe mantenerse por debajo del 93 % y no exceder del 95 %, para evitar el desarrollo de retinopatía de la prematuridad (ROP) y displasia broncopulmonar (DBP)8,14. Por otra parte, los estudios emprendidos para valorar el posible efecto preventivo de mantener las SaO2 por encima de estos niveles no demostraron una mejoría del fondo de ojo, mientras que presentaron más signos respiratorios y mayor dependencia al oxígeno15. También hay datos que sugieren que las fluctuaciones marcadas de la SaO2 pueden asociarse al desarrollo de ROP16.
Tras la administración de surfactante, pueden producirse episodios hiperóxicos que han sido relacionados con un aumento de las tasas de hemorragia intraventricular (HIV) de grados I y II17.
Recomendaciones para el manejo de FiO2 y SaO2 en neonatos pretéminoDada la ausencia de evidencia, ningún rango debe convertirse en práctica estándar hasta que se resuelvan las preguntas en torno a riesgos y beneficios a corto y largo plazo. Los rangos deberán ser determinados según la edad gestacional, las condiciones clínicas y el conocimiento de la relación cambiante entre oxígeno, hemoglobina, PaO2 y SaO2, así como el tipo de monitor transcutáneo utilizado18–20.
Manejo de la FiO2 y SaO2 en RNPRM- •
El oxígeno es una droga con efectos adversos potencialmente importantes.
- •
El criterio de SaO2 debe ser fijado individualmente para cada niño, y se seguirá hasta las 8 semanas posnatales o hasta completar la vascularización retiniana.
- •
Programar los límites de alarma de SaO2:
- –
Utilizar un monitor de saturación inmediatamente al nacer.
- –
Usar un límite inferior del 85 % y superior al 93 % (o no > 95 % en los > 32 semanas).
- –
- •
Ante alarma de saturación baja hay que preguntarse:
- –
¿Es apropiada la onda de pulso?
- –
¿Es problema del sensor?
- –
¿Cómo están la frecuencia cardíaca y el esfuerzo respiratorio?
- –
¿Cómo de baja es la SaO2 y durante cuánto tiempo ha estado por debajo de límites aceptables?
- –
- •
Sala de partos y transporte a la unidad de cuidados intensivos neonatales (UCIN):
- –
Utilizar mezcladores de gases para minimizar el aporte de oxígeno. Si no se dispone de ellos, recordar que las bolsas autoinflables de reanimación sin reservorio aportan una FiO2 aproximada del 0,4 (40 % de O2).
- –
Monitorizar la SaO2 y disminuir la FiO2 rápidamente, si la SaO2 supera el 93 %.
- –
- •
La SaO2 ha proporcionado un falso sentido de “exactitud” y seguridad.
- •
Cada vez hay más pruebas de que las SaO2 elevadas, aceptadas por algunos como “normales” son innecesarias y probablemente perjudiciales.
- •
La relación entre PaO2 y SaO2 se pierde en niveles “altos” de SaO2, cuando un niño respira oxígeno suplementario y, por lo tanto, ignoramos cuál es la PaO2.
- •
La relación y predicibilidad entre la PaO2 y la SpO2 son muy buenas, cuando la SaO2 no es elevada.
- •
Con los conocimientos actuales, es imposible recomendar una práctica clínica “óptima”, pero seguramente podemos erradicar la mal praxis.
- •
Una PaO2 inferior a 80mmHg cuando un niño respira oxígeno suplementario puede lograrse en la mayoría de los casos si se mantienen los límites (y las alarmas) de la SaO2 en el 95 %, evitando SaO2 más elevadas. No hay pruebas de que las saturaciones del 86–93 % sean perjudiciales.
El patrón de referencia sigue siendo la medición intermitente de la PaO2 en muestras de sangre arterial, acompañada de una monitorización continua no invasiva, usando saturómetros transcutáneos (pulsioxímetros) de nueva generación, con algoritmos de medición que evitan las interferencias generadas por los movimientos del neonato21.
Resumen de la evidencia científicaComo se ha mencionado, el nivel de conocimientos científicos sobre el uso del oxígeno en la reanimación, y de hecho durante todo el período neonatal, son muy escasos. Por ello, son pocas las recomendaciones basadas en la evidencia que pueden hacerse.
- 1.
Período neonatal inmediato y reanimación.
- a)
En la resucitación debe usarse la FiO2 más baja posible siempre que la frecuencia cardíaca sea mayor de 100 lat./min, dado que esto puede reducir la vasoconstricción cerebral (grado de recomendación-evidencia B) y quizás la mortalidad (B).
- b)
La medición de la SaO2 puede guiar la administración de oxígeno, para prevenir los picos de hiperoxia (B).
- c)
Hay que recordar que durante la transición a la vida extrauterina al nacer, la SpO2 puede ascender lentamente desde valores del 50 al 80 % (D).
- a)
- 2.
Resto del período neonatal.
- a)
En neonatos que reciben oxigenoterapia, la SaO2 debe mantenerse siempre por debajo del 95 %, porque con ello es posible disminuir las tasas de ROP y DBP (D).
- b)
Después de administrar surfactante, debe reducirse rápidamente la FiO2 para evitar los picos de hiperoxia que pueden asociarse a HIV de grados I y II (C).
- a)
La ventilación no invasiva (VNI) es la aplicación de un soporte ventilatorio sin intubación endotraqueal. Las principales modalidades que se aplican en neonatos son:
Presión positiva continua en la vía aérea nasal (CPAP-N)La CPAP-N es la aplicación de un gas a una determinada presión de forma continua en la vía aérea, a través de la nariz. En el año 1971 se introdujo como modalidad precoz de tratamiento del SDR22. Posteriormente, aparecieron estudios que mostraban que su instauración temprana modificaba el curso de esta enfermedad, disminuyendo la necesidad de ventilación mecánica y reduciendo su agresividad23–25.
Por otra parte, el uso de CPAP-N tras la extubación ha demostrado una reducción de fracasos en la misma26,27. En las pausas de apnea del prematuro también se han observado efectos beneficiosos28.
Ventilación con presión positiva intermitente nasal (IPPV-N)En esta modalidad, además de aplicar CPAP-N se intercalan ciclos de presión positiva a una frecuencia y características predeterminadas. Puede aplicarse de forma sincronizada o no. En los últimos años su uso ha aumentado, y estudios recientes sugieren buenos resultados en el “destete” y pausas de apnea, disminuyendo los días de oxigenoterapia y de ventilación en neonatos pretérmino29,30.
Efectos fisiológicos- –
Mantiene la permeabilidad de la vía aérea. Disminuye la resistencia supraglótica al aumentar el diámetro de la apertura laríngea.
- –
Previene del colapso alveolar al final de la espiración.
- –
Aumenta el tiempo inspiratorio y el volumen corriente.
- –
Aumenta la capacidad residual funcional (CRF).
- –
Reduce la distorsión torácica durante la inspiración.
- –
Disminuye la asincronía toracoabdominal.
- –
Mejora la función diafragmática.
- –
Patologías con alteración en la CRF (SDR, mala adaptación pulmonar, etc.) y/o que cause aumento del trabajo respiratorio.
- –
“Destete” ventilatorio.
- –
Pausas de apnea idiopáticas.
- –
Edema pulmonar.
- –
Parálisis/paresia diafragmática.
- –
Laringomalacia-traqueomalacia.
- –
Enfermedades restrictivas de las vías aéreas como la DBP.
- –
Disminución del cortocircuito izquierda-derecha a nivel ductal.
- –
Faríngea. Por tubo mononasofaríngeo. Es fácil de fijar y tiene pocas fugas, pero aumenta la resistencia de la vía aérea.
- –
Nasal. Puede aplicarse mediante cánulas o mascarilla nasal. Son difíciles de fijar, pueden originar deformidades, traumatismos y las fugas son frecuentes. Su efectividad es mayor que la faríngea. Las interfases más utilizadas son las binasales.
Los generadores de presión pueden ser de flujo continuo o variable. En los de flujo continuo la presión se regula modificando la resistencia a la salida del gas en el asa espiratoria del circuito y típicamente son aplicados usando el propio respirador, mediante una de las interfases indicadas.
En los generadores de flujo variable, la presión se consigue con el flujo de gas administrado, y es el interfasegenerador del sistema el que regula los cambios de flujo y da lugar a una presión constante durante todo el ciclo respiratorio, condicionando menor trabajo respiratorio (sistema Benveniste-Ventil, CPAP-N de burbuja, Infant Flow Driver®, Arabella®).
La aplicación de IPPV-N con estos dispositivos puede administrarse con o sin sincronización. Los sistemas disponibles en la actualidad para sincronizar el esfuerzo del paciente son por cambios de flujo, de presión o impedancia (movimiento diafragmático).
Uso clínico del CPAP-N y IPPV-NInicialmente la CPAP-N se aplica a una presión de 4–5 cmH2O, con la FiO2 necesaria para mantener una SaO2 adecuada a su edad gestacional. El gas administrado debe tener una alta humedad y adecuada temperatura. Progresivamente se incrementa la presión del sistema hasta alcanzar el efecto deseado (CPAP-N entre 7 y 8 cmH2O y en algunas ocasiones se puede llegar a 10 cmH2O).
El IPPV-N es preferible usarlo de forma sincronizada, aunque requiere cierta experiencia, dado que los dispositivos actuales están lejos de conseguir una adecuada sincronización. Se pueden regular la presión inspiratoria y espiratoria, el tiempo inspiratorio y la frecuencia respiratoria según las necesidades. En general, a excepción que destetemos al paciente desde la modalidad respiratoria en forma de AC, la frecuencia empleada es la que recibía el paciente en el momento de la extubación (10–15 resp./ min); la presión inspiratoria 2 cmH2O por encima de la ajustada en el respirador previo a la extubación, la presión espiratoria 4–6 cmH2O y la FiO2 se adecua a la SaO2 deseada.
Fracaso de la ventilación no invasivaAntes de considerar que ha fracasado hay que:
- –
Asegurar la correcta posición de la vía aérea, evitando la flexión y rotación excesiva del cuello.
- –
Descartar obstrucción por secreciones de la interfase y la vía aérea.
- –
Comprobar el correcto funcionamiento del generador y de la posición de la interfase.
- –
Comprobar el cierre de la boca, ya que puede generar pérdidas de 2–3 cmH2O.
Se considera fracaso:
- –
Si no se consigue la PaO2 o SaO2 deseada y se precisa FiO2 altas (30-50 %).
- –
Necesidad de administrar terapias por vía endotraqueal (surfactante exógeno).
- –
Aumento de la PaCO2 > 60mmHg en patología aguda.
- –
Pausas de apnea que requieran reanimación vigorosa o de una frecuencia superior a tres episodios por hora y que cursen con desaturación y/o bradicardia.
Ha de ser lenta, iniciándola cuando la PaO2 o SaO2 deseada se consigan con FiO2 bajas (el 30 % en patología aguda) o cuando el paciente no haya tenido pausas de apneas en las últimas 48h. Se reduce la presión en decrementos de 1–2 cmH2O cada hora según la respuesta, hasta llegar a 3–4 cmH2O, suprimiéndola cuando la presión sea inferior a 4.
En menores de 30 semanas es posible que en fases tempranas después de la administración de surfactante, no necesite oxígeno, pero mantenga un trabajo respiratorio elevado. En esta situación el uso de CPAP-N puede ser también beneficioso. En IPPV-N, el destete será similar al empleado en la ventilación invasiva.
Efectos secundarios- –
Escape aéreo.
- –
Puede aumentar las resistencias vasculares pulmonares, dificultar el retorno venoso y disminuir el gasto cardíaco.
- –
Favorecer el cortocircuito ductal derecha-izquierda.
- –
Presiones excesivas pueden disminuir el volumen minuto y aumentar la PaCO2.
- –
El llanto, la fuga por boca o la distensión abdominal pueden disminuir su eficacia.
- –
Puede producir deformidades o necrosis del tabique nasal, si la interfase aplicada está mal posicionada.
- –
Induce un aumento de las secreciones en vías respiratorias altas que pueden ocasionar apneas obstructivas.
En la sala de partos, la CPAP-N está siendo profusamente empleada, sin que de momento exista evidencia sobre disminución de la necesidad de surfactante y/o ventilación mecánica31,32.
La CPAP-N se usa frecuentemente como soporte respiratorio alternativo a la ventilación mecánica en el SDR, a pesar de que faltan datos que muestren fehacientemente su eficacia en estos pacientes33. Dado que la ventilación mecánica puede lesionar el pulmón inmaduro, debe evitarse su uso. La aplicación de CPAP-N reduce la reintubación, si se aplica tras la extubación a una presión de 5 cmH2O34. No hay evidencia de que la CPAP-N prevenga la necesidad de aplicar surfactante y, sin embargo, en el SDR moderado muchos pacientes son tratados con CPAP-N sin aplicárseles surfactante35. De hecho, está demostrado que la aplicación precoz de CPAP-N aumenta las posibilidades de poder evitar la ventilación mecánica (riesgo relativo [RR]: 0,55; intervalo de confianza [IC] del 95 %: 0,32-0,96; número necesario que tratar [NNT]: 6)36. No hay evidencia de que a largo plazo haya diferencias entre los sistemas usados para aplicar CPAP-N37. Sin embargo, se ha demostrado que en comparación con el tubo único, las piezas bi-nasales reducen la necesidad de reintubación (RR: 0,59; IC 95 %: 0,41-0,85; NNT: 5)38.
Recomendaciones- –
La CPAP-N debe ser aplicada en todos los pacientes con riesgo de desarrollar un SDR, sobre todo en menores 30 semanas de gestación que no reciben ventilación mecánica, hasta que su estado clínico pueda ser evaluado con precisión (D).
- –
El uso de CPAP-N conjuntamente con la aplicación precoz de surfactante debe ser considerado en casos de SDR para reducir la necesidad de aplicar ventilación mecánica (A).
- –
Las interfaces binasales deben ser preferidas sobre el tubo nasofaríngeo, dado que se reduce la necesidad de intubación (C), si la presión aplicada es al menos de 6 cmH2O (A).
F. Castillo (Hospital Vall d'Hebron, Barcelona); D. Elorza (Hospital La Paz, Madrid); M.L. Franco (Hospital Gregorio Marañón, Madrid); J. Fernández (Hospital Clínico, Santiago de Compostela); M. Gresa (Hospital Materno-Infantil, Las Palmas); A. Gutiérrez (Hospital la Fe, Valencia); I. López de Heredia (Hospital de Cruces, Baracaldo); X. Miracle (Hospital Clínico-Maternidad, Barcelona); J. Moreno (Hospital Sant Joan de Déu, Barcelona); A. Losada (Hospital el Rocío, Sevilla); A. Valls (Hospital de Cruces, Baracaldo).