Con la implantación del programa de cribado neonatal en España desde el año 1980, y la mejora de los resultados, se ha logrado un aumento del número de gestantes con fenilcetonuria (PKU)1.
Durante la gestación el paso transplacentario de fenilalanina (Phe) aumenta, pudiendo ser neurotóxica y teratogénica para un feto en desarrollo y con inmadurez hepática1–6. Las anomalías en los hijos de mujeres con PKU no controlada durante el embarazo fueron informadas por Dent en 1957 y Mabry et al. en 19632.
Los efectos teratógenos de la Phe sobre el feto en desarrollo, denominado síndrome de PKU materna (SFM), hacen referencia a los efectos físicos y cognitivos que origina la exposición intrauterina de este metabolito sobre el feto1,2. La teratogenicidad es mínima o nula si se logran niveles de Phe entre 120 y 360μmol/l (2-6mg/dl) durante los 3 meses previos a la concepción y durante toda la gestación1–6, aunque niveles sanguíneos de Phe<120μmol/l se han asociado a embriopatía4,6.
Aportamos el caso una paciente de 32 años con una PKU clásica fenotipo leve con un perfecto control metabólico preconcepcional. Las ecografías prenatales fueron normales y la Phe sérica <240μmol/l.
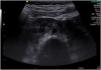
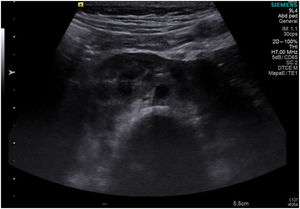
El neonato nació a término con fenotipo normal, cribado neonatal negativo, ecografía transfontanelar normal, detectándose en la ecografía abdominal al mes de vida un riñón en herradura (fig. 1).
El riñón en herradura es la anomalía de fusión más frecuente, ocurriendo en 0,4-1,6/10.000recién nacidos vivos. Consiste en 2 masas renales situadas verticalmente en la línea media o a uno de sus lados, unidos por un istmo de parénquima o fibrosis que cruza el plano medio del cuerpo. En más del 90% de los casos, la fusión ocurre en los polos distales.
El SFM puede cursar con retraso mental (92% de los casos), microcefalia (73%), retraso de crecimiento intrauterino (40%), cardiopatía (12%) y atresia de esófago y dismorfias faciales1–6. Gokmen et al. describen por primera vez un caso de agenesia renal unilateral en una caso de SFM3. Sin embargo, no se conoce el efecto de los niveles elevados de Phe en el desarrollo renal. Las dismorfias faciales son similares a las que se observan en el síndrome alcohólico fetal2.
Con respecto al tratamiento de la gestante con PKU, no todos los medicamentos y suplementos alimenticios disponibles para su uso en individuos afectos de PKU son adecuados para su uso durante la gestación. Así, no se recomienda el empleo de aminoácidos neutros de cadena larga durante la gestación, ya que no modifican las cifras de Phe en sangre de manera constante2.
La sapropterina es un fármaco que puede emplearse durante la gestación tras la consideración de los beneficios y riesgos para la madre y el feto. Se recomienda que las mujeres con PKU que, previamente al embarazo la estaban tomando, continúen con dicho fármaco1.
Las necesidades de Phe materna no son iguales durante todo el embarazo, de tal manera que, durante el primer y segundo trimestre estas son menores y aumentan en el tercer trimestre, momento en el que la maduración hepática en el feto es mayor. Por ello se debe realizar un estricto control nutricional en la madre para evitar restricciones severas alimentarias que den lugar a una ingesta calórica y proteica deficiente1,2,6.
Se aconseja realizar una monitorización de la ingesta de vitaminas y minerales1,2. Los alimentos para uso médico empleados en la PKU pueden proporcionar un aumento de vitamina A, que se asocia a defectos congénitos. La ingesta deficitaria de vitamina B12 se ha asociado a aumento del riesgo de defectos cardiacos congénitos4,5.
Durante el posparto, las necesidades maternas de Phe disminuyen y deberá continuarse con un estricto control metabólico y nutricional. No existe contraindicación para la lactancia materna en estas mujeres, ya que los lactantes no afectados por el déficit de Phe hidroxilasa son capaces de metabolizar los niveles de Phe ligeramente superiores de la leche materna sin dificultad.
Consideramos interesante la aportación del presente caso, ya que se trata de la primera gestante con PKU de nuestra región, donde a pesar de un estricto seguimiento prenatal, el hijo presenta una malformación renal. Puede ser casual, pero también podría ser una malformación secundaria a la hiperPhe materna no descrita hasta la actualidad. Resaltamos además, la importancia del diagnóstico de PKU a las gestantes procedentes de países donde el cribado neonatal no sea universal, de esta forma se podrán detectar mujeres PKU cuyos hijos pueden beneficiarse de un tratamiento dietético en la madre durante el embarazo, evitando el SPM1.