El síndrome opsoclonus mioclonus (SOM) es un trastorno neuroinmune definido por la presencia de 3 de 4 criterios clínicos: opsoclonus o flutter ocular; neuroblastoma; mioclonus y/o ataxia; cambios de humor y/o trastorno del sueño con frecuencia asociado a marcada irritabilidad1. Se ha estimado una incidencia de 0,27-0,40 casos por millón de niños2. Hasta en el 50% de los casos se asocia con tumores de la cresta neural. Se hipotetiza un mayor porcentaje, no siendo detectados algunos de ellos por destrucción previa de la masa tumoral por una posible respuesta inmune3. En ausencia de tumor se propone una relación con infecciones, aunque una verdadera causalidad es difícil de establecer y quizá sea mejor hablar de una etiología «criptogénica» o «idiopática». En ambas situaciones una base inmunomediada parece la responsable de la sintomatología, por afectación a nivel no solo de troncoencéfalo o cerebelo, sino también supratentorial4.
Aunque una proporción de pacientes mantienen un desarrollo normal tras haber experimentado un SOM, otra reseñable presenta ciertos déficits cognitivos o neuropsicológicos (afectándose atención, memoria, visomotor, etc.) en el seguimiento, generalmente con un pronóstico motor normal o casi normal2,5. Factores como la menor edad al diagnóstico, el retraso en el tratamiento inmunosupresor, una presentación clínica inicial más grave, o las recidivas se han discutido como posibles factores de mal pronóstico. En los últimos años se ha producido un cambio en los regímenes de tratamiento, que abogan por la intensificación precoz del mismo, instaurando una biterapia desde el principio (generalmente esteroides e inmunoglobulinas) y asociando un fármaco de 2.a línea precozmente si la respuesta no es satisfactoria. Incluso algunos autores plantean la triterapia inicial6. Todo ello persigue un mejor control de la base inmunopatológica de la enfermedad, a fin de conseguir la resolución de la clínica neurológica aguda, y sobre todo minimizar las repercusiones cognitivas.
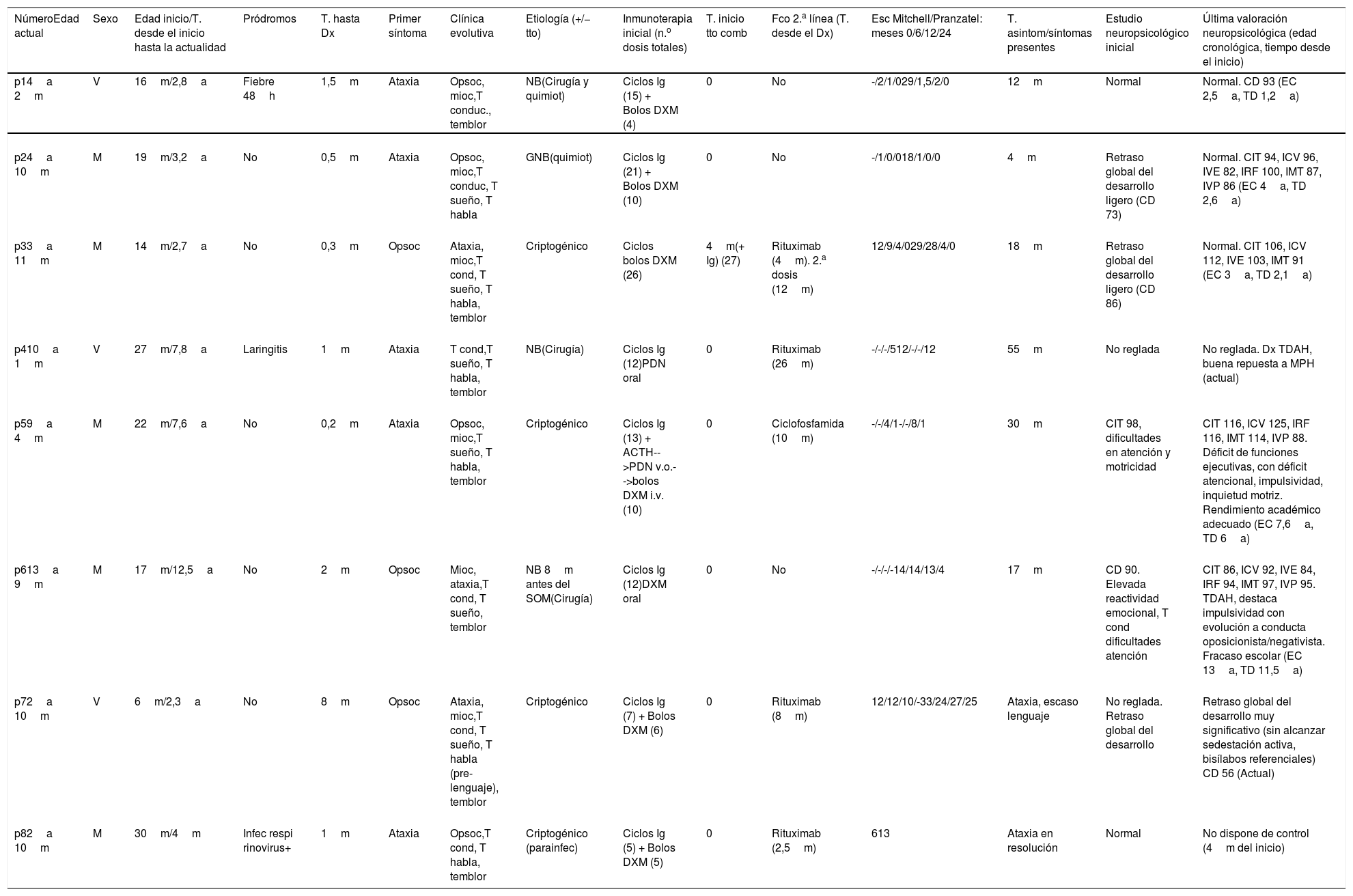
Se describe una serie pediátrica de pacientes con SOM, diagnosticados entre los años 2006 y 2018, valorados y seguidos en una consulta de enfermedades neuroinmunes. Se analizan características clínico-epidemiológicas, tratamiento recibido y evolución a medio-largo plazo (tabla 1).
Características clínico-epidemiológicas y manejo terapéutico
| NúmeroEdad actual | Sexo | Edad inicio/T. desde el inicio hasta la actualidad | Pródromos | T. hasta Dx | Primer síntoma | Clínica evolutiva | Etiología (+/− tto) | Inmunoterapia inicial (n.o dosis totales) | T. inicio tto comb | Fco 2.a línea (T. desde el Dx) | Esc Mitchell/Pranzatel: meses 0/6/12/24 | T. asintom/síntomas presentes | Estudio neuropsicológico inicial | Última valoración neuropsicológica (edad cronológica, tiempo desde el inicio) |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| p14a 2m | V | 16m/2,8a | Fiebre 48h | 1,5m | Ataxia | Opsoc, mioc,T conduc., temblor | NB(Cirugía y quimiot) | Ciclos Ig (15) + Bolos DXM (4) | 0 | No | -/2/1/029/1,5/2/0 | 12m | Normal | Normal. CD 93 (EC 2,5a, TD 1,2a) |
| p24a 10m | M | 19m/3,2a | No | 0,5m | Ataxia | Opsoc, mioc,T conduc, T sueño, T habla | GNB(quimiot) | Ciclos Ig (21) + Bolos DXM (10) | 0 | No | -/1/0/018/1/0/0 | 4m | Retraso global del desarrollo ligero (CD 73) | Normal. CIT 94, ICV 96, IVE 82, IRF 100, IMT 87, IVP 86 (EC 4a, TD 2,6a) |
| p33a 11m | M | 14m/2,7a | No | 0,3m | Opsoc | Ataxia, mioc,T cond, T sueño, T habla, temblor | Criptogénico | Ciclos bolos DXM (26) | 4m(+ Ig) (27) | Rituximab (4m). 2.a dosis (12m) | 12/9/4/029/28/4/0 | 18m | Retraso global del desarrollo ligero (CD 86) | Normal. CIT 106, ICV 112, IVE 103, IMT 91 (EC 3a, TD 2,1a) |
| p410a 1m | V | 27m/7,8a | Laringitis | 1m | Ataxia | T cond,T sueño, T habla, temblor | NB(Cirugía) | Ciclos Ig (12)PDN oral | 0 | Rituximab (26m) | -/-/-/512/-/-/12 | 55m | No reglada | No reglada. Dx TDAH, buena repuesta a MPH (actual) |
| p59a 4m | M | 22m/7,6a | No | 0,2m | Ataxia | Opsoc, mioc,T sueño, T habla, temblor | Criptogénico | Ciclos Ig (13) + ACTH-->PDN v.o.-->bolos DXM i.v. (10) | 0 | Ciclofosfamida (10m) | -/-/4/1-/-/8/1 | 30m | CIT 98, dificultades en atención y motricidad | CIT 116, ICV 125, IRF 116, IMT 114, IVP 88. Déficit de funciones ejecutivas, con déficit atencional, impulsividad, inquietud motriz. Rendimiento académico adecuado (EC 7,6a, TD 6a) |
| p613a 9m | M | 17m/12,5a | No | 2m | Opsoc | Mioc, ataxia,T cond, T sueño, temblor | NB 8m antes del SOM(Cirugía) | Ciclos Ig (12)DXM oral | 0 | No | -/-/-/-14/14/13/4 | 17m | CD 90. Elevada reactividad emocional, T cond dificultades atención | CIT 86, ICV 92, IVE 84, IRF 94, IMT 97, IVP 95. TDAH, destaca impulsividad con evolución a conducta oposicionista/negativista. Fracaso escolar (EC 13a, TD 11,5a) |
| p72a 10m | V | 6m/2,3a | No | 8m | Opsoc | Ataxia, mioc,T cond, T sueño, T habla (pre-lenguaje), temblor | Criptogénico | Ciclos Ig (7) + Bolos DXM (6) | 0 | Rituximab (8m) | 12/12/10/-33/24/27/25 | Ataxia, escaso lenguaje | No reglada. Retraso global del desarrollo | Retraso global del desarrollo muy significativo (sin alcanzar sedestación activa, bisílabos referenciales) CD 56 (Actual) |
| p82a 10m | M | 30m/4m | Infec respi rinovirus+ | 1m | Ataxia | Opsoc,T cond, T habla, temblor | Criptogénico (parainfec) | Ciclos Ig (5) + Bolos DXM (5) | 0 | Rituximab (2,5m) | 613 | Ataxia en resolución | Normal | No dispone de control (4m del inicio) |
a: años; ACTH: corticotropina; CD: cociente de desarrollo global, referido a inventario de desarrollo de Batelle; CIT: cociente intelectual total, referido a la Escala Wechsler de Inteligencia versión para preescolar y primaria (WPPSI) o para niños (WISC) según edad; comb: combinado; Dx: diagnóstico; DXM: dexametasona; EC: edad cronológica; Esc: escala; Fco: fármaco; GNB: ganglioneuroblastoma; h: horas; ICV: índice de comprensión verbal; IMT: índice de memoria de trabajo; IRF: índice de razonamiento fluido; i.v: intravenoso; IVE: índice visoespacial; IVP: índice de velocidad de procesamiento; Ig: inmunoglobulina; Infec: infección/infeccioso; m: meses; M: mujer; mioc: mioclonus; NB: neuroblastoma; opsoc: opsoclonus; p: paciente; PDN: prednisona; quimiot: quimioterapia; respi: respiratoria; SOM: síndrome opsoclonus mioclonus; T.: tiempo; T. asintom: tiempo hasta quedar asintomático; T cond: trastorno de conducta; T habla: trastorno del habla; T. inicio: tiempo hasta el inicio; T sueño: trastorno de sueño; TD: tiempo desde el inicio; TDAH: trastorno de déficit de atención e hiperactividad; tto: tratamiento; V: varón; v.o.: vía oral; -: no realizada escala en ese momento.
En nuestra cohorte se objetivó un ligero predominio de SOM en el sexo femenino (62,5%) y una edad media de inicio (18,8 meses) similares a los referidos en cohortes previas3.
La ataxia fue el síntoma inicial más frecuente, seguido del opsoclonus. El inicio con ataxia aislada3 dificulta el diagnóstico diferencial con la ataxia aguda cerebelosa postinfecciosa, entidad más común; que suele presentarse a una edad discretamente mayor y con mayor frecuencia de pródromos que el SOM. La aparición de otros síntomas cardinales motores facilita claramente el diagnóstico de SOM y su retraso o ausencia lo dificulta. En nuestra serie uno de los pacientes (p4) no presentó mioclonías ni opsoclonus, siendo las alteraciones conductuales las que permitieron el diagnóstico de SOM y la detección de un neuroblastoma. Debe plantearse el SOM como causa de ataxia aguda persistente con alteraciones conductuales, aun sin otros síntomas motores cardinales.
La frecuencia de casos paratumorales (50%) fue similar a la reportada en series mundiales previas3. El tumor fue detectado en el primer cribado en todos los pacientes, si bien en 2 de ellos tanto la gammagrafía con metayodobencilguanidina como los metabolitos de las catecolaminas en orina fueron normales y en uno de ellos incluso la ecografía abdominal, siendo detectado únicamente mediante resonancia magnética. Dado que los tumores asociados al SOM son frecuentemente de bajo grado, el diagnóstico basado únicamente en pruebas que dependen de la actividad metabólica puede no ser lo suficientemente sensible, y deberían acompañarse de pruebas de imagen protocolizadas. Así mismo, por su menor tamaño pueden no ser detectados por imágenes de radiografía simple o ecografía3,4.
En nuestra serie una proporción de pacientes con seguimiento a medio-largo plazo presentaban cierta afectación a nivel neurocognitivo, aunque la mayoría en menor intensidad que lo descrito clásicamente. Entre los pacientes que se mantienen sin síntomas de SOM, la proporción que presentó afectación cognitiva a los 2 años fue similar entre aquellos que empezaron antes de los 18 meses (2/3) y los de inicio posterior (2/3). Los pacientes que presentan algún tipo de alteración a este nivel (p4-6) comenzaron a edades similares o ligeramente superiores a aquellos cuyas valoraciones no detectaban alteraciones cognitivas (p1-3).
De los 3 pacientes con valoración cognitiva normal a los 2 años del inicio, 2 de ellos (p1 y p2) precisaron solamente biterapia para el control clínico completo; si bien son los únicos casos paratumorales que recibieron quimioterapia. Esto podría tener relación con la hipótesis planteada por algunos autores de un mejor pronóstico de los casos paratumorales que podría deberse, al menos en parte, a un efecto positivo de la quimioterapia sobre el control de la base autoinmune-inflamatoria de la enfermedad. El otro caso sin alteraciones cognitivas (p3) fue el único que no recibió biterapia desde el inicio. El control de la clínica cardinal fue difícil, precisando inmunoterapia prolongada y ahorrador de corticoide; si bien es la paciente en la que más precozmente se inició triterapia, asociándose rituximab a los 5 meses del inicio del SOM, con 19 meses de edad. Llama la atención la ausencia de secuelas cognitivas frente a lo costoso del control de la clínica de SOM y el inicio relativamente precoz. En el resto de los casos que precisaron triterapia, el tercer fármaco se asoció a los 53, 32 y 23 meses de edad (p4, p5 y p7), entre 10 y 26 meses tras el inicio. Uno de ellos (p7) corresponde al paciente con el inicio de SOM más precoz y mayor retraso diagnóstico y terapéutico, el cual persiste sintomático y presenta la mayor afectación psicomotora y cognitiva si se compara con el mismo momento evolutivo del resto de pacientes de la serie. Los otros 2 casos desarrollaron un TDAH, pero sin repercusión en el rendimiento escolar uno de ellos y con buena respuesta a estimulantes el otro. Por otro lado, el otro paciente con mayor afectación neurocognitiva y comportamental (p6) recibió solamente biterapia y la corticoterapia se mantuvo por vía oral.
El SOM es una enfermedad de origen inmunomediado, en ocasiones asociada a un tumor subyacente y en la que la precocidad del tratamiento y su intensificación adecuada podría tener implicaciones pronósticas a medio-largo plazo (especialmente a nivel neurocognitivo). Por todo lo anterior, a pesar de su baja frecuencia, esta entidad debe tenerse presente ante el inicio agudo de cualquiera de los signos cardinales, especialmente la ataxia. Analizando la evolución en el tiempo de los pacientes y de los regímenes terapéuticos empleados, es posible que un mayor conocimiento de esta enfermedad, y de la importancia de un tratamiento intensivo precoz, haya modificado en parte nuestro manejo de esta. No obstante, las limitaciones de nuestro trabajo son importantes al ser retrospectivo y con una muestra pequeña. En este sentido no es posible establecer una relación entre los cambios terapéuticos y la evolución neurocognitiva, para lo cual sería preciso realizar un estudio prospectivo con un tratamiento protocolizado. Sin embargo, consideramos de gran interés el realizar aportaciones de experiencias clínicas que puedan contribuir a un mejor conocimiento de esta enfermedad.