La enfermedad de Cushing (EC), debida fundamentalmente a un microadenoma hipofisario, es un cuadro clínico poco frecuente en la edad pediátrica y se asocia a una significativa morbilidad. La principal indicación terapéutica es la cirugía transesfenoidal, aunque se reserva el ketoconazol como alternativa terapéutica temporal durante el período de espera previo, a fin de controlar el hipercortisolismo.
A continuación se presenta el caso de una niña de 13 años y 8 meses con EC. Sus manifestaciones clínicas eran obesidad, disminución de la velocidad del crecimiento, fenotipo cushingoide, cefaleas e hipertensión arterial. Las determinaciones hormonales pusieron de manifiesto valores elevados de cortisol libre urinario y de corticotropina (ACTH). El ritmo de cortisol y de ACTH así como el test corto y largo de dexametasona confirmaron un hipercortisolismo dependiente de ACTH. La resonancia magnética craneal con gadolinio mostró la presencia de microadenoma en hemiadenohipófisis derecha. El diagnóstico se confirmó tras realizar un cateterismo selectivo de senos petrosos inferiores con estímulo de corticoliberina.
En espera de cirugía transesfenoidal, el tratamiento con ketoconazol (200mg/24h) durante 6 meses controló el cuadro de hipercortisolismo. Tras la adenomectomía transesfenoidal, recibió tratamiento sustitutivo con hidrocortisona durante un mes. En la actualidad, la niña lleva 2 años y medio en remisión clínica y hormonal sin cumplir los criterios iniciales posquirúrgicos de curación.
Cushing's disease (CD), which is caused fundamentally by a pituitary microadenoma, is a rare endocrine disease in the paediatric age and which is associated with significant morbidity. The current treatment of choice for CD is trans-sphenoidal selective adenomectomy resulting in long-term remission rates. Pharmacological management of CD is directed at decreasing adrenal steroid secretion. Ketoconazole inhibits adrenal enzyme activity and decreases cortisol secretion.
Our patient is a girl of 13 years and eight months of age with CD. The clinical manifestations were obesity, decrease in growth rate, Cushingoid phenotype, headache and arterial hypertension. The hormone determinations showed elevated values of UFC and ACTH. The circadian rhythm cortisol and ACTH and the short and long dexamethasone tests of provide definitive diagnosis of CD. The cranial MRI with gadolinium suggests the presence of microadenoma in the right pituitary lobe. The diagnosis is confirmed after performing a selective catheterisation of the inferior petrosal sinuses with CRH stimulus.
While waiting for trans-sphenoidal surgery, the treatment with ketoconazole (200mg/24h) controlled the hypercortisolism. After the surgical procedure, the patient received replacement therapy with hydrocortisone for 1 month. At the present time, the patient, without fulfilling the post surgery cure criteria, has been 2 and a half years in clinical and hormonal remission.
El diagnóstico diferencial y el tratamiento del síndrome de Cushing (SC) es un reto de la endocrinología pediátrica1. La diferenciación de los diferentes subtipos del SC es esencial para seleccionar el tratamiento adecuado. La causa más frecuente del SC en la infancia es la producción excesiva de corticotropina (ACTH) (entre el 80 y el 85%) debida fundamentalmente a un adenoma hipofisario (enfermedad de Cushing [EC])2–4. La sintomatología puede pasar desapercibida por mucho tiempo; asimismo, los síntomas más constantes son el retraso del crecimiento y la obesidad. Debido a los efectos devastadores del exceso de cortisol es fundamental el diagnóstico precoz y la localización correcta de la lesión causal para establecer el tratamiento más apropiado5. El tratamiento dirigido a conseguir una rápida normalización del cortisol sérico es esencial, particularmente en los sujetos pediátricos3. En la actualidad, la principal opción terapéutica en la EC es la adenomectomía transesfenoidal, que presenta buenos resultados. El tratamiento farmacológico de la EC está dirigido a disminuir la secreción esteroidea suprarrenal y se utiliza como una alternativa terapéutica temporal hasta poder realizar la cirugía. Hay escasa experiencia con este fármaco en la edad pediátrica6.
A continuación se presenta el caso de una niña de 13 años con EC, que recibió tratamiento con ketoconazol durante 6 meses en espera de la cirugía transesfenoidal.
Caso clínicoNiña de 13 años y 8 meses con incremento ponderal progresivo desde hacía un año, sin aumento de su ingesta y con disminución de la velocidad de crecimiento, característica que coincidió con un aumento del vello corporal y con hipertensión arterial tratada con restricción de sal. No presentaba antecedentes familiares ni personales de interés. Tenía un peso de 60 kg, una talla de 152,6cm (percentil 25 a 50), un índice de masa corporal de 25,86 (desviación estándar de ±2,1) y una edad ósea de 13 años y medio. En el fenotipo resaltaba obesidad troncular, cara de «luna llena» congestiva, cabello quebradizo y ralo, y jiba de «búfalo». Estaba en el período de la pubertad, sin menarquia, y no había signos de miopatía.
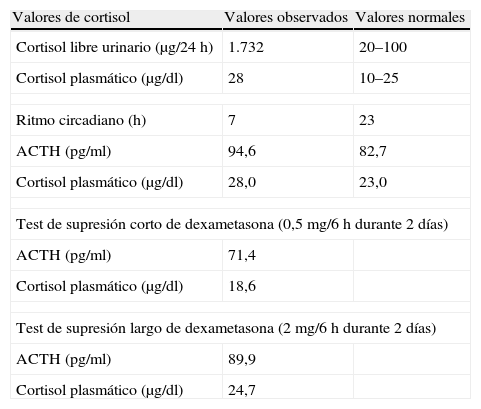
En el estudio analítico, el hemograma y la bioquímica general fueron normales. Las determinaciones hormonales, reflejadas en la tabla 1, indicaron una persistente elevación del cortisol urinario y plasmático así como una pérdida del ritmo circadiano de cortisol y ACTH. Además, se observó la ausencia de supresión del cortisol tras la realización del test corto y largo de supresión de la dexametasona.
Pruebas realizadas para el diagnóstico de hipercortisolismo dependiente de corticotropina
| Valores de cortisol | Valores observados | Valores normales |
| Cortisol libre urinario (μg/24h) | 1.732 | 20–100 |
| Cortisol plasmático (μg/dl) | 28 | 10–25 |
| Ritmo circadiano (h) | 7 | 23 |
| ACTH (pg/ml) | 94,6 | 82,7 |
| Cortisol plasmático (μg/dl) | 28,0 | 23,0 |
| Test de supresión corto de dexametasona (0,5mg/6h durante 2días) | ||
| ACTH (pg/ml) | 71,4 | |
| Cortisol plasmático (μg/dl) | 18,6 | |
| Test de supresión largo de dexametasona (2mg/6h durante 2días) | ||
| ACTH (pg/ml) | 89,9 | |
| Cortisol plasmático (μg/dl) | 24,7 | |
ACTH: corticotropina.
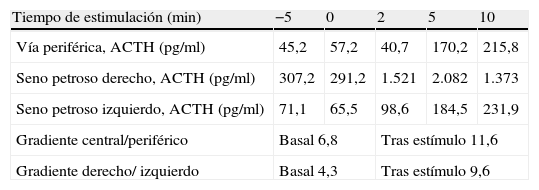
Con diagnóstico de hipercortisolismo dependiente de ACTH, se realizó resonancia magnética (RM) craneal con gadolinio intravenoso que mostró datos indicativos de microadenoma en hemiadenohipófisis derecha. Para su confirmación se realizó un cateterismo selectivo de senos petrosos inferiores con estímulo de corticoliberina (100μg intravenoso) y determinación de ACTH; los resultados se muestran en la tabla 2.
Valores de corticotropina centrales y periféricos y gradientes central/periférico y derecho/izquierdo, tras cateterismo de senos petrosos inferiores: determinaciones basales y a distintos tiempos tras estímulo con corticoliberina (100μg intravenosa)
| Tiempo de estimulación (min) | −5 | 0 | 2 | 5 | 10 |
| Vía periférica, ACTH (pg/ml) | 45,2 | 57,2 | 40,7 | 170,2 | 215,8 |
| Seno petroso derecho, ACTH (pg/ml) | 307,2 | 291,2 | 1.521 | 2.082 | 1.373 |
| Seno petroso izquierdo, ACTH (pg/ml) | 71,1 | 65,5 | 98,6 | 184,5 | 231,9 |
| Gradiente central/periférico | Basal 6,8 | Tras estímulo 11,6 | |||
| Gradiente derecho/ izquierdo | Basal 4,3 | Tras estímulo 9,6 | |||
ACTH: corticotropina.
Con el diagnóstico de EC, y en espera de la cirugía transesfenoidal, se comenzó un tratamiento con 200mg/24h de ketoconazol. Tras 72h la cortisoluria mostró valores de 798μg/24h y tras 12 días mostró valores de 66,42μg/cada 24h. Este control se mantuvo durante 3 meses, tras los que se incrementó la dosis de ketoconazol a 600mg/24h al producirse un «fenómeno de escape». No presentó efectos secundarios a la medicación ni efectos clínicos o bioquímicos.
El estudio anatomopatológico no mostró proliferación adenomatosa en una intervención realizada por vía transesfenoidal a los 6 meses del diagnóstico. Se inició tratamiento sustitutivo con hidrocortisona (10mg/12h) que se suspendió al mes por no presentar en ese momento datos analíticos de insuficiencia suprarrenal.
DiscusiónLa EC es poco frecuente en niños y adolescentes, y se conocen bien las peculiaridades en la edad pediátrica6–12. Tras la confirmación bioquímica de EC es importante intentar ver el microadenoma hipofisario, que es positivo en entre el 22 y el 59% de los sujetos8. El cateterismo de los senos petrosos, que no debe realizarse sistemáticamente, es de gran utilidad para confirmar el origen hipofisario de la ACTH y debe hacerse, sobre todo, cuando la RM no pone de manifiesto el microadenoma. En esta niña, aunque la imagen de la RM era indicativa, se prefirió la confirmación con el cateterismo.
Las alternativas terapéuticas para la EC son la microcirugía pituitaria transesfenoidal y la radioterapia, aunque el tratamiento farmacológico es una alternativa temporal de control6. La microcirugía transesfenoidal da lugar a una alta tasa de remisión inicial en la EC (del 64 al 93% de los casos)5. El término de remisión «aparente» es más apropiado que el de curación2,13 al aparecer recurrencia tras cirugía en seguimientos a largo plazo14. Esta niña lleva 2 años y medio en remisión, aunque el estudio anatomopatológico no mostró pruebas de microadenoma.
Los medicamentos que inhiben la síntesis de esteroides son efectivos para el control del hipercortisolismo y se deben utilizar de manera temporal15. Dentro de los fármacos inhibidores enzimáticos de la síntesis de cortisol, el ketoconazol es de primera elección16. Distintos estudios demuestran que este fármaco es efectivo y generalmente bien tolerado en el tratamiento de la EC17,18; sin embargo, hay que tener en cuenta que el tratamiento medicamentoso es paliativo y que su uso se debe reservar como coadyuvante en la cirugía, en la irradiación de tumores cuando estas 2 opciones hayan fallado o durante el período de espera hasta efectuar radioterapia o cirugía5.
En esta niña se controló el hipercortisolismo con ketokonazol durante el período de 6 meses previo a la cirugía transesfenoidal y, pese al «fenómeno de escape» (solucionado con un aumento de la dosis), tuvo un buen control del hipercortisolismo y de la presión arterial, con una buena tolerancia y sin efectos secundarios destacables. Como el ketoconazol puede elevar las enzimas hepáticas, éstas deben controlarse periódicamente. Un pequeño aumento de éstas puede ser transitorio y suele aparecer entre la primera semana y las 4 semanas siguientes; no obstante, en la mayoría de los casos se puede continuar con el tratamiento6.
Las dosis habituales para el control del hipercortisolismo son de entre 400/24h y 800mg/24h, estas dosis suelen ser bien toleradas14. Aunque hay escasa experiencia de su utilización en la edad pediátrica, también ha demostrado ser eficaz en este grupo de edad6.
El tratamiento sustitutivo de cortisol tras la intervención quirúrgica se encuentra actualmente en discusión5. La niña recibió este tratamiento, que se suspendió al mes tras la normalización de los valores de cortisol y ACTH plasmáticos. A los 7 meses se observó un cambio ostensible en el fenotipo, con aparición de la menarquia, desaparición del hirsutismo y normalización de la presión arterial. Distintos trabajos muestran cómo una determinada proporción de sujetos no presenta valores muy bajos de cortisol sérico tras la cirugía transesfenoidal, aunque permanecen en remisión durante largos períodos de tiempo19,20. Esta niña, si bien no cumple los criterios posquirúrgicos inmediatos de curación2, lleva 2 años y medio en remisión.