Sr. Editor:
La hiperhomocisteinemia es un factor de riesgo conocido en la arterioesclerosis vascular y en la tromboembolia venosa. Presentamos el caso de un recién nacido homocigótico para la mutación C677T en la enzima metil-tetrahidrofolato reductasa (MTHFR) que cursó con trombosis del miembro superior de extraordinaria gravedad.
Neonato varón de 2.490g, hijo único de segunda gestación de 36 semanas, bien controlada y con serología negativa, que nació mediante cesárea urgente por sufrimiento fetal. Sin malformación congénita aparente, pero con pequeña lesión necrótica en flexura brazo izquierdo. Test de Apgar: 3-6-7. Precisó intubación orotraqueal y naloxona. Padres sin relación de consaguineidad y sin historia familiar de fenómenos tromboembólicos. Gestación a término previa sin antecedentes de interés. La madre recibió tratamiento con lorazepam, fluoxetina, periciacina y clomipramina durante la gestación por trastorno obsesivo-compulsivo. Anticuerpos anticardiolipina y antinucleares maternos negativos.
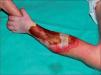
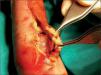
A las 6h de vida se observó una extensión de la escara necrótica al tercio inferior del brazo y antebrazo izquierdo (fig. 1), brazo edematoso y pulsos periféricos palpables simétricos. Se inició antibioterapia intravenosa (ceftazidima y vancomicina) ante la sospecha de un proceso séptico y se realizó amplio desbridamiento quirúrgico de las áreas necrosadas. Se objetivaron necrosis muscular y vasos subcutáneos trombosados (fig. 2).
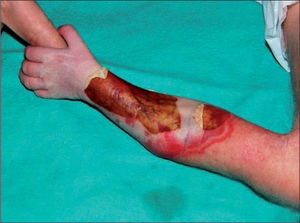
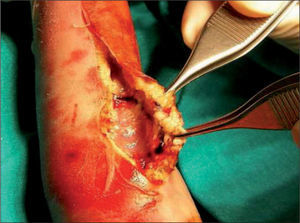
Un día después de la intervención presentaba ausencia de relleno vascular en pulpejos de la mano izquierda. Diagnosticado de trombosis de brazo izquierdo de etiología a filiar, se instauró tratamiento con enoxaparina 4mg/12h por vía subcutánea. Todos los parámetros analíticos fueron normales, excepto unos valores de homocisteína ajustados a la edad de 8,9μm/l, niveles elevados de dímeros D (905μg/l) y una plaquetopenia de 33.000/μl, que impidió la realización de una arteriografía. Se transfundieron dos unidades de plasma fresco. La ecografía Doppler del miembro superior izquierdo mostró las arterias humeral y subclavia de calibre normal y permeables, sin visualizar venas a partir del límite entre tejido sano y necrótico. Se realizó una ecografía cardíaca que no evidenció masas intracardíacas ni alteraciones estructurales, con buena contractilidad. La mala evolución durante los 2 días siguientes hizo necesaria la amputación supracondílea del miembro. Se continuó con la administración de heparina, se suspendió la antibioterapia y el paciente mostró una evolución favorable que le permitió ser extubado 15 días después. Fue dado de alta en tratamiento con enoxaparina y está siendo controlado mensualmente; no ha presentado otro episodio trombótico en 1 año de seguimiento.
El informe anatomopatológico de la pieza amputada describió una trombosis venosa y en capilares en distintos estadios evolutivos de organización que ocluían venas del panículo adiposo y capilares dérmicos sin signos de inflamación vascular, inmunofluorescencia negativa y ausencia de gérmenes. Tras la supresión transitoria de la heparina se realizó un estudio de trombofilia que demostró una actividad de antitrombina III, de proteína C y S y resistencia a la proteína C activada con valores normales. No se detectó la mutación factor V Leiden ni la mutación 20210A del gen de la protrombina. El paciente era homocigótico para la mutación C677T del gen de la enzima MTHFR. Ambos progenitores resultaron ser heterocigotos para el polimorfismo C677T en la enzima MTHFR con valores de homocisteína dentro de los límites normales.
No existen en la actualidad datos que relacionen ninguno de los fármacos consumidos por la madre durante el embarazo con alteraciones metabólicas del folato ni con fenómenos trombóticos perinatales. La mayoría de los fenómenos tromboembólicos comunicados en niños con hiperhomocisteinemia debida a mutación C677T asocian esta alteración con episodios trombóticos cerebrales1–3. La asociación entre la hiperhomocisteinemia moderada y la trombosis venosa ha sido descrita en numerosos estudios4–6. La mutación C677T es también un factor de riesgo para el infarto hemorrágico, independientemente de otros factores de riesgo aterotrombóticos7, y para la aterosclerosis coronaria, cerebral y periférica8, aunque en el paciente estudiado no existían datos clínicos que sugirieran su existencia.
La hiperhomocisteinemia surge como resultado de la combinación de factores genéticos y de componentes relacionados con el estilo de vida. Se ha demostrado que, en pacientes con la mutación C677T en el gen de la MTHFR, las concentraciones de homocisteína son mayores en aquellos con bajas concentra ciones plasmáticas de folato6,9. Sin embargo, no hemos encontrado en la literatura médica asociación entre las variaciones plasmáticas de homocisteína y factores desencadenantes, como el episodio de asfixia perinatal que tuvo lugar en nuestro paciente. No existe ningún caso publicado que relacione la presencia de la mutación homocigótica C677T en el gen de la MTHFR con fenómenos trombóticos en miembro superior de un neonato, en ausencia de otros factores de riesgo aterotrombóticos. En consecuencia, ante un episodio trombótico se deberá descartar hiperhomocisteinemia en todos los pacientes jóvenes y en aquéllos con historia familiar de trombosis o con episodios recurrentes o de localización infrecuente10.