Describir los datos epidemiológicos, clínicos y actitud terapéutica empleada en los lactantes hospitalizados por bronquiolitis en nuestro medio.
Material y métodosEstudio observacional, descriptivo y prospectivo de lactantes menores de 18 meses ingresados en Hospital Virgen de la Arrixaca (Murcia) con el diagnóstico de bronquiolitis, durante el periodo de máxima incidencia (diciembre 2008-abril 2009).
ResultadosIngresaron 235 lactantes, de los que el 78,7% tenía una edad menor o igual a 5 meses de vida. Había una correlación positiva entre el número de cigarrillos consumidos por la madre en la gestación y el número de días de oxigenoterapia y los días de estancia. Los niños cuya madre era fumadora en el momento de su ingreso fueron tratados con oxígeno un mayor número de días. Los lactantes que no habían recibido lactancia materna precisaron oxígeno durante más tiempo. El 23,8% tenía patología de base, siendo la prematuridad la más frecuente, la cual fue un factor de riesgo para la prolongación del tratamiento con oxígeno y de la estancia hospitalaria. La utilización de exploraciones complementarias y el uso de broncodilatadores, corticoides y antibióticos fueron elevados. La aparición de fiebre se asoció a un mayor uso de antibióticos en el medio extra e intrahospitalario y lo mismo sucedía si la radiografía de tórax era patológica o existía una elevación de la proteína C reactiva (PCR). El VRS fue el principal agente etiológico, seguido por rinovirus, bocavirus, adenovirus y metapneumovirus.
ConclusionesLa mayoría de los ingresos por bronquiolitis ocurrieron en los primeros meses de la vida. La exposición al tabaco durante la gestación se asoció a una peor evolución clínica. A pesar de las indicaciones de las guías de práctica clínica, en nuestro medio, el uso de exploraciones complementarias y de tratamientos farmacológicos fue elevado.
To describe the epidemiology, clinical characteristics and treatments prescribed in children with bronchiolitis admitted to our hospital.
Material and methodsObservational, descriptive and prospective study of children younger than 18 months, admitted to Hospital Virgen de la Arrixaca of Murcia (Spain), with the diagnosis of bronchiolitis, during the season of maximum incidence (December 2008-April 2009).
ResultsA total of 235 infants were admitted, of whom 78.7% of them were aged 5 months or less. We found a positive correlation between the number of cigarettes smoked by their mothers during pregnancy and the number of hospitalization and oxygen therapy days. Children whose mothers were smokers at the time of their admission needed a greater number of oxygen therapy days. Also infants who were not breastfed needed oxygen therapy during more days. Just under one quarter (23.8%) of them had underlying diseases, with prematurity being the most frequent and a risk factor for the ongoing of oxygen therapy and hospital stay. The use of diagnostic tests, bronchodilators, corticosteroids and antibiotics was high. The onset of high temperature was associated with an increased use of antibiotics in outside and inside the hospital setting. An abnormal chest X-ray or a raised C-reactive protein was associated with a higher use of antibiotics. Respiratory Syncytial virus (RSV) was the main aetiological agent, followed by Rhinovirus, Bocavirus, Adenovirus and Metapneumovirus
ConclusionsThe majority of hospital admissions due to bronchiolitis took place during the first months of life. Infants whose mothers smoked during pregnancy had a worse clinical outcome. Despite the availability of clinical practice guidelines in our area, the use of diagnostic tests and pharmacological treatment was high.
La bronquiolitis es una enfermedad infecciosa aguda que provoca una obstrucción inflamatoria de la vía respiratoria inferior. Afecta a niños menores de 2 años, con pico máximo de incidencia entre los 3 y los 6 meses. Es considerada la primera causa de ingreso en lactantes menores de un año1. El riesgo de hospitalización varía según los estudios, pero en nuestro medio se establece entre un 1-4%2. En EE. UU. se estimó una tasa de ingreso de 31.2/1.000 lactantes menores de un año en 19963, generando unos costes aproximados de 700 millones de dólares por año4.
El principal virus causante de la bronquiolitis es el virus respiratorio sincitial (VRS)5. Sin embargo, existen múltiples virus implicados en esta patología detectados gracias al desarrollo de nuevas técnicas de biología molecular6,7, como el metapneumovirus8 y el bocavirus9.
La presencia de bronquiolitis está muy relacionada con el ciclo biológico de los virus respiratorios. La estacionalidad de la infección por VRS varía según la zona geográfica10. En nuestro país aparece en los meses fríos (noviembre-abril), con un pico máximo de incidencia entre noviembre y febrero.
El tratamiento es actualmente motivo de controversia. Se basa en medidas de soporte, ya que la mayor parte de los tratamientos farmacológicos no han demostrado una relevancia clínica significativa.
El objetivo principal de nuestro grupo es describir las características epidemiológicas y clínicas y los tratamientos más frecuentemente empleados en los lactantes hospitalizados por bronquiolitis en nuestro entorno.
Material y MétodosEstudio observacional, descriptivo y prospectivo, realizado por observadores externos. Para obtener la población a estudio se incluyó a todos los lactantes menores de 18 meses ingresados en Hospital Universitario Virgen de la Arrixaca de Murcia con el diagnóstico de bronquiolitis, durante el periodo comprendido entre el 1 de diciembre del 2008 y el 30 de abril del 2009.
Criterios de inclusión: el diagnóstico de bronquiolitis se estableció según los criterios de McConnochie11: primer episodio agudo de dificultad respiratoria con sibilancias asociado a cuadro catarral de vías altas en menores de 2 años.
Se obtuvo el consentimiento informado de los padres o tutores legales para la inclusión en el estudio. Se recogieron mediante cuestionario los antecedentes epidemiológicos, los datos clínicos y analíticos y los tratamientos empleados durante el ingreso. Usamos como valoración de gravedad al ingreso el score de Wood-Downes modificado por Ferrés (WDF)12.
Criterios de exclusión: se excluyó a todos los lactantes con episodios previos catalogados de bronquiolitis. De igual forma, se excluyeron las bronquiolitis adquiridas en el medio hospitalario.
Estudio microbiológicoEn todos los pacientes se recogió aspirado nasofaríngeo al ingreso. Se realizó la extracción de ácidos nucleicos mediante el sistema automatizado EasyMag (Biomérieux). Para las pruebas de identificación genética se utilizó una reacción en cadena de la polimerasa reversa (RT-PCR) mediante el kit CLART® Pneumovir (Genómica), que detecta 16 virus respiratorios: VRS A/B, influenza A/B/C, coronavirus (229E), adenovirus, rinovirus, parainfluenza 1-4, metapneumovirus A/B, bocavirus y enterovirus.
Estudio estadísticoSe procesaron los datos mediante el programa estadístico SPSS (Statistical Package of Social Science) versión 16.0. Las variables cuantitativas vienen expresadas por la media±desviación estándar; las cualitativas mediante proporciones. Para los contrastes de hipótesis hemos utilizado los siguientes test estadísticos según el caso: t de Student, U de Mann Whitney, ANOVA, Kruskral-Wallis, χ2, test exacto de Fischer y correlación de Pearson. Hemos considerado estadísticamente significativo un valor de p<0,05.
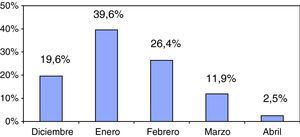
ResultadosSe incluyó en el estudio a 235 lactantes, de los que 126 (53,6%) eran varones. La edad media al ingreso fue de 3,4±3,3 meses. El 78,7% de los lactantes tenían una edad menor o igual a 5 meses de vida y el 11% (26) de los ingresados tenían menos de un mes de vida. La distribución por meses fue: diciembre 19,6% (46 casos), enero 39,6% (93 casos), febrero 26,4% (62 casos), marzo 11,9% (28 casos) y abril 2,5% (6 casos) (fig. 1). Al ingreso, la media de días de evolución fue de 2,83±1,8 días.
Al analizar el hábito tabáquico, encontramos una correlación positiva entre el número de cigarrillos consumidos por la madre durante la gestación con el número de días de oxigenoterapia (p<0,001) y el número de días de estancia (p=0,011), independientemente del hábito tabáquico de los padres en el momento del ingreso. Los niños cuya madre era fumadora en el momento de su ingreso fueron tratados con oxígeno un número mayor de días (p=0,022) (tablas 1 y 2).
Análisis de regresión. Variable dependiente: días de estancia
| Coeficiente | IC del 95% | ||
| Sexo | –0,58 | –1,67; 0,49 | p=0,29 |
| Edad (meses) | –0,26 | –0,47; –0,1 | p=0,003 |
| N.° cigarrillos/día durante el embarazo | 0,34 | 0,08; 0,60 | p=0,011 |
| Edad gestacional (semanas) | –0,40 | –0,57; –0,23 | p<0,001 |
| Score Wood-Downes-Ferrés | 0,89 | 0,53; 1,23 | p<0,001 |
| Madre fuma en la actualidad (sí) | 1,10 | –0,79; 2,99 | p=0,251 |
| Padre fuma en la actualidad (sí) | 1,13 | –0,068; 2,33 | p=0,064 |
Análisis de regresión. Variable dependiente: días de oxigenoterapia
| Coeficiente | IC del IC | ||
| Sexo | –0,45 | –1,37; 0,47 | p=0,333 |
| Edad (meses) | –0,24 | –0,41; –0,08 | p=0,004 |
| N.° cigarrillos/día durante el embarazo | 0,44 | 0,22; 0,66 | p<0,001 |
| Edad gestacional (semanas) | –0,32 | –0,46; –0,18 | p<0,001 |
| Score Wood-Downes-Ferrés | 0,81 | 0,51; 1,10 | p<0,001 |
| Madre fuma en la actualidad (sí) | 1,89 | 0,28; 3,48 | p=0,022 |
| Padre fuma en la actualidad (sí) | 0,91 | –0,12; 1,94 | p=0,083 |
Habían recibido lactancia materna el 68,9% (media de 2±1,7 meses), aunque solo mantenían la misma al ingreso el 46,9%. En el análisis de los lactantes que no había recibido lactancia materna observamos que permanecían más tiempo ingresados, aunque las diferencias no son estadísticamente significativas (media 8,2±4,4 versus 7,3±3,6 días; p=0,129); sin embargo, sí encontramos significación en el número de días que precisaban oxígeno frente a los alimentados al pecho (media 5,2±4,3 versus 3,7±2,9 días; p=0,04).
El 23,8% (56) tenían patología de base, siendo la prematuridad la causa más frecuente (46-19,5%), seguida de la cardiopatía (9 casos: 4 aislada, 5 asociada a prematuridad). La prematuridad es un factor de riesgo para la prolongación del tratamiento con oxígeno y de la estancia hospitalaria (tablas 1 y 2) (p<0,001).
En cuanto a la clínica, el 37,8% (89) presentaba fiebre con temperatura máxima media de 38,6±0,6°C. En el 81% de los casos la fiebre fue ≤39°C. La saturación de O2 fue ≤94% en el 46,8%. El score de Wood-Downes medio fue de 4,8±1,5 puntos. La puntuación de WDF es un factor de riesgo para la prolongación del tratamiento con oxígeno y de la estancia hospitalaria (tablas 1 y 2) (p<0,001).
Se realizó control analítico (hemograma y proteína C reactiva [PCR]) al ingreso en el 92,3% (217) de los casos y gasometría venosa en el 82,1% (193) de los lactantes.
Respecto de las pruebas de imagen, en el 85,5% de los niños (201) se realizó una radiografía de tórax, con los siguientes hallazgos: normalidad 14,4% (29), atrapamiento aéreo 58,7% (118), infiltrado 18,4% (37) y atelectasia 8,5% (17). En el análisis de datos consideramos radiografía de tórax patológica aquella que presentaba atelectasia o infiltrado (excluyendo el atrapamiento aéreo), lo que supone casi el 27% de las radiografías.
El 9% (21) había recibido tratamiento antibiótico previo al ingreso, siendo los más usados amoxicilina-clavulánico y cefixima. Encontramos asociación significativa entre la aparición de fiebre (Ta>38°C) y el uso de antibióticos previos (χ213,8; p<0,001).
Un 32,7% de los pacientes (77) recibieron tratamiento antibiótico durante el ingreso. Los antibióticos más usados en nuestro medio fueron las cefalosporinas de tercera generación. En el análisis comparativo de los lactantes que recibían antibióticos frente a los no tratados (tabla 3) encontramos que existía una relación positiva significativa entre la presencia de fiebre (T.ª≥38°C), tener una radiografía patológica y unos valores de la PCR más elevados. Los lactantes que recibían antibióticos en nuestra muestra tenían, además, una mayor edad, permanecían más tiempo en el hospital, recibían más oxigenoterapia y durante más tiempo, e ingresaban con mayor puntuación de gravedad.
Análisis de lactantes que recibieron antibióticos frente a los no tratados
| ATB sí (n=77) | ATB no (n=158) | ||
| Edad (días) | 143,6±116,4 | 106,8±93,4 | p=0,006 |
| Estancia (días) | 9,4±4,7 | 6,4±2,8 | p<0,001 |
| Fiebre (T.a>38°C) | 42 (54,5%) | 47 (29,7%) | p<0,001 |
| Wood-Downes (p) | 5,3±1,6 | 4,5±1,5 | p=0,001 |
| PCR (mg/dl) | 3,6±3,5 | 1,4±1,8 | p<0,001 |
| Rx tórax anormal | 40 (54%) | 14 (9,2%) | p<0,001 |
| Oxígeno | 52 (67,5%) | 77 (48,7%) | p=0,007 |
| Oxígeno (días) | 5,1±4,4 | 3,3±2,2 | p=0,012 |
Respecto del uso de otros tratamientos destacamos: adrenalina 82,1% (193), salbutamol 20,8% (49) y dexametasona por vía oral 15,7% (37). El uso de adrenalina estaba asociado a lactantes de menor edad (media tratados 2,7±2,5 versus no tratados 7,1±4,2 meses; p<0,001), mientras que el uso de salbutamol (media tratados 7,2±3,7 versus no tratados 2,48±2,4 meses; p<0.001) y el de los corticoides (media tratados 6,3±4,6 versus no tratados 2,9±2,8 meses; p<0,001) se asociaba a niños de mayor edad.
Un 55% de los pacientes requirieron oxigenoterapia (129), con una media de 4±3,4 días. En el análisis comparativo de los lactantes que precisaron oxigenoterapia frente a los que no la precisaron (tabla 4) encontramos las siguientes asociaciones estadísticamente significativas: prematuridad, menor saturación de O2 al ingreso, mayor puntuación de gravedad al ingreso, mayor hipercapnia, mayor porcentaje de alteraciones radiográficas y mayor tiempo de estancia.
Análisis de lactantes que recibieron oxigenoterapia frente a los no tratados
| O2 sí (n=129) | O2 no (n=106) | ||
| Estancia (días) | 8,7±4,2 | 5,7±2,5 | p<0,001 |
| Prematuridad | 32 (24,8%) | 14 (13,2%) | p=0,028 |
| Saturación O2 (%) | 93,3±3,9 | 95,8±2,7 | p<0,001 |
| Wood-Downes (p) | 5,3±1,6 | 4,2±1,3 | p<0,001 |
| pCO2 | 48,6±9,7 | 42,9±8,4 | p<0,001 |
| Rx tórax anormal | 44/118 (37,3%) | 10/83 (12%) | p<0,001 |
Catorce lactantes (5,9%) precisaron ingreso en sala de cuidados intensivos (UCI) para soporte respiratorio. La estancia media global fue de 7,4±3,8 días y todos los pacientes evolucionaron satisfactoriamente.
En el estudio etiológico por RT-PCR de las 235 muestras se detectaron 287 virus. El VRS fue el principal agente detectado (56,4%), seguido de rinovirus (13,2%), bocavirus (9,7%), adenovirus (7,3%), metapneumovirus (7,3%), influenza (2,1%), parainfluenza (1,8%), enterovirus (1%) y coronavirus (1%). En el 32% de las muestras se detectó doble infección y en el 4% se aislaron 3 virus. En el 13,2% de las muestras no se detectó ningún virus.
DiscusiónEl objetivo fundamental de nuestro estudio es conocer las características clínicas, epidemiológicas y terapéuticas de la bronquiolitis en lactantes que precisan ingreso hospitalario en nuestro medio, así como comparar nuestra actuación respecto a las indicaciones actuales de las guías de práctica clínica13–17.
La mayoría de los ingresos ocurrieron en los primeros meses de vida, principalmente por debajo de los 5 meses. Publicaciones previas en nuestro país2 han determinado una tasa de ingreso del 3,7% en los menores de 6 meses de vida, descendiendo hasta el 2,5% para los menores de 12 meses.
Detectamos ligero predominio de varones, concordante con estudios previos que establecen un mayor riesgo de ingreso por bronquiolitis en lactantes varones18–20.
Algunos autores19,21 han demostrado que el hábito tabáquico materno durante el embarazo aumentaba significativamente el riesgo de bronquiolitis en el lactante. Este hecho puede explicarse por la peor función pulmonar de niños de madres fumadoras durante la gestación22,23. Nuestros datos demuestran una correlación significativa entre el número de cigarrillos consumidos durante el embarazo y una peor evolución clínica, independientemente del hábito tabáquico de los padres al momento del ingreso. Hemos podido demostrar además que la exposición pasiva al humo de tabaco, medida por el hecho de que la madre sea fumadora en el momento de su ingreso, es también un factor que prolonga los días necesarios de oxigenoterapia.
La importancia de la lactancia materna como factor protector de ingreso por infecciones respiratorias de vías bajas ha sido bien establecida18,24–26. En efecto, en nuestra revisión encontramos una clara tendencia a que los niños que no recibieron lactancia materna presentaran una evolución más tórpida, con mayor tiempo de estancia, aunque no alcanza nivel estadísticamente significativo, pero sí en el caso del tiempo necesario de tratamiento con oxígeno (p=0,04).
La prematuridad fue un factor de riesgo para la prolongación de su estancia y de la oxigenoterapia, dato concordante con revisiones previas16,27.
A pesar de la escasa utilidad demostrada de las exploraciones complementarias, detectamos un uso elevado. El papel de la radiografía de tórax debería limitarse a pacientes con evoluciones tórpidas28–30. De hecho, no existen suficientes datos que relacionen las alteraciones radiográficas como predictivas de un curso evolutivo diferente31. En nuestra serie, encontramos un 27% de radiografías patológicas, excluyendo el atrapamiento aéreo aislado, concordante con datos de otras series publicadas30,32. A menudo, una radiografía de tórax con atelectasias y/o infiltrados es probablemente interpretada como una sobreinfección bacteriana, asociándose a un mayor uso de antibióticos, como muestran nuestros resultados.
El estudio analítico para el cribado de infecciones bacterianas no está recomendado de rutina; se puede valorar su utilización en pacientes con fiebre persistente, cuadros graves o en el periodo neonatal16. Sin embargo, en nuestro medio su utilización es muy frecuente.
Las actuales guías de práctica clínica13–17 no recomiendan el uso rutinario de salbutamol en el tratamiento de la bronquiolitis por no haberse demostrado una mejoría clínica significativa. Se acepta que puede ensayarse en pacientes con cuadros moderados-graves, evaluando estrechamente la respuesta clínica. La revisión Cochrane sobre la adrenalina nebulizada33 establece que su uso no debe ser rutinario en pacientes ingresados, valorándose de manera individual en formas moderadas-graves en menores de 6 meses. En nuestra experiencia detectamos una amplia utilización de salbutamol en lactantes mayores de 6 meses y adrenalina en niños por debajo de esta edad.
La revisión Cochrane sobre el uso de corticoides en la bronquiolitis34 no encuentra beneficios significativos en el score clínico y/o el tiempo de estancia de pacientes ingresados; a pesar de ello un 15,7% de nuestros niños recibieron dexametasona por vía oral. Sin embargo, continúa el debate dada la existencia de estudios35,36 que encuentran datos favorables con dexametasona. Destacamos el grupo de Plint et al.36, que describe un descenso en la hospitalización de lactantes a los 7 días de recibir en urgencias adrenalina nebulizada y dexametasona por vía oral oral frente al placebo.
La utilización de antibióticos en nuestro medio fue elevada aunque, como es conocido, el riesgo de infección bacteriana en la bronquiolitis es bajo (1-2%)37–39. El grupo que recibió antibióticos tenía mayor edad y permanecía más tiempo en el hospital; la presencia de valores de PCR más elevados y el mayor porcentaje de fiebre y de radiografías patológicas podrían explicar la sospecha del clínico de sobreinfección bacteriana en nuestra muestra.
El VRS ha sido el principal agente etiológico detectado en nuestra población, aunque la presencia de otros virus respiratorios ha sido elevada. La frecuencia de coinfecciones es similar a datos publicados por otros autores en los últimos años6,40.
En conclusión, la mayor parte de los ingresos por bronquiolitis ocurrieron en los primeros meses de la vida. En nuestra muestra la exposición al tabaco durante la gestación fue un factor asociado a una peor evolución clínica. Los datos sugieren que los lactantes alimentados al pecho tienen una evolución más favorable. A pesar de las indicaciones de las guías de práctica clínica, en nuestro medio, el uso de exploraciones complementarias y del resto de los tratamientos farmacológicos fue elevado. La fiebre, las alteraciones radiográficas y la elevación de la PCR se relacionaron con un mayor uso de antibióticos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.