Las hemoglobinopatías constituyen uno de los desórdenes hereditarios más comunes en humanos, y en Venezuela representan un problema de salud pública. En esta investigación se evaluó la prevalencia de las hemoglobinopatías en neonatos de diferentes áreas de Venezuela, en cooperación con el sistema de cribado neonatal de la Unidad de Estudios de Errores Innatos del Metabolismo del Instituto de Estudios Avanzados.
Materiales y métodosLas muestras de sangre del talón de 101.301 neonatos se estudiaron por medio de la técnica de cromatografía líquida de alta resolución de intercambio catiónico (HPLC-CE), utilizando el equipo Variant® Bio-Rad y los programas Sickle Cell Short para el análisis en papel de filtro y Beta Thal Short para el estudio confirmatorio y familiar.
ResultadosSe encontró una alta prevalencia de neonatos heterocigotos para las hemoglobinas (Hb) S y C (Hb S y Hb C). Se observó que el 1,96% (1.989) de los neonatos fueron portadores de alguna variante, y el fenotipo más frecuente fue Hb fetal AS (67,92%), seguido de Hb fetal AC (23,18%), Hb fetal AD (7,49%), Hb fetal SC (0,96%) y Hb fetal SD (0,20%). A todos los niños estudiados (positivos en el cribado), luego de los 3 meses de edad se les confirmó la presencia de alguna variante estructural mediante una segunda prueba confirmatoria.
ConclusionesLas frecuencias de las variantes encontradas en este estudio confirman que las hemoglobinopatías representan un problema de salud pública en Venezuela, y debe enfatizarse la importancia de instaurar en este país un programa de detección sistemática de hemoglobinopatías que comprenda no sólo un tratamiento precoz, sino también un programa de educación y consejo genético para el grupo familiar.
Hemoglobinopathies are the most common hereditary disorders in humans representing a public health problem in Venezuela. In this study the prevalence of hemoglobinopathies was evaluated in newborns from different areas of Venezuela, in cooperation with the neonatal screening system of the Study Unit of Inborn Errors of Metabolism (IDEA).
Materials and methodsThe heel blood samples of 101,301 newborns were analysed by high performance liquid chromatography (HPLC-CE) technique using Variant* Bio Rad System with the Sickle Cell Short program for the filter paper samples in and the Beta Tal Short program for the family studies.
ResultsWe found a high prevalence of newborns heterozygous for hemoglobin S and C (Hb S and Hb C). It was observed that 1.96% (1989) of the newborns were carriers, with Hb FAS (67.92) being the most frequent phenotype, followed by Hb FAC (23.18%), Hb FAD (7.49%), Hb FSC (0.96%),) and Hb FSD (0.20%). All the neonatal positives cases were confirmed at 3 months of age.
ConclusionsThe frequencies of the variants found in this study confirms that the hemoglobin disorders are a public health problem in Venezuela, emphasizing the importance of instituting a national program of screening for hemoglobinopathies throughout the country, comprising not only an early treatment, but also an educational program and genetic counseling for the family group.
Las hemoglobinopatías resultan de mutaciones en los genes que codifican las cadenas globínicas α y β de la molécula de hemoglobina (Hb), y son los desórdenes hereditarios más comunes en los seres humanos1: afectan aproximadamente al 7% de la población mundial2 y están caracterizados por la síntesis reducida o la ausencia de las cadenas globina (talasemias), o por la síntesis de cadenas estructuralmente anormales de la molécula de Hb (variantes estructurales).
Actualmente, se han descrito más de 1.200 mutaciones en los genes que codifican las cadenas globinas. No obstante, las más frecuentes en Venezuela y clínicamente significativas son las variantes estructurales S, C y la betatalasemia3,4.
La Hb S es la variante estructural más común y resulta de la sustitución del ácido glutámico por valina en la posición 6 de la cadena betaglobina5. Su herencia en forma homocigota produce un cuadro clínico denominado drepanocitosis o anemia falciforme. Pertenece al grupo de las hemoglobinopatías estructurales, que son una enfermedad genética autosómica recesiva, que puede expresarse bajo 4 formas diferentes: primero, la forma heterocigota, conocida también como rasgo falciforme, rasgo drepanocítico o portador de Hb AS; segundo, la forma homocigota o anemia de células falciforme; tercera, el doble heterocigoto HbS-betatalasemia y, por último, el doble heterocigoto con otras variantes estructurales, tales como Hb C y Hb D6.
El gen falciforme generalmente sólo produce manifestaciones clínicas en el estado homocigoto o en los dobles heterocigotos; los individuos con el rasgo falciforme, por lo general, son asintomáticos y no presentan anemia.
La Hb C es una variante de la Hb que se forma por la sustitución del ácido glutámico por lisina; es una mutación puntual en la posición 6 de la cadena betaglobina y representa la segunda en frecuencia mundial. La Hb C induce la deshidratación del eritrocito y la formación intracelular de cristales. Los individuos homocigotos (CC) presentan sintomatología caracterizada por anemia hemolítica de intensidad de leve a moderada7. El doble heterocigoto Hb SC frecuente en nuestra población conduce a un desorden falciforme grave; sin embargo, es menos grave comparado con el que produce la anemia drepanocítica.
En Venezuela, desde hace varias décadas, se han estudiado la frecuencia y la distribución de las diferentes hemoglobinopatías, teniendo siempre como meta la búsqueda y la implementación de diferentes metodologías para identificar los pacientes antes de que aparezcan síntomas clínicos irreversibles8–16.
La anemia falciforme o anemia drepanocítica cumple con todas las características que se exigen para incluirla en los estudios de diagnóstico precoz17, por lo que su estudio sistemático se hace inminente.
Se ha establecido que el diagnóstico neonatal de la anemia falciforme puede disminuir sustancialmente la morbimortalidad durante los 5 primeros años de vida de los infantes18,19. De allí la necesidad de incorporar en Venezuela, donde la drepanocitosis representa un problema de salud pública, una red de cribado neonatal. En Venezuela, el programa de diagnóstico neonatal de hemoglobinopatías se inició en el año 2006, y se unió a la red de cribado neonatal de fenilcetonuria e hipotiroidismo de la Unidad de Errores Innatos del Metabolismo del Instituto de Estudios Avanzados (IDEA).
En algunos países de Europa20–22 y Norteamérica1,23, la detección de hemoglobinopatías estructurales como parte de sus programas de cribado neonatal23 es de carácter obligatorio, lo que ha aportado importantes datos sobre la distribución y la prevalencia de estas variantes en la población infantil.
Por otro lado, esta información proporciona a los trabajadores de la salud una oportunidad para realizar supervisión médica precozmente a los neonatos, incorporarlos al tratamiento profiláctico, y darles asesoramiento genético y orientación a sus familiares20.
Materiales y métodosEste estudio se llevó a cabo en el Laboratorio de Investigación de Hemoglobinas Anormales (LIHA), ubicado en el Hospital Universitario de Caracas, y en el Instituto Anatómico José Izquierdo de la Facultad de Medicina de la Universidad Central de Venezuela, en cooperación con el IDEA. El Comité de Bioética del Hospital Universitario de Caracas aprobó este estudio siguiendo las directrices de la declaración de Helsinki y del Código de Bioética y Bioseguridad del FONACIT.
MuestrasSe analizaron 101.301 neonatos provenientes de diferentes centros hospitalarios del país. Previa exposición de los beneficios del programa y obtenido el consentimiento informado de los padres, se tomaron muestras de sangre del talón de infantes entre los 2 y los 5 días de vida, y se impregnaron en papel de filtro siguiendo el método de Guthrie. Las muestras se remitieron al IDEA, donde se codificaron y se cortaron en discos de 3mm de diámetro. Luego se colocaron en placas de ELISA y se trasladaron al LIHA, donde se catalogaron, se eluyeron y se procesaron.
Elusión de las muestrasLas muestras se colocaron en tubos eppendorf de 1,5ml, se eluyeron del papel de filtro con 500μl de KCN 0,5mM, y se incubaron 12h a 4°C.
Análisis de las muestrasPara realizar el diagnóstico de las muestras, se empleó la técnica de cromatografía líquida de alta resolución de intercambio catiónico (HPLC-CE), usando el equipo automatizado Variant I Hemoglobin Testing System® y el programa Sickle Cell Short (Bio-Rad, Cal, EE. UU.).
El Variant Hemoglobin Testing System® es un equipo de HPLC automatizado que usa una minicolumna que contiene en su interior una resina o material polimérico de intercambio catiónico. El sistema usa 2 soluciones amortiguadoras de fosfato para la elución, con diferentes concentraciones, que se introducen dentro del flujo analítico a una tasa controlada de 2ml/min. El analizador muestra los cromatogramas e imprime los resultados a los 3 min de la inyección. El número máximo de muestras en cada proceso analítico fue de 97, con un tiempo total de 5h. Se usaron controles de Hb fetal AES y Hb fetal ADC de concentraciones conocidas, aproximadas a las esperadas en las muestras de los neonatos.
Una vez que se determinó la presencia de alguna de las variantes estructurales de la Hb (casos positivos), los resultados se enviaron a los diferentes centros hospitalarios de procedencia.
Todos aquellos casos positivos se estudiaron nuevamente junto con su grupo familiar pasados los 3 meses de edad, y así se confirmó la presencia de esas enfermedades.
Confirmación de casos positivosPara realizar la confirmación de los casos positivos, se empleó la misma técnica del HPLC pero con el programa Beta-Thalassemia Short (Bio-Rad), que es un método diseñado para cuantificar las Hb A2 y F. Este programa se demora 6,5min en analizar cada muestra. Este método también permite cuantificar otras Hb, incluyendo la A, la S, la C, la D y la E, en muestras de sangre periférica.
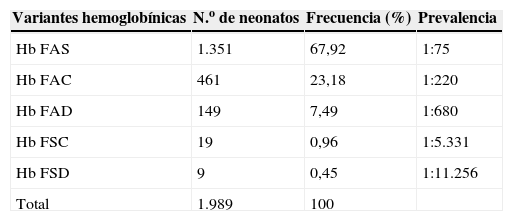
ResultadosLuego del análisis de las 101.301 muestras de sangre de talón de neonatos provenientes de diferentes centros hospitalarios de Venezuela, se encontró que 1.989 (1,96%) recién nacidos presentaron alguna variante estructural conocida. Los fenotipos más frecuentes fueron Hb fetal AS y Hb fetal AC, seguidos de Hb fetal AD, Hb fetal SC y Hb fetal SD (tabla 1), lo que confirmó, una vez más, que la Hb S es la variante estructural más frecuente en Venezuela, seguida por las variantes C y D.
Prevalencia de las variantes hemoglobínicas diagnosticadas en recién nacidos provenientes de diferentes centros hospitalarios de Venezuela
| Variantes hemoglobínicas | N.o de neonatos | Frecuencia (%) | Prevalencia |
| Hb FAS | 1.351 | 67,92 | 1:75 |
| Hb FAC | 461 | 23,18 | 1:220 |
| Hb FAD | 149 | 7,49 | 1:680 |
| Hb FSC | 19 | 0,96 | 1:5.331 |
| Hb FSD | 9 | 0,45 | 1:11.256 |
| Total | 1.989 | 100 |
Hb FAC: hemoglobina fetal AC; Hb FAD: hemoglobina fetal AD; Hb FAS: hemoglobina fetal AS; Hb FSC: hemoglobina fetal SC; Hb FSD: hemoglobina fetal SD.
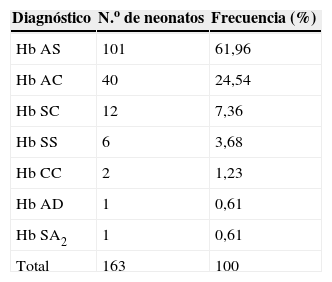
De los neonatos que resultaron positivos para alguna de las variantes estructurales, se les realizó estudios de confirmación a 163 de ellos (tabla 2). En todos los casos estudiados no se encontró ningún caso falso positivo.
Frecuencia de las variantes hemoglobínicas confirmadas en recién nacidos de diferentes centros hospitalarios de Venezuela
| Diagnóstico | N.o de neonatos | Frecuencia (%) |
| Hb AS | 101 | 61,96 |
| Hb AC | 40 | 24,54 |
| Hb SC | 12 | 7,36 |
| Hb SS | 6 | 3,68 |
| Hb CC | 2 | 1,23 |
| Hb AD | 1 | 0,61 |
| Hb SA2 | 1 | 0,61 |
| Total | 163 | 100 |
Hb AC: hemoglobina AC; Hb AD: hemoglobina AD; Hb AS: hemoglobina AS; Hb CC: hemoglobina CC; Hb SA2: hemoglobina SA2; Hb SC: hemoglobina SC; Hb SS: hemoglobina SS.
En el estudio confirmatorio, la variante S siguió siendo la más frecuente. De los 163 neonatos reestudiados, 120 presentaron la Hb S en cualquiera de sus combinaciones (73,62%); de éstos, 101 fueron portadores (Hb AS) y 6 fueron homocigotos para la Hb S (tabla 2). Sólo se encontró un infante con Hb SA2, al que se catalogó inicialmente como Hb AS en la prueba de primera intención. El diagnóstico se complementó con el estudio de todo el grupo familiar.
DiscusiónEste estudio confirmó que la Hb S es la de mayor prevalencia entre las variantes estructurales encontradas en los neonatos estudiados. Estos resultados están en concordancia con los obtenidos en diferentes estudios de tamizaje neonatal llevados a cabo en varias regiones de Brasil y Colombia, donde la Hb S también fue la de mayor prevalencia24–27, lo que indica que la alta incidencia de esta variante posiblemente se deba a la mezcla racial, con un alto componente africano proveniente de diferentes regiones de África e introducido durante la colonia con la llegada de los esclavos a América5,26–27.
Los beneficios del diagnóstico y la intervención precoz en esta enfermedad tienen una amplia difusión en todo el mundo con sistemas para la detención temprana de estas afecciones28. Por medio de los programas de cribado neonatal de hemoglobinopatías se logra reducir las tasas de morbimortalidad en los primeros 5 años de vida. Además, el uso profiláctico de penicilina, la administración de vacunas antineumococo y otros cuidados especializados29 aumentan significativamente la sobrevida y la calidad de vida de los niños con anemia drepanocítica, y disminuyen las secuelas y las complicaciones clínicas30; éste es el fundamento principal del cribado neonatal de hemoglobinopatías31.
La cromatografía líquida de alta resolución con el programa Sickle Cell Short está específicamente diseñada para proporcionar un resultado cualitativo de las Hb A, F, S, C, D y E. Para los propósitos del cribado o el tamizaje neonatal, un resultado cualitativo es todo lo que se requiere inicialmente. Esta técnica es ampliamente usada para el cribado y la confirmación de hemoglobinopatías en recién nacidos, con una alta especificidad y sensibilidad. Con ella se pueden detectar las variantes estructurales más ampliamente extendidas por todo el mundo en un tiempo muy corto (3min/muestra), lo que es necesario debido al gran número de muestras que deben procesarse. Otra de las bondades que presenta esta metodología es que permite trabajar con concentraciones de muestras muy pequeñas, lo que facilita el trabajo en conjunto con otros programas de cribado, como es nuestro caso, pues debe recordarse que por la corta edad de los neonatos existe la dificultad de tomar grandes cantidades de sangre. Recientemente, se han reportado las ventajas de la utilización de la técnica de HPLC-CE en el estudio de las hemoglobinopatías en Venezuela16, que ha demostrado ser sensible y precisa en el estudio de grandes volúmenes de muestras, así como tener alto poder de resolución y reproducibilidad de los resultados.
Otro objetivo importante de los programas de cribado neonatal de hemoglobinopatías es el estudio del grupo familiar, lo que permite diagnosticar a uno o a ambos padres y a otros hijos, si los hubiera, con la finalidad de informarles su riesgo y, al mismo tiempo, proporcionarles consejo genético y sobre las opciones para evitar nuevos embarazos, debido a que en varios de los casos estudiados se encontró a hermanos también portadores e incluso de otras variantes hemoglobínicas.
Las técnicas de detección utilizadas hasta ahora han demostrado ser de gran sensibilidad y especificidad; el 100% de las familias a las que se les realizó la reconfirmación (estudio de segunda intención, tabla 2) fueron positivas para una o 2 alteraciones. Actualmente se está optimizando el canal de comunicación entre el laboratorio de diagnóstico, los diferentes centros hospitalarios y los familiares, con el fin de que cada vez sean más los grupos familiares estudiados. En este sentido, se está coordinando un grupo multidisciplinario que permita orientar al paciente no sólo desde el punto de vista clínico, sino también psicológico y social, lo que permitirá una atención integral y su incorporación total a la sociedad.
La alta incidencia de variantes estructurales en Venezuela5,16 se ha convertido en un problema de salud pública y, aunado a la alta distribución de la Hb S entre los neonatos estudiados, evidencia la necesidad de establecer de manera permanente el cribado universal de hemoglobinopatías en la población venezolana.
FinanciaciónEste trabajo fue financiado por el FONACIT S1-200200539, G-2005000373, MC 2007001066. ECOS- NORD PI2007001066 y CODECIH-UC 2005-011.
A los padres de los recién nacidos por haber permitido realizar este estudio. Al IDEA por la codificación y el traslado de las muestras. Al personal de toma de muestra por su valioso trabajo.