El tratamiento nutricional primario (TNP), que consiste en la administración de dieta exclusiva con fórmula enteral (polimérica, semielemental o elemental) durante un período no inferior a 6-8 semanas, ha demostrado ser efectivo para inducir la remisión clínica en niños afectados de enfermedad de Crohn. La remisión clínica no siempre conlleva la remisión histológica o la curación de la mucosa. La calprotectina fecal es un excelente marcador de la actividad inflamatoria intestinal y sus concentraciones se correlacionan estrechamente con el grado de inflamación de la mucosa intestinal.
Pacientes y métodosSe ha realizado un estudio prospectivo observacional en el que se incluyeron todos los pacientes menores de 14 años diagnosticados de enfermedad de Crohn entre enero de 2002 y octubre de 2007 que recibieron alimentación exclusiva con fórmula polimérica (Modulen IBD, Nestlé, Vevey, Suiza) durante su primer brote de enfermedad. Se establecieron controles clínicos (peso, talla, índice de masa corporal, índice de actividad de la enfermedad de Crohn pediátrica [PCDAI]) y determinaciones de calprotectina fecal al inicio, y a las 4 y 8 semanas de tratamiento. La remisión clínica se definió cuando el PCDAI era igual o inferior a 10. Se consideraron normales valores de calprotectina fecal inferiores a 50 μg/g de heces.
ResultadosSe incluyeron 14 pacientes (9 varones), con una edad media en el momento del diagnóstico de 10,74±2,56 años. A las 4 semanas, el 71 % de los pacientes alcanzaron la remission clínica, que se acompañó de un descenso no significativo de las cifras de calprotectina fecal. A las 8 semanas, el 85 % de los pacientes logró la remisión clínica y los valores de calprotectina fecal habían descendido de forma significativa, aunque sin alcanzar concentraciones normales.
ConclusiónEl TNP administrado durante un período de 8 semanas puede inducir la remisión clínica y mejorar el grado de inflamación de la mucosa intestinal.
The primary nutritional therapy (PNT), which consists in the administration of exclusive enteral formula feeds (polymeric, semi-elemental or elemental formula) for a period of no less than 6-8 weeks, has proven to be effective in inducing clinical remission in children with Crohn's disease. The clinical remission does not always include histological remission or cure of the mucosa. Faecal calprotectin is closely correlated with endoscopic and histological findings but is slightly associated with clinical activity scores.
Patients and methodsAn observational prospective study including all patients under 14 years of age diagnosed with Crohn's disease between January 2002 and October 2007, and who were fed exclusively with polymeric formula (Modulen IBD, Nestle, Vevey, Switzerland) during the onset of the disease. Clinical controls were carried out (weight, height, body mass index [BMI) and the Paediatric Crohn's Disease Activity Index [PCDAI)) and faecal calprotectin was measured at the beginning and at weeks 4 and 8 of treatment. The clinical remission was defined as having a PCDAI less than or equal to 10. Faecal calprotectin values below 50 μg/g faeces were considered as normal.
ResultsThere were 14 patients (9 males), mean age at diagnosis of 10.74±2.56 years. At week 4, 71 % of patients (10/14) had achieved clinical remission and a decrease in faecal calprotectin levels that was not significant. After 8 weeks, 85 % of our patients were in clinical remission and faecal calprotectin values had declined significantly without reaching normal levels.
ConclusionPrimary nutritional therapy administered over a period of 8 weeks is capable of inducing clinical remission and improving the degree of inflammation of the intestinal mucosa.
La enfermedad de Crohn es un trastorno inflamatorio crónico que afecta a uno o a varios segmentos del tracto digestivo (desde la boca hasta el ano) de forma discontinua, que cursa en forma de brotes y que, en ocasiones, se acompaña de manifestaciones extradigestivas. La inflamación se extiende a menudo hasta la serosa, las zonas inflamadas se alternan con áreas sanas y es frecuente que se formen fístulas. El intestino delgado está afectado en el 90 % de los casos, sobre todo el íleon terminal (en el 70% de los casos). En más del 50 % de las ocasiones la localización es ileocólica y en el 10 %, sólo colónica. La incidencia de la enfermedad de Crohn en España oscila entre 0,4 y 5,5 casos × 105 habitantes/año, con un valor medio de 1,9 casos × 105 habitantes/año y con una importante variabilidad geográfica1. El 20-30 % de los nuevos casos de enfermedad de Crohn se diagnostican en menores de 18 años. Una peculiaridad de la enfermedad de Crohn pediátrica es su repercusión sobre el crecimiento y el desarrollo puberal. En el 5 % de los pacientes el fallo del crecimiento puede ser la única manifestación de la enfermedad. El objetivo fundamental del tratamiento de la enfermedad de Crohn es la curación de la mucosa y a éste se añaden: mejorar la calidad de vida, recuperar y mantener un crecimiento adecuado, asegurar un desarrollo puberal correcto y prevenir complicaciones a largo plazo derivadas de la enfermedad y del tratamiento empleado2.
El tratamiento nutricional primario (TNP) consiste en la administración de dieta exclusiva con fórmula enteral durante un período no inferior a 6–8 semanas. Esta pauta ha demostrado ser efectiva para inducir la remisión clínica en niños afectados de enfermedad de Crohn con tasas de respuesta cercanas al 80%3–5. La remisión clínica no siempre se asocia con la remisión histológica o con la curación de la mucosa. La endoscopia digestiva con toma de biopsias y su posterior análisis histológico es la herramienta utilizada con patrón de referencia para conocer el grado de inflamación intestinal. Es una técnica invasiva y cara, que precisa una preparación cuidadosa del colon y anestesia general para su realización. Las colonoscopias seriadas para comprobar la remisión histológica no están al alcance de todos los centros sanitarios y suelen ser mal aceptadas por parte de los pacientes y de sus familiares. En la actualidad se dispone de métodos de laboratorio que informan acerca del estado inflamatorio intestinal. Entre ellos destacan la cuantificación en sangre/heces de proteínas derivadas de los leucocitos (proteína catiónica eosinofílica, esterasa, mieloperoxidasa, lisozima, lactoferrina o calprotectina). Esta última es la proteína que más abunda en el citoplasma del neutrófilo y del macrófago, es muy estable en las heces, permanece inalterada durante más de 7 días, permitiendo la conservación de las muestras hasta su envío y análisis. Es un marcador no invasivo, con alta sensibilidad y especificidad, que permite monitorizar la actividad inflamatoria en niños y adultos, y predecir la recaída clínica6,7. Las concentraciones de calprotectina fecal están estrechamente relacionadas con los hallazgos endoscópicos e histológicos. Es un test de ELISA simple y económico, que requiere una cantidad mínima de heces (50–100 mg) para su realización. Los valores aceptados como normales de calprotectina fecal en niños mayores de 1 año son de 50 μg/g de heces, con una sensibilidad del 90 % y una especificidad del 83 % para correlacionarlos con procesos inflamatorios intestinales8–13.
Los objetivos de nuestro estudio son los siguientes:
- 1.
Determinar la eficacia del TNP para inducir la remisión clínica en el primer brote de enfermedad de Crohn en niños.
- 2.
Determinar la eficacia del TNP para mejorar el grado de inflamación de la mucosa intestinal utilizando como marcador la calprotectina fecal.
- 3.
Estimar la tasa de cumplimiento del TNP.
En este estudio prospectivo observacional se incluyeron todos los pacientes menores de 14 años diagnosticados de enfermedad de Crohn atendiendo a criterios clínicos, radiológicos, endoscópicos y anatomopatológicos entre enero de 2002 y octubre de 2007, y que recibieron alimentación exclusiva con fórmula polimérica (Modulen IBD, Nestlé, Vevey, Suiza) durante el primer brote de su enfermedad. Quedaron excluidos los pacientes diagnosticados de colitis ulcerosa, colitis indeterminada, colitis eosinofílica o colitis infecciosa, así como los diagnosticados de enfermedad de Crohn que recibieron tratamiento concomitante o previo con corticoides y/o fármacos inmunosupresores (azatioprina, 6-mercaptopurina, entre otros).
Modulen IBD se preparó mezclando 1.700 ml de agua con 400 g de producto, lo que daba lugar a 2.000 ml de una fórmula normocalórica (1 kcal/ml). El cálculo de las necesidades energéticas se estimó mediante la fórmula de Schofield. La pauta de administración fue de 4–5 tomas al día, y sólo se permitía la ingestión de agua durante el tratamiento.
Los datos recogidos fueron edad, sexo, antecedentes familiares de enfermedad inflamatoria intestinal crónica (EIIC), tiempo transcurrido hasta el diagnóstico y tratamiento farmacológico asociado (5-aminosalicilatos [5-ASA] y/o metronidazol). El fenotipo de la enfermedad de Crohn se estableció atendiendo a la clasificación de Montreal (tabla 1)14.
Clasificación de Montreal de la enfermedad de Crohn14
| Edad en el momento del diagnóstico | (A) | |
| < 16 años | A1 | |
| 17-40 años | A2 | |
| > 40 años | A3 | |
| Localización | (L) | |
| Íleon terminal | L1 | L1 + L4 (íleon + tracto digestivo alto) |
| Colon | L2 | L2 + L4 (colon + tracto digestivo alto) |
| Ileocólica | L3 | L3 + L4 (ileocólica + tracto digestivo alto) |
| Tracto digestivo alto | L4 | |
| Patrón clínico | (B) | |
| Inflamatorio | B1 | B1p (inflamatorio con afección perianal asociada) |
| Estenosante | B2 | B2p (estenosante con afección perianal asociada) |
| Fistulizante | B3 | B3p (fistulizante con afección perianal asociada) |
Todos los pacientes fueron valorados al inicio del tratamiento, a las 4 semanas y al final de la octava semana de tratamiento. En estos tres controles se recogieron los siguientes datos: peso, talla, índice de masa corporal (IMC), calprotectina fecal (Calprest, Eurospital, Italia) y se determinó el índice de actividad de la enfermedad de Crohn pediátrica (PCDAI)15 (tabla 2). La remisión clínica se definió cuando el PCDAI era igual o inferior a 10. Se consideraron como normales valores de calprotectina fecal inferiores a 50 μg/g de heces.
Índice de actividad de la enfermedad de Crohn en niños (PCDAI)14
| Puntos | ||||
| 1. Historia clínica (recuerdo de una semana) | ||||
| Dolor abdominal | ||||
| Ninguno | 0 | |||
| Leve, de corta duración, no interfiere con la actividad normal | 5 | |||
| Intenso, de larga duración, afecta a la actividad normal, nocturno | 10 | |||
| Deposiciones (por día) | ||||
| 0-1 deposiciones líquidas, con ausencia de sangre | 0 | |||
| Hasta 2 deposiciones semiblandas con sangre o 2–5 deposiciones líquidas | 5 | |||
| Sangrado abundante o > 6 deposiciones líquidas o diarrea nocturna | 10 | |||
| Estado general y capacidad funcional | ||||
| Bueno. Actividad no limitada | 0 | |||
| Regular. Dificultades ocasionales para mantener las actividades habituales | 5 | |||
| Muy deficiente. Limitaciones frecuentes de las actividades | 10 | |||
| 2. Analítica | ||||
| Velocidad de sedimentación globular (mm/h) | ||||
| < 20 | 0 | |||
| 20-50 | 2,5 | |||
| > 50 | 5 | |||
| Albúmina (g/l) | ||||
| > 35 | 0 | |||
| 31-34 | 5 | |||
| < 30 | 10 | |||
| Hematocrito (%) | ||||
| < 10 anos | Varón 11-14 años | Varón 15–19 años | Mujer 11–19 años | |
| > 33 | > 35 | > 37 | > 34 | 0 |
| 28–32 | 30–34 | 32–36 | 29–33 | 2,5 |
| < 28 | < 30 | < 32 | < 29 | 5 |
| 3. Exploración | ||||
| Peso | ||||
| Aumento de peso, peso estable voluntario o adelgazamiento | 0 | |||
| Peso estable involuntario, adelgazamiento del 1 al 9 % | 5 | |||
| Adelgazamiento > 10 % | 10 | |||
| Abdomen | ||||
| No se observan masas abdominales ni dolor con la palpación | 0 | |||
| Dolor con la palpación o masas abdominales sin dolor con la palpación | 5 | |||
| Dolor con la palpación, contractura abdominal o masa abdominal definida | 10 | |||
| Talla (completar sólo en el momento del diagnóstico) | ||||
| Disminución de menos de 1 escala (1 escala = 2 percentiles) | 0 | |||
| Disminución de 1 a 2 escalas | 5 | |||
| Disminución de más de 2 escalas | 10 | |||
| Talla (completar sólo durante el seguimiento) | ||||
| Velocidad de crecimiento > —1 DE | 0 | |||
| Velocidad de crecimiento < —1 DE o > —2 DE | 5 | |||
| Velocidad de crecimiento > —2 DE | 10 | |||
| Enfermedad perirrectal | ||||
| Número de colgajos o papilomas cutáneos asintomáticos | 0 | |||
| 1-2 fístulas indoloras, drenaje, sin dolor con la palpación | 5 | |||
| Fístulas activas, drenaje, dolor con la palpación o absceso | 10 | |||
| Manifestaciones extraintestinales | ||||
| No | 0 | |||
| 1 | 5 | |||
| 2 o más | 10 | |||
Puntuación total (0 a 100): PCDAI ≥ 30: enfermedad moderada o grave; PCDAI > 11 e < 30: enfermedad leve; PCDAI ≤ 10: remisión clínica.
DE: desviación estándar; PCDAI: índice de actividad de la enfermedad de Crohn pediátrica.
Utilizamos el programa estadístico SPSS versión 13.0. El contraste de muestras apareadas se realizó con el contraste de Wilcoxon. El coeficiente de correlación entre las variables se estableció con el coeficiente de Spearman. Se consideró un valor de p < 0,05 como estadísticamente significativo.
RESULTADOSSe incluyó un total de 14 pacientes (9 varones), con una edad media en el momento del diagnóstico de 10,74 ± 2,56 años. Sólo 2 pacientes tenían antecedentes familiares de EIIC (uno de colitis ulcerosa y otro de enfermedad de Crohn). El tiempo medio transcurrido desde el inicio de los síntomas hasta la confirmación diagnóstica fue de 104,72 ± 52,7 días. El fenotipo más frecuente fue L3B1A1 (50 %), seguido de L3-L4B1A1 (21,4 %) (tabla 3). La afectación perianal se observó en 3 pacientes (21,4 %). En todos los casos el patrón clínico fue inflamatorio. Modulen IBD fue bien tolerado, ningún paciente requirió sonda nasogástrica para su administración y ninguno abandonó la dieta antes de las 8 semanas. Todos recibieron aminosalicilatos (50–100 mg/kg/día) y cuatro de ellos, además, metronidazol (20–30 mg/kg/día) (tabla 3).
Aspectos epidemiológicos, fenotípicos, clínicos y analíticos
| Número | Edad | Sexo | Fenotipo* | PCDAI 0 | PCDAI 4 | PCDAI 8 | CF 0 | CF 4 | CF 8 |
| 1 | 12 años y 8 meses | V | L3B1A1 | 20 | 10 | 2,5 | 256 | 245 | 358 |
| 2 | 7 años y 6 meses | M | L3B1A1 | 25 | 5 | 5 | 283 | 201 | 173 |
| 3 | 7 años y 8 meses | V | L3B1A1 | 25 | 10 | 5 | 797 | 514 | 189 |
| 4 | 7 años y 7 meses | V | L3 + L4B1A1 | 32,5 | 2,5 | 2,5 | 973 | 445 | 255 |
| 5 | 12 años y 6 meses | V | L3B1A1 | 35 | 15 | 10 | 819 | 366 | 129 |
| 6 | 11 años y 8 meses | V | L3B1A1 | 20 | 25 | 20 | 250 | 724 | 724 |
| 7 | 11 años y 1 meses | M | L3B1A1 | 55 | 7,5 | 7,5 | 283 | 385 | 173 |
| 8 | 8 años y 1 meses | V | L2B1pA1 | 32,5 | 15 | 5 | 590 | 563 | 680 |
| 9 | 12 años y 10 meses | M | L3 + L4B1A1 | 45 | 7,5 | 5 | 687 | 158 | 348 |
| 10 | 6 años y 2 meses | V | L3B1A1 | 30 | 10 | 10 | 290 | 614 | 282 |
| 11 | 11 años y 3 meses | M | L3 + L4B1pA1 | 40 | 37,5 | 25 | 492 | 423 | 171 |
| 12 | 13 años y 8 meses | M | L3 + L4B1A1 | 30 | 5 | 5 | 484 | 268 | 264 |
| 13 | 12 años y 7 meses | V | L3 + L2B1pA1 | 15 | 5 | 5 | 446 | 155 | 373 |
| 14 | 13 años y 9 meses | V | L2B1A1 | 17,5 | 10 | 5 | 529 | 630 | 241 |
CF: calprotectina fecal (a las 0, 4 y 8 semanas de tratamiento); PCDAI: índice de actividad de la enfermedad de Crohn pediátrica.
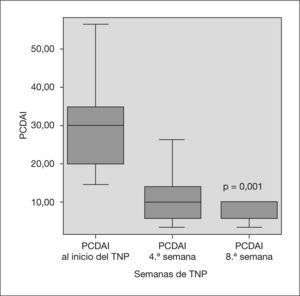
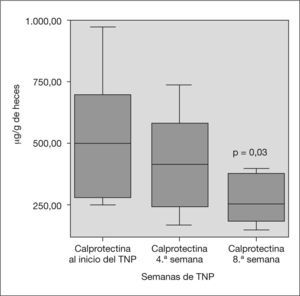
Al inicio del TNP, el peso fue de 37,03 ± 11,29 kg, el PCDAI de 30,17 ± 11,15 y los valores de calprotectina fecal de 512 ± 235 μg/g heces. A las 4 semanas, el 71% de los pacientes (10 de 14 casos) había alcanzado la remisión clínica (fig. 1), que se acompañó de un descenso no significativo de las cifras de calprotectina fecal (p = 0,221). A las 8 semanas, el 85 % de los pacientes estaba en remisión clínica (p = 0,001) y la excreción fecal de calprotectina había experimentado un descenso significativo (p = 0,03), sin alcanzar en ningún momento valores normales (fig. 2).
Se observó un incremento de peso y talla al final del TNP (tabla 4). El coeficiente de Spearman entre el PCDAI y la calprotectina fecal de nuestra muestra fue de 0,449 (p = 0,003).
Contraste de Wilcoxon para muestras apareadas*
| Inicio de TNP (T1) | Semana 4 (T4) | Fin TNP (T8) | (T1-T4) p | (T1-T8) p | |
| Peso (kg)** | 37,03 ± 11,38 | 37,7 ± 10,39 | 37,25 ± 10,12 | 0,799 (NS) | 0,689 (NS) |
| Talla (m)** | 1,39 ± 0,11 | 1,40 ± 0,11 | 1,40 ± 0,11 | 0,027 | 0,008 |
| IMC (kg/m2)** | 18,71 ± 3,92 | 18,72 ± 3,50 | 18,57 ± 3,10 | 0,445 (NS) | 0,859 (NS) |
| PCDAI** | 30,17 ± 11,15 | 11,75 ± 9,21 | 8,17 ± 6,99 | 0,002 | 0,001 |
| Calprotectina fecal** | 512,78 ± 235,15 | 406,5 ± 185,26 | 311,42 ± 182,06 | 0,221 | 0,030 |
IMC: índice de masa corporal; NS: no significativo; PCDAI: índice de actividad de la enfermedad de Crohn pediátrica; TNP: tratamiento nutricional primario.
Los mecanismos de acción de la nutrición enteral sobre la inflamación intestinal en la enfermedad de Crohn se desconocen; entre las hipótesis se incluyen la modificación en la flora intestinal, la eliminación de la captación de antígenos alimentarios, la disminución de la síntesis intestinal de mediadores inflamatorios a causa de una reducción de la grasa en la dieta o el aporte de micronutrientes al intestino enfermo16. Numerosos ensayos realizados en adultos y en niños ponen de manifiesto que no existen diferencias en la tasa de remisión ni en el cumplimiento del tratamiento nutricional en relación con la fórmula enteral empleada (polimérica, semielemental o elemental)17–19. Tampoco se han demostrado ventajas con suplementos en glutamina ni con triglicéridos de cadena media20,21.
Actualmente no existen datos que demuestren la eficacia de los aminosalicilatos (5-ASA) en la inducción a la remisión en niños con enfermedad de Crohn. Sí se han referido datos en adultos; en un metaanálisis llevado a cabo en 600 pacientes adultos con enfermedad de Crohn22 se ha puesto de manifiesto un descenso significativo del CDAI de 63 puntos en los pacientes tratados con 5-ASA frente a 45 puntos en los que recibieron placebo. Esta diferencia de 18 puntos, pese a ser significativa, carece de relevancia clínica. En cuanto al empleo de metronidazol, un estudio controlado con placebo en la enfermedad de Crohn activa no demostró la existencia de diferencias significativas con respecto al placebo, tras 16 semanas de tratamiento23. Estos argumentos apoyan que el tratamiento coadyuvante con 5-ASA y/o metronidazol en nuestra muestra no haya influido en la tasa final de remisión.
En la tabla 5 se exponen los datos de los estudios realizados en niños (duración, tipo de fórmula, criterios para definir la remisión clínica y tasa de remisión).
Tasa de remisión clínica en niños con enfermedad de Crohn y tratamiento nutricional primario
| Referencia | Número | Fórmula | T | Criterios de remisión clínica | R* (%) | R** (%) | C (%) |
| Sanderson (1987)24 | 8 | Elemental | 6 | Mejoría DAIS | 100 | 88 | 88 |
| Ruuska (1993)25 | 10 | Polimérica | 8 | PCDAI < 10 | 100 | 90 | 100 |
| Thomas (1993)26 | 12 | Elemental | 4 | DAIS > 80 | 100 | 100 | 100 |
| Papadopoulou (1995)27 | 19 | Elemental | 6 | DAIS > 80 + ausencia de síntomas | 83 | 83 | 100 |
| Akobeng (2000)20 | 16 | Polimérica | 4 | PCDAI < 10 | 56 | 50 | 88 |
| Fell (2000)28 | 29 | Polimérica | 8 | PCDAI < 10 | 85 | 79 | 93 |
| Terrin (2002)29 | 10 | Semielemental | 8 | PCDAI < 10 | 90 | 90 | 100 |
| Ludvigsson (2004)18 | 17 | Polimérica | 6 | PCDAI < 10 o ↓ 45 % o ↓ 15 puntos | 82 | 82 | 100 |
| 16 | Elemental | 6 | PCDAI < 10 o ↓ 45 % o ↓ 15 puntos | 69 | 69 | 100 | |
| Afzal (2004)30 | 26 | Polimérica | 8 | PCDAI < 20 | 88 | 88 | 100 |
| Knight (2005)31 | 40 | Elemental | 6 | CDAI | 90 | 90 | 100 |
| 4 | Polimérica | 6 | CDAI | 90 | 90 | 100 | |
| Day (2006)32 | 27 | Polimérica | 6-8 | PCDAI < 15 | 79 | 70 | 89 |
| Borrelli (2006)33 | 19 | Polimérica | 10 | PCDAI < 10 | 88 | 79 | 89 |
| Johnson (2006)34 | 24 | Elemental | 6 | PCDAI < 10 | 62 | 41 | 66 |
| Berni Canani (2006)35 | 12 | Elemental | 8 | PCDAI < 10 | 86,5 | 86,5 | 100 |
| 13 | Semielemental | 8 | PCDAI < 10 | 86,5 | 86,5 | 100 | |
| 12 | Polimérica | 8 | PCDAI < 10 | 86,5 | 86,5 | 100 | |
| Rodrigues (2007)36 | 53 | Elemental | 6 | No especificados*** | 89 | 64 | 71 |
| 45 | Polimérica | 6 | No especificados*** | 88 | 51 | 51 | |
| Navas (2008) | 14 | Polimérica | 8 | PCDAI < 10 | 85 | 85 | 100 |
C: tasa de cumplimiento; CDAI: índice de actividad de la enfermedad de Crohn; DAIS: índice de actividad de Lloyd-Still; Número: número de pacientes incluidos en el estudio; PCDAI: índice de actividad de la enfermedad de Crohn pediátrica; R: pacientes que alcanzan la remisión; T: tiempo en semanas.
Ludvigsson et al18 incluyeron a 31 pacientes menores de 17 años diagnosticados de enfermedad de Crohn; 16 recibieron fórmula elemental (Elemental 028, SHS, Reino Unido) y 17, fórmula polimérica (Nutrison Standard, Nutricia, Países Bajos), durante 6 semanas. Se encontró una tasa de remisión del 69 % para los pacientes que tomaban fórmula elemental frente al 82 % de los que tomaron fórmula polimérica (p = NS). Fell et al28 administraron Modulen IBD a 29 pacientes (17 en primer brote y 12 en recaída) durante 8 semanas; el 79 % se encontraba en remisión clínica al final de este período. Day et al32 seleccionaron a 27 pacientes (15 en primer brote y 12 en recaída); todos recibieron fórmula polimérica durante 6–8 semanas, bien Modulen IBD (Nestlé, Sidney, NSW, Australia) u Osmolite (Abbott Nutrition Internacional, Botany, NSW, Australia). La tasa global de remisión, por protocolo, fue del 79% (del 80 % en los nuevos pacientes y del 58 % en los pacientes en recaída). Borrelli et al33, en un estudio prospectivo y aleatorizado que comparaba la eficacia de la fórmula polimérica (Modulen IBD) frente a los corticoides para inducir la remisión clínica, endoscópica e histológica en una muestra de 19 pacientes con nuevo diagnóstico de enfermedad de Crohn, encontraron que al final de las 10 semanas de tratamiento nutricional el 79 % de los pacientes se encontraban en remisión clínica.
Sanderson et al24 administraron por sonda nasogástrica a 9 pacientes una dieta elemental (Flexical) durante 6 semanas, al final de las cuales se encontraba en remisión el 89 % de los pacientes. Ruuska et al25 obtuvieron también esta tasa de remisiones tras administrar a 10 niños Nutrison Standard (Nutricia) durante 8 semanas. Thomas et al26 utilizaron Elemental 028 en 12 niños durante 4 semanas, con una respuesta clínica excelente.
Johnson et al34 compararon dos modalidades distintas de tratamiento nutricional en un grupo de 50 pacientes diagnosticados de enfermedad de Crohn. Emplearon la fórmula Elemental 028 Extra (SHS, International) en todos los pacientes durante 6 semanas; 26 de ellos recibieron la mitad de sus necesidades calóricas diarias en forma de fórmula elemental y el resto mediante dieta normal (modalidad nutrición enteral parcial, NEP). Por otro lado, 24 pacientes recibieron todas sus necesidades calóricas en forma de fórmula elemental (modalidad nutrición enteral total, NET). Al final de las 6 semanas, el 62 % de los pacientes con NET frente al 25 % de los que recibían NEP se encontraban en remisión clínica. Afzal et al30 administraron una fórmula polimérica (ACD004, Nestlé) similar a Modulen IBD pero con diferente composición grasa durante 8 semanas, sin permitir otros alimentos a 26 pacientes, alcanzando el 85 % de ellos la remisión clínica al final del tratamiento. Akobeng et al20 dividieron en dos grupos a 18 pacientes con enfermedad de Crohn; a nueve de ellos les administraron una fórmula polimérica con bajo contenido en glutamina y al resto una fórmula polimérica enriquecida en glutamina. No se encontraron diferencias significativas en la tasa de remisión entre ambos grupos y al final de las 4 semanas de tratamiento el 56% había alcanzado la remisión clínica.
Terrin et al29 administraron alimentación exclusiva con fórmula semielemental (Pregomin, Milupa) durante 8 semanas a un grupo de 10 pacientes; el 90 % alcanzó la remisión clínica. Papadopoulou et al27 encontraron una tasa de remisión del 83 % en un grupo de 19 pacientes tratados con dieta elemental (E028, SHS, Liverpool, Reino Unido) durante 6 semanas.
Beattie et al37 utilizaron una dieta polimérica enriquecida con TGF-β en 7 pacientes menores de 18 años durante 8 semanas, al final de las cuales observaron una mejoría clínica muy significativa en todos los pacientes, junto con una aceptable ganancia ponderal y una normalización de los valores de proteína C reactiva (PCR) y de albúmina plasmáticas. Rodrigues et al36 dividieron a 98 niños con enfermedad de Crohn en su primer brote de enfermedad en dos grupos para recibir una fórmula polimérica (Clinutren, Nestlé Clinical Nutrition, Deerfield, IL, EE.UU.), Fortisip (Nutricia, Trowbridge, Reino Unido) o Ensure plus (Abbott Laboratories, Chicago, IL, EE.UU.) o una elemental (Elemental 028 o Elemental 028 Extra [SHS International, Liverpool, Reino Unido]) durante 6 semanas. Las tasas de remisión fueron del 51 y del 64 % (p = 0,19), respectivamente. Knight et al31 publicaron los datos de 44 niños que habían recibido durante 6 semanas bien Elemental 028 (SHS International Limited, Liverpool, Reino Unido) o bien Ensure Plus (Abbott Laboratories Limited, Maidenhead, Reino Unido). La tasa de remisión global fue del 90 %. Berni Canani et al35 emplearon Modulen IBD en 12 pacientes, Pregomin en 13 casos y fórmula elemental (Neocate, Nutricia, Italia) en 12 pacientes. El 86,5 % alcanzó la remisión al final de las 8 semanas.
Analizando los datos expuestos en la tabla 5, la tasa global de remisión, por intención de tratar, fue del 76,5 %, y por protocolo, del 84,4 %, con una tasa de cumplimiento del 90 %. Si agrupamos los estudios de 8 semanas de duración y con el criterio de remisión clínica de PCDAI inferior a 10 y los comparamos con nuestra serie, los resultados son similares (tasa de remisión por protocolo del 90,3% frente al 85 % y por intención de tratar del 86,5 % frente al 85 %; cumplimiento del 98,25% frente al 100 %)25,28,29,35. Para asegurar el cumplimiento terapéutico es importante explicarles a los pacientes y a sus familiares el objetivo y la duración del tratamiento, así como las alternativas de las que se dispone para su administración en caso de falta de tolerancia oral. La diferencia apreciada entre los distintos estudios puede deberse al tamaño de la muestra, a los distintos criterios de remisión empleados y a la fórmula administrada.
El objetivo principal en el tratamiento de la enfermedad de Crohn es la remisión histológica o la curación de la mucosa. En relación con este aspecto, existen varios trabajos que evalúan de una u otra forma la mejoríacuración de la mucosa intestinal. En este sentido, Fell et al28 repitieron la colonoscopia a 26 pacientes al finalizar las 8 semanas de TNP y encontraron una mejoría en el 50 % de los casos y curación en el 30 %. Cuando analizaron los hallazgos del íleon terminal, el 68 % había mejorado y se había curado el 53 %. El análisis histológico puso de manifiesto una mejoría en el 48 % de las biopsias colónicas (curación histológica en el 8 %) y en el 65 % de las de íleon terminal (curación histológica en el 40 %).
Borrelli et al33, tras las 10 semanas de nutrición enteral con fórmula polimérica, observaron una mejoría significativa en los índices endoscópicos e histológicos, tanto en el íleon terminal como en el colon. También Berni Canani et al35 constataron una mejoría significativa en los índices histológicos y endoscópicos de los pacientes sometidos a TNP, independientemente de la fórmula utilizada. Beattie et al37, tras el análisis de las muestras obtenidas después de 8 semanas de tratamiento, demostraron una mejoría histológica en el 85 % de los casos (6 de 7 casos), y dos de ellos alcanzaron la remisión histológica.
En nuestra serie encontramos una disminución de los valores de calprotectina fecal al final de las 8 semanas en el 71 % de los pacientes, lo que puede interpretarse como una mejoría del grado de inflamación intestinal, y en ningún caso se alcanzaron valores inferiores a 50 μg/g de heces.
Existía una idea inicial de que el tratamiento nutricional era más efectivo en pacientes con afectación ileal que en los que presentaban una enfermedad de localización exclusivamente colónica. En la actualidad no existen datos que permitan establecer una correlación entre la respuesta al TNP y el fenotipo de la enfermedad.
Uno de los aspectos más debatidos en las últimas dos décadas es la eficacia del tratamiento nutricional frente a los esteroideos para inducir la remisión en pacientes afectados de enfermedad de Crohn. Trabajos realizados en niños como los de Sanderson et al24 o de Thomas et al26 ya ponían de manifiesto hace 15–20 años que la efectividad de los corticoides para inducir la remisión era similar a la de la nutrición enteral. Esos datos no se reflejaban en los estudios llevados a cabo en adultos ni en los tres metaanálisis4,38,39 que analizaban conjuntamente resultados de series pediátricas y de adultos, en los que se observaba mayor eficacia con el tratamiento esteroideo.
Dos metaanálisis de ensayos pediátricos llegan a la conclusión de que el tratamiento nutricional en la enfermedad de Crohn pediátrica es tan eficaz como los corticoides en la inducción de la remisión de la enfermedad, pero sin sus efectos deletéreos40,41. También dos estudios recientes han comprobado que el tratamiento nutricional es más eficaz que los esteroides para mejorar la inflamación intestinal, recuperar el crecimiento y mantener la remisión clínica33,35.
En conclusión, el TNP ha demostrado ser efectivo en la inducción a la remisión clínica e histológica en niños con enfermedad de Crohn, independientemente del fenotipo. En general es bien tolerado y su eficacia para inducir la remisión clínica es similar a la de los esteroides, pero sin sus efectos secundarios.
La correlación entre PCDAI y calprotectina fecal es baja, y se necesitan las dos herramientas para el seguimiento de los pacientes. Una explicación detallada del plan de tratamiento al paciente y a sus familiares puede desembocar en el éxito del cumplimiento del TNP. Debemos informar a nuestros pacientes de la posibilidad del uso de sonda nasogástrica y dejar a su elección la vía de administración de la fórmula polimérica. Debido al corto período de tiempo en el que se ha de administrar el TNP no creemos indicada la realización de una gastrostomía.
El TNP administrado durante un período de 8 semanas puede inducir la remisión clínica y mejorar el grado de inflamación de la mucosa intestinal, lo que se refleja en la disminución de las cifras de calprotectina fecal.