Evaluar la seguridad renal del tratamiento con polietilenglicol 3350 con electrolitos durante 1, 3 y 6 meses, la tolerancia digestiva y la dosis de eficacia.
Pacientes y métodosFueron evaluados 3 grupos de 30 pacientes sanos, 2-10 años (media 6,2) con estreñimiento funcional (criterios de Roma III), con 1, 3 y 6 meses de tratamiento. La eficacia fue evaluada por el número de deposiciones/semana y la consistencia de las heces (escala de Bristol). La natriuria y la osmolaridad urinaria se midieron al inicio, 1, 3 y 6 meses. Los principios inmediatos en heces (análisis de reflexión de infrarrojos [FENIR]) y un test de hidrógeno espirado fueron efectuados en el grupo de un mes de tratamiento.
ResultadosLa dosis efectiva fue de 0,37g/kg/día (rango 0,18-0,8). El número de deposiciones/semana en la inclusión (2,4±0,64) muestra diferencia significativa (p<0,001) vs. (6,21±1,5) tras el tratamiento. También se demostró una diferencia significativa en la puntuación en la escala de Bristol (1,9±0,75 vs. 4,9±1,1 [p<0,001]). La ingesta media de sodio fue de 112mg (5mg/kg/día [rango de 4-12mg/kg/día]). Los valores de sodio y osmolaridad en orina fueron normales en todos los grupos sin diferencia estadística con respecto a controles (90 niños sanos sin tratamiento). Los valores de FENIR fueron normales en todos los pacientes. La prueba de aliento con hidrógeno fue normal, con una media de 7ppm.
ConclusiónNo se observaron parámetros bioquímicos renales adversos ni alteraciones digestivas. La tolerancia y la eficacia demostraron ser óptimas. El polietilenglicol 3350 con electrolitos puede ser recomendado con seguridad para el tratamiento del estreñimiento funcional en los niños a corto y largo plazo.
To assess the renal safety of treatment with polyethylene glycol 3350 with electrolytes at 1, 3 and 6 months, its gastrointestinal tolerance and dose effectiveness.
Patients and methodsThree groups of 30 healthy patient aged 2-10 years (mean 6.2 years) who suffered functional constipation (Rome III criteria) with 1, 3 and 6 months of treatment were evaluated. Efficacy was evaluated by the change in the number of stools per week and stool consistency (Bristol scale). Urine screens, sodium and osmolality, were performed at the beginning and after 1, 3 and 6 months of treatment. Stool sample NIRA (near-infrared reflectance analysis) and hydrogen breath test analysis samples were performed on the one-month treatment group.
ResultsThe mean dose was 0.37g/kg/day (range 0.18 to 0.8) titrated according to age, weight and response. The number of stools per week during treatment (2.4±0.64) showed a significant difference (P<.001) vs (6.21±1.5) after treatment. There was also a significant difference in the Bristol scale score (1.9±0.75 vs 4.9±1.1 [P<.001]). The mean sodium intake was 112mg (5mg/kg/day [range 4-12mg/kg/day]). The values of sodium and urine osmolality were normal in all groups with no statistical difference compared to normal control values (90 healthy children without treatment). NIRA values were normal in all patients. The hydrogen breath test was normal with a median of 7ppm.
ConclusionThere were no adverse renal biochemical parameters or gastrointestinal disorders. Tolerance and efficacy was shown to be optimal. Polyethylene glycol 3350 with electrolytes can be safely recommended for the treatment of functional constipation in children in the short and long term.
El estreñimiento es un trastorno frecuente en la infancia, responsable de aproximadamente el 5% de las consultas pediátricas ambulatorias y de un 18-25% de las consultas en las unidades de gastroenterología pediátrica1-3. La definición del estreñimiento funcional en niños menores y mayores de 4 años fue dada en 2006 en los criterios de Roma III4,5.
En el año 2006, la North American Society for Pediatric Gastroenterology, Hepatology and Nutrition (NASPGHAN) elaboró una guía práctica para el tratamiento del estreñimiento infantil. Consiste en la aplicación de medidas dietéticas y educacionales, así como el inicio de tratamiento laxante para garantizar una adecuada evacuación intestinal6.
Numerosos estudios avalan la eficacia del polietilenglicol (PEG) 3350, con electrolitos y sin electrolitos, y del PEG 4000 en el tratamiento del estreñimiento crónico y la impactación fecal en niños7-13. Sin embargo, pocos trabajos han evaluado su seguridad en pediatría13,14, solicitándose estudios que los refrenden en su más amplio contexto15,16.
El objetivo de este estudio es evaluar la seguridad, tolerancia y eficacia del PEG con electrolitos (PEG+E) en el tratamiento del estreñimiento funcional. Variable principal: seguridad renal a corto plazo (un mes de tratamiento) y largo plazo (3 y 6 meses de tratamiento). Variable secundaria: tolerancia y seguridad gastrointestinal, eficacia clínica, dosis de efectividad a corto y largo plazo, y seguimiento de posibles efectos adversos.
Pacientes y métodoTipo de estudioEstudio multicéntrico, observacional, con 2 diseños:
- –
Prospectivo, longitudinal en un grupo de pacientes para evaluar la seguridad renal y digestiva a corto plazo.
- –
Retrospectivo, transversal en 2 grupos de pacientes para evaluar la seguridad renal a largo plazo.
- –
En ambos diseños se evalúan la eficacia clínica, la dosis de efectividad y los efectos adversos.
A todos los responsables legales de los niños se les invitó a participar en el estudio, aceptando dicha participación con consentimiento informado. El trabajo contó con el permiso oficial del comité ético del centro coordinador Vall d’Hebron (EPA[AMI]18/2012[3327]).
PacientesGrupo ACriterios de inclusiónFueron incluidos 30 niños sanos, con ausencia de enfermedad aguda o crónica, de 2-10 años de edad que consultaron por estreñimiento funcional, basado en los criterios de Roma III4,5, después de haber seguido un período mínimo de un mes con medidas educativas y dieta rica en fibra, sin resolución de los síntomas. No presentaban impactación fecal en el momento de la inclusión y no recibían tratamiento con ningún otro laxante.
Una vez obtenidos los resultados bioquímicos y descartada cualquier posible alteración renal subyacente, se administró PEG+E (Movicol Pediátrico® [Norgine, España]) en sobres de 6,9g que contienen 6,56g de PEG 3350, 175,4mg de cloruro de sodio, 89,3mg de bicarbonato de sodio y 25,1mg de cloruro de potasio.
La dosis inicial se estableció en función de la edad:
- –
Un sobre al día para pacientes entre 2 y 6 años de edad.
- –
Dos sobres al día para los pacientes entre 7 y 9 años de edad.
Esta dosis se ajustó en el curso de una semana mediante llamada telefónica. El ajuste se realizó sobre la base de la respuesta clínica, que consistía en conseguir unas heces más blandas, sin molestias al defecar, sin superar la dosis máxima recomendada de 27,6g por día. La dieta no fue cambiada, continuando con los hábitos individuales de cada sujeto.
Grupo A-4ST (después de 4 semanas de tratamiento)Se efectuó:
- –
Valoración de eficacia y tolerancia clínica.
- –
Estudio de seguridad renal.
- –
Estudio de seguridad digestiva.
Fueron incluidos 30 pacientes en cada grupo (2-10 años de edad), que ya estaban en tratamiento con PEG 3350 y controlados en los diferentes centros que han participado en el estudio. Se efectuó:
- –
Valoración de eficacia y tolerancia clínica.
- –
Estudio de seguridad renal.
Fueron recogidos los valores de sodio y osmolaridad en orina de 90 niños sanos, de 2-10 años edad, con dieta normal.
MetodologíaEstudio de seguridad renalCon el fin de asegurar la normalidad renal de los pacientes incluidos en el grupo A, se les determinó: urea, creatinina, potasio y sodio plasmáticos, antes de su inclusión. Se calculó el filtrado glomerular. Para evaluar la repercusión de la ingesta de sodio aportada con el tratamiento, se determinaron la osmolaridad urinaria (mOsm/kg) y el sodio en la orina (mEq/L) antes de iniciar el tratamiento con PEG+E y tras 4 semanas de tratamiento (grupo A-4ST [estudio a corto plazo]). Similar estudio urinario se efectuó en los pacientes de los grupos B y C (estudio a largo plazo). Al ser un estudio transversal, no hay datos retrospectivos de orina de estos pacientes.
Una osmolaridad y una natruria sin modificaciones estadísticas demuestran una sobrecarga de sodio mínima o una compensación renal adecuada, para lo cual se ha efectuado: estudio estadístico entre el sodio y la osmolaridad en orina antes (grupo A basal) y después del tratamiento (grupo A-4ST), y estudio estadístico entre el sodio y la osmolaridad en orina entre todos los grupos y respecto al grupo control.
Se tomo la presión arterial en todos los pacientes y se evaluó de la ingesta de sodio 48 h antes de la muestra de orina.
Valoración de eficacia y tolerancia clínicaSe recogió información del número de deposiciones por semana y de su consistencia. Para la valoración de la forma y consistencia, se empleó la escala Bristol, que evalúa la consistencia de las heces en una puntuación de 1-717, según la cual una puntuación de 1 corresponde a heces duras con evacuación difícil y 7, heces acuosas.
Fueron recogidos los posibles efectos adversos: dolor abdominal, diarrea, flatulencia, náuseas y aceptación de la palatabilidad del producto.
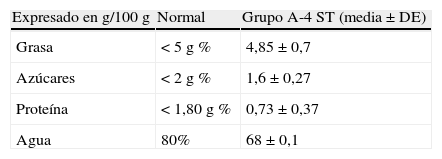
Estudio de seguridad digestivaMetodología del estudio de principios inmediatos en heces (FENIR)La determinación a las 4 semanas de tratamiento (grupo A-4ST) de la grasa, nitrógeno, agua, almidón y azúcar en las heces se efectuó mediante medición de las radiaciones en el espectro cercano de infrarrojos (FENIR 8820-infrared Analyzer-Perten, Hamburgo, Alemania [FENIR]). Los valores normales expresados en g/100g de heces (con una cantidad de agua del 75-80%) son: < 5% para la grasa, < 1,8% para el nitrógeno y < 2,5% para el almidón y azúcares.
Metodología del test de hidrógeno espiradoLa determinación del hidrógeno en aire espirado (cromatografía SC MicroLyzr para detección simultánea de H2, CO2) se efectuó a las 4 semanas de tratamiento (grupo A-4ST), con el fin de estudiar el efecto osmótico del PEG+E. Se considera normal un valor de hidrógeno inferior a 15 ppm.
Análisis estadísticoLos resultados se expresan como media aritmética ± desviación estándar cuando las variables siguieron una distribución normal y como mediana-rango en el resto de los casos. Se utilizó un test no paramétrico (U de Mann-Whitney) para las variables numéricas y el test de la chi al cuadrado y Fisher para las variables categóricas, cuando se compararon varios grupos. Los valores de p menores de 0,05 se consideraron significativos. El análisis estadístico se realizó mediante el programa SPSS 18.0 (SPSS Inc, Chicago, EE. UU.).
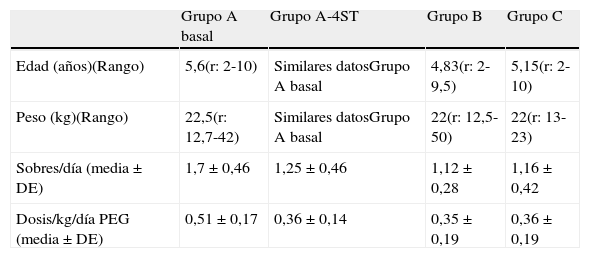
ResultadosDosis polietilenglicol con electrolitosLa eficacia inicial se consiguió en el plazo máximo de una semana (media de 5 días) con una dosis media de 1,7±0,45 sobres/día (rango 1-3 sobres). La dosis eficaz de PEG+E, referenciando las dosis de los pacientes en su totalidad (n=90) en el mantenimiento, arrojó una mediana de 1,16 sobres/día (rango 0,5-2,5). El peso de nuestros pacientes, referenciando el valor de los pacientes en su totalidad (n=90), arrojó una media de 21,5 kg (rango 12,5-50), equivaliendo a una dosis de PEG+E de 0,37g/kg/día (rango 0,18-0,8) (véase la tabla 1).
Pacientes y dosis de PEG+E administrada
| Grupo A basal | Grupo A-4ST | Grupo B | Grupo C | |
| Edad (años)(Rango) | 5,6(r: 2-10) | Similares datosGrupo A basal | 4,83(r: 2-9,5) | 5,15(r: 2-10) |
| Peso (kg)(Rango) | 22,5(r: 12,7-42) | Similares datosGrupo A basal | 22(r: 12,5-50) | 22(r: 13-23) |
| Sobres/día (media±DE) | 1,7±0,46 | 1,25±0,46 | 1,12±0,28 | 1,16±0,42 |
| Dosis/kg/día PEG (media±DE) | 0,51±0,17 | 0,36±0,14 | 0,35±0,19 | 0,36±0,19 |
La creatinina (mg/dL): 0,57±0,1, la natremia (mmol/L): 137±1,95 y el cálculo del filtrado glomerular: 124±35 eran normales en todos los pacientes reclutados del grupo A. La determinación de la presión arterial fue normal en todos los pacientes de todos los grupos. La ingesta de sodio 48 h antes de la recogida de las muestras de orina no cambió con respecto a la dieta habitual en ninguno de los pacientes, según encuesta dietética de una semana previa a la recogida de orina.
Un sobre de PEG+E proporciona 93mg de Na (0,27g de cloruro sódico). Teniendo en cuenta que 1g de cloruro sódico proporciona 333mg de sodio, la ingesta media de sodio (todos los pacientes) fue de 112mg (5mg/kg/día [rango de 4-12mg/kg/día]), equivalente a una ingesta media de 0,31g de cloruro sódico. La mayor ingesta absoluta fue de 184mg de Na (0,55g de cloruro sódico).
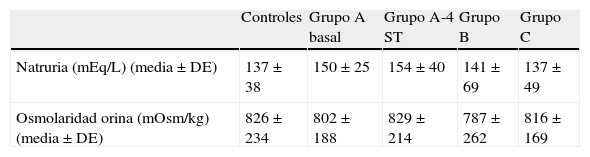
Los datos correspondientes a los parámetros de orina de los controles y todos los grupos se muestran en la tabla 2. No se observaron diferencias estadísticamente significativas entre los controles y ninguno de los grupos, ni entre los valores de los grupos entre sí.
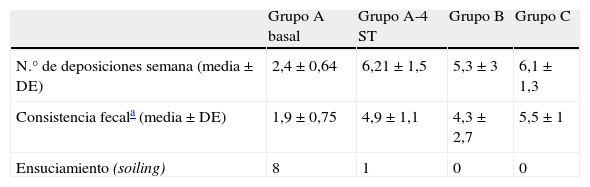
La eficacia y la tolerancia clínicaEl número de deposiciones/semana del grupo A en la inclusión (2,4±0,64) muestra una diferencia significativa (p<0,001) vs. (6,21±1,5) tras el tratamiento (grupo A-4ST). El tratamiento con PEG+E también demostró una diferencia significativa en la puntuación de la escala de Bristol (1,9±0,75 vs. 4,9±1,1 [p<0,001]). No se encontraron diferencias entre el número de deposiciones ni en la escala de Bristol para los pacientes en tratamiento (grupo A-4ST, grupo b y grupo C). Los datos se muestran en la tabla 3. Ningún paciente interrumpió el tratamiento ni tampoco fueron observados efectos secundarios. En el momento de la inclusión, 8 pacientes presentaban ensuciamiento y a las 4 semanas de tratamiento solo uno mantenía el síntoma. Ningún paciente de los otros grupos presentaba incontinencia fecal.
Datos clínicos de la defecación
| Grupo A basal | Grupo A-4 ST | Grupo B | Grupo C | |
| N.° de deposiciones semana (media±DE) | 2,4±0,64 | 6,21±1,5 | 5,3±3 | 6,1±1,3 |
| Consistencia fecala (media±DE) | 1,9±0,75 | 4,9±1,1 | 4,3±2,7 | 5,5±1 |
| Ensuciamiento (soiling) | 8 | 1 | 0 | 0 |
Los resultados del análisis de los principios inmediatos en heces de los pacientes del grupo A-4ST mostraron valores dentro del rango normal (tabla 4). No hubo diferencia estadística con respecto a los valores normales
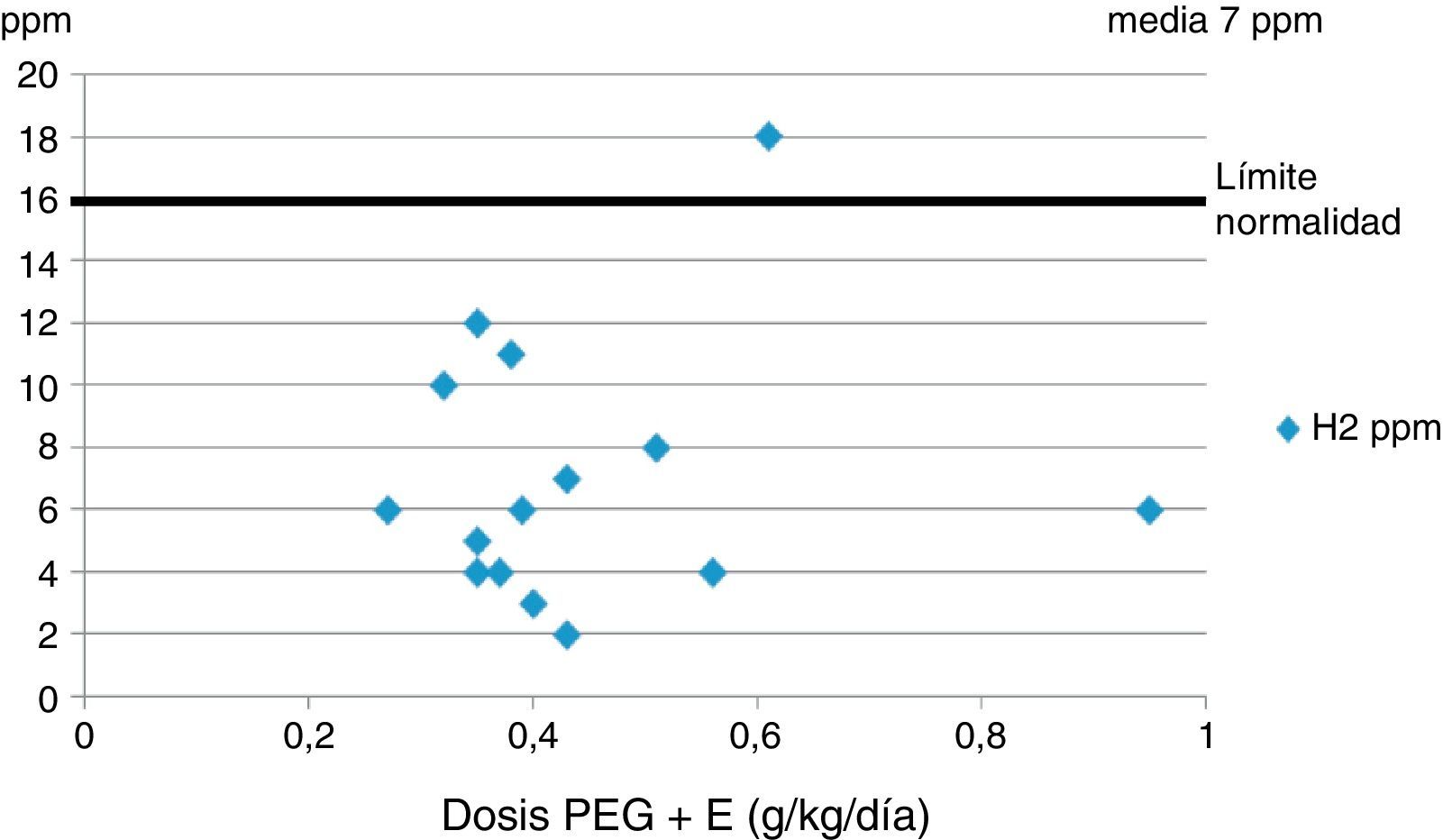
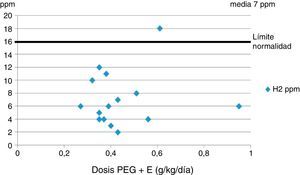
La figura 1 muestra los valores (media de 2 determinaciones) de H2 espirado (grupo A-4ST). Todos los valores, con la excepción de un paciente que tenía un ligero aumento, estaban dentro del rango normal (mediana de 7ppm [rango 2-18] [valor normal<15ppm]), y no guardaban relación con la dosis de PEG+E.
DiscusiónLa NASPGHAN elaboró una guía práctica para el tratamiento del estreñimiento infantil6. Hace unas décadas, la suplementación con altas dosis de fibra fue la primera línea de tratamiento para el estreñimiento funcional. Los laxantes formadores de masa fecal, como la esterculina, el salvado, la ispágula, los polisacáridos naturales o semisintéticos o los derivados de celulosa, producen meteorismo, flatulencia y además su mala palatabilidad, los hacen inviables en la edad pediátrica.
El uso de laxantes salinos, como el magnesio y las sales de fosfato sódico, aparece asociados con una absorción sustancial de los iones que los componen, lo cual puede provocar una toxicidad sistémica que incluye: diarrea crónica, deshidratación y desequilibrio electrolítico por absorción excesiva de magnesio y eliminación de potasio y calcio18,19. Deben ser usados con precaución dado que su eficacia está unida a altas dosis.
Los laxantes estimulantes, como las antraquinonas, el sen, la cáscara sagrada o el bisacodilo, viajan sin ser absorbidos hasta el intestino grueso, donde son metabolizados y transformados en agliconas. Causan a menudo calambres abdominales y lesiones irreversibles en las neuronas mioentéricas20. Su uso está contraindicado en niños.
Los lubricantes orales oleosos, como el aceite mineral o la parafina líquida, pueden causar incontinencia y malabsorción de vitaminas liposolubles21,22. En lactantes han sido comunicadas aspiraciones lipoideas23.
Los agentes orgánicos hiperosmolares/osmóticos comprenden solutos orgánicos no absorbibles (sorbitol, lactulosa y lactitol) que actúan ablandando y aumentando el contenido hídrico de las heces. El principal lugar de acción se localiza en el colon, donde es fermentada por la microbiota colónica, reteniendo agua y produciendo importante cantidad de gas: CO2, metano e hidrógeno. Puede provocar síntomas como dolor abdominal, meteorismo y flatulencia24,25.
Los macrogoles actúan, básicamente, reteniendo en la luz intestinal el líquido y los electrolitos ingeridos. A fin de evitar las posibles pérdidas netas se han añadido electrolitos a la solución oral de PEG 3350 (Movicol Pediátrico®). La osmolaridad de la solución obtenida es de 288mOsm/L y contiene 65mmol/L de sodio. Este bajo contenido en sodio de la solución conlleva un gradiente de concentración elevado y una tasa reducida de absorción activa del mismo, compensada con una tasa de secreción plasmática pasiva de sodio mínima, lo que conlleva un movimiento neto de sodio cercano a cero y la correspondiente retención de agua intestinal lo que favorece la acción laxante del producto.
Se han erigido como tratamiento eficaz y seguro del estreñimiento crónico funcional en la edad pediátrica7-13. Como soluciones de preparación de fibroendoscopias y tratamiento de desimpactación fecal26-29. Un mayor grado de eficacia ha sido demostrada en estudios comparativos con respecto a otros laxantes salinos e hiperosmolares osmóticos30-34. Otros trabajos han demostrado la eficacia y la seguridad en edades inferiores a 2 años35,36.
No existe una dosis establecida para el PEG+E y las dosis efectivas de mantenimiento empleadas por los diferentes autores oscilan entre 0,4-0,8g/kg/día, si bien las dosis de ataque, hasta el inicio de respuesta, sobre todo cuando se ha empleado para la desimpactación fecal, son más elevadas (alrededor de 1g/kg/día)37. En nuestra experiencia, la eficacia inicial se consiguió en el plazo máximo de una semana (media de 5 días), con una dosis media de 1,7±0,45 sobres/día (rango 1-3 sobres). La dosis eficaz de PEG+E en el mantenimiento arrojó una mediana de 1,16 sobres/día (rango 0,5-2,5). Diferentes factores, como grado de estreñimiento, tipo de dieta e ingesta de líquidos, se implican en la dosis terapéutica de efectividad37. El peso de nuestros pacientes referenció una media de 21,5kg (rango 12,5-50), equivaliendo a una dosis de PEG+E de 0,37g/kg/día (rango 0,18-0,8).
Dado que no se absorbe y que el mecanismo de acción es local, la dosis debe ser pautada por sobres/día más que por peso, buscando la dosis terapéutica eficaz. La dosis variaría ampliamente si el cálculo se efectuase referenciado a peso. Con dichas dosis, el número de heces por semana se normaliza, así como la consistencia, desapareciendo la dificultad defecatoria (tabla 3). De los 8 pacientes que presentaban ensuciamiento inicial, solo uno siguió presentando el síntoma. Ningún paciente interrumpió el tratamiento durante las 4 semanas de seguimiento ni ningún efecto adverso relevante fue comunicado por el paciente o sus padres. La duración del tratamiento dependerá de la edad del niño, de los hábitos dietéticos y del aprendizaje en la normal defecación (toilet training). No debe retirarse de forma brusca ni hasta que la rutina de defecación se haya instaurado de forma correcta y en el sitio adecuado38. En nuestra experiencia, el 80% se resuelve antes de los 6 meses de tratamiento.
La dosis media de sodio/día aportado con el tratamiento fue de 110mg (rango 47mg-223mg), lo que equivale a una media de 0,33g de cloruro sódico (rango 0,15g-0,6g). Se asume que, en un niño con función renal sana, el aumento de la ingesta oral de sodio, dentro de la variación dietética normal permitida, no comportará variaciones de la natremia. La cantidad de sodio aportada con la terapia representa un incremento escaso en relación al contenido de sal ingerido por una población infantil sana. La Food and Agriculture Organization/Organización Mundial de la Salud en 2003 recomendó una ingesta <2g sodio/día=5g de cloruro sódico/día. Recordemos, a modo de ejemplo, que 100g de leche aportan 40mg de Na, de queso unos 500mg, y de pan, entre 300 y 500mg.
En nuestro trabajo, los valores de osmolaridad urinaria de todos los grupos tras 1, 3 y 6 meses de tratamiento fueron normales, sin diferencias significativas con respecto al grupo control. La seguridad renal a corto plazo ya había sido estudiada13,30.
Ya hemos comentado que el estreñimiento funcional suele presentarse una vez cumplidos los 2 años y coincidiendo con el aprendizaje de la defecación2. En ocasiones, hemos empleado el preparado en lactantes por debajo de los 2 años y en muchas ocasiones hemos sido preguntados sobre el riesgo de su utilización. La capacidad de concentración máxima del riñón puede alcanzar, a partir del segundo o tercer mes de edad, el 75% de la de los adultos (800 a 1.600 mOsm/L). Se ha observado que la ingesta de 100mEq de sodio (1mEq=23mg Na) al día no produce efectos perjudiciales y se ha calculado de forma indirecta que la tolerancia máxima de los lactantes es de 12mEq/kg39,40. Recordemos que un biberón de leche de continuación de 250ml aporta una media de 100mg de sodio, cantidad que sería similar a lo aportado en la dosis de efectividad del PEG+E en nuestro estudio. Nuestra opinión es que, dada la pequeña cantidad de sodio que aporta la dosis terapéutica de PEG+E, no supondría ningún problema para un riñón de lactantes sanos en caso de que fuera preciso su empleo. No obstante, futuros estudios al respecto deben ser evaluados.
Nuestra experiencia y criterio es que la pequeña cantidad de sodio que aporta la dosis terapéutica de PEG+E no supondría ningún problema para un riñón de lactantes sanos en caso de que fuera preciso su empleo.
Los valores de hidrógeno espirado se encontraban dentro de la normalidad (mediana de 7ppm [rango 2-18]), lo cual demuestra y confirma que el PEG+E no tiene efectos osmóticos y no es degradado por la flora intestinal. Solamente un paciente mostró un valor levemente elevado (18ppm) con una dosis no elevada de PEG+E (0,6g/kg/día), por lo cual dicha elevación se supuso más ligada a algún componente de la dieta.
El estudio del FENIR realizado en nuestros pacientes evidenció unos valores de grasa, nitrógeno y azúcares dentro de la normalidad, demostrando que la administración de PEG+E no produce malabsorción de ningún tipo de nutriente13,31.
En definitiva, nuestro estudio demuestra que el PEG+E es absolutamente seguro a nivel renal a corto (un mes) y largo plazo (3 y 6 meses), en los pacientes estudiados de edad superior a los 2 años. Su tolerancia a nivel digestivo es excelente, sin consecuencias clínicas ni bioquímicas indeseables. Demuestra ser eficaz a una dosis de mantenimiento de 1-2 sobres al día, independientemente del peso. El PEG+E pediátrico puede ser recomendado con seguridad y eficacia para el tratamiento del estreñimiento funcional en la infancia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.