Introducción
Los primeros registros sobre el uso terapéutico o recreativo del consumo de cannabis aparecen ya en los vedas hindúes, y en textos chinos o árabes de hace más de mil años 1-4. Existen datos sobre el uso de derivados del cannabis hasta el siglo xix en Europa, con pacientes tan ilustres como la reina Victoria del Imperio Británico, quien los empleaba para aliviar sus migrañas y la dismenorrea. Incluso existen referencias de preparados a la venta en Estados Unidos a finales de ese siglo, que incluían derivados del cannabis para el tratamiento de los cólicos del lactante. A partir de la Primera Guerra Mundial, y en gran medida ante la alarma generada por la proliferación de morfinómanos, su uso empezó a ser cuestionado, hasta que en 1924 el cannabis fue declarado narcótico en la Conferencia Internacional sobre Opiáceos, y su tráfico perseguido; en 1941 se retiró de la farmacopea norteamericana y, en 1971, la División de Narcóticos de la Organización de la Naciones Unidas (ONU) lo declara sustancia con alto potencial de abuso, y sin efecto terapéutico; actualmente este último concepto está siendo sometido a revisión 4.
Paralelamente, la búsqueda del responsable de los efectos psicoactivos clásicos del cannabis (euforia, relajación, hipotermia, taquicardia refleja) permitió en los años sesenta que Mechoulam y Gaoni descubrieran el principio activo, un derivado del benzopireno denominado Δ 9-tetrahidrocannabinol (THC) 5. Esta sustancia se aisló en la resina amarillenta que cubre las hojas, pero sobre todo la inflorescencia de la planta hembra; posteriormente se han ido describiendo varios compuestos con actividad similar al THC, que iniciaron la familia de los llamados cannabinoides 1-3. Como en el caso de los opioides, el aislamiento de una molécula foránea con efectos en nuestro cerebro orientó a la búsqueda de los posibles receptores sobre los que actuaría dicha sustancia. Tras demostrarse su existencia en los años ochenta, en los años noventa se consiguió describir la estructura de un receptor, vinculado a proteínas G, específico para cannabinoides, denominado CB1 6 (fig. 1). Este receptor es el más abundante y ubicuo de los de su tipo presentes en el sistema nervioso central (SNC), con una densidad similar a la de los receptores de GABA o glutamato 7. Tres años después se consiguió describir la existencia de un segundo receptor, llamado CB2 (de distribución preferentemente extraneural, especialmente en tejidos del sistema inmunitario) 8 (fig. 1).
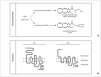
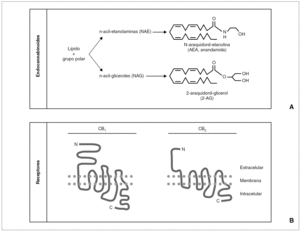
Figura 1. A)Esquema de la estructura química general de los endocannabinoides, y un ejemplo del principal representante de cada grupo.B)Esquema de la estructura bidimensional de los receptores cannabinoides CB1 y CB2.
Descubiertos y descritos unos receptores específicos para los cannabinoides fue sólo cuestión de tiempo el hallazgo de sus ligandos endógenos, que pasarían a denominarse endocannabinoides 1-3,9 (fig. 1). Su aislado fue dificultoso, por su estructura química y sus características sintéticas, pero apenas 2 años después de la descripción del CB1 se aisló una sustancia lipofílica de características funcionales similares al THC; esta sustancia, la etanolamida del ácido araquidónico (AEA), recibió el poético nombre de anandamida (de "ananda", "paz interior" en sánscrito) 10. Desde entonces, se han descrito múltiples moléculas que comparten una estructura básica común (un radical lipídico, habitualmente derivado del ácido araquidónico, y un grupo polar), con actividad cannabimimética 2,3,9. Junto con la AEA, el endocannabinoide más importante es el 2-araquidonoilglicerol (2-AG) 11, hasta 200 veces más abundante que la AEA en condiciones normales en diferentes tejidos y fluidos corporales 2,9. Siguiendo la estructura de estos endocannabinoides, se han definido dos grupos generales: las N-acil-etanolaminas (NAE), como, por ejemplo, AEA, virodamina, palmitoiletanolamina, oleiletanolamina, etc.; y los N-acil-gliceroles (NAG), como, por ejemplo, 2-AG, noladin-éter, N-araquidonil-dopamina, etc. 2,3,9. Finalmente, la secuenciación de los receptores y la identificación de los ligandos endógenos permitió el diseño de antagonistas específicos de los receptores CB, lo que posibilitó acelerar los estudios sobre el papel fisiológico y terapéutico de los cannabinoides, así como el descubrimiento de nuevos receptores con los que interactuarían los cannabinoides, como los vanilloides (VR1) y otros 2,7,12.
En la tabla 1 se resumen los diversos efectos de los cannabinoides y los receptores implicados en éstos.
Fisiología de los endocannabinoides
La síntesis de los endocannabinoides es un proceso dependiente de calcio y que responde a la demanda, es decir, que los endocannabinoides se sintetizan cuando son necesarios, pero no se almacenan 1-3,9. El aumento del calcio intracelular activa diferentes enzimas, como N-acetiltransferasa, fosfolipasas A, C y D, o diacilglicerolipasa, que a partir de lípidos de membrana como la fosfatidiletanolamina y la fosfatidilcolina, o el diacilglicerol, sintetizan el endocannabinoide correspondiente. El endocannabinoide es liberado, y se une al receptor CB. Los NAE, especialmente la AEA, son ligandos de CB1 y de VR1, mientras que los NAG, especialmente el 2-AG, son ligandos tanto de CB1 como de CB2. La unión al receptor, especialmente si es CB1, induce la inhibición de la adenilatociclasa; la hiperpolarización presináptica debido al cierre de canales de calcio dependientes de voltaje y la apertura de canales de potasio; la expresión de cinasas como la regulada por señales extracelulares (ERK), la c-Jun N-terminal (JNK), la proteincinasa activada por el mitógeno p38 (MAPK), o la proteincinasa B (PKB); la inhibición del factor nuclear κ -B (NF-κB); y la activación de ceramidas 1-3,9,13.
Posteriormente, el endocannabinoide es recaptado gracias a un transportador de membrana, y se ha descrito al menos uno, el transportador de membrana de anandamida (AMT). Una vez recaptado, el endocannabinoide es degradado por una enzima ligada a la membrana, la hidrolasa de amidas de ácidos grasos (FAAH, especialmente para NAE) o la monoglicerolipasa (MGL, especialmente para NAG), que producen, respectivamente, ácido araquidónico más etanolamina o glicerol 2,3. Así, la degradación de los endocannabinoides puede participar en la síntesis de prostanoides.
Los receptores CB1 se han hallado principalmente en el SNC; en el adulto, se distribuyen sobre todo en ganglios de la base (sustancia negra y pálido), cerebelo, hipocampo y corteza límbica; también se han hallado en médula y en terminaciones nerviosas sensitivas, y en nervios autonómicos 7,12. En virtud de estas localizaciones, los endocannabinoides participan en circuitos relacionados con la coordinación y el control del movimiento, funciones cognitivas superiores, en la respuesta al estrés y al dolor, en la regulación del sueño y en los mecanismos de recompensa; también intervendrían en la regulación de la temperatura corporal, el vómito y las náuseas, y el hambre 2-4.
Los receptores CB2 se encuentran preferentemente en tejido linfoide, sobre todo en bazo, amígdalas y timo, atribuyéndosele un efecto inmunomodulador 4,7,12-14. Se ha localizado en linfocitos B, células natural killer, macrófagos, monocitos, microglia, mastocitos y linfocitos T 7.
Funciones de los endocannabinoides
Sistema nervioso
Para muchos autores, el principal papel de los endocannabinoides es el de actuar como moduladores de la transmisión sináptica 2,9,15 (fig. 2). Llegado el estímulo nervioso despolarizante al terminal presináptico, la apertura de canales de calcio induce un aumento de calcio intracelular, que determina la translocación de las vesículas conteniendo el neurotransmisor, y su liberación; unido al receptor postsináptico, el neurotransmisor induce la apertura de canales de calcio, despolarizando la célula y culminando así la transmisión sináptica. El aumento del calcio intracelular en la neurona postsináptica activa la síntesis de endocannabinoides, que hiperpolarizan la neurona presináptica, anulando la liberación del neurotransmisor 2,3,9. Este proceso se denomina supresión inducida por la despolarización (DS); si se desarrolla sobre neuronas que liberan neurotransmisores inhibidores, como el GABA, se considera una DS de la inhibición (DSI), proceso dependiente de receptores CB1; si el neurotransmisor es excitador, como el glutamato, será una DS de la excitación (DSE), proceso que puede verificarse en ausencia de receptores CB1 2,15. El papel del endocannabinoide como inductor de DSE o DSI depende por tanto del tipo de neurona, pero también parece influido por ciertas condiciones basales, especialmente en relación con la concentración de calcio 2,3. La DSE y la DSI son de crucial importancia en procesos de plasticidad sináptica y de reafirmación de circuitos y redes neuronales determinados, base de los procesos de aprendizaje y memoria 2. Por otra parte, los endocannabinoides también modulan la liberación de otros neurotransmisores como acetilcolina, serotonina, dopamina, adrenalina, etc., por lo que se postula su implicación en otros muchos procesos neurofisiológicos 2,7.
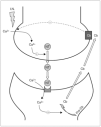
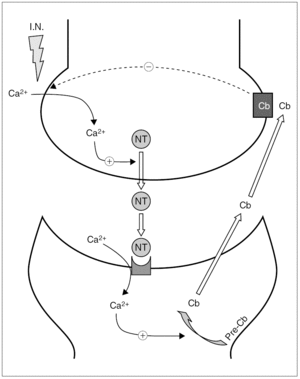
Figura 2.Esquema de la supresión de la neurotransmisión inducida por despolarización (DS) por parte de los endocannabinoides. Llegado el impulso nervioso (IN) al botón terminal sináptico, se induce la entrada de calcio, que determina la translocación de la vesícula con el neurotransmisor (NT) y su consiguiente liberación al espacio intersináptico. Unido a su receptor postsináptico, el neurotransmisor activa la entrada de calcio en la neurona postsináptica. El aumento de calcio intracelular activa las enzimas responsables de transformar el precursor endocannabinoideo (Pre-Cb) en el cannabinoide (Cb). Éste, tras ser liberado, se une retrógradamente con el receptor cannabinoide presináptico, cuya activación tiene como consecuencia final la inhibición de la entrada de calcio y, por ende, de la liberación del neurotransmisor.
Un efecto adicional, pero de importancia, es que los endocannabinoides liberados en virtud de la transmisión sináptica aumentan la actividad enzimática de los astrocitos vecinos, proceso esencial para que estas células garanticen la nutrición de las neuronas 9. Así, los endocannabinoides, además de modular la transmisión sináptica, preservarían el aporte energético a las neuronas necesario para mantener dicha actividad 2,9.
Sistema inmunitario
Los cannabinoides han demostrado diferentes efectos inmunomoduladores; en dosis bajas, los cannabinoides son inmunoestimulantes, y en dosis altas, inmunosupresores 4,13. Estos efectos requieren la intermediación de receptores CB2, y probablemente también VR1, pero igualmente pueden ser independientes de receptores 14. Se ha demostrado un aumento de la producción de endocannabinoides, así como de la expresión de receptores CB2, en células inmunitarias estimuladas por bacterias o por lipopolisacárido; diversos estudios sugieren que los endocannabinoides serían importantes moduladores de la quimiotaxis 14. Por otra parte, los cannabinoides han demostrado un potente efecto antiinflamatorio en diversos modelos de enfermedad, como neurodegeneración, neuroinflamación, enfermedad inflamatoria intestinal o artritis 4,14. Este efecto antiinflamatorio se debe especialmente a la inhibición de la liberación y la síntesis de citocinas (especialmente IL-1 y factor de necrosis tumoral alfa [TNF-α] 4,14), efecto este último que incluye la inhibición de la expresión génica 14. Además, los cannabinoides ejercen efecto modulador sobre linfocitos T helper 4,13,14.
Sistema cardiovascular
Los cannabinoides son vasodilatadores, por un doble mecanismo: en primer lugar, por modular la liberación de catecolaminas 4 y, en segundo lugar, por acción directa sobre los VR1 y posiblemente sobre otros receptores aún no definidos, que inducen la relajación de la fibra muscular vascular mediante un mecanismo dependiente de calcio y que conduciría a la hiperpolarización de dicha fibra muscular en virtud de la apertura de canales de potasio 12. El hecho de que este mecanismo vasodilatador sea especialmente potente en las arterias mesentéricas ha hecho suponer a algunos autores que los endocannabinoides podrían participar en la vasodilatación esplácnica posprandial, que se pondría en marcha tras el aumento de calcio extracelular que conlleva la absorción de nutrientes 12.
Muerte celular
Los cannabinoides han demostrado un efecto inductor de apoptosis en células en cultivo, especialmente en precursores gliales 13. Este efecto, relacionado con la estimulación de la producción de ceramida y la expresión de genes de respuesta rápida, parece muy dependiente del grado de diferenciación celular, lo que ha motivado la investigación del posible uso de los cannabinoides en el tratamiento de tumores de baja diferenciación, como los gliomas o el adenocarcinoma de mama 4,13.
Funciones específicas relacionadas con la perinatología
Gestación
Se ha descrito la presencia de cannabinoides en todos los tejidos y fluidos relacionados con la procreación 16: se encuentran receptores CB en espermatozoides, y se han detectado concentraciones significativas de endocannabinoides en líquido seminal, capa granulosa del ovocito, líquido folicular y líquido oviductal, y en útero. Estos datos, junto con el hecho de que el THC reduzca la movilidad de los espermatozoides, ha llevado a algunos autores a hipotetizar que los endocannabinoides desempeñarían un papel en la capacitación de los espermatozoides, ayudando a seleccionar los más activos para alcanzar el ovocito, y que además garantizarían la fecundación monoespermática: mediante un proceso similar al DSI, la entrada de un espermatozoide induciría la liberación de AEA por el ovocito, lo que inmovilizaría al resto de espermatozoides 16.
Por otra parte, se sabe que en presencia de altas concentraciones de THC o de AEA no progresa la división celular del ovocito fecundado para alcanzar la fase de mórula, y no se verifica el anidamiento del zigoto en el útero 17,18. Estudios histológicos demuestran una disminución de la densidad de receptores CB y un aumento de la actividad de FAAH, tanto en el blastocisto en las horas siguientes a la fecundación, como selectivamente en la zona de implantación del útero, lo que avalaría la necesidad de reducir la actividad de AEA 17. Aunque aún no hay pruebas decisivas que avalen la importancia de los endocannabinoides en la fisiología de la fecundación, estudios en mujeres sometidas a fertilización in vitro han hallado una correlación negativa entre la actividad de FAAH medida en linfocitos y la probabilidad de una nidación exitosa del óvulo fecundado, lo que sugiere realmente cierto papel de los endocannabinoides en los mecanismos de implantación 18. Además, la actividad inmunomoduladora de los endocannabinoides podría ser importante, ya que las células NK (natural killer), fundamentales en la inmunotolerancia al embrión, son ricas en CB2 7.
Finalmente, estudios in vitro con fibras miometriales extraídas tras cesárea han demostrado un efecto inhibidor de la AEA sobre la contractilidad del útero gestante 19, aunque no hay pruebas que impliquen de forma destacada a los cannabinoides, tanto en la quiescencia uterina durante la gestación como en el inicio de la actividad contráctil durante el parto.
Lactancia
Se han detectado concentraciones significativas de endocannabinoides, sobre todo de 2-AG (200 veces más abundante que la AEA) en la leche. Estudios del grupo de la Dra. Fride realizados con ratones recién nacidos han demostrado la función esencial de la activación de los receptores CB1 en el inicio y mantenimiento de la lactancia, especialmente en las primeras 24 h de vida 20,21. Así, la administración de un bloqueante de CB1 a los ratones recién nacidos en su primer día de vida conduce a la muerte por inanición de todas las crías tratadas, mortalidad que se reduce al 50 % si el tratamiento se inicia el segundo día, y al 0 % si se inicia a partir del tercer día 20,21. Asimismo, las crías recién nacidas de ratones manipulados genéticamente para no expresar CB1 no lactan el primer día de vida, presentando una mortalidad espontánea mucho más elevada que los ratones no manipulados 20,21. Los estudios más detallados demuestran que la ausencia de activación de los CB1 el primer día de vida anula el interés de las crías por alimentarse, y en caso de obligarles a introducir el pezón en la boca no son capaces de sujetarlo con fuerza 20. Todos estos resultados, junto con el hallazgo de un espectacular pico de producción de 2-AG en el cerebro en el primer día de vida 22, llevaron al grupo de la Dra. Fride a proponer que los endocannabinoides serían básicos para el inicio de la conducta de lactancia, que luego se preservaría con el auxilio de otros sistemas, especialmente el opioide 21.
Desarrollo cerebral
Existen múltiples datos indirectos que apuntan a un papel relevante de los endocannabinoides en el desarrollo del SNC 23. En primer lugar, la densidad, localización y actividad de los receptores CB en el cerebro varía desde la etapa prenatal a la neonatal, y desde ésta a la edad adulta. Así, dichos receptores se encuentran abundantemente expresados en el feto y el recién nacido en "áreas atípicas", como región subventricular, neocorteza, tronco encefálico y, lo más llamativo, en la sustancia blanca, especialmente en fibras comisurales como cuerpo calloso o comisura anterior 23,24. Todas estas localizaciones desaparecen en el adulto, y, por el contrario, las zonas con más riqueza de receptores en el adulto son notablemente pobres en el feto y el recién nacido. Ya que, como se ha expuesto previamente, la abundancia de receptores CB en las zonas típicas del adulto explica los efectos psicoactivos de los cannabinoides, la diferente distribución de receptores explicaría, en primer lugar, la ausencia dichos efectos observada en niños con cáncer tratados con cannabinoides como antieméticos o analgésicos 20. Por otra parte, las zonas ricas en receptores CB en el feto y recién nacido son precisamente las más implicadas en procesos de proliferación 23. Todo ello apunta a que los endocannabinoides podrían estar involucrados en procesos de migración, proliferación y sinaptogénesis. Finalmente, la presencia de receptores CB en la sustancia blanca 24, junto con la descripción de receptores para endocannabinoides en precursores gliales y el efecto remielinizante de los cannabinoides en modelos animales de desmielinización 25 sugieren que los endocannabinoides, además de participar en procesos proliferativos, podrían ser importantes en procesos de mielinización del cerebro inmaduro.
Por el contrario, también se ha descrito que los cannabinoides actúan sobre la expresión de enzimas reguladoras de la síntesis de neurotransmisores 23. Aunque se duda de la significación fisiológica de este hecho, no cabe duda de que éste podría ser uno de los mecanismos que explicarían los efectos a largo plazo de la exposición prolongada a cannabinoides durante la época fetal, ya que esto podría determinar algún tipo de impronta sobre un cerebro en formación.
Neuroprotección
Diversos estudios en los últimos años sugieren que los cannabinoides podrían desarrollar un importante papel en la neuroprotección, tanto ante los procesos neurodegenerativos agudos como el daño cerebral hipóxico-isquémico o el traumático, como ante procesos crónicos como la esclerosis múltiple, la enfermedad de Parkinson o la de Alzheimer 26,27. El ámbito neonatológico del presente escrito hará que nos ciñamos al posible papel de los cannabinoides en la encefalopatía hipóxico-isquémica neonatal (EHIN).
Varios efectos fisiológicos de los cannabinoides justificarían este papel. Es conocido que tras un episodio hipóxico-isquémico, la disfunción de las bombas iónicas, con la consiguiente alteración de la polaridad transmembrana, permite la entrada de masivas cantidades de calcio en la neurona, lo que activa diferentes enzimas destructivas 28; la disfunción de las bombas permite asimismo la acumulación de neurotransmisores excitotóxicos, como el glutamato, que diversos estudios, incluidos algunos realizados por nuestro grupo 29, han señalado como una pieza de extraordinaria importancia en la cascada neurotóxica 28,29. La acumulación de glutamato crece progresivamente, como causa y efecto de un aumento de la entrada de calcio en la célula 28; asimismo, el glutamato coadyuva a la activación de la síntesis de citocinas, como el factor de necrosis tumoral α (TNF-α), así como a la inducción de la sintetasa de óxido nítrico inducible (iNOS) 29 que conduce a la producción de masivas cantidades de NO 28; tanto citocinas como NO resultan lesivos para la neurona, per se y por participar en la inducción de mecanismos de apoptosis. Finalmente, durante la fase de reperfusión la llegada de grandes cantidades de radicales libres de oxígeno inicia un proceso de estrés oxidativo, ampliado y agravado por el NO, así como por la llegada de células inflamatorias activadas que liberan más radicales libres y más citocinas 28.
En este escenario, los cannabinoides aportan, como primer efecto positivo, el de reducir sustancialmente la entrada de calcio en la neurona 2,3,9. Además, cannabinoides como la AEA son antioxidantes, vasodilatadores, inmunomoduladores y potencian la actividad de los astrocitos 9,26,27. Estos datos explican resultados como el de nuestro grupo, demostrando que el agonista cannabinoide WIN55212 ejerce un potente efecto neuroprotector en ratas recién nacidas 30. En este trabajo, ratas de 7 días de vida fueron sometidas a una variante del llamado modelo de Rice-Vannucci, siéndoles ligada la carótida izquierda y siendo sometidas posteriormente a asfixia con N2 al 100 % durante 10 min; este procedimiento provoca una lesión cerebral, cuantificable en términos de muerte neuronal precoz y tardía 30. En este modelo, el WIN55212 previene ambos tipos de muerte neuronal, y, lo que es más importante, lo consigue pese a ser administrado después del episodio asfíctico 30; este tipo de eficacia, además de ser poco frecuente en los modelos experimentales, que a menudo administran el neuroprotector antes del episodio asfíctico, avala su posible empleo en situación real. En sintonía con estos resultados, otros grupos han demostrado similar efecto protector en modelos de excitotoxicidad cerebral en ratas recién nacidas 31, así como previamente se había demostrado en modelos de isquemia cerebral en animales adultos 32.
En la actualidad, nuestro grupo trabaja con un modelo ex vivo de EHIN, denominado privación de oxígeno y glucosa (POG), en el que unas secciones de cerebro de rata recién nacida (ratas Wistar de 7 días de vida), mantenidas en una solución fisiológica oxigenada, son privadas de oxígeno y glucosa durante 20 min, lo que induce una lesión prácticamente idéntica a la que se obtiene en modelos in vivo29. El modelo de POG de secciones cerebrales no sólo permite el estudio histológico de la lesión, sino que tiene además la ventaja de que la gravedad de dicha lesión puede cuantificarse en términos de cantidad de lactato deshidrogenasa (LDH), enzima intracelular, liberada al medio; esta liberación de LDH sigue un perfil temporal, con un pico 30 min después de la POG y un descenso posterior durante 180 min, por lo que el cálculo del área bajo la curva ofrece un valor correspondiente con la severidad del daño. En este modelo ex vivo, el agonista cannabinoide WIN-55212 previene la muerte celular inducida por la POG, efecto visible en el estudio histológico del cerebro (fig. 3); en el análisis cuantitativo, la protección es aún más eficaz que la de un neuroprotector tan reputado en estudios in vitro como el MK-801, bloqueador de los receptores NMDA (tabla 2). Además, en este modelo se comprueba que el agonista cannabinoide consigue su efecto neuroprotector actuando precisamente sobre varios de los factores más determinantes del daño cerebral hipóxico-isquémico, ya que el WIN-55212 reduce la liberación de glutamato y de TNF-a, e impide la inducción de la iNOS (tabla 2). Además, nuestros datos sugieren que este efecto neuroprotector se media tanto por receptores CB1 como CB2, ya que tanto el SR141716 (antagonista de receptores CB1), como el SR144528 (antagonista de receptores CB2), inhiben los efectos del WIN-55212 (tabla 2).
Figura 3. Microfotografías mostrando la celularidad del núcleo estriado de secciones de cerebro de ratas de 7 días de vida, teñidas con técnica de Nissl (microscopia óptica, x400 aumentos en el original; escala: 100 μm).A)Secciones mantenidas en solución fisiológica con glucosa y oxigenada.B)Secciones expuestas a privación de oxígeno y glucosa (POG) durante 30 min.C)Secciones sometidas a POG pero en presencia del agonista cannabinoide WIN55212 (50 μM). Obsérvese la disminución de la densidad de neuronas viables en B, y el efecto protector del WIN en C.
Las características de los endocannabinoides han conducido a varios autores a postular que el cannabinoide podría constituir un sistema natural de neuroprotección 1. El que eventos relevantes de la cascada neurotóxica, como el aumento intracelular de calcio y la activación de lipasas, sean precisamente los inductores de la síntesis de cannabinoides, justificaría este papel. Experimentos que demuestran una elevación de la concentración cerebral de NAE tras inducir una lesión cerebral en ratas recién nacidas mediante inyección intracerebral de NMDA o mediante un traumatismo cerrado 33, apuntan en este sentido. No deja de ser sugerente el hallazgo ya comentado de una importante elevación de la concentración cerebral de 2-AG en el cerebro en el primer día de vida 22, justo después de que el cerebro haya tenido que afrontar las vicisitudes del parto y se vea expuesto a un aumento dramático del estrés oxidativo. El principal problema de este efecto neuroprotector natural estriba en que la recaptación y posterior degradación de los endocannabinoides es tan rápida que la vida media de estos compuestos es extraordinariamente breve 1-3.
El posible uso de los cannabinoides como neuroprotectores en la EHIN queda limitado por el riesgo, no confirmado pero teórico, de unos posibles efectos secundarios sobre el cerebro en desarrollo incluso con la administración de estos compuestos durante breve tiempo. Mientras este extremo se dilucida, dos grandes vías de investigación podrían aportar una solución. Una contempla la posibilidad de prolongar el "tono endocannabinoide", inhibiendo la recaptación y/o degradación de éstos, ya que actualmente se han sintetizado compuestos que bloquean tanto la AMT como la FAAH; habida cuenta de que, tras un episodio isquémico cerebral en animales, se ha observado un aumento de la expresión de los receptores CB en las zonas de penumbra periisquémicas, esta estrategia conseguiría un mayor efecto precisamente en la zona cerebral de mayor potencial de rescate 27. La otra alternativa proviene de resultados como el de nuestro grupo, demostrando un papel destacado de los receptores CB2 en el efecto neuroprotector del WIN55212 en el modelo ex vivo de EHIN; el empleo de agonistas selectivos CB2 eliminaría todo el potencial efecto psicoactivo del tratamiento, ya que este se desarrolla exclusivamente a través de los receptores CB1 7.