En este momento existen todavía grandes interrogantes acerca de las características de enfermedad causada por el nuevo coronavirus (COVID-19) en los niños, así como acerca de los factores asociados al desarrollo de formas graves de la enfermedad.
MétodosEstudio retrospectivo que incluye pacientes menores de 18 años ingresados debido a infección por SARS-CoV-2. La infección fue confirmada por la reacción en cadena de la transcriptasa inversa-polimerasa (RT-PCR) en tiempo real o por serología. Describimos los datos epidemiológicos y clínicos, los hallazgos de laboratorio y de imágenes, así como el tratamiento y la evolución de estos pacientes. Los pacientes se clasificaron en dos grupos de gravedad y luego se compararon.
ResultadosSe incluyeron 39 niños, con una mediana de edad de nueve años (rango 12 días-16 años); 23 eran varones. Los casos con evolución no complicada (24) se presentaron en su mayoría con fiebre y/o síntomas respiratorios sin alteraciones significativas en los hallazgos de laboratorio. De los 15 niños con enfermedad complicada, 12 desarrollaron shock. Además de la fiebre, frecuentemente presentaban alteraciones de la apariencia, taquicardia extrema, dolor abdominal, vómitos, diarrea, erupción cutánea y/o hiperemia conjuntival. También mostraron mayor linfopenia (p = 0,001), elevación de la proporción neutrófilos/linfocitos (p = 0,001), proteína C reactiva (p < 0,001), procalcitonina (p = 0,001), dímero D (p < 0,001) y ferritina (p < 0,001).
ConclusionesLa infección por SARS-CoV-2 en niños ingresados se presenta con una gran variabilidad clínica. Cuando se les proporciona tratamiento de soporte, los pacientes con síntomas respiratorios que no tienen alteración de las pruebas de laboratorio, generalmente tienen una enfermedad no complicada. Los pacientes con enfermedad complicada se presentan principalmente con fiebre y síntomas abdominales y/o mucocutáneos, la mayoría desarrollan un shock. La elevación de los marcadores inflamatorios puede permitir una detección temprana y el pronóstico final es bueno.
At this time there are still major questions about the characteristics of disease caused by the new coronavirus (COVID-19) in children as well as factors associated with the development of severe forms of the disease.
Study designRetrospective study including patients under 18 years of age admitted with SARS-CoV-2 infection from March 1 to April 30, 2020. Infection was confirmed by realtime reverse transcriptase–polymerase chain reaction (RT-PCR) or antibody testing. We describe the epidemiological and clinical data, laboratory and imaging findings, as well as treatment and outcome in these patients. In light of these findings, patients were classified into two severity groups and then compared.
ResultsThirty-nine children were included, with a median age of 9 years (range 12 days-16 years); 23 were boys. Cases with uncomplicated disease course (24) mostly presented to the emergency department (ED) with fever and/or respiratory symptoms without significant alterations in laboratory findings. Of the 15 children with a complicated course, 12 developed shock. In addition to fever, they frequently presented altered appearance, extreme tachycardia, abdominal pain, vomiting, diarrhea, rash, and/or conjunctival hyperemia. They also showed greater lymphopenia (p = 0.001), elevated neutrophil/lymphocyte ratio (p = 0.001), C-reactive protein (p < 0.001), procalcitonin (p = 0.001), D-dimer (p < 0.001), and ferritin (p < 0.001).
ConclusionsSARS-CoV-2 infection in admitted children presents with great clinical variability. When provided supportive care, patients with predominant respiratory symptoms without altered laboratory-test results generally have an uncomplicated course. Patients with complicated disease present mainly with fever and abdominal and/or mucocutaneous symptoms. Most develop shock. Elevation of inflammatory markers may allow for early detection and the final outcome is good.
En España, el primer caso de coronavirus 2019 (COVID-19), causado por el nuevo coronavirus SARS-CoV-21, fue detectado el 31 de enero de 2020. En las semanas siguientes, el SARS-CoV-2 se propagó por todo el país, afectando más intensamente a la región de Madrid2.
Con el fin de optimizar los recursos sanitarios, a partir del 20 de marzo, la atención pediátrica urgente se centralizó en dos hospitales terciarios de la Comunidad Autónoma. Estos dos centros se encargaron de proporcionar atención urgente, hospitalización y cuidados intensivos a una población de aproximadamente 1.345.000 menores de 18 años.
Aunque el SARS-CoV-2 puede infectar a personas de cualquier edad, la incidencia general de la infección entre los niños se ha estimado en un 1 a 2%3–5. La prevalencia en niños en nuestro país, según el estudio de seroprevalencia llevado a cabo en mayo de 2020 oscila entre el 1 y el 5%6. Los niños desarrollan formas de la enfermedad menos graves que los adultos y tienen en general mejor pronóstico que éstos7.
Los síntomas más comúnmente descritos en los niños con infección por el SARS-CoV-2 se parecen a los observados en otras infecciones de las vías respiratorias superiores8, es decir, tos, fiebre, dolor de garganta, rinorrea y mialgias9. Los síntomas gastrointestinales también son frecuentes en esta población e incluyen hiporexia, náuseas, vómitos y diarrea. Se ha descrito en niños un síndrome inflamatorio múltiple con shock secundario a la infección por SARS-CoV-2, que puede cursar con fallo multiorgánico, y se considera una de las formas más graves de la enfermedad en la población pediátrica10–12. Esta forma clínica de la enfermedad habitualmente cursa con fiebre alta y síntomas digestivos (en casi todos los casos con dolor abdominal intenso).
En el momento actual, no se ha categorizado bien el espectro de enfermedad por la infección SARS-CoV-2 en edad pediátrica. Faltan datos sobre el curso clínico y los marcadores de pronóstico en los niños ingresados. En el presente trabajo se describen los datos epidemiológicos, las diferentes formas de presentación clínica y los factores de riesgo de enfermedad complicada entre los niños hospitalizados con COVID-19.
Pacientes y métodosPoblación del estudioSe realizó un estudio observacional retrospectivo entre el 1 de marzo y el 30 de abril de 2020 en el Hospital Infantil Universitario Niño Jesús, que es un hospital terciario pediátrico de Madrid, España. El comité de ética del hospital aprobó este estudio. Todos los datos se obtuvieron con el consentimiento de los padres o cuidadores.
Los criterios de inclusión fueron los siguientes:
- -
Pacientes menores de 18 años de edad que requirieron ingreso a consecuencia de la infección por SARS-CoV-2.
- -
Infección por SARS-CoV-2 confirmada utilizando la reacción en cadena de la transcriptasa inversa-polimerasa (RT-PCR) en tiempo real en una muestra recogida con hisopo nasal y faríngeo o por la presencia de anticuerpos IgG en una muestra de sangre.
Los criterios de exclusión fueron los siguientes:
- -
Niños con enfermedades oncológicas.
- -
Pacientes ingresados en los que se obtuvo PCR positiva para SARS-CoV-2, pero dicha infección no fue el motivo del ingreso.
Los criterios para confirmar la infección por SARS-CoV-2 en los casos sospechosos variaron a lo largo de la pandemia. No se buscó la infección en los pacientes que no tenían criterios de ingreso. Antes del 11 de marzo, se realizó RT-PCR a los pacientes ingresados en el hospital si presentaban síntomas de infección respiratoria aguda y habían viajado a zonas en las que se habían encontrado pruebas de transmisión en la comunidad o si los pacientes habían estado en contacto estrecho con un caso probable o confirmado en los 14 días anteriores. A partir del 11 de marzo se encontraron pruebas de propagación en la comunidad en la Comunidad Autónoma, por lo que se solicitó RT-PCR a todos los pacientes ingresados con síntomas compatibles con COVID-19. También se buscó la infección en los niños que requerían cirugía urgente o que habían estado en contacto con casos confirmados o sospechosos de COVID-19 en el hogar y requerían ingreso, siendo estos casos excluidos del análisis en nuestro trabajo. La indicación para confirmar la infección fue valorada individualmente en los pacientes con una enfermedad de base. Las pruebas serológicas estuvieron disponibles a finales de abril y se realizaron en muestras de sangre venosa. No se realizaron pruebas para confirmar la presencia de otros virus respiratorios de forma rutinaria. Se obtuvieron cultivos de sangre en caso de fiebre. Los criterios de ingreso fueron los mismos que se aplican habitualmente, según los protocolos habituales del centro para el manejo de cada entidad clínica, sin que éstos se vieran influidos por la positividad de las pruebas para detectar la infección por SARS-CoV-2.
Definiciones- -
Enfermedad complicada: necesidad de estabilización hemodinámica (infusión de volumen o fármacos vasopresores) o de soporte respiratorio (cánula nasal de alto flujo, ventilación no invasiva o ventilación mecánica) o presencia de encefalopatía.
- -
Enfermedad no complicada: pacientes que no requieren estabilización hemodinámica o asistencia respiratoria que no sea oxígeno suplementario administrado a través de una cánula nasal o pacientes que no presentan encefalopatía.
- -
Taquicardia: frecuencia cardíaca superior al percentil 90 por grupo de edad y taquicardia extrema para las frecuencias cardíacas superiores al percentil 99, según los valores de referencia13.
Se obtuvieron datos epidemiológicos, clínicos y de laboratorio en el momento del ingreso, hallazgos radiológicos durante la estancia hospitalaria, así como el tratamiento y la evolución. Estos datos se recopilaron a partir de las historias clínicas de los pacientes y mediante entrevista telefónica con los padres después del alta para reunir datos sobre las complicaciones y la evolución después del alta. La indicación de pruebas complementarias la decidió el médico responsable de cada paciente, siguiendo los protocolos habituales previos a la pandemia.
Pruebas de imagenSe realizó una radiografía de tórax en caso de sospecha de neumonía, basada en los hallazgos clínicos.
Se indicó ecografía abdominal en caso de sospecha de abdomen agudo o en pacientes que presentaban inestabilidad hemodinámica con dolor abdominal asociado.
Los resultados de todas las pruebas radiológicas fueron interpretados por un radiólogo pediátrico.
Análisis estadísticoEl análisis descriptivo de los resultados se llevó a cabo utilizando el software SPSS© para Windows (versión 20.0). Se utilizaron la mediana y el rango intercuartílico para los datos cuantitativos. Para los datos cualitativos se utilizaron el porcentaje, el rango y el rango intercuartil. Se utilizó la prueba U de Mann-Whitney para comparar las variables continuas, y se consideró la significación estadística cuando α fue inferior a 0,05.
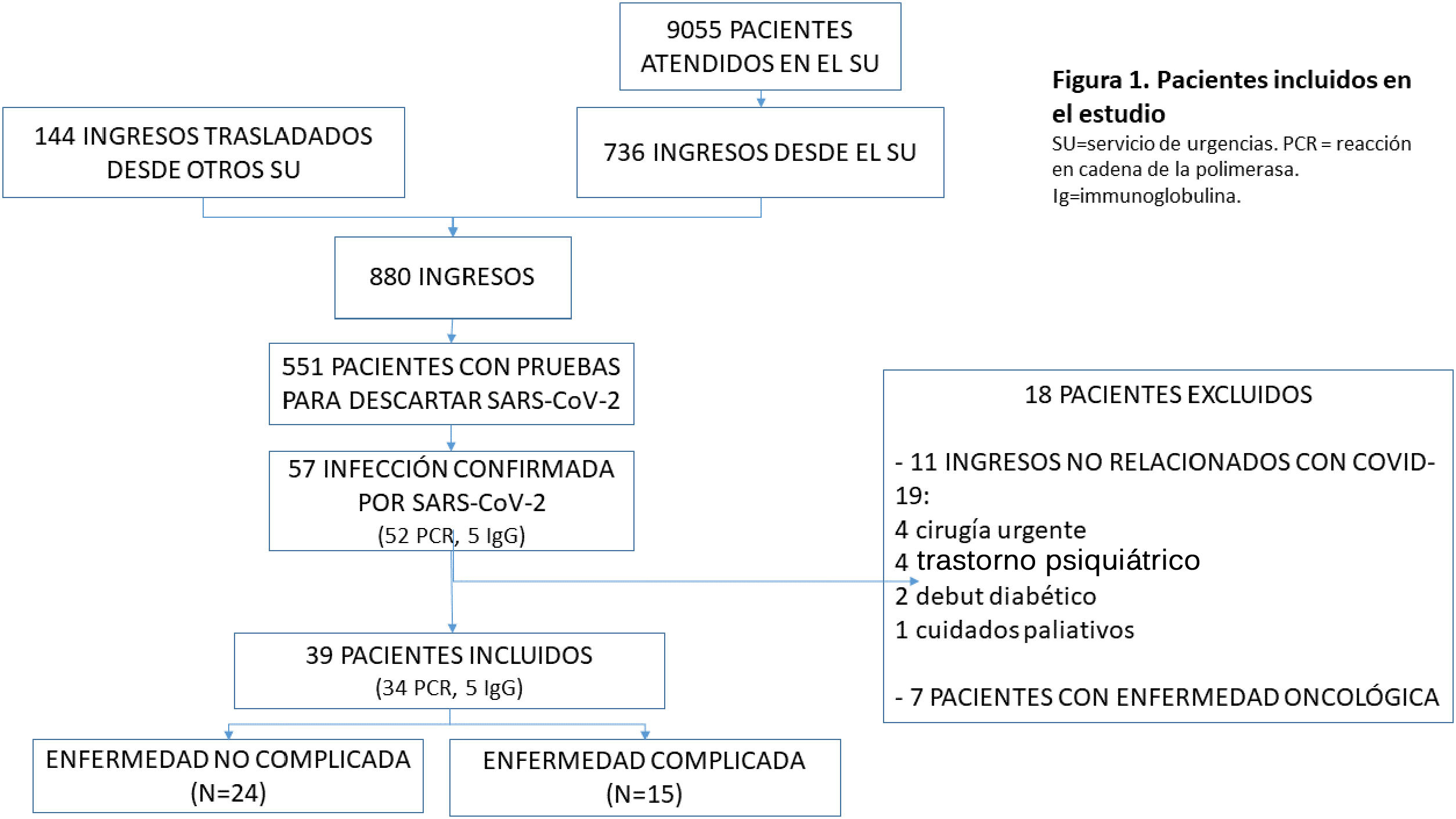
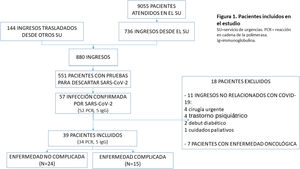
ResultadosDurante el período de estudio, 880 pacientes fueron ingresados en el hospital. En 551 se realizó RT-PCR para SARS-CoV-2 en frotis nasofaríngeo; 52 tuvieron un resultado positivo. Cinco pacientes con resultado negativo en la RT-PCR y una presentación clínica muy sugestiva de COVID-19 tenían anticuerpos Ig G detectables frente al SARS-CoV-2. Once pacientes fueron excluidos porque el motivo de ingreso no estaba directamente relacionado con la infección por el SARS-CoV-2; todos eran asintomáticos o presentaban síntomas respiratorios o gastrointestinales leves. Siete pacientes en tratamiento con quimioterapia fueron excluidos. Finalmente, se analizaron 39 pacientes para este estudio (fig. 1).
Características epidemiológicasLa mediana de era de edad nueve años (rango: 12 días-16 años); 12 (31%) tenían menos de un año de edad, cinco (13%) tenían entre uno y cinco años de edad, nueve (23%) tenían entre seis y 10 años, y 13 (33%) eran mayores de 10 años; 23 (59%) eran varones; 27 pacientes (69%) tuvieron contacto en el hogar con un caso confirmado (siete) o sospechado (20) de COVID-19. En 12 niños se desconocía la posible exposición.
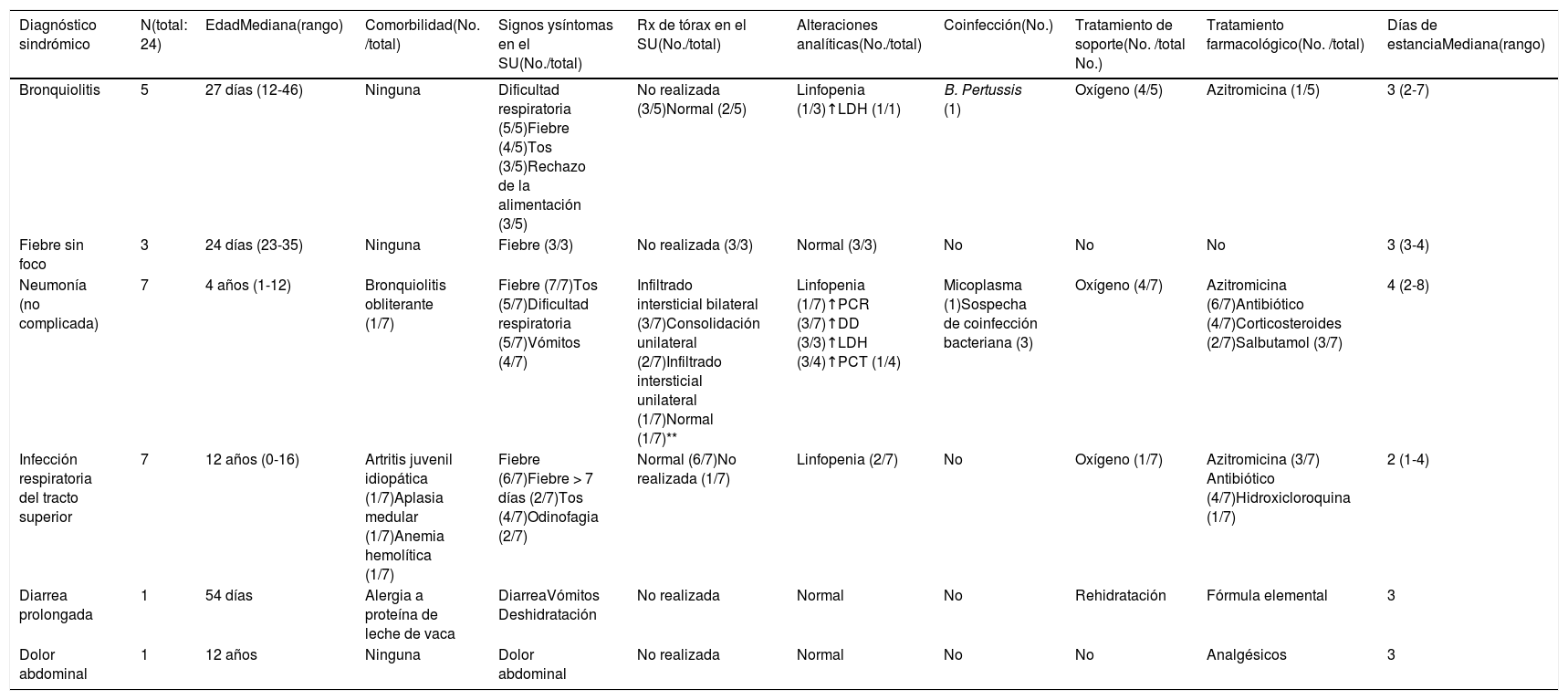
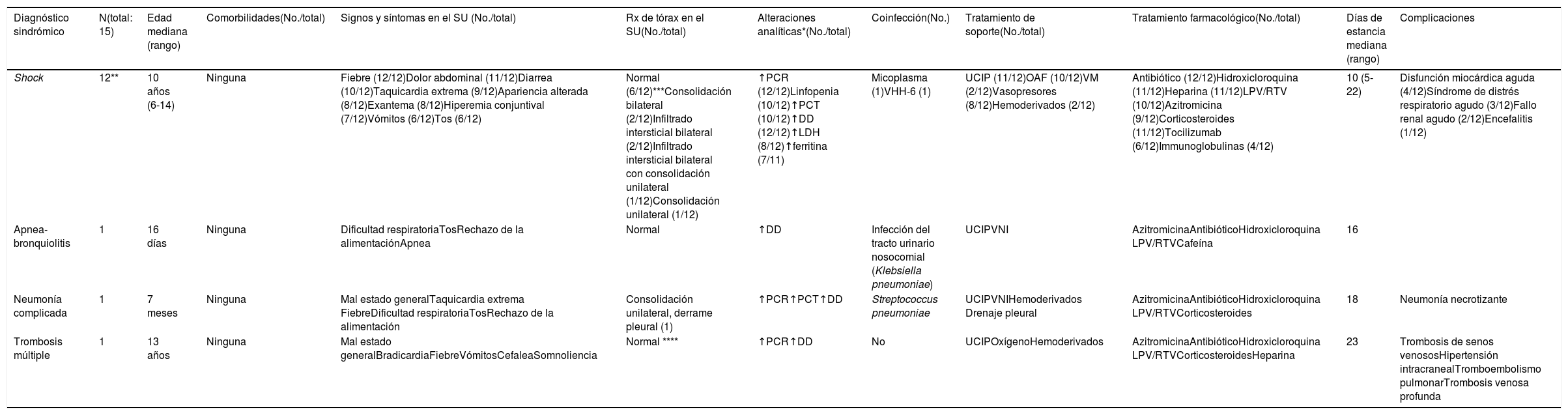
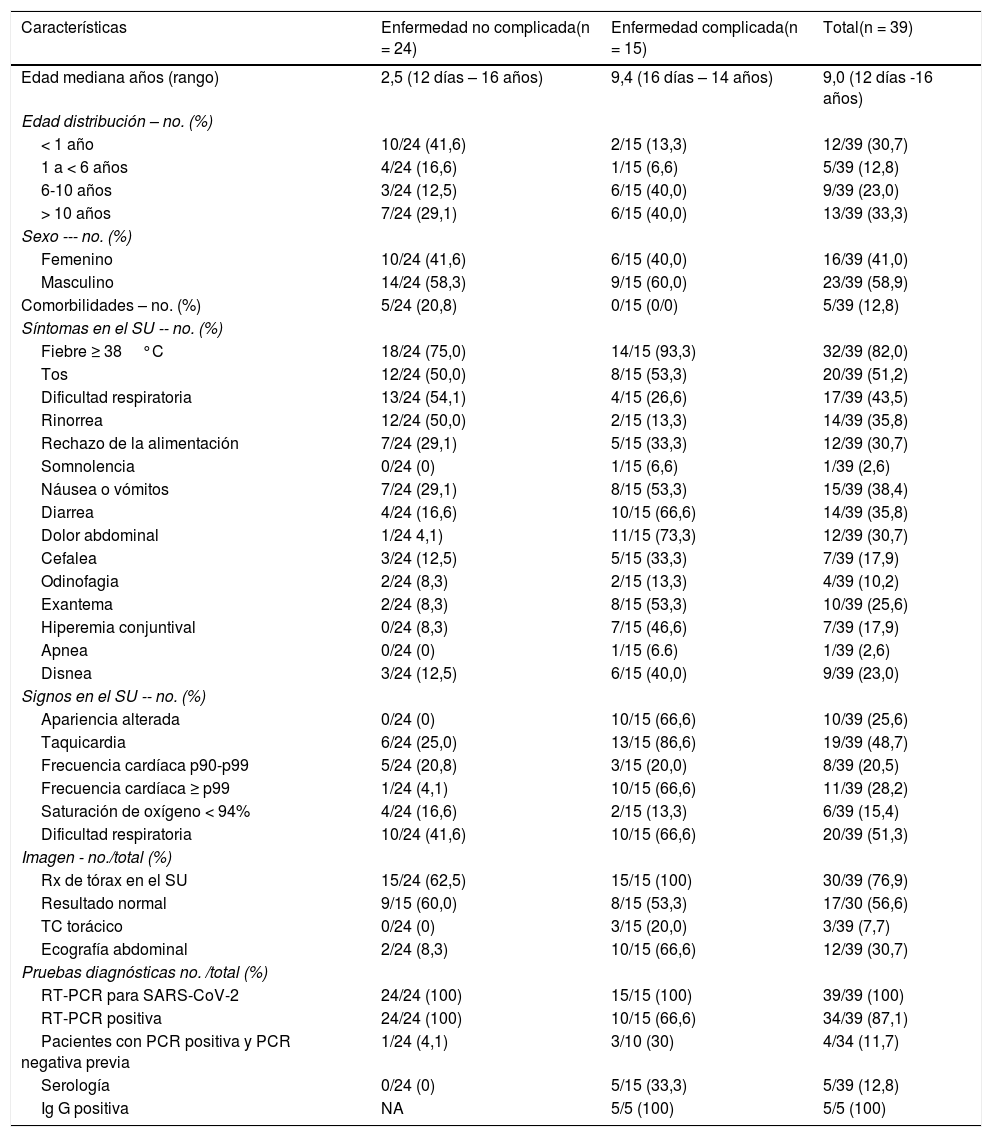
Características clínicas y analíticas, curso no complicado versus curso complicadoSe utilizó un diagnóstico sindrómico para clasificar a los pacientes incluidos. Se encontró que 24 pacientes tenían una enfermedad no complicada (tabla 1) y 15 una enfermedad complicada (tabla 2). Los cinco pacientes que tenían una enfermedad subyacente desarrollaron una enfermedad no complicada. La mayoría de los niños con enfermedad complicada mostraron alteración en la apariencia (10/15) y taquicardia extrema (10/15) en la evaluación inicial en el servicio de urgencias (SU). La saturación de oxígeno < 94% fue poco frecuente en ambos grupos. Las características clínicas de todos los casos se resumen en la tabla 3.
Características epidemiológicas, hallazgos clínicos y tratamiento de los pacientes ingresados con enfermedad no complicada
| Diagnóstico sindrómico | N(total: 24) | EdadMediana(rango) | Comorbilidad(No. /total) | Signos ysíntomas en el SU(No./total) | Rx de tórax en el SU(No./total) | Alteraciones analíticas(No./total) | Coinfección(No.) | Tratamiento de soporte(No. /total No.) | Tratamiento farmacológico(No. /total) | Días de estanciaMediana(rango) |
|---|---|---|---|---|---|---|---|---|---|---|
| Bronquiolitis | 5 | 27 días (12-46) | Ninguna | Dificultad respiratoria (5/5)Fiebre (4/5)Tos (3/5)Rechazo de la alimentación (3/5) | No realizada (3/5)Normal (2/5) | Linfopenia (1/3)↑LDH (1/1) | B. Pertussis (1) | Oxígeno (4/5) | Azitromicina (1/5) | 3 (2-7) |
| Fiebre sin foco | 3 | 24 días (23-35) | Ninguna | Fiebre (3/3) | No realizada (3/3) | Normal (3/3) | No | No | No | 3 (3-4) |
| Neumonía (no complicada) | 7 | 4 años (1-12) | Bronquiolitis obliterante (1/7) | Fiebre (7/7)Tos (5/7)Dificultad respiratoria (5/7)Vómitos (4/7) | Infiltrado intersticial bilateral (3/7)Consolidación unilateral (2/7)Infiltrado intersticial unilateral (1/7)Normal (1/7)** | Linfopenia (1/7)↑PCR (3/7)↑DD (3/3)↑LDH (3/4)↑PCT (1/4) | Micoplasma (1)Sospecha de coinfección bacteriana (3) | Oxígeno (4/7) | Azitromicina (6/7)Antibiótico (4/7)Corticosteroides (2/7)Salbutamol (3/7) | 4 (2-8) |
| Infección respiratoria del tracto superior | 7 | 12 años (0-16) | Artritis juvenil idiopática (1/7)Aplasia medular (1/7)Anemia hemolítica (1/7) | Fiebre (6/7)Fiebre > 7 días (2/7)Tos (4/7)Odinofagia (2/7) | Normal (6/7)No realizada (1/7) | Linfopenia (2/7) | No | Oxígeno (1/7) | Azitromicina (3/7) Antibiótico (4/7)Hidroxicloroquina (1/7) | 2 (1-4) |
| Diarrea prolongada | 1 | 54 días | Alergia a proteína de leche de vaca | DiarreaVómitos Deshidratación | No realizada | Normal | No | Rehidratación | Fórmula elemental | 3 |
| Dolor abdominal | 1 | 12 años | Ninguna | Dolor abdominal | No realizada | Normal | No | No | Analgésicos | 3 |
PCR = proteína C reactiva. PCT= procalcitonina. DD = dímero D. LDH = lactato deshidrogenasa, Rx = radiografía. SatO2 = saturación de oxígeno. SU = Servicio de Urgencias.
*Alteración analítica: considerada si PCR ≥ 5 mg/dL, PCT ≥ 2 ng/mL, DD ≥ 500 ng/mL, ferritina ≥ 500 ng/mL, LDH ≥ 300 U/L y linfocitos < 1.000 x 109/L
Características epidemiológicas, clínicas y evolución de los pacientes ingresados con enfermedad complicada
| Diagnóstico sindrómico | N(total: 15) | Edad mediana (rango) | Comorbilidades(No./total) | Signos y síntomas en el SU (No./total) | Rx de tórax en el SU(No./total) | Alteraciones analíticas*(No./total) | Coinfección(No.) | Tratamiento de soporte(No./total) | Tratamiento farmacológico(No./total) | Días de estancia mediana (rango) | Complicaciones |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Shock | 12** | 10 años (6-14) | Ninguna | Fiebre (12/12)Dolor abdominal (11/12)Diarrea (10/12)Taquicardia extrema (9/12)Apariencia alterada (8/12)Exantema (8/12)Hiperemia conjuntival (7/12)Vómitos (6/12)Tos (6/12) | Normal (6/12)***Consolidación bilateral (2/12)Infiltrado intersticial bilateral (2/12)Infiltrado intersticial bilateral con consolidación unilateral (1/12)Consolidación unilateral (1/12) | ↑PCR (12/12)Linfopenia (10/12)↑PCT (10/12)↑DD (12/12)↑LDH (8/12)↑ferritina (7/11) | Micoplasma (1)VHH-6 (1) | UCIP (11/12)OAF (10/12)VM (2/12)Vasopresores (8/12)Hemoderivados (2/12) | Antibiótico (12/12)Hidroxicloroquina (11/12)Heparina (11/12)LPV/RTV (10/12)Azitromicina (9/12)Corticosteroides (11/12)Tocilizumab (6/12)Immunoglobulinas (4/12) | 10 (5-22) | Disfunción miocárdica aguda (4/12)Síndrome de distrés respiratorio agudo (3/12)Fallo renal agudo (2/12)Encefalitis (1/12) |
| Apnea-bronquiolitis | 1 | 16 días | Ninguna | Dificultad respiratoriaTosRechazo de la alimentaciónApnea | Normal | ↑DD | Infección del tracto urinario nosocomial (Klebsiella pneumoniae) | UCIPVNI | AzitromicinaAntibióticoHidroxicloroquina LPV/RTVCafeína | 16 | |
| Neumonía complicada | 1 | 7 meses | Ninguna | Mal estado generalTaquicardia extrema FiebreDificultad respiratoriaTosRechazo de la alimentación | Consolidación unilateral, derrame pleural (1) | ↑PCR↑PCT↑DD | Streptococcus pneumoniae | UCIPVNIHemoderivados Drenaje pleural | AzitromicinaAntibióticoHidroxicloroquina LPV/RTVCorticosteroides | 18 | Neumonía necrotizante |
| Trombosis múltiple | 1 | 13 años | Ninguna | Mal estado generalBradicardiaFiebreVómitosCefaleaSomnoliencia | Normal **** | ↑PCR↑DD | No | UCIPOxígenoHemoderivados | AzitromicinaAntibióticoHidroxicloroquina LPV/RTVCorticosteroidesHeparina | 23 | Trombosis de senos venososHipertensión intracranealTromboembolismo pulmonarTrombosis venosa profunda |
DD = dímero D. LDH = lactato deshidrogenasa. LPV/RTV = lopinavir/ritonavir. OAF = oxigenoterapia de alto flujo. PCR= proteína C reactiva. PCT = procalcitonina. Rx = radiografía. SatO2 = saturación de oxígeno. SU: Servicio de Urgencias. UCIP = unidad de cuidados intensivos pediátricos. VM = ventilación mecánica con intubación endotraqueal. VNI = ventilación no invasiva.
Características epidemiológicas y clínicas de los pacientes
| Características | Enfermedad no complicada(n = 24) | Enfermedad complicada(n = 15) | Total(n = 39) |
|---|---|---|---|
| Edad mediana años (rango) | 2,5 (12 días – 16 años) | 9,4 (16 días – 14 años) | 9,0 (12 días -16 años) |
| Edad distribución – no. (%) | |||
| < 1 año | 10/24 (41,6) | 2/15 (13,3) | 12/39 (30,7) |
| 1 a < 6 años | 4/24 (16,6) | 1/15 (6,6) | 5/39 (12,8) |
| 6-10 años | 3/24 (12,5) | 6/15 (40,0) | 9/39 (23,0) |
| > 10 años | 7/24 (29,1) | 6/15 (40,0) | 13/39 (33,3) |
| Sexo --- no. (%) | |||
| Femenino | 10/24 (41,6) | 6/15 (40,0) | 16/39 (41,0) |
| Masculino | 14/24 (58,3) | 9/15 (60,0) | 23/39 (58,9) |
| Comorbilidades – no. (%) | 5/24 (20,8) | 0/15 (0/0) | 5/39 (12,8) |
| Síntomas en el SU -- no. (%) | |||
| Fiebre ≥ 38°C | 18/24 (75,0) | 14/15 (93,3) | 32/39 (82,0) |
| Tos | 12/24 (50,0) | 8/15 (53,3) | 20/39 (51,2) |
| Dificultad respiratoria | 13/24 (54,1) | 4/15 (26,6) | 17/39 (43,5) |
| Rinorrea | 12/24 (50,0) | 2/15 (13,3) | 14/39 (35,8) |
| Rechazo de la alimentación | 7/24 (29,1) | 5/15 (33,3) | 12/39 (30,7) |
| Somnolencia | 0/24 (0) | 1/15 (6,6) | 1/39 (2,6) |
| Náusea o vómitos | 7/24 (29,1) | 8/15 (53,3) | 15/39 (38,4) |
| Diarrea | 4/24 (16,6) | 10/15 (66,6) | 14/39 (35,8) |
| Dolor abdominal | 1/24 4,1) | 11/15 (73,3) | 12/39 (30,7) |
| Cefalea | 3/24 (12,5) | 5/15 (33,3) | 7/39 (17,9) |
| Odinofagia | 2/24 (8,3) | 2/15 (13,3) | 4/39 (10,2) |
| Exantema | 2/24 (8,3) | 8/15 (53,3) | 10/39 (25,6) |
| Hiperemia conjuntival | 0/24 (8,3) | 7/15 (46,6) | 7/39 (17,9) |
| Apnea | 0/24 (0) | 1/15 (6.6) | 1/39 (2,6) |
| Disnea | 3/24 (12,5) | 6/15 (40,0) | 9/39 (23,0) |
| Signos en el SU -- no. (%) | |||
| Apariencia alterada | 0/24 (0) | 10/15 (66,6) | 10/39 (25,6) |
| Taquicardia | 6/24 (25,0) | 13/15 (86,6) | 19/39 (48,7) |
| Frecuencia cardíaca p90-p99 | 5/24 (20,8) | 3/15 (20,0) | 8/39 (20,5) |
| Frecuencia cardíaca ≥ p99 | 1/24 (4,1) | 10/15 (66,6) | 11/39 (28,2) |
| Saturación de oxígeno < 94% | 4/24 (16,6) | 2/15 (13,3) | 6/39 (15,4) |
| Dificultad respiratoria | 10/24 (41,6) | 10/15 (66,6) | 20/39 (51,3) |
| Imagen - no./total (%) | |||
| Rx de tórax en el SU | 15/24 (62,5) | 15/15 (100) | 30/39 (76,9) |
| Resultado normal | 9/15 (60,0) | 8/15 (53,3) | 17/30 (56,6) |
| TC torácico | 0/24 (0) | 3/15 (20,0) | 3/39 (7,7) |
| Ecografía abdominal | 2/24 (8,3) | 10/15 (66,6) | 12/39 (30,7) |
| Pruebas diagnósticas no. /total (%) | |||
| RT-PCR para SARS-CoV-2 | 24/24 (100) | 15/15 (100) | 39/39 (100) |
| RT-PCR positiva | 24/24 (100) | 10/15 (66,6) | 34/39 (87,1) |
| Pacientes con PCR positiva y PCR negativa previa | 1/24 (4,1) | 3/10 (30) | 4/34 (11,7) |
| Serología | 0/24 (0) | 5/15 (33,3) | 5/39 (12,8) |
| Ig G positiva | NA | 5/5 (100) | 5/5 (100) |
RT-PCR = reacción en cadena de la transcriptasa inversa-polimerasa en tiempo real. Rx = radiografía. SatO2 = saturación de oxígeno. SU = Servicio de Urgencias. TC = tomografía computarizada.
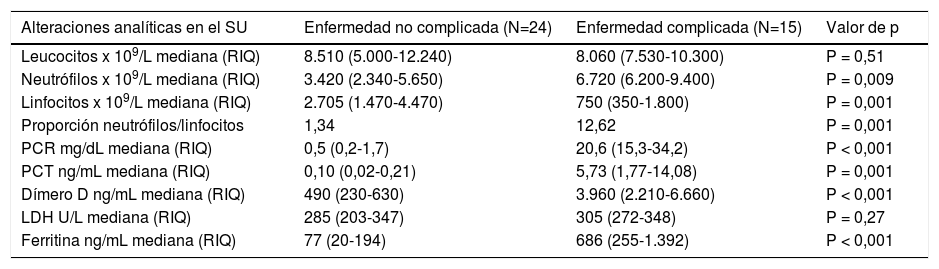
Las pruebas de laboratorio y los resultados de los biomarcadores se resumen y comparan en la tabla 4. Encontramos una diferencia significativa entre ambos grupos en términos de recuento de linfocitos, nivel de proteína C reactiva, procalcitonina, ferritina y dímero D. Además, la proporción de neutrófilos/linfocitos fue mayor entre los pacientes con enfermedad complicada (p = 0,001).
Alteraciones analíticas en el SU
| Alteraciones analíticas en el SU | Enfermedad no complicada (N=24) | Enfermedad complicada (N=15) | Valor de p |
|---|---|---|---|
| Leucocitos x 109/L mediana (RIQ) | 8.510 (5.000-12.240) | 8.060 (7.530-10.300) | P = 0,51 |
| Neutrófilos x 109/L mediana (RIQ) | 3.420 (2.340-5.650) | 6.720 (6.200-9.400) | P = 0,009 |
| Linfocitos x 109/L mediana (RIQ) | 2.705 (1.470-4.470) | 750 (350-1.800) | P = 0,001 |
| Proporción neutrófilos/linfocitos | 1,34 | 12,62 | P = 0,001 |
| PCR mg/dL mediana (RIQ) | 0,5 (0,2-1,7) | 20,6 (15,3-34,2) | P < 0,001 |
| PCT ng/mL mediana (RIQ) | 0,10 (0,02-0,21) | 5,73 (1,77-14,08) | P = 0,001 |
| Dímero D ng/mL mediana (RIQ) | 490 (230-630) | 3.960 (2.210-6.660) | P < 0,001 |
| LDH U/L mediana (RIQ) | 285 (203-347) | 305 (272-348) | P = 0,27 |
| Ferritina ng/mL mediana (RIQ) | 77 (20-194) | 686 (255-1.392) | P < 0,001 |
PCR = proteína C reactiva. PCT = procalcitonina. DD = dímero D. LDH = lactato deshidrogenasa. RIQ = rango intercuartílico.
Se realizó una radiografía de tórax en el SU a 30 pacientes, de las cuales 13 presentaron alteraciones (tabla 3). Durante el ingreso, otros cuatro pacientes desarrollaron neumonía.
Se realizó una ecografía abdominal a 12 pacientes; los hallazgos más frecuentes fueron la inflamación de la pared intestinal (4/12) y la presencia de líquido libre (4/12). Tres pacientes tuvieron una ecografía normal.
Curso clínico e ingreso en cuidados intensivos pediátricosCatorce pacientes (36%) requirieron ingreso en la unidad de cuidados intensivos pediátricos (UCIP): 10 directamente desde el SU y 4 desde la planta de hospitalización (todos en las primeras 36 horas desde su ingreso). Durante las primeras cinco semanas del período de estudio, tres pacientes fueron admitidos en la UCIP con síntomas neurológicos o respiratorios (uno trombosis múltiple, uno apnea, uno neumonía neumocócica). En las dos semanas siguientes, 11 niños requirieron cuidados en la UCIP con sospecha de un cuadro de respuesta inflamatoria sistémica pediátrico temporalmente asociado a COVID-19, la mayoría presentando síntomas abdominales y shock.
La mediana de estancia en el hospital fue de cuatro días (rango 1-23) y de estancia en la UCIP fue de cinco días (rango 2-21). Todos los niños fueron dados de alta sin secuelas aparentes y ninguno de ellos desarrolló complicaciones después del alta.
DiscusiónA pesar de la propagación mundial de la COVID-19, el espectro clínico en los niños sigue sin estar aclarado. Aún no se conoce completamente el papel que juegan los niños en la transmisión de la enfermedad y el mecanismo de infección infantil. La agrupación de casos en familias se ha descrito en varios trabajos7,8,10,14,15 y parece que los niños son los más comúnmente infectados por los adultos, probablemente como resultado de las medidas de confinamiento aplicadas para frenar la propagación del virus. En nuestro estudio, la mayoría de los niños (70%) tuvieron una exposición previa a un adulto con COVID-19 confirmado o sospechado en el hogar, lo que sugiere que los niños no eran el caso índice.
Se ha afirmado que la COVID-19 es más leve y menos frecuente en los niños que en los adultos16–20. Durante el período de estudio, 57 niños con infección por SARS-CoV-2 fueron ingresados en uno de los dos hospitales de referencia para niños hospitalizados en la Comunidad Autónoma de Madrid, aunque éstos sólo representaron el 6,4% de los ingresos hospitalarios. En el mismo período, el número total de adultos con COVID-19 ingresados en diferentes hospitales de la comunidad autónoma superó los 40.0003. Esta disparidad apunta claramente a un curso de la enfermedad más leve y menos frecuente en los niños. En series anteriores, entre el 5 y el 67% de los niños infectados fueron hospitalizados4,9,14. Se ha descrito que la hospitalización es más común entre los pacientes pediátricos menores de un año de edad y los que tienen una enfermedad de base. En nuestra serie, 12 de los 39 pacientes eran menores de un año (32% de los casos), cifra que es similar al 40% comunicado por Cantoni y a la tasa del 30% comunicada por Garazzino14 en Italia, aunque un porcentaje mucho más alto que en China (18% en la serie Lu9 y 11% en la de Dong8) y la tasa contenida en un informe de CDC (15%)21. La mayoría de los lactantes de nuestro hospital tuvieron una enfermedad no complicada, con la excepción de un recién nacido con apnea22 y un lactante con neumonía neumocócica23. Más de la mitad de los niños ingresados eran mayores de seis años, y la edad media de los niños con shock fue de 10 años. Se desconoce si los niños mayores tienen un mayor riesgo de desarrollar un síndrome de respuesta inflamatoria sistémica temporalmente asociado a COVID-19.
Los criterios de hospitalización pueden variar significativamente de un centro a otro. Los pacientes pueden ser ingresados como un medio preventivo de aislamiento, debido a su condición clínica (signos y síntomas de mayor gravedad), o debido a la presencia de factores de riesgo para un curso complicado de la enfermedad. En nuestro hospital, los niños fueron ingresados principalmente debido a la gravedad de la enfermedad. Los criterios clínicos de ingreso que se aplicaron no diferían de los protocolos institucionales previamente establecidos para cada entidad nosológica. La mayoría de los pacientes estaban previamente sanos, y no podemos descartar que aquellos con una condición subyacente tengan un mayor riesgo de deterioro.
La mayoría de nuestros pacientes presentaron fiebre (87%), lo cual fue más común que en los informes de China (71%)9 e Italia (36%)15. Esto podría estar relacionado con un sesgo de selección porque todos los niños incluidos en nuestra serie requirieron ingreso. En estos pacientes, la fiebre podría ser una expresión de una forma más grave de la enfermedad.
Los niños con enfermedad no complicada desarrollaron principalmente síntomas respiratorios parecidos a un resfriado o una enfermedad similar a la gripe, bronquiolitis o neumonía. Algunos lactantes menores de tres meses de edad se presentaron con fiebre sin foco. Los síntomas clínicos eran inespecíficos y pueden superponerse con otras infecciones respiratorias virales o bacterianas. No tuvieron alteraciones significativas en las pruebas de laboratorio, excepto la elevación aislada de la PCR en unos pocos casos. Los pacientes con enfermedad no complicada mejoraron con tratamiento de soporte y fueron dados de alta en pocos días. La mayoría no recibió ninguno de los medicamentos empíricos propuestos para el tratamiento de COVID-199,15,24–28.
Las infecciones respiratorias también pueden provocar complicaciones más graves como la apnea (en niños muy pequeños), la coinfección bacteriana o la insuficiencia respiratoria. En nuestra serie, un neonato presentó apnea repetida y otro presentó sepsis neumocócica y neumonía con derrame pleural, desarrollando posteriormente una neumonía necrotizante. No está claro si el curso de la enfermedad en esta última estaba relacionado sólo con la infección bacteriana o con ambas.
Es notable que después de las primeras cinco semanas de la epidemia observamos una nueva forma de presentación clínica10. Estos pacientes eran de mayor edad, tenían fiebre alta y referían síntomas gastrointestinales significativos (dolor abdominal intenso, diarrea, vómitos) y/o erupción y/o hiperemia conjuntival. Los síntomas respiratorios eran menos frecuentes en estos casos. La mayoría se presentó en el servicio de urgencias con apariencia visiblemente alterada y taquicardia extrema. El sello distintivo de estos nuevos casos es el desarrollo de un shock en un corto período de tiempo desde la consulta en el SU29,30. Los pacientes recibieron soporte respiratorio y hemodinámico en la UCIP y tratamiento con fármacos antivirales, hidroxicloroquina, antibióticos y antiinflamatorios. Todos los hemocultivos fueron negativos. Esta entidad tiene características clínicas en común con otras condiciones inflamatorias pediátricas, incluyendo la enfermedad de Kawasaki, miocarditis, síndromes de shock tóxico, sepsis bacteriana o abdominal y síndromes de activación de macrófagos11. Su reconocimiento precoz es crucial. Cabe destacar que estos pacientes presentaron una elevación significativa de los marcadores inflamatorios (proteína C reactiva, procalcitonina, dímero D, ferritina) y linfopenia, así como una mayor proporción de neutrófilos/linfocitos. Esta relación se ha notificado como un biomarcador útil relacionado con el diagnóstico de otras afecciones como la infección por el virus de la gripe y la sepsis31. Recientemente se ha publicado la asociación entre la elevación de esta proporción y formas graves de la enfermedad en adultos, pero no hay datos al respecto en niños hasta el momento32. La LDH no parece ser un marcador analítico de gravedad en nuestros pacientes, lo que contrasta con los adultos33. También es importante señalar que ocho de los 12 pacientes desarrollaron neumonía radiológica aunque los síntomas respiratorios no eran predominantes en el momento del ingreso34. Debido a los hallazgos clínicos y de laboratorio y a la agrupación de casos en un período fuera de los niveles máximos de la epidemia, formulamos la hipótesis de que la infección por SARS-CoV-2 puede desencadenar una respuesta inflamatoria que lleve al shock. Siete de estos pacientes dieron positivo en la prueba de SARS-CoV-2 con RT-PCR, pero sólo cinco dieron positivo en anticuerpos IgG, lo que sugiere que esta respuesta inflamatoria puede ocurrir durante el período agudo o después de que la infección haya pasado35.
Este estudio tiene varias limitaciones. Debido al pequeño tamaño de la muestra y al diseño retrospectivo utilizado, es necesario seguir investigando para confirmar estos hallazgos. Dado que sólo se analizaron en nuestro hospital aquellos pacientes que necesitaban hospitalización o que tenían factores de riesgo de padecer una enfermedad grave, los datos presentados aquí no reflejan la incidencia total de COVID-19 en niños y no pueden compararse con algunas series publicadas anteriormente. Además, realizamos un sesgo de selección de la gravedad, por lo que nuestros resultados y conclusiones están influenciados por él. En los pacientes con una prueba serológica positiva, pero una PCR negativa, la relación entre la infección por SARS-CoV-2 y las manifestaciones clínicas no se puede determinar. Sin embargo, este estudio proporciona información clínica importante sobre las diferentes formas de presentación clínica de la COVID-19 en niños y que puede ayudar a reconocer precozmente a los pacientes con riesgo de complicaciones.
Este estudio describe una serie de niños de un solo centro que fueron admitidos para recibir atención hospitalaria con la infección por SARS-CoV-2. Los pacientes con enfermedad respiratoria aislada y sin elevación de los biomarcadores inflamatorios clásicos mostraron un curso sin complicaciones de la enfermedad. En estos casos, el uso rutinario de las drogas empíricas propuestas para el COVID-19 parecía innecesario. En contraste, los niños mayores con fiebre, síntomas abdominales, elevación de los biomarcadores inflamatorios, linfopenia y una alta proporción de neutrófilos/linfocitos desarrollaron un empeoramiento clínico con shock. Estos pacientes con enfermedad complicada requirieron cuidados intensivos que consistieron en tratamiento de soporte y recibieron medicamentos antivirales y antiinflamatorios. Se necesitan más estudios multicéntricos y prospectivos para ampliar la base de conocimiento sobre esta nueva enfermedad en los niños, como el estudio EPICO-AEP que se está llevando a cabo en España. Sus resultados arrojarán mayor luz sobre las cuestiones planteadas en este trabajo.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.