Introducción
La pubertad precoz central (PPC) en el niño se define como la presencia de un volumen testicular igual o superior a 4 ml, junto a un pico de hormona luteinizante (LH) tras estimulación con la hormona estimuladora de gonadotropinas (GnRH) superior a 7-10 U/l antes de los 9 años 1,2. La incidencia de este trastorno es claramente inferior a la presentada por las niñas; sin embargo, la posibilidad de presentar patología orgánica cerebral es claramente mayor entre los niños 3,4.
A la patología de base asociada a PPC en niños, podemos sumar otras dos circunstancias fundamentales: por un lado, la repercusión psicológica asociada al adelanto puberal 5 y, por otro, un pronóstico de talla adulta en torno a 156 cm sin tratamiento 6. En este sentido, desde hace 2 décadas se han utilizado los análogos de GnRH para frenar el desarrollo puberal, evitar trastornos psicológicos y mejorar la talla adulta 7,8.
La evaluación de la eficacia de los análogos de GnRH en la PPC hace referencia generalmente a estudios realizados en niñas, ya que el número de niños afectados es relativamente pequeño 9-12. Esta circunstancia, junto a un patrón de crecimiento puberal diferente en ambos sexos, hace que el análisis y la interpretación de los resultados tras la supresión del desarrollo puberal en niñas no se pueda extrapolar al grupo de niños; sin embargo, parece que la talla adulta de niños con PPC tratados con análogos no difiere de la talla genética 4.
Motivo de controversia es la utilización de un método de predicción de talla adecuado 2. Así, un trabajo que aglutina 26 niños con PPC tratados con análogos de GnRH 4 presenta una ganancia de talla (diferencia entre la talla adulta y la predicción de talla al diagnóstico) de 0,3 ± 8,6 cm utilizando la predicción de talla para la edad ósea avanzada según el método de Bayley-Pinneau, aumentando esta ganancia a 6,2 ± 8,7 cm utilizando la predicción de talla para la edad ósea acorde con la edad cronológica. Por tanto, los análogos son eficaces en la mejora de la talla adulta, pero la magnitud de este efecto es desconocido.
En este estudio, hemos efectuado un análisis retrospectivo de los niños diagnosticados de pubertad precoz central, con los siguientes objetivos: a) conocer el porcentaje de PPC secundaria a patología orgánica en niños, y b) estudiar las características clínicas-biológicas al diagnóstico, durante y al final del tratamiento.
Pacientes y métodos
Se ha realizado un estudio retrospectivo de los niños diagnosticados de PPC en el servicio de Endocrinología del Hospital Infantil Universitario Niño Jesús de Madrid entre 1990 y 2005. Los criterios de inclusión fueron: inicio de síntomas antes de los 9 años de edad, volumen testicular igual o superior a 4 ml y, un pico de LH tras estimulación con GnRH superior a 7 U/l que confirmase el origen central de la pubertad 4. Confirmado el diagnóstico de PPC, a todos los pacientes se les realizó una resonancia magnética (RM) craneal con el objeto de descartar patología orgánica.
Los datos recogidos al diagnóstico fueron los siguientes: edad de inicio de la pubertad, patología de base, parámetros antropométricos tales como la talla (en cm y en desviación estándar [DE] para la población española) 13, el peso (en kg y en DE), el índice de masa corporal (IMC) en DE, y la velocidad de crecimiento (en cm/año y DE). El volumen testicular se determinó mediante el orquidómetro de Prader 14, el grado de pubarquia según el estadio puberal de Tanner 15, el pico de LH tras estimulación con GnRH, las concentraciones de testosterona, la edad ósea mediante el método de Greulich y Pyle 16, la talla diana (media entre la talla del padre y la madre + 6,5 cm) y el pronóstico de talla (acorde a la edad cronológica [average] y para edad ósea acelerada [accelerated]) mediante el método de Bayley y Pinneau 17. Todos los pacientes recibieron tratamiento con análogos de GnRH (triptorelina), intramuscular, con periodicidad cada 28 días.
Tras la intervención terapéutica, se determinaron las siguientes variables con periodicidad anual: velocidad de crecimiento (cm/año y DE), talla, peso, IMC, edad ósea y concentraciones de testosterona. Finalmente, se recopilaron los datos de talla adulta en los sujetos que presentaban velocidad de crecimiento inferior a 1 cm/año y edad ósea superior a 16 años (98 % de la talla adulta) 17.
La eficacia terapéutica se valoró mediante la realización de un test de GnRH al mes del tratamiento y, posteriormente, mediante el análisis de la velocidad de crecimiento, la edad ósea y las concentraciones plasmáticas de testosterona.
Se incluyen 8 niños con el diagnóstico de PPC. La edad media al diagnóstico fue de 5,9 ± 2,9 años; la edad ósea de 7 ± 3 años; la velocidad de crecimiento (DE) de 2,2 ± 1,9 cm/año; el pico de LH de 12,9 ± 6,5 mU/ml y el volumen testicular de 6,1 ± 3,1 ml (rango: 4-12 ml). Del total, 6 niños presentaban patología orgánica (75 %): hamartoma hipotalámico (n = 1), secuelas de un traumatismo craneoencefálico grave (n = 1), neurofibromatosis tipo 1 (n = 2, ambos con gliomas del nervio y del quiasma óptico), quiste supraselar con ventriculomegalia (n = 1) y astrocitoma hipotálamo-quiasmático (n = 1) (tabla 1). La dosis inicial de tratamiento con análogos de GnRH fue de 65 ± 6 μg/kg/28 días, y se mantuvo durante un período de 6 ± 3,4 años, ajustándose periódicamente al peso.
La determinación de las concentraciones de gonadotropinas, hormona foliculoestimulante (FSH) y LH fueron determinados por ensayo radioinmunométrico (IRMA, Soria Biomedica, Vercelli, Italia), siendo los coeficientes de variación intraensayo e interensayo de 2,7 y 3,5 % para la FSH y de 2,7 y 3,1 % para la LH. Los valores de testosterona se realizaron mediante radioinmunoanálisis (RIA) (Diagnostic Products Corporation) siendo los coeficientes de variación intraensayo e interensayo de 0,5 y 10,8 %, respectivamente.
Estadística
Los datos se expresan como media ± DE. Los cambios debidos al tratamiento fueron evaluados mediante análisis de la varianza (ANOVA) para medias repetidas. Se consideró p < 0,05 como significativo. El análisis estadístico se realizó mediante SAS software package (SAS Institute Inc., Cary, NC).
Resultados
Cambios antropométricos y hormonales tras tratamiento con triptorelina
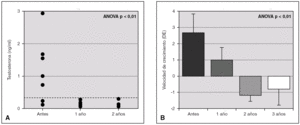
Durante el tratamiento, 7 pacientes mostraron un test GnRH frenado al mes de su inicio. Un único paciente no cumplió adecuadamente las indicaciones terapéuticas, y a los 3 meses presentó un pico de LH > 7 U/l junto a valores de testosterona de 3 ng/ml (VN < 0,5 ng/ml), mientras el resto presentó valores por debajo de 0,5 ng/ml durante el tratamiento (fig. 1A). Así mismo, tras la instauración de análogos de GnRH, se evidenció una disminución significativa de la velocidad de crecimiento (fig. 1B), sin presentar cambios en la diferencia entre la edad ósea menos la edad cronológica durante el tratamiento, debido a la escasa diferencia existente al diagnóstico (1,1 ± 2,4). Durante la terapia con triptorelina no hubo alteraciones del peso ni del IMC.
Figura 1. A) Niveles séricos de testosterona en el momento del diagnóstico de pubertad precoz central en niños y tras uno y dos años de tratamiento con triptorelina.B)Velocidad de crecimiento en cm de los mismos pacientes en el momento del diagnóstico y tras uno, dos y tres años de tratamiento con triptorelina.
Talla adulta
La edad cronológica media a la que se retiró la triptorelina fue de 12,4 ± 1,9 años con una edad ósea similar (12,6 ± 1,4 años). Sólo disponemos de la talla adulta en 3 pacientes: paciente 2: 171 cm (0,76 DE); paciente 4: 169 cm (1,09 DE) y paciente 8: 171,8 cm (0,62 DE). La talla media de estos 3 pacientes es de 170 ± 1,4 cm, sin presentar diferencias significativas con la talla diana: 174,6 ± 2,5 cm, ni con la predicción de talla antes del tratamiento utilizando las tablas de edad ósea acorde a la edad cronológica (average) (171,1 ± 7,6 cm), ni con las tablas para edad ósea acelerada (accelerated) (173 ± 5,9 cm). No obstante, estos datos deben ser interpretados con prudencia al tratarse únicamente de 3 pacientes.
Discusión
En este estudio descriptivo hemos encontrado los siguientes hallazgos: a) un elevado porcentaje de patología orgánica entre los niños afectados de PPC; b) la talla adulta de estos niños tras tratamiento con análogos de GnRH se encontraba dentro de la normalidad, y c) la determinación de los valores de testosterona puede ser de utilidad en el control terapéutico en este grupo de niños.
Los datos de este trabajo son fruto de un estudio observacional lo cual implica los siguientes inconvenientes: a) un escaso número de pacientes, dada la baja prevalencia de la enfermedad; b) únicamente disponemos de datos referentes a la talla adulta en 3 pacientes, y c) el abordaje terapéutico y el control clínico-analítico ha sido individualizado según el criterio del médico responsable, sin existir un diseño prospectivo.
La serie más amplia de niños con PPC publicada hasta el momento muestra un 46 % de patología orgánica 4. Este dato contrasta con lo visto en nuestra serie, donde en un 75 % de niños se objetivó patología de base. Estas diferencias pueden ser debidas al criterio de selección de los pacientes, como por ejemplo la aparición de caracteres sexuales antes de los 9 años. En este sentido, la edad media de aparición de signos puberales precoces (volumen testicular ≥ 4 ml: testes de 6,1 ± 3,1 ml de Prader; rango: 4-12) en nuestra cohorte es de 5,8 ± 2,9 años (rango: 1-8,5) frente a los 6,4 ± 2,2 del trabajo de Mul et al. Un único paciente inició los signos puberales entre los 8 y 9 años, siendo diagnosticado de PPC idiopática. Por otro lado, junto a los datos clínicos, es fundamental la confirmación biológica de la activación central de la pubertad mediante la realización de un test de GnRH, donde todos nuestros sujetos mostraban pico de LH tras la estimulación con GnRH > 7 U/l (12,9 ± 6,5 U/l; rango: 8,9-26). Así mismo, otro parámetro biológico que ayuda al diagnóstico de pubertad precoz son los valores séricos de testosterona, encontrándose en 6 de los 8 pacientes en rango puberal, mientras que en dos de ellos se encontraban en rango prepuberal 10 pero con activación central de la pubertad, lo cual indica un diagnóstico precoz (pacientes 3 y 7). Por tanto, una selección cuidadosa de pacientes, excluyendo los niños con pubertad adelantada, ha permitido confirmar un elevado porcentaje de patología orgánica en niños con PPC a diferencia de trabajos previos 4,10.
Parece claro que el tratamiento con análogos de GnRH es efectivo en el tratamiento de la PPC, por un lado frenando la progresión puberal y el impacto psicológico derivado de esta circunstancia, y por otro, alcanzando una talla final dentro de la normalidad. En nuestro estudio disponemos de los datos de 3 pacientes, que alcanzan una talla final normal. Dada la escasez de pacientes no podemos sacar conclusiones respecto a si el tratamiento es efectivo en cuanto a la predicción de talla utilizada al diagnóstico (acorde a la edad cronológica average o para edad ósea acelerada accelerated), aunque parece intuirse que las diferencias son menores mediante el método average, pero de todos es bien sabido la controversia existente sobre la realización de métodos de predicción de talla en los niños 2. En nuestra opinión, si uno no se aventura a la realización de métodos de predicción de talla, y se fija en los controles históricos (talla adulta en torno a 156 cm sin tratamiento) 6, parece claro que los análogos son eficaces; sin embargo, es necesario crear bases de datos nacionales e internacionales con el objeto de analizar las diferentes variables que influyen en la talla adulta.
Habitualmente, tras iniciar la terapia con los análogos de GnRH, se siguen varios criterios clínico-biológicos para el adecuado control terapéutico. Uno de ellos, es la reevaluación del pico de LH tras el estímulo con GnRH, donde debemos observar una respuesta suprimida. A diferencia de lo que ocurre en niñas, donde la detección de estradiol presenta una escasa sensibilidad en los trastornos puberales, en niños, la cuantificación de testosterona presenta una sensibilidad adecuada en el diagnóstico de problemas puberales. Así, valores por encima de 0,5 ng/ml se consideran en rango puberal 10. Por tanto, mantener los valores de testosterona por debajo de ese nivel puede ser un objetivo terapéutico adecuado, junto a la valoración de la velocidad de crecimiento y la maduración ósea, pudiendo sustituir al test de estimulación de GnRH, que presenta mayores problemas logísticos y, en ocasiones, de interpretación.
En conclusión, la presencia de pubertad precoz central en los niños obliga a descartar patología orgánica, especialmente un tumor intracraneal. Así mismo, los pacientes afectados de PPC tratados con GnRH presentan talla adulta normal; sin embargo, se necesitan más estudios para conocer diferentes variables que pudieran mejorar dicho resultado. Finalmente, la determinación de testosterona parece igual de efectiva y más eficiente, que la estimulación con GnRH en el control biológico de esta patología.
Correspondencia: Prof. J. Argente Oliver.
Servicio de Pediatría. Hospital Infantil Universitario Niño Jesús.
Avda. Menéndez Pelayo, 65. 28009 Madrid. España.
Correo electrónico: argentefen@terra.es
Recibido en noviembre de 2005. Aceptado para su publicación en julio de 2006.