La leishmaniasis es una enfermedad infecciosa, granulomatosa crónica, endémica, causada por distintas especies del parásito Leishmania. Afecta a 88 países y su incidencia está aumentando. Puede presentarse a cualquier edad, y un 10% de los casos se describe en niños menores de 12 años. El protozoo se transmite mediante la picadura de un insecto y da lugar a distintas formas clínicas dependiendo del género de Leishmania y de la respuesta inmunitaria del individuo: forma visceral, mucocutánea o cutánea. En la población pediátrica, la forma clínica más frecuente es la cutánea.
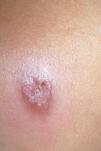
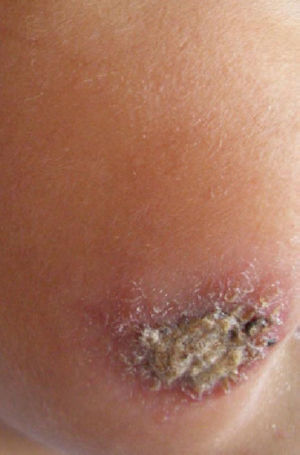
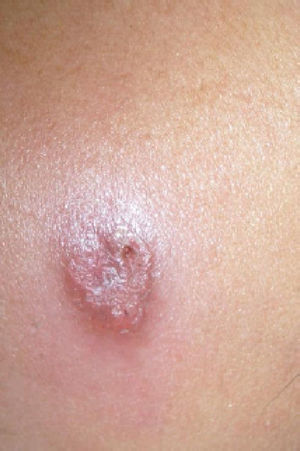
Se presenta el caso de un niño de 3 años y 9 meses de edad, procedente de Lima, Perú, que consulta por presentar una lesión costrosa en la mejilla derecha (1×1,5cm), caliente e indurada, con bordes sobreelevados y eritematosos y otra lesión de características similares pero de menor tamaño (0,5×0,8cm) en la región temporal derecha (fig. 1). Se realiza raspado de los bordes de la lesión y se recoge una muestra para frotis y cultivo en medio Novy-MacNeal-Nicolle. El resultado de estas técnicas muestra amastigotes de Leishmania en el frotis y promastigotes en el cultivo. Ante la procedencia geográfica del paciente, se asume que la etiología más probable de la lesión es Leishmania (Vianna) peruviana (no se disponía de la técnica de reacción en cadena de la polimerasa en el momento del diagnóstico). El resto de pruebas complementarias fue normal. Se inicia tratamiento con estibogluconato sódico intramuscular (dosis de 20mg/kg/día) durante 20 días, con remisión parcial de las lesiones. Un mes más tarde, las lesiones comienzan de nuevo a aumentar de tamaño y se reinicia tratamiento antimonial, que se mantiene 5 días por la escasa respuesta clínica. Se inicia tratamiento con anfotericina B (dosis de 0,7mg/kg/día) y se mantiene hasta alcanzar una dosis máxima acumulada de 1g con buena evolución (fig. 2) y sin que se evidencien efectos secundarios.
Los parásitos protozoarios intracelulares obligados de las células del sistema fagocítico monocitario que pertenecen al género Leishmania causan la leishmaniasis. Se pueden presentar en forma flagelada (promastigote) o no flagelada (amastigote). El género Leishmania se clasifica a su vez en 2 subgéneros: Leishmania y Vianna, dentro de los cuales se incluyen distintas especies. En Perú, las 2 especies más prevalentes de Leishmania son L. (Vianna) peruviana en la sierra y L. (Vianna) braziliensis en la selva1. Los principales reservorios son roedores salvajes y, menos frecuentemente, animales domésticos como el perro. El protozoo se transmite mediante la picadura de un insecto (Lutzomyia en el Nuevo Mundo y Phlebotomus en el Viejo Mundo) y da lugar a distintas formas clínicas: visceral, mucocutánea o cutánea, dependiendo del género de Leishmania y del tipo de respuesta inmunitaria (Th1 o Th2) que activen los antígenos del parásito. Estudios recientes indican la importancia de las células dendríticas en la iniciación y la regulación de la respuesta inmunitaria. Este hallazgo podría ser clave para la obtención de vacunas2.
La leishmaniasis cutánea consiste en la aparición de una lesión cutánea después de un período de incubación (2 semanas–2 meses). Se trata de una mácula eritematosa que se convierte en pápula o pústula, cuya base es firme, indurada, hiperémica y a veces pruriginosa. Después de varios días se ulcera y se recubre de un líquido amarillento y adherente que da lugar a la costra. La úlcera característica es redondeada, indolora, con bordes bien definidos y en forma de sacabocado. En niños es frecuente la localización en la cara y las áreas expuestas de las extremidades. Algunas lesiones cutáneas se curan espontáneamente en varios meses, pero la mayoría de las úlceras tienen un curso crónico de meses o años y dan lugar incluso a mutilaciones o a deformidades1.
En el diagnóstico se utilizan métodos directos e indirectos. Los métodos directos más utilizados son el examen directo de la muestra (obtenida mediante raspado de los bordes de la lesión, aspiración-punción con aguja fina o biopsia) y posterior tinción Wright o Giemsa para observar los amastigotes, y el cultivo en medio Novy-MacNeal-Nicolle para buscar promastigotes3. Los principales métodos indirectos son la intradermorreacción de Montenegro (leishmanina) y la reacción en cadena de la polimerasa4.
El tratamiento de elección es el antimonio pentavalente (antimoniato de meglumina o estibogluconato sódico) por vía intramuscular o por vía intravenosa, aunque también localmente. La dosis recomendada es de 20mg/kg/día y se administra en ciclos de 10 días con descanso de una semana; el número promedio de ciclos son 35. La anfotericina B (convencional y liposomal) es el fármaco de segunda elección. La dosis intravenosa de anfotericina B convencional es de 0,5–1mg/kg/día hasta un máximo de 50mg/día; se debe administrar hasta la curación clínica, generalmente cuando se llega a una dosis acumulada de 1 a 1,5g5. Hay pocos casos en la literatura médica sobre la aplicación de anfotericina B liposomal, aunque parece que es más segura y presenta menos efectos secundarios que el estibogluconato sódico6. Otras alternativas terapéuticas cuando falla el tratamiento con antimoniales son isetionato de pentamidina, ketoconazol, fluconazol o itraconazol. Recientemente se ha empleado miltefosina por vía oral con tasas de curación de hasta el 94%7. En cuanto al tratamiento combinado, la inyección diaria de interferón γ junto con antimoniales pentavalentes ha mostrado aceleración de la respuesta clínica y la respuesta a largo plazo en casos que no responden a antimoniales. El uso de imiquimod al 7,5% tópico junto con antimoniato de meglumina podría ser una combinación prometedora8. En la actualidad se está investigando acerca del papel del interferón > y de la superóxido dismutasa 1 en la infección por L. braziliensis y Leishmania amazonensis para iniciar una nueva estrategia terapéutica9. También se han empleado métodos físicos, como calor local, raspado y crioterapia, aunque el mejor tratamiento sigue siendo la prevención10.