El síndrome de Klinefelter (SK) es la cromosomopatía sexual más frecuente y asocia un hipogonadismo hipergonadotropo como manifestación endocrinológica. El fenotipo es masculino con talla alta, adiposidad abdominal y testículos pequeños, y aparece habitualmente después de la pubertad.
Se presentan 2 casos clínicos: un paciente de 2 años con talla baja que requirió tratamiento con hormona de crecimiento. Al no progresar el desarrollo puberal y presentar niveles basales elevados de gonadotropinas, se realiza cariotipo con resultado 48XXYY (SK). El segundo es un paciente de 8 años con clínica de pubertad precoz, en el que se constata un aumento de las concentraciones de β-gonadotropina. En la tomografía computarizada torácica se halló una masa mediastínica. Se realiza estudio citogenético con cariotipo 48XXYY (SK).
La talla baja no excluye el diagnóstico de SK y ante un paciente con masa mediastínica y retraso neurocognitivo debemos sospechar un SK y solicitar cariotipo.
Klinefelter syndrome (KS) is the most common sex chromosomal abnormality and is associated with hypergonadotropic hypogonadism as an endocrine disorder. The phenotype is characterized by tall stature, abdominal adiposity and small testicles, and often appears after puberty.We report two cases of SK. The first patient is a 2-year-old boy with short stature who received growth hormone therapy. Because of non-progressive puberty, an evaluation of the reproductive axis was performed, showing increased basal gonadotropins. The karyotype (48 XXYY) confirmed the presence of KS. The second patient is an 8 year-old boy in whom peripheral precocious puberty was suspected. Laboratory tests showed high chorionic gonadotropin levels, and a chest CT scan revealed a mediastinal mass. The karyotype in peripheral blood disclosed a 48 XXYY formula (KS).Short stature does not exclude SK. In patients with a mediastinal mass and neurobehavioral deficits, KS should be suspected.
El síndrome de Klinefelter (SK) es la cromosomopatía sexual más frecuente, con una prevalencia de 1/600, que ha aumentado en las últimas décadas debido a la edad materna más elevada y al diagnóstico prenatal1. Existen 2 variantes citogenéticas: las formas homogéneas o puras y los mosaicos (no homogéneas). Entre las primeras, la forma clásica (47, XXY) es la más frecuente, existiendo también las variantes triple X (48, XXXY) y doble X doble Y (48, XXYY)2. La alteración genética conlleva un hipogonadismo hipergonadotropo (HH) como manifestación endocrinológica y se acompaña de un fenotipo característico: talla alta desproporcionada, adiposidad abdominal, ginecomastia, vello púbico, facial y axilar escasos, y testículos pequeños3.
El diagnóstico en la adolescencia suele realizarse por falta de desarrollo puberal completo. En la edad adulta, el motivo de diagnóstico es la infertilidad o la impotencia sexual2. El retraso neurocognitivo es variable, siendo característico el retraso en la adquisición del lenguaje. Los pacientes con SK tienen mayor riesgo de tumores mediastínicos de células germinales y de linfoma no Hodgkin, así como de enfermedades autoinmunitarias, prolapso de la válvula mitral, osteoporosis y síndrome metabólico4. El tratamiento sustitutivo con testosterona tiene como objetivo preservar desde edades tempranas la densidad mineral ósea, prevenir el síndrome metabólico y minimizar en la edad adulta tanto la disminución de la libido como la impotencia3.
Debido a la gran heterogeneidad clínica, solo se diagnostican el 25% de casos de SK y en solo un 10% el diagnóstico se realiza antes de la pubertad1. Dado que la entidad puede asociarse a trastornos con potencial morbilidad, es importante su detección temprana. En este artículo, se describen 2 casos clínicos de SK de especial interés por su historia diagnóstica.
Caso 1Paciente de sexo masculino que acude al Servicio de Endocrinología a los 2 años por talla baja. En los antecedentes familiares destaca una talla paterna de 179cm y una talla materna de 160cm (talla diana 176cm, –0,21 DE5). Como antecedentes obstétricos y perinatales, presenta embarazo controlado sin incidencias. Parto por cesárea a las 42,3 semanas de edad gestacional (EG) por inducción fallida por posmadurez. Peso al nacimiento de 2.800g (–1,9 DE5) y longitud de 46cm (–3,0 DE5), motivo por el cual se diagnostica de pequeño para la EG (PEG6). Dificultades en la marcha y en la psicomotricidad, por lo que acudía a centro de estimulación precoz.
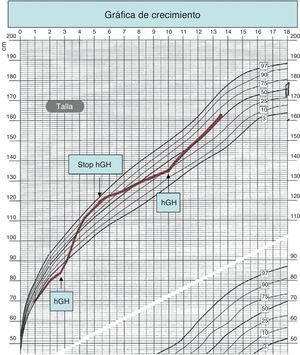
En la exploración física destacaba talla 80,8cm (–2,9 DE5) y peso 10kg (–2,2 DE5), proporciones de segmentos armónicas, sin otros hallazgos relevantes. Ante la talla baja y los antecedentes de PEG, se solicita una analítica sanguínea que muestra IGF-I=42 ng/ml (normal, 77-148), perfil tiroideo normal y marcadores de celiaquía negativos. Edad ósea retrasada 6 meses. El test de estimulación de hormona de crecimiento (HC) con clonidina muestra un pico de 10,9 ng/ml (normal > 7,4). Se inicia tratamiento con HC por el antecedente de PEG sin recuperación posnatal6, en el contexto de ensayo clínico, con buena respuesta (fig. 1). El tratamiento se interrumpe a los 5 años y 6 meses, por finalización del estudio, reintroduciéndose a los 10 años por enlentecimiento progresivo de la velocidad de crecimiento.
A los 7 años se diagnostica de trastorno de déficit de atención e hiperactividad (TDAH) iniciando tratamiento con metilfenidato. A los 11 años inicia desarrollo puberal, alcanzando un volumen testicular de 6ml, sin progresión durante el año siguiente. Por este motivo, se solicita analítica sanguínea, destacando LH de 4,8 U/l (normal,1,5-8) y FSH de 13,7 U/l (normal,1-6) y testosterona de 285 ng/dl (normal, 25-345). Con la sospecha diagnóstica de HH, se solicita cariotipo en sangre periférica que muestra 48, XXYY (SK).
Caso 2Paciente de sexo masculino que acude al Servicio de Endocrinología a los 8 años y 4 meses de edad por inicio de vello pubiano y aumento del tamaño del pene en los últimos 6 meses. Antecedentes familiares: abuela materna con síndrome X frágil. Embarazo controlado sin incidencias. Parto eutócico a las 40 semanas de EG, peso al nacer de 3.130g (–0,7 DE5). Retraso en la adquisición del habla; en seguimiento por Neurología por un retraso global del aprendizaje. El aumento del tamaño peneano y la aparición de vello púbico se acompañaban de un aumento de la velocidad de crecimiento. En otro centro se había descartado pubertad precoz central e hiperplasia suprarrenal congénita por déficit de 21-hidroxilasa (17-hidroxiprogesterona post-ACTH normal)7.
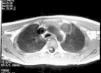
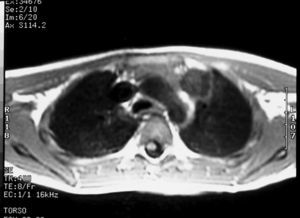
En la exploración física destacaba talla 143cm (+2,0 DE5); peso de 32,3kg (+0,2 DE5), botón mamario bilateral y estadio de Tanner8 A2P3G3-4 con volumen testicular de 4-5 cc. Con orientación diagnóstica inicial de pubertad precoz periférica, la edad ósea muestra un retraso de 2 años; en la analítica sanguínea destacan α-fetoproteína de 15,7μg/l (normal, < 15), sulfato de dehidroepiandrosterona < 0,78μmol/l (normal < 4,7), testosterona < 26 ng/dl (rango prepuberal) y β-coriogonadotropina 6,8 U/l (normal, < 0,8). El aumento de los valores de β-coriogonadotropina hace sospechar la existencia de carcinoma embrionario que se confirma mediante TC torácica, demostrándose una masa mediastínica de 2×2cm, sin otros hallazgos en el estudio de extensión, con indicación quirúrgica (fig. 2). Se realiza la resección de la masa sin incidencias, con anatomía patológica de teratoma maduro.
Ante el trastorno generalizado del desarrollo y el diagnóstico de tumor mediastínico de células germinales, se solicita cariotipo en sangre periférica, indicativo de SK (48, XXYY).
DiscusiónLos individuos con SK presentan fenotipo masculino y un cromosoma X extra con variabilidad de cariotipo4. Las características clínicas del SK aparecen como consecuencia de una sobreexpresión de genes del cromosoma X que escapan a la inactivación, como sería el gen SHOX implicado en la talla1. En los 2 casos descritos la citogenética es compatible con cariotipo 48XXYY, variante menos frecuente del SK que resulta de una no disyunción durante la meiosis con una incidencia de 1:18.000/1:40.000, de origen paterno en el 100% de los casos, y que estudios epidemiológicos han asociado con más frecuencia a linfoma no Hodgkin9.
En el SK, los testículos presentan una degeneración progresiva con la aparición de hialinización y fibrosis extensa de los túbulos seminíferos implicando aumento de gonadotropinas (la FSH se eleva a partir de los 12 años antes que la LH) y la disminución de los niveles de testosterona en la edad adulta1-3. El HH conlleva una alteración de la composición corporal, con obesidad abdominal y resistencia periférica a la insulina, y a medio-largo plazo aparición de síndrome metabólico4. Por ello, el diagnóstico es vital para la prevención y/o modulación tanto de las consecuencias metabólicas como de los trastornos neurocognitivos, que podrían beneficiarse de una intervención precoz4.
En la literatura están descritos casos de SK con talla baja por déficit de HC10.11, pero no con talla baja, antecedente de PEG y buena respuesta a tratamiento con HC. En la figura 1, se objetiva la respuesta al tratamiento con HC en el paciente descrito en el caso 1. En estos pacientes, la pubertad aparece a una edad normal sin un progreso adecuado del volumen testicular adulto1. En la época prepuberal, el SK es de difícil diagnóstico, siendo el hallazgo clínico más frecuente la criptorquidia y, en segundo lugar, los trastornos neurocognitivos2,12. Aun así, el diagnóstico precoz del SK está aumentando en los últimos años por un nivel de alerta mayor12.
Los tumores mediastínicos de células están descritos con un riesgo entre 50 y 66 veces superior en los SK que en la población general13,14. Como fisiopatología se ha descrito un trastorno de la migración de las células germinales durante la embriogénesis; son de indicación quirúrgica y, debido a su riesgo de recidiva y asociación a otros procesos malignos, debe realizarse un seguimiento estricto15. El diagnóstico de estos tumores se realiza por efectos locales de extensión de la masa o por aparición de clínica por hipersecreción hormonal, ya que los testículos de los SK en la edad prepuberal son capaces de producir niveles de testosterona altos para inducir caracteres sexuales periféricos si son estimulados por niveles altos de β-coriogonadotropina16.
En conclusión, se debe destacar que la talla baja no excluye el diagnóstico de SK, siendo clave en estos pacientes la no progresión del volumen testicular junto al hallazgo analítico de elevación de gonadotropinas y, por otro lado, la importancia de realizar un cariotipo en pacientes con tumores mediastínicos de células germinales, sobre todo si se asocia a trastornos neurocognitivos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.