Revisar la evidencia científica disponible sobre la eficacia de la suplementación universal con vitaminaD en población pediátrica sana, sin factores de riesgo, y actualizar posibles modificaciones en las recomendaciones de las principales guías de práctica clínica.
MétodosRevisión de alcance mediante búsqueda bibliográfica en PubMed durante los últimos 15años utilizando los siguientes términos de búsqueda MeSH: (vitamin D) AND (supplementation) en inglés o español. Se obtuvieron 2.133 artículos, de los que finalmente se seleccionaron 22.
ResultadosEn niños sin factores de riesgo menores de 1año la administración de 400UI/día mejora los niveles séricos de calcidiol; sin embargo, en la mayoría de los estudios no se relaciona con una mejoría en la salud ósea valorada por densitometría. En mayores de 1año con niveles de calcidiol <35ng/ml, la administración de entre 400 y 800UI al día de vitaminaD disminuye el riesgo de padecer una infección respiratoria. En niños aún no se ha demostrado que la suplementación con vitaminaD disminuya el riesgo ni la gravedad de otros procesos infecciosos, ni suponga una mejoría clínica para el resto de las funciones extraesqueléticas.
ConclusionesSegún las principales guías de práctica clínica, se recomienda suplementar con 400UI/día de vitaminaD a los niños menores de un año que reciban lactancia materna o que no alcancen la ingesta diaria recomendada a través de la fórmula infantil adaptada. En los mayores de 1año, la suplementación debe ser individualizada.
To review the current scientific evidence on the efficacy of universal vitaminD supplementation in healthy children with no risk factors and to propose updated modifications to the recommendations provided in the main clinical practice guidelines.
MethodsScoping review through a literature search conducted in PubMed for articles published in English or Spanish in the past 15years using the following MeSH search terms: (vitamin D) AND (supplementation). The search yielded 2133 articles, of which 22 were selected.
ResultsIn infants aged less than 1year without risk factors, administration of 400IU/day improves serum levels of calcifediol, but most studies have not found an association with improved bone health assessed by dual-energy X-ray absorptiometry. In children aged more than 1year with calcifediol levels of less than 35ng/mL, supplementation with 400 to 800IU/day of vitaminD decreases the risk of respiratory infection. There is still no evidence in the pediatric population that vitaminD supplementation either decreases the risk or severity of other infections or offers any other clinically significant extraskeletal benefits.
ConclusionBased on the main clinical practice guidelines, supplementation with vitaminD at a dose of 400IU/day is recommended for breastfed infants aged less than 1year or infants who do not achieve the recommended daily intake through infant formula. In children aged more than 1year, supplementation should be individualized.
El interés por la vitaminaD ha ido creciendo en los últimos años de forma manifiesta, en gran medida por el descubrimiento de sus funciones extraesqueléticas. Sin embargo, a pesar de los avances en el conocimiento y el incremento exponencial de publicaciones científicas, la evidencia sobre la suplementación en niños de forma universal es limitada y las guías de práctica clínica apenas han modificado sus recomendaciones en las últimas décadas1. Las últimas actualizaciones del comité de nutrición de la AEP y de la sociedad Europea de Gastroenterología, Hepatología y Nutrición Pediátrica fueron publicadas en los años 20122 y 20133, respectivamente. Este es un tema que sigue generando un intenso debate en las sociedades científicas4.
Existen pocos alimentos que aporten vitaminaD de manera natural. Entre las principales fuentes se encuentran los pescados grasos, el hígado y las yemas de huevo, además de productos fortificados como la leche y los cereales. No obstante, las cantidades proporcionadas por estos alimentos suelen ser insuficientes para alcanzar las necesidades diarias recomendadas: 400UI en menores de 1año y 600UI entre 1 y 18años5.
Nuestro objetivo es actualizar el conocimiento sobre la necesidad de suplementación y monitorización de la vitaminaD en niños sanos, así como plantear hipótesis dirigidas a aportar luz sobre el motivo del fracaso de muchos estudios experimentales para demostrar la eficacia de la administración de esta vitamina con actividad hormonal que juega un papel tan importante en el funcionamiento de nuestro organismo.
Material y métodosPara revisar la evidencia disponible sobre la eficacia de la suplementación universal con vitaminaD en población pediátrica se ha realizado una revisión de alcance mediante una búsqueda bibliográfica en PubMed de metaanálisis y ensayos clínicos publicados durante los últimos 15años (fecha en la que realizó la búsqueda: 1 de junio de 2024). Se utilizaron los siguientes términos («Vitamin D»[MeSH Terms] AND («supplemental»[All Fields] OR «supplementating»[All Fields] OR «supplementation»[All Fields] OR «supplementation s»[All Fields] OR «supplementations»[All Fields] OR «supplemention»[All Fields])) AND ((2009/6/1:2024/6/1[pdat]) AND (english[Filter] OR spanish[Filter]) AND (allchild[Filter])), recuperándose 2.133 artículos, de los cuales 22 fueron finalmente seleccionados como ensayos clínicos (13) y metaanálisis (9). En el material suplementario (tablas 1s, 2s y 3s) se especifica el diagrama de flujo, los artículos seleccionados y los estándares según la guía PRISMA. En la tabla 1 se resumen los resultados de los ensayos clínicos seleccionados. Además de la revisión de alcance, se hizo una revisión de las principales guías de práctica clínica vigentes con el objetivo de recoger las recomendaciones actuales de las distintas sociedades científicas.
Ensayos clínicos relacionados con la eficacia de la suplementación con vitaminaD en población sana pediátrica sobre la salud ósea y el riesgo de infecciones respiratorias
| Autor y año | Tipo de estudio | Población | Edad | Intervención | Calcidiol al inicio | Resultados |
|---|---|---|---|---|---|---|
| Salud ósea | ||||||
| Gharibeh N, 2023. Canadá | Ensayo clínico doble ciego aleatorizado no controlado con placebo | Niños sanos lactancia materna en ambos grupos (100% 1.er mes, 93% 3.er mes, 85-83% 6.° mes y 44-40% al año) | 1 mes | 400 (n=49) vs 1.000 (n=49) UI de vitamina D3 al día durante 11 meses | Todos <20 ng/ml | Al año de vida: no diferencias en la densitometría ni marcadores resorción ósea, calcidiol más alto en el grupo de 1000 UI/día |
| Gallo S, 2016. Canadá | Ensayo clínico doble ciego aleatorizado no controlado con placebo | Niños sanos con lactancia materna | 1 mes | 400 (n=25) vs 800 (n=25) vs 1.200 (n=26) vs 1.600 (n=11) UI/día vitamina D3 durante 11 meses | Media 22.44 ng/ml(6% <12 ng/ml) | A los 3 años de vida: no diferencias en la densitometría ni en los niveles séricos |
| Gallo S, 2013. Canadá | Ensayo clínico doble ciego aleatorizado no controlado con placebo | Niños sanos con lactancia materna | 1 mes | 400 (n=39) vs 800 (n=39) vs 1.200 (n=38) vs 1.600 (n=16) UI/día vitamina D3 durante 11 meses | Media entre 20,3 y 24,8 ng/ml | A los 12 meses de vida: mejoría progresiva en la densitometría en todos los grupos por igual |
| Lin CH, 2022. Taiwan | Ensayo clínico doble ciego aleatorizado controlado con placebo | Niños sanos con lactancia materna | 10 días | 400 UI al día vitamina D3 (n=37) vs placebo (n=35) durante 4 meses | Todos > 10 ng/ml Media Grupo vitamina D: 18,7 vs 19,6 placebo | A los 4 meses: grupo tratamiento aumento de niveles de vitamina D, descenso PTH, no diferencias en densitometría. Grupo placebo 45% calcidiol <10 ng/ml |
| Middelkoop K, 2024. Suráfrica | Ensayo clínico doble ciego aleatorizado controlado con placebo | Niños raza negra no infectados por VIH | 6-11 años | 10.000 UI vitamina D3 semanales (n=228) vs placebo (n=222) durante 3 años | Vitamina D 28,2 ng/ml placebo 27,9 ng/ml | Tras 3 años: aumento niveles de vitamina D, no diferencias en densitometría ni en número de fracturas |
| Ganmaa D, 2024. Mongolia | Ensayo clínico doble ciego aleatorizado controlado con placebo | Niños de 18 colegios públicos | 6-13 años | 14.000 UI por semana vitamina D (n=4176) vs placebo (n=4172) durante 3 años | 95,5% <20 ng/ml | No diferencias en el número de fracturas tras 3 años de seguimiento |
| Rosendahl J, 2018, Helsinki | Ensayo clínico doble ciego aleatorizado no controlado con placebo | Recién nacidos con alimentación lactancia materna >85% | 2 semanas | 400 (n=489) vs 1.200 (n=486) UI vitamina D3 al día durante 24 meses | 95% >20 ng/ml | A los 2 años no diferencias en la densidad mineral ósea (tomografía), calcidiol más alto en el grupo 1.200 UI |
| Infecciones respiratorias | ||||||
| Ganmaa D, 2020. Mongolia | Ensayo clínico doble ciego aleatorizado controlado con placebo | Niños de 18 colegios públicos | 6-13 años | 14.000 UI por semana vitamina D (n=4418) vs placebo (n=4433), durante 3 años | Media: 11,9 ng/ml95,4% <20 ng/ml | No diferencias en las infecciones por TBC ni ingreso por infección respiratoria tras 3 años de seguimiento |
| Loeb, 2019. Vietnam | Ensayo clínico doble ciego aleatorizado controlado con placebo | Niños sanos procedentes de un distrito rural | 3-17 años | vitamina D:14.000 UI D3 por semana (n=650) vs placebo (n=650), durante 8 meses | 26,3 ng/ml grupo vitamina D vs 26,1 ng/ml placebo | Grupo vitamina D disminución infecciones respiratorias víricas HR (0,81, IC95%: 0,66-0,99), no de las infecciones por influenza |
| Rosendahl J, 2018. Helsinki | Ensayo clínico doble ciego aleatorizado no controlado con placebo | Recién nacidos. Lactancia materna >85% | 2 semanas | 400 (n=489) vs 1.200 (n=486) UI vitamina D3 al día durante 24 meses | 95% >20 ng/ml | A los 2 años no diferencias infecciones respiratorias reportadas por los padres |
| Aglipay M, 2017. Canadá | Ensayo clínico doble ciego aleatorizado no controlado con placebo | Niños sanos | 1-5 años | 400 (n=354) vs 2.000 (n=349) UI vitamina D3 al día durante 4 meses entre septiembre y mayo | 36,9 (400 UI) vs 35.9 (2.000 UI) | Tras 4 meses no diferencias infecciones respiratorias reportadas clínicamente, ni microbiológicamente ni el tiempo hasta la primera infección |
| Huang YN, 2022. Taiwan | Ensayo clínico doble ciego aleatorizado controlado con placebo | Niños preescolares de guardería | Media 4 años | Placebo (n=113) vs 2.000 (n=135) UI vitamina D3 al día durante 1 mes | No disponible | Tras 6 meses disminución infección por influenza no significativo (p=0,095) no cambios en infección enterovirus |
| Urashima M, 2010. Japón | Ensayo clínico doble ciego aleatorizado controlado con placebo | Niños sanos (70%) y patología de base (30%) | 6-15 años | Placebo (n=213) vs 1.200 (n=217) UI vitamina D3 al día durante 4 meses | No disponible | Disminución infección por Influenza (RR: 0,58; IC95%: 0,34- 0,99; p=0,04) |
| Manaseki-Holland S, 2012. Kabul | Ensayo clínico doble ciego aleatorizado controlado con placebo | Lactantes | 1-11 meses | Placebo (n=1.522) vs 100.000 (n=1.524) UI cada 3 meses durante 18 meses | No disponible | No diferencia en primer episodio de neumonía. Grupo vitamina D más riesgo neumonía de repetición |
TBC: tuberculosis; VIH: virus de la inmunodeficiencia humana; HR: hazard ratio.
Según la última revisión Cochrane6 y otros metaanálisis recientes7, la suplementación con 400UI/día en los niños menores de 1año ha demostrado ser segura y eficaz para mejorar el estado nutricional de la vitaminaD y disminuir el porcentaje de niños con niveles de calcidiol <20ng/ml. Sin embargo, esta mejoría en los niveles séricos no se relaciona en todas las ocasiones con una mejoría en la salud ósea medida por densitometría. Una de las limitaciones principales es la falta de estudios bien diseñados, dado que en este grupo de edad únicamente se han publicado tres ensayos clínicos que comparen el uso de vitaminaD contra placebo, y con un número muy reducido de pacientes.
La manifestación más grave de la deficiencia de vitaminaD es el raquitismo, cuya incidencia está en aumento en los últimos años en Europa, principalmente en los grupos de riesgo. Estudios observacionales han demostrado que el uso de la suplementación con vitaminaD, así como la utilización de alimentos fortificados como política de salud pública, disminuye la prevalencia de raquitismo8,9. También se han publicado grandes series de lactantes sanos que reciben suplementación con 400UI/día sin ningún diagnóstico de raquitismo10.
Se han realizado varios ensayos clínicos en los que se compara la administración de varias dosis de vitaminaD durante el primer año de vida (desde 400 hasta 2.000UI/día), aunque son ensayos dosis-respuesta sin comparación con placebo. En ellos se observa que la administración de dosis superiores a 400UI/día no supone ningún beneficio en la composición corporal, la motricidad gruesa o la densitometría tras 3años de seguimiento11,12. En un ensayo reciente, un grupo de lactantes sanos que recibían lactancia materna y que al mes de vida tenían niveles de calcidiol por debajo de 20ng/ml se aleatorizaron para recibir 400 vs 800UI/día. Tras 12meses de seguimiento no encontraron diferencias en la salud ósea evaluada mediante densitometría ni en los niveles séricos de calcidiol entre ambos grupos. Estos estudios ponen de manifiesto que, en lactantes sanos, suplementar por encima de 400UI/día no parece aportar beneficios, así como que en ausencia de factores de riesgo no se deben monitorizar los niveles séricos, dado que, independientemente de la cifra de calcidiol, una dosis de 400UI al día parece suficiente para alcanzar el objetivo nutricional que permita una adecuada salud ósea en este grupo de edad.
Salud ósea en niños entre 1 y 18añosEn este grupo etario la evidencia es todavía menor. En un reciente metaanálisis publicado, la suplementación con vitaminaD durante un año en niños con niveles de calcidiol por encima de 8ng/ml tiene un mínimo efecto sobre la densidad mineral ósea de las caderas en la densitometría, aumentando 6,8mg/cm2 (IC95%: 0,7-1,9)13, sin demostrar cambios en el resto de zonas. Por ello, estos autores no apoyan la suplementación universal con vitaminaD, aunque matizan que los resultados no podrían extrapolarse a aquellos con niveles de vitaminaD fuera del rango estudiado. Tampoco se ha demostrado que la suplementación sea eficaz para disminuir el número de fracturas en este grupo de edad.
Salud extraesqueléticaUna de las funciones extraesqueléticas con mayor evidencia disponible es la antimicrobiana: varios ensayos clínicos y metaanálisis14 demuestran que la suplementación con vitaminaD puede disminuir en determinadas circunstancias el riesgo de presentar algún tipo de infección respiratoria (tabla 1). Uno de los metaanálisis más recientes15 ha demostrado que de forma global la suplementación con vitaminaD disminuye el riesgo de infecciones respiratorias (OR: 0,92; IC95%: 0,86-0,99), siendo más eficaz en aquellos entre 1 y 18años que recibían dosis bajas de vitaminaD (entre 400-800UI al día) sin patología de base y con niveles de calcidiol <35ng/ml (OR: 0,56; IC95%: 0,38-0,82). Si tenemos en cuenta que se utilizaron métodos muy heterogéneos para la definición de los distintos tipos de infección respiratoria (otitis, neumonía, infección respiratoria del tracto superior…), que esta mejoría se reduce a un grupo concreto y que la magnitud del efecto es baja (OR>0,9, con un IC prácticamente de 1), estos resultados siguen pareciendo insuficientes para recomendar la suplementación universal con vitaminaD.
No se ha demostrado que la suplementación disminuya la incidencia ni la gravedad de otro tipo de infecciones. Es más, en estudios en países en vías de desarrollo se observó que la utilización de pautas de choque con vitaminaD en lactantes desnutridos aumenta el riesgo de neumonías de repetición16. Estos resultados podrían deberse a los ascensos y descensos bruscos en los niveles de vitaminaD que pueden suprimir las respuestas adaptativas a la infección, así como potenciar las respuestas innatas y bloquear la actividad de las enzimas que sintetizan y catabolizan el calcitriol en tejidos extrarrenales. Esto podría generar concentraciones reducidas de este metabolito activo en los focos de la enfermedad. Tampoco se ha demostrado que la suplementación con vitaminaD en población pediátrica sana disminuya el riesgo de atopia, enfermedades autoinmunes, oncológicas…17,18.
Principales guías de práctica clínicaSuplementación con vitaminaDEn los menores de 1año, la práctica totalidad de las guías recomiendan la suplementación universal con 400UI al día de vitaminaD, independientemente del tipo de alimentación3,19-24. Únicamente en el grupo reducido de lactantes que alcancen una ingesta diaria de al menos 1litro de fórmula adaptada infantil (equivalente a 400UI/día) se podría evitar la suplementación1,2. Los autores se basan principalmente en la imposibilidad de alcanzar las ingestas diarias recomendadas mediante la dieta, en la escasa exposición solar en este grupo de edad, en el papel como estrategia de salud pública respecto a la prevención del raquitismo, así como en los múltiples estudios de seguridad que avalan el uso de esta dosis25 y las dificultades desde un punto de vista ético para realizar ensayos clínicos placebo controlado en este grupo de edad, principalmente en aquellos que reciben lactancia materna.
En los mayores de 1año la mayoría de las guías no recomiendan la suplementación universal, sino individualizar según la presencia de factores de riesgo, la exposición solar y la ingesta de vitaminaD. Únicamente algunos países muy concretos del hemisferio norte recomiendan suplementación universal o durante los meses de invierno (tabla 2).
Recomendaciones de las principales sociedades científicas sobre suplementación con vitamina D en pacientes pediátricos según grupos de edad (menores y mayores de 1 año)
| Sociedad Científica | Recomendaciones menores de 1 año |
|---|---|
| AEPED (2012), AAP (2008), Sociedad Polaca de Endocrinología Infantil (2018) | Lactancia materna: 400 UI/día. Los niños que no alcancen 1 litro de formula adaptada: 400 UI/Día |
| ESPGHAN (2013), Academia Europea de Pediatría (2017) Academia India Pediatría (2021), Sociedad Italiana de Pediatría (2018) | Universal: 400 UI/día |
| Comité expertos Francés (2022) | Universal: Mínimo de 400 UI/día y máximo de 800 UI/día |
| Sociedades Científicas | Recomendaciones 1-18 años |
|---|---|
| AAP (2008) | Grupos de riesgo si no alcanzan RDAS (600 UI/día) |
| Sociedad Italiana de Pediatría (2018) Academia Europea de Pediatría (2017), ESPGHAN (2013), APED (2012), Academia India de Pediatría (2021) Sociedad Alemana de Pediatría (2019) | 400-1000 UI/Día en grupos de riesgo |
| Departamento inglés de salud (2016) | 400 UI/Día universal en meses de invierno |
| Comité Expertos Francés (2022) | Universal todo el año 400-800 UI/Día. Doble dosis en grupos de riesgo |
AEPED: Asociación española de pediatría, ESPGHAN: Sociedad Europea de gastroenterología, hepatología y nutrición pediátrica, AAP: Academia Americana Pediatría
A pesar de la disparidad de criterios sobre la suplementación con vitaminaD (principalmente en los mayores de 1año), todas las guías se posicionan en contra de monitorizar los niveles de esta vitamina en población sana sin factores de riesgo y asintomática. Esta estrategia no ha demostrado ser coste-efectiva, y a la escasa evidencia sobre la suplementación en esta población se une la ausencia de consenso sobre los puntos de corte para definir su deficiencia. Todo ello puede conllevar una prescripción inadecuada de la suplementación con vitaminaD, así como un exceso de extracciones analíticas26. Solo en algunos casos, según las principales sociedades científicas, existen indicaciones para analizar los niveles de calcidiol (tabla 3). En aquellos que requieren monitorización periódica se recomienda su determinación en los últimos meses de invierno.
Indicaciones para determinar los niveles de calcidiol en población pediátrica
| SINTOMÁTICOS | - Alteraciones óseas: craneotabes prominencia condro costal, genu varo-valgo.- Lactantes con irritabilidad no justificada, retraso de hitos desarrollo motor y talla baja.- Dolor óseo y/o muscular no justificado, debilidad muscular.- Fracturas múltiples y por mecanismos de baja energía.- Alteraciones analíticas: Hipocalcemia, elevación fosfatasa alcalina. |
| GRUPO DE RIESGO | - Prematuros o lactantes con lactancia materna que no reciben suplementos de vitamina D.- Lactantes y niños de piel oscura y escasa exposición solar que viven en altas latitudes.- Tratamientos crónicos (anticonvulsionantes, antirretrovirales, corticoides).- Restricciones dietéticas, niños que no alcanzan ingesta recomendada: ARFID, veganos, alergia alimentaria... |
| ENFERMEDADES CRÓNICAS | - Malabsorción: Insuficiencia pancreática exocrina (Fibrosis quística, Shwachman-Diamond…) Enfermedad inflamatoria intestinal, intestino corto, Enfermedad Celiaca (al diagnóstico, mal control…)- Enfermedad renal o hepática crónica.- Colestasis.- Obesidad con factores de riesgo asociados. |
ARFID: Trastorno de la conducta alimentaria tipo evitación/restricción
La adherencia a las guías de práctica clínica en España es baja27, y según estudios recientes en Europa y en Estados Unidos, la adherencia en algunos países se encuentra por debajo del 15%. En esta línea, algunos centros han puesto en marcha una serie de medidas para tratar de mejorar sus resultados (fomentar la formación del personal sanitario, prescripción desde la maternidad con información por escrito a familias sobre la importancia de la suplementación, control ambulatorio de adherencia mediante receta electrónica…)28.
Toxicidad por vitaminaDEn la mayoría de los casos publicados de toxicidad por vitaminaD los niños recibían dosis muy altas (ingestas totales acumuladas durante días o semanas entre 240.000 y 4.500.000UI)29. Un metaanálisis reciente analizó 32 ensayos clínicos en pacientes entre 0 y 6años que recibían entre 1.200 y 10.000IU/día, sin observar diferencias en el número de eventos adversos serios (muerte o ingreso) respecto a aquellos que recibían dosis más bajas30. Sin embargo, debemos ser cautos, dado que hay un grupo de niños con determinados polimorfismos, así como mutaciones en el gen CYP24A1 que tienen más susceptibilidad para desarrollar hipercalcemia e intoxicación por vitaminaD a dosis más bajas. Además, un exceso de vitaminaD podría actuar de forma negativa sobre la mineralización ósea durante la infancia y la adolescencia, considerados periodos críticos.
El límite superior de ingesta tolerable (UL) varía según las sociedades científicas; para la Autoridad Europea de Seguridad Alimentaria (EFSA) es de 1.000UI/día para los menores de 1año y de 2.000UI/día para aquellos entre 1 y 10años, mientras que para el Instituto de Medicina (IOM) es de 1.000UI/día para los menores de 6meses y de 1.500UI/día para aquellos entre 6 y 12meses5,31. No se han descrito casos de intoxicaciones por debajo de estas cifras, por lo que las recomendaciones de suplementación con 400UI/día en menores de 1año son totalmente seguras y no se requiere bajar la dosis de suplementación con vitaminaD a medida que aumente la ingesta en el lactante.
Sin embargo, en los últimos años se ha descrito un incremento de casos de intoxicaciones32, probablemente secundario al aumento del número de prescripciones, así como de la oferta de suplementos de vitaminaD con concentraciones muy diversas que pueden dar lugar a errores en su administración. Por ello se recomienda dar instrucciones siempre por escrito, incluyendo el horario, el preparado, la concentración y la dosis, así como asegurarse en las revisiones periódicas de atención primaria de su correcta administración. El uso de la receta electrónica puede ser útil para comprobar el número de envases dispensados y recogidos por el paciente.
DiscusiónSalvo en los menores de un año, actualmente no hay evidencia científica suficiente que apoye la suplementación universal con vitaminaD en población pediátrica sana como medida efectiva para mantener un buen estado de salud. Existen escasos ensayos clínicos, y la mayoría de los estudios publicados tienen limitaciones metodológicas.
Administrar exclusivamente vitaminaD con el objetivo de mejorar la salud ósea y/o las funciones extraesqueléticas cuando estas dependen de muchos factores (aspectos nutricionales como el calcio, el fósforo o el magnesio, el estilo de vida, la actividad física, los factores genéticos, raciales, hormonales…) parece difícil. Tampoco debemos olvidar la importancia de la exposición solar (mediante la acción de la radiación UVB) como catalizador para la síntesis de la vitaminaD, y que además el estado de vitaminaD depende de otros múltiples factores. La presencia de obesidad, la toma de fármacos, los factores genéticos, las enfermedades crónicas o en los primeros meses de vida juegan un importante papel el estatus materno de vitaminaD, y todos estos factores deberían tenerse en cuenta a la hora del diseño de ensayos clínicos, y no siempre es así.
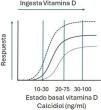
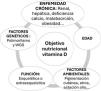
Por otra parte, como ocurre con cualquier otro nutriente, la magnitud del efecto de una misma intervención o suplementación dependerá del estado basal (fig. 1: gráfica dosis-respuesta); por lo tanto, para interpretar correctamente los ensayos clínicos necesitamos conocer el estado nutricional de vitaminaD. Sin embargo, es difícil determinar cuándo un niño sano tiene realmente una deficiencia o insuficiencia de vitaminaD, pues, a pesar de las bondades del calcidiol por su elevada vida media (2-3semanas) y su estabilidad comparada con otros metabolitos, tiene algunas limitaciones. De hecho, se ha comprobado que en los niños no existe una relación lineal entre el calcidiol con la mayoría de las variables resultado, y esto, entre otras razones, hace que las sociedades científicas no se pongan de acuerdo sobre los puntos de corte. Si nos referimos a salud ósea, el punto de corte más «bajo» es 10-12ng/ml, dado que la mayoría de los pacientes pediátricos con raquitismo tienen niveles <10ng/ml; sin embargo, se han reportado casos con valores más altos33. En adultos, a partir de menos de 20ng/ml la disminución de las concentraciones de calcidiol da como resultado un aumento abrupto de la PTH; sin embargo, desconocemos este valor en los pacientes pediátricos (podría ser incluso más bajo)34, lo que demuestra que esta asociación depende, entre otros factores, de la edad, aunque también de la duración de la deficiencia. Para las funciones extraesqueléticas parecen necesarios incluso niveles superiores de vitaminaD, pero la evidencia es todavía menor. Por lo tanto, más que de puntos de corte universales, deberíamos hablar de un objetivo nutricional que probablemente será diferente para cada paciente o individuo según su edad, genética, raza, dieta, patología de base, factores de riesgo, niveles de calcio y el efecto que quiera conseguir, ya sea salud ósea o extraesquelética (fig. 2).
Modelo didáctico de la curva dosis-respuesta de un nutriente, que indica cuál sería la eficacia de la suplementación con una misma dosis de vitaminaD según el estado basal del nutriente.
Nota: se desconoce con exactitud la forma de las curvas y los valores de los puntos de corte mencionados.
Adaptado de Heaney RP. N Engl J Med. 2012;367(1):77-78.
Desde hace unos años se ha intentado avanzar en el conocimiento de nuevos marcadores, y la teoría de la vitaminaD libre sugiere que es la porción libre no unida a proteínas (25 hidroxivitaminaD libre) la que permite que las moléculas de calcidiol estén más fácilmente disponibles para producir sus efectos biológicos y que podría reflejar mejor el estado nutricional. Esta teoría parece tener mayor aplicación cuando los niveles de proteínas y/o albúmina están bajos (cirrosis hepática, embarazo, desnutrición…)35; sin embargo, en población pediátrica sana la correlación entre el calcidiol total y la vitaminaD libre es lineal y robusta, por lo que la determinación de vitaminaD libre por sí sola en esta población no parece aportar grandes beneficios con respecto al calcidiol36.
Los factores genéticos cada vez están cobrando mayor protagonismo, y se han descrito cuatro grupos de polimorfismos implicados en la síntesis y transporte de las formas activas de vitaminaD (hidroxilación, síntesis, transporte) y el clúster de polimorfismos del gen que codifica el receptor VDR presente en diferentes tejidos. Los polimorfismos condicionan la mayor o menor afinidad de la proteína de unión a la vitaminaD (VDBP) por la vitaminaD y sus receptores (VDR), lo que podría explicar hasta el 10% de los niveles de calcidiol37; la respuesta a una dosis de vitaminaD difiere según el polimorfismo38, y además, algunos polimorfismos están relacionados o pueden ser factores de riesgo para determinadas entidades patológicas39. Recientemente, en algunas enfermedades crónicas, mediante la secuenciación del genoma completo (WGS) se han desarrollado diversos scores de riesgo poligénico relacionados con el estado nutricional de la vitaminaD, así como con la respuesta a la suplementación de esta vitamina40.
La prevalencia de deficiencia de vitaminaD en la población infantil española es una cuestión poco documentada. Además, factores como las diferencias geográficas en la exposición al sol y las variaciones en los hábitos alimentarios complican aún más la interpretación y la comparación de los datos disponibles. Este vacío en la información limita la capacidad de diseñar estrategias efectivas sobre la necesidad de suplementación.
ConclusionesLa evidencia sobre la suplementación universal con vitaminaD en población pediátrica sana es limitada.
Según las principales guías de práctica clínica, se recomienda suplementar con 400UI/día de vitaminaD a los niños menores de 1año que reciban lactancia materna o que no alcancen la ingesta diaria recomendada a través de la fórmula infantil adaptada. En los mayores de 1año la suplementación debe ser individualizada.
No se recomienda la determinación de calcidiol en población pediátrica sin factores de riesgo y en ausencia de síntomas.
La prescripción de vitaminaD debe realizarse a través de una receta médica que indique la dosis y la duración del tratamiento. Además, es importante garantizar su correcta administración mediante revisiones periódicas.
En nuestro país existen muy pocos estudios experimentales o de cohortes bien diseñados sobre suplementación con vitaminaD en niños sanos. Si tenemos en cuenta la relevancia de factores como la exposición solar y la genética, debemos promover dicha investigación para poder formular recomendaciones adaptadas a nuestro entorno.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.