La asociación entre tumores y malformaciones congénitas está bien establecida, pero no existen datos exclusivos en el período neonatal y se desconocen los mecanismos subyacentes que generan dicha relación.
ObjetivosEste trabajo tiene dos objetivos: primero, analizar la frecuencia de los tumores neonatales asociados a malformaciones congénitas, y segundo, comentar las posibles hipótesis etiopatogénicas de la relación entre ambas entidades.
Materiales y métodoEstudio retrospectivo de las historias clínicas de los tumores neonatales, en el Hospital Universitario Materno-Infantil La Fe de Valencia, desde enero de 1990 hasta diciembre de 1999. Selección y descripción de las variedades histológicas asociadas a malformaciones congénitas. Éstas se han agrupado siguiendo los criterios de la Clasificación Internacional de Enfermedades CIE-9, códigos 740.0-759.9. Revisión sistemática bibliográfica de los últimos 25 años, obtenida del Medline, Cancerlit, Index Citation Science y Embase. El perfil de búsqueda utilizado fue la combinación de “neonatal/congenital-tumors/cancer/neoplasms” y “congenital malformations/birth defects”.
ResultadosSe identificaron 72 tumores neonatales (2,8 % del total de tumores pediátricos diagnosticados en dichos años) y 15 de ellos (20,8 %) asociados a malformaciones congénitas, enfermedades o síndromes congénitos. Las asociaciones entre tumores neonatales y malformaciones congénitas fueron las siguientes: a) angioma en 3 pacientes: con dos cardiopatías congénitas y una atresia de coanas-laringomalacia; b) neuroblastoma en 2 pacientes: uno con riñón en herradura y anomalías vertebrales, y otro con cardiopatía congénita; c) teratoma en 2 pacientes: uno con fisura palatina y anomalías vertebrales, y otro con metatarso varo; d) tumor del sistema nervioso central en un paciente con hernia de Bochdaleck; e) tumor cardíaco en 4 pacientes con esclerosis tuberosa; f) leucemia aguda en un paciente con síndrome de Down y cardiopatía congénita; g) tumor renal en un caso con hidrocefalia triventricular, y h) tumor adrenal en un caso con hemihipertrofia.
En la bibliografía específica, las publicaciones engloban tumores de diferentes épocas pediátricas y sin unanimidad de criterios para clasificar las malformaciones congénitas. Apenas existen datos en el período neonatal y la asociación entre ambas entidades se obtiene de registros de instituciones médicas. La prevalencia oscila entre el 15 y el 31,6 %. Las hipótesis etiopatogénicas que explican la asociación entre tumores neonatales y malformaciones congénitas están basadas en las exposiciones prenatales (preconcepcionales y transplacentarias) a factores de riesgo potencialmente mutagénicos y carcinogénicos.
ConclusionesProbablemente, los tumores neonatales se asocian con mayor frecuencia a malformaciones congénitas que los tumores diagnosticados en épocas posteriores de la vida. Para conocer la prevalencia real de la asociación entre tumors neonatales y malformaciones congénitas, es necesario unificar los criterios de inclusión y definición de ambas entidades. La obtención de una minuciosa historia medioambiental en todos los tumores neonatales asociados a malformaciones congénitas, donde se detallen y registren todos los factores de riesgo constitucionales y ambientales, es fundamental para mejorar nuestros escasos conocimientos de los mecanismos prenatales subyacentes y avanzar en su prevención.
The association between pediatric cancer and congenital abnormalities is well known but, there is no exclusive data on the neonatal period and the underlying etiopathogenic mechanisms are unknown.
ObjectivesFirst, to analyze the frequency of neonatal tumours associated with congenital abnormalities; and second, to comment on the likely etiopathogenic hypotheses of a relationship between neonatal tumours and congenital abnormalities.
Materials and methodHistorical series of neonatal tumours from La Fe University Children's Hospital in Valencia (Spain), from January 1990 to December 1999. Histological varieties of neonatal tumours and associated congenital abnormalities were described. A systematic review of the last 25 years was carried out using Medline, Cancerlit, Index Citation Science and Embase. The search profile used was the combination of “neonatal/congenital-tumors/cancer/neoplasms” and “congenital malformations/birth defects”.
Results72 neonatal tumours were identified (2.8 % of all pediatric cancers diagnosed in our hospital) and in 15 cases (20.8 %) there was some associated malformation, disease or syndrome. The association between congenital abnormalities and neonatal tumours were: a) angiomas in three patients: two patients with congenital heart disease with a choanal stenosis, laryngomalacia; b) neuroblastomas in two patients: horseshoe kidney with vertebral anomalies and other with congenital heart disease; c) teratomas in two patients: one with cleft palate with vertebral anomalies and other with metatarsal varus; d) one tumour of the central nervous system with Bochdaleck hernia; e) heart tumours in four patients with tuberous sclerosis; f) acute leukaemia in one patient with Down syndrome and congenital heart disease; g) kidney tumour in one case with triventricular hydrocephaly, and h) adrenocortical tumour: hemihypertrophy.
The publications included the tumours diagnosed in different pediatric periods and without unified criteria to classify the congenital abnormalities. Little data exist on the neonatal period and the majority are from medical institutions registers. The prevalence varies from 15 to 31.6 %. To explain this association, the hypotheses are based on prenatal exposures (preconceptional and transplacental exposure), to mutagenic and carcinogenic risk factors.
ConclusionsNeonatal tumours are more often associated to congenital abnormalities than other pediatric cancers. The inclusion and classification criteria needs to be unified to better understand the association between the neonatal tumours and congenital abnormalities. The environmental history in all neonatal tumours associated to congenital abnormalities, including the constitutional and environmental risk factors, will help to improve our knowledge of the underlying prenatal mechanisms and to an advance in its prevention.
La asociación entre las malformaciones congénitas y los tumores pediátricos es bien conocida. Diversos estudios poblacionales encuentran un mayor riesgo tumoral en niños con malformaciones congénitas (9,6-10,8 %) respecto a los que no las presentan (2,5-4,9 %)1,2. Hallazgos similares se encuentran en estudios poblacionales para los menores de 12 meses3,4. En el período neonatal apenas existen datos y la asociación entre ambas patologías se obtiene de registros de diferentes instituciones médicas, situándose entre el 15 y el 31,6%5–7. Otro problema adicional consiste en que los autores no siguen los mismos criterios para incluir los diversos tipos de malformaciones congénitas. La presente revisión tiene dos objetivos: primero, analizar la frecuencia de los tumores neonatales asociados a malformaciones congénitas, y segundo, comentar las probables hipótesis etiopatogénicas de la relación entre los tumores neonatales y las malformaciones congénitas.
MATERIALES Y MÉTODOEstudio retrospectivo de las historias clínicas de los tumores neonatales (primeros 28 días de vida), atendidos en el Hospital Infantil Universitario La Fe de Valencia, desde enero de 1990 hasta diciembre de 1999. Descripción de las variedades histológicas y malformaciones congénitas asociadas. Las malformaciones congénitas se han agrupado siguiendo los criterios de la Clasificación Internacional de Enfermedades CIE-9, códigos 740.0-759 9 (http://icd9cm.chrisendres.com/2007/). Se excluyeron las siguientes entidades: hamartomas, hemangiomas cutáneos planos y cavernosos, nevus, lipomas, fibromas subcutáneos, linfangiomas y quistes epidérmicos. Las historias clínicas se obtuvieron a través del Servicio de Documentación y Archivo del Hospital Infantil Universitario La Fe, realizando una búsqueda según el diagnóstico del tumor y/o de sus diferentes tipos específicos.
Realizamos una revisión bibliográfica sistemática de los últimos 25 años obtenida de Medline, Cancerlit, Index Citation Science y Embase. El perfil de búsqueda utilizado fue la combinación de “neonatal/congenital-tumors/cancer/neoplasms” y “congenital malformations/birth defects”. Seleccionamos los trabajos más interesantes y, de sus referencias, recuperamos las más relevantes publicadas antes del período de la búsqueda.
RESULTADOSSe identificaron 72 tumores neonatales, que corresponden al 2,8 % de los tumores pediátricos diagnosticados en nuestro hospital durante dicha década. Las variedades histológicas más frecuentes son hemangioma, neuroblastoma, teratoma y tumor de partes blandas (tabla 1).
Variedades histológicas de los tumores neonatales
Angiomas
| 15 |
| Neuroblastomas | 12 |
| Teratomas | 9 |
Tumores de partes blandas
| 7 |
Tumores del sistema nervioso central
| 6 |
| Tumores cardíacos | 6 |
Leucemias agudas
| 4 |
| Tumores renales (nefromas mesoblásticos) | 4 |
| Histiocitosis | 4 |
| Tumores adrenocorticales | 3 |
| Retinoblastoma | 1 |
| Hepatoblastoma | 1 |
En 15 casos (20,8 %) existía alguna malformación congénita, enfermedad o síndrome asociado (tablas 2 y 3). Las asociaciones entre tumores neonatales y malformaciones congénitas fueron las siguientes: a) angioma en 3 pacientes: con dos cardiopatías congénitas y una atresia de coanas (laringomalacia); b) neuroblastoma en 2 pacientes: uno con riñón en herradura y anomalías vertebrales, y otro con cardiopatía congénita; c) teratoma en 2 pacientes: uno con fisura palatina y anomalías vertebrales, y otro con metatarso varo; d) tumor del sistema nervioso central en 1 paciente con hernia de Bochdaleck; e) tumor cardíaco en 4 pacientes con esclerosis tuberosa; f) leucemia aguda en 1 paciente con síndrome de Down y cardiopatía congénita; g) tumor renal en un caso con hidrocefalia triventricular, y h) tumor adrenal en un caso con hemihipertrofia. Entre ellas, como puede observarse, las cardiopatías congénitas y la esclerosis tuberosa fueron las más frecuentes.
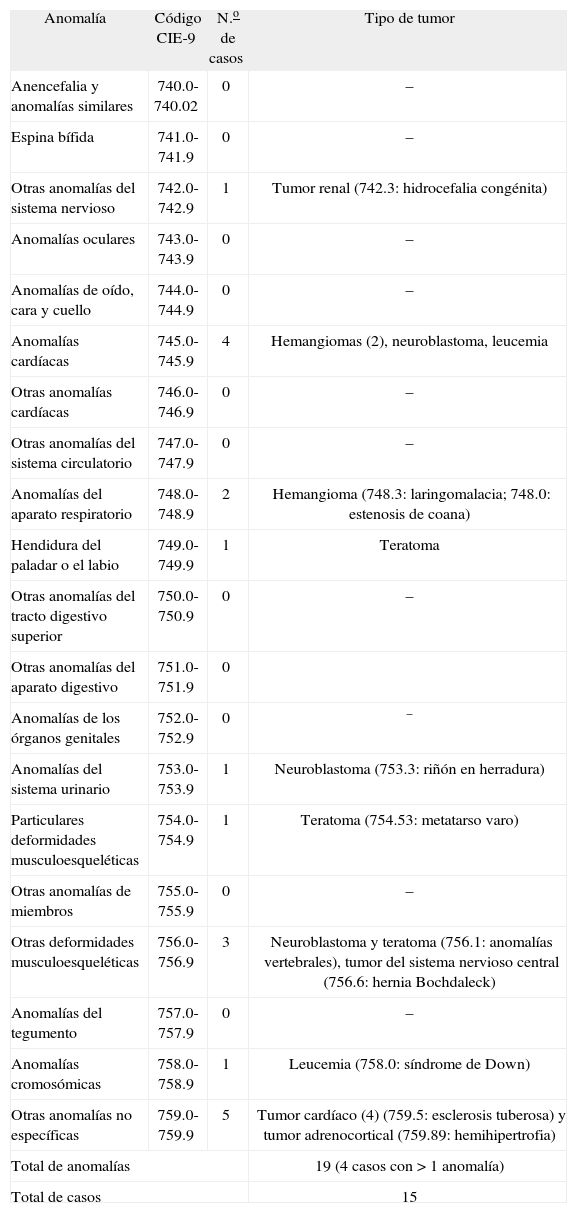
Anomalías congénitas y variedad de tumor neonatal, según la Clasificación Internacional de Enfermedades (CIE-9 códigos 740.0-759.9)
| Anomalía | Código CIE-9 | N.o de casos | Tipo de tumor |
| Anencefalia y anomalías similares | 740.0-740.02 | 0 | – |
| Espina bífida | 741.0-741.9 | 0 | – |
| Otras anomalías del sistema nervioso | 742.0-742.9 | 1 | Tumor renal (742.3: hidrocefalia congénita) |
| Anomalías oculares | 743.0-743.9 | 0 | – |
| Anomalías de oído, cara y cuello | 744.0-744.9 | 0 | – |
| Anomalías cardíacas | 745.0-745.9 | 4 | Hemangiomas (2), neuroblastoma, leucemia |
| Otras anomalías cardíacas | 746.0-746.9 | 0 | – |
| Otras anomalías del sistema circulatorio | 747.0-747.9 | 0 | – |
| Anomalías del aparato respiratorio | 748.0-748.9 | 2 | Hemangioma (748.3: laringomalacia; 748.0: estenosis de coana) |
| Hendidura del paladar o el labio | 749.0-749.9 | 1 | Teratoma |
| Otras anomalías del tracto digestivo superior | 750.0-750.9 | 0 | – |
| Otras anomalías del aparato digestivo | 751.0-751.9 | 0 | |
| Anomalías de los órganos genitales | 752.0-752.9 | 0 | – |
| Anomalías del sistema urinario | 753.0-753.9 | 1 | Neuroblastoma (753.3: riñón en herradura) |
| Particulares deformidades musculoesqueléticas | 754.0-754.9 | 1 | Teratoma (754.53: metatarso varo) |
| Otras anomalías de miembros | 755.0-755.9 | 0 | – |
| Otras deformidades musculoesqueléticas | 756.0-756.9 | 3 | Neuroblastoma y teratoma (756.1: anomalías vertebrales), tumor del sistema nervioso central (756.6: hernia Bochdaleck) |
| Anomalías del tegumento | 757.0-757.9 | 0 | – |
| Anomalías cromosómicas | 758.0-758.9 | 1 | Leucemia (758.0: síndrome de Down) |
| Otras anomalías no específicas | 759.0-759.9 | 5 | Tumor cardíaco (4) (759.5: esclerosis tuberosa) y tumor adrenocortical (759.89: hemihipertrofia) |
| Total de anomalías | 19 (4 casos con > 1 anomalía) | ||
| Total de casos | 15 | ||
Disponible en: http://icd9cm.chrisendres.com/2007/
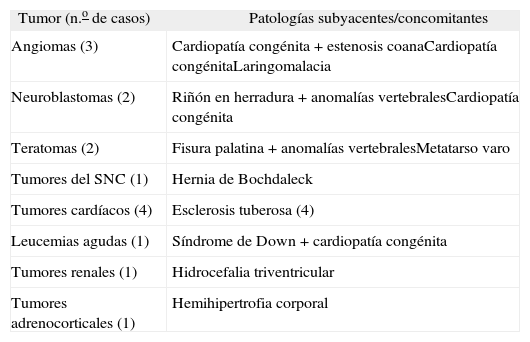
Anomalías congénitas agrupadas por variedades histológicas
| Tumor (n.o de casos) | Patologías subyacentes/concomitantes |
| Angiomas (3) | Cardiopatía congénita + estenosis coanaCardiopatía congénitaLaringomalacia |
| Neuroblastomas (2) | Riñón en herradura + anomalías vertebralesCardiopatía congénita |
| Teratomas (2) | Fisura palatina + anomalías vertebralesMetatarso varo |
| Tumores del SNC (1) | Hernia de Bochdaleck |
| Tumores cardíacos (4) | Esclerosis tuberosa (4) |
| Leucemias agudas (1) | Síndrome de Down + cardiopatía congénita |
| Tumores renales (1) | Hidrocefalia triventricular |
| Tumores adrenocorticales (1) | Hemihipertrofia corporal |
SNC: sistema nervioso central.
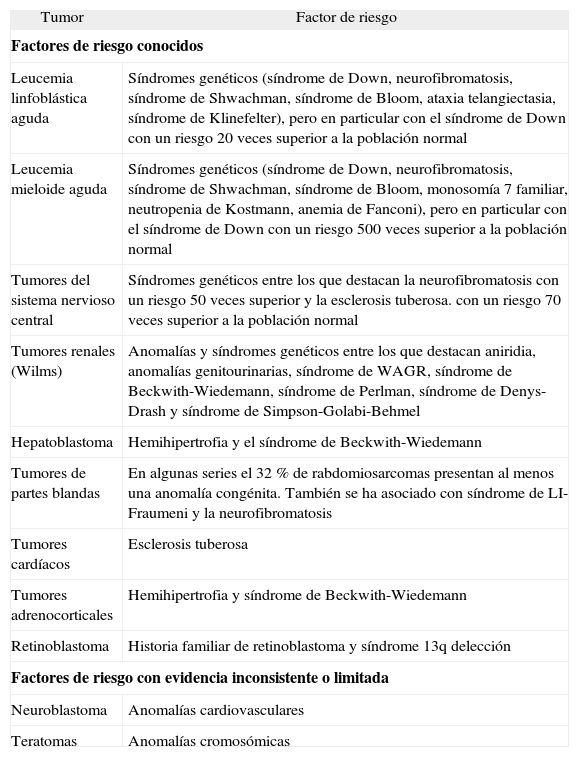
La primera descripción de una asociación entre malformación congénita y tumor pediátrico se realizó en un paciente con síndrome de Down y leucemia aguda8. Posteriormente, diversos trabajos han descrito la asociación entre diferentes malformaciones congénitas y tumores pediátricos benignos y malignos9–11, como causas o factores de riesgo relacionados con mayor o menor evidencia científica en su desarrollo (tabla 4).
| Tumor | Factor de riesgo |
| Factores de riesgo conocidos | |
| Leucemia linfoblástica aguda | Síndromes genéticos (síndrome de Down, neurofibromatosis, síndrome de Shwachman, síndrome de Bloom, ataxia telangiectasia, síndrome de Klinefelter), pero en particular con el síndrome de Down con un riesgo 20 veces superior a la población normal |
| Leucemia mieloide aguda | Síndromes genéticos (síndrome de Down, neurofibromatosis, síndrome de Shwachman, síndrome de Bloom, monosomía 7 familiar, neutropenia de Kostmann, anemia de Fanconi), pero en particular con el síndrome de Down con un riesgo 500 veces superior a la población normal |
| Tumores del sistema nervioso central | Síndromes genéticos entre los que destacan la neurofibromatosis con un riesgo 50 veces superior y la esclerosis tuberosa. con un riesgo 70 veces superior a la población normal |
| Tumores renales (Wilms) | Anomalías y síndromes genéticos entre los que destacan aniridia, anomalías genitourinarias, síndrome de WAGR, síndrome de Beckwith-Wiedemann, síndrome de Perlman, síndrome de Denys-Drash y síndrome de Simpson-Golabi-Behmel |
| Hepatoblastoma | Hemihipertrofia y el síndrome de Beckwith-Wiedemann |
| Tumores de partes blandas | En algunas series el 32 % de rabdomiosarcomas presentan al menos una anomalía congénita. También se ha asociado con síndrome de LI-Fraumeni y la neurofibromatosis |
| Tumores cardíacos | Esclerosis tuberosa |
| Tumores adrenocorticales | Hemihipertrofia y síndrome de Beckwith-Wiedemann |
| Retinoblastoma | Historia familiar de retinoblastoma y síndrome 13q delección |
| Factores de riesgo con evidencia inconsistente o limitada | |
| Neuroblastoma | Anomalías cardiovasculares |
| Teratomas | Anomalías cromosómicas |
Entre los diversos estudios poblacionales que encuentran un mayor riesgo tumoral en pacientes con malformaciones congénitas, queremos destacar dos de ellos. El primero, realizado en el Reino Unido en 1993, objetivó que el 10,8 % de los niños con tumores presentaban malformaciones congénitas frente al 4,9 % del grupo control, siendo esta diferencia estadísticamente significativa (p < 0,001)2. El segundo, realizado en Australia en 19981, evidenció que 55 (9,6 %) de 570 niños con tumores tenían una malformación congénita asociada, comparada con el 2,5 % del grupo control, con una odds ratio (OR) de 4,5 (intervalo de confianza del 95 % [IC 95 %]: 3,1-6,7). El incremento de riesgo era directamente proporcional al número de malformaciones asociadas y los niños con defectos cromosómicos tenían el riesgo más alto para desarrollar tumores (OR: 16,7; IC 95 %: 6,1-45,3), y era el síndrome de Down el que presentaba un riesgo 27 veces mayor. Hallazgos similares se encuentran en estudios poblacionales para menores de 12 meses de edad3,4, y un trabajo reciente basado en el seguimiento de 90.400 niños encuentra que el riesgo de desarrollar un tumor durante el primer año de vida es seis veces mayor entre la población con malformación congénita, respecto al normal12. También evidenció que las anomalías más frecuentes eran las cromosómicas, seguidas de las del sistema nervioso central y genitourinarias. Las asociaciones más prevalentes fueron la leucemia aguda y anomalías cromosómicas (síndrome de Down, principalmente), tumores hepáticos y anomalías digestivas y malformaciones musculoesqueléticas con linfomas, tumores óseos y de células germinales.
En el período neonatal no existen datos concretos y la asociación entre ambas patologías se obtiene de registros de diferentes instituciones médicas, incluyendo tumoraciones de histología benigna y maligna, dado que su comportamiento biológico es diferente al del resto de la época pediátrica. Moore et al5, documentó en 2003 que el 15 % de los tumores neonatales se asocian a malformaciones congénitas, mientras que Agha et al6 en 2006, encuentran que entre 38 tumores neonatales, 12 pacientes (31,6 %) tenían malformaciones congénitas. En nuestro estudio, el 20,8 % (15 pacientes) de los tumores neonatales presentaban malformaciones congénitas, enfermedades o síndromes asociados, y las más frecuentes eran las cardiopatías congénitas y la esclerosis tuberosa. Nuestros resultados están basados en una exhaustiva selección de pacientes, basada en: a) el período neonatal estricto; b) la variedad histológica tumoral, y c) el tipo de malformación. Muchos trabajos, para aumentar casuísticas prolongan la inclusión de tumores hasta los 3, 6 o 12 meses de edad y algunos de ellos no registran las malformaciones congénitas menores (metatarso varo, atresia de coanas, etc.) registradas en nuestra revisión. Recomendamos a los futuros autores la importancia de seguir los criterios de las malformaciones congénitas según la Clasificación Internacional de Enfermedades CIE-9, códigos 740.0-759.9 (http://icd9cm.chrisendres.com/2007/). Por todo lo expuesto y aunque nuestra serie de tumores neonatales constituye una de las más amplias del mundo7,13–15, no nos permite comparar con los tipos de malformaciones congénitas encontradas en estudios poblacionales no exclusivos del período neonatal. En referencia a la bibliografía (tabla 4), en nuestra serie existen tres asociaciones descritas con mayor frecuencia: a) asociación entre leucemia aguda y síndrome de Down; b) esclerosis tuberosa y tumores cardíacos, y c) tumores adrenocorticales e hemihipertrofia corporal. Las restantes asociaciones encontradas en nuestros neonatos también han sido descritas en casos únicos o pequeños grupos tumorales.
La importancia de incluir sólo los tumores neonatales radica en la exclusión de los hipotéticos factores de riesgo posnatales en su etiopatogenia. Las hipótesis que pueden explicar la asociación entre los tumores neonatales y las malformaciones congénitas están centradas en los conceptos de la tumorogénesis preconcepcional16–18 y transplacentaria18–22, y son las siguientes:
- 1.
Mutación espontánea o adquirida, por la acción de un carcinógeno sobre una célula germinal. Afecta a uno o varios genes cuya integridad es necesaria para la correcta morfogénesis y para el normal crecimiento y desarrollo celular17,23,24. Son los cánceres familiares o hereditarios con herencia autosómica dominante o recesiva con malformaciones congénitas asociadas, como la esclerosis tuberosa, la neurofibromatosis y el retinoblastoma familiar, todos ellos con un mayor riesgo para el desarrollo de tumores, no sólo en el período neonatal, sino también en la edad pediátrica o adulta.
- 2.
Mutación espontánea o adquirida, por la acción de un carcinógeno físico, químico o biológico sobre una célula somática. Pueden diferenciarse tres variedades dependiendo del período fetal o ventana de exposición25,26:
- –
Blastogénesis (semanas 0–2 de vida fetal): existe una resistencia innata antitumoral y una baja susceptibilidad de anomalías morfológicas. Si los agentes tumorogénicos superan estas barreras, dan lugar a los síndromes cromosómicos entre los que destacan la trisomía 21 y las disgenesias gonadales. Estos síndromes presentan un riesgo elevado para el desarrollo de tumores, no sólo en el período neonatal, sino también en la edad pediátrica o adulta. Tal es el caso del desarrollo de una leucemia aguda en un paciente con síndrome de Down.
- –
Organogénesis (semanas 3–8 de vida fetal): estudios en animales de experimentación y en autopsias fetales humanas sugieren que determinados factores potencialmente tóxicos, mutagénicos y cancerígenos transplacentarios producirán malformaciones entre las semanas 2 y 8, y tumores entre la sexta y la cuadragésima semana de gestación. Así se explican los casos coexistentes de malformaciones congénitas y tumores, en los que la actuación de un mismo agente entre la sexta a la octava semana de vida fetal desencadena el desarrollo asociado de una malformación y un tumor16,20. Ejemplos de ello serían los restantes tipos de malformaciones congénitas asociadas a diferentes tumores.
- –
Histogénesis (semanas 8–40 de vida fetal): período de tumorogénesis en el que el desarrollo del tumor puede dar lugar, por compresión o infiltración, una malformación congénita3. Ejemplo de ello sería la hidrocefalia ocasionada por un tumor cerebral.
- –
Según los mecanismos etiopatogénicos comentados en nuestra serie, los 4 pacientes que presentaban una tumoración cardíaca y esclerosis tuberosa y el tumor adrenocortical asociado a un síndrome de hipercrecimiento (hemihipertrofia corporal), serían causados por una mutación originada por un factor o agente tumorogénico en una célula germinal. Asimismo, uno de los pacientes de nuestra serie, hijo de una madre afectada de la misma patología, presentaba un retinoblastoma y, aunque no tenía una malformación congénita asociada, se trataría de un cáncer familiar perteneciente a este grupo etiopatogénico. Los restantes casos se producirían por una mutación en una célula somática en el período fetal de blastogénesis (el paciente con síndrome de Down y leucemia aguda) u organogénesis (los restantes casos), sin encontrarse, a nuestro juicio, ningún caso en la fase de la histogénesis (tabla 5).
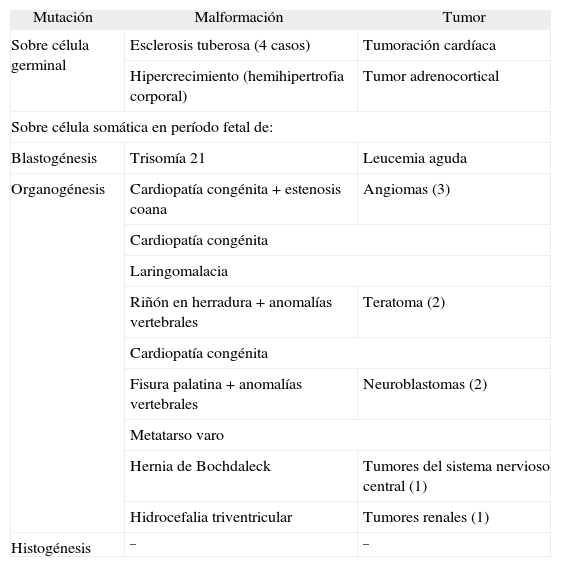
Clasificación de malformaciones congénitas y tumores en función de los factores etiopatogénicos
| Mutación | Malformación | Tumor |
| Sobre célula germinal | Esclerosis tuberosa (4 casos) | Tumoración cardíaca |
| Hipercrecimiento (hemihipertrofia corporal) | Tumor adrenocortical | |
| Sobre célula somática en período fetal de: | ||
| Blastogénesis | Trisomía 21 | Leucemia aguda |
| Organogénesis | Cardiopatía congénita + estenosis coana | Angiomas (3) |
| Cardiopatía congénita | ||
| Laringomalacia | ||
| Riñón en herradura + anomalías vertebrales | Teratoma (2) | |
| Cardiopatía congénita | ||
| Fisura palatina + anomalías vertebrales | Neuroblastomas (2) | |
| Metatarso varo | ||
| Hernia de Bochdaleck | Tumores del sistema nervioso central (1) | |
| Hidrocefalia triventricular | Tumores renales (1) | |
| Histogénesis | – | – |
Aunque el diseño metodológico de nuestra revisión permite generar hipótesis, no sirve para evaluarlas, y la presencia de esta asociación entre malformaciones congénitas y tumores neonatales una probable coincidencia. No obstante, los tumores neonatales nos brindan la oportunidad de estudiar los factores de riesgo ambientales preconcepcionales y gestacionales, que conjuntamente con los constitucionales, han contribuido a su genésis y desarrollo. Así, eliminamos la influencia de los factores de riesgo posnatales, que se suman a los anteriores en los restantes tumores diagnosticados en épocas posteriores de la vida. Además, estudiar su asociación con las malformaciones congénitas nos orienta hacia los factores de riesgo ambientales que han intervenido durante la ventana fetal de exposición entre las semanas 6 y 8 de vida fetal. Por todo ello, consideramos conveniente unificar criterios de inclusión, tanto para los tumores neonatales como para las malformaciones congénitas y estas últimas desglosarlas en los grupos etiopatogénicos descritos anteriormente.
Al mismo tiempo, la obtención de una detallada y exhaustiva historia medioambiental, en la que se consignen y detallen la ausencia o presencia de los factores de riesgo constitucionales y ambientales, potencialmente cancerígenos, es fundamental para avanzar en el conocimiento de su prevalencia real y de su prevención.