La espectroscopia cercana al infrarrojo (NIRS, por sus siglas en inglés) es un método no invasivo de monitorización continua que se ha utilizado con éxito en algunos estudios para monitorizar la saturación regional cerebral y esplácnica de oxígeno en recién nacidos prematuros1–4. La espectroscopia resuelta espacialmente utiliza luz cercana al infrarrojo (600–900nm) para detectar la presencia de cromóforos, principalmente la hemoglobina, pero también el citocromo aa3 y la mioglobina. La NIRS mide la oxigenación venosa, arterial y capilar, reflejando el transporte de oxígeno a los tejidos y su consumo. Permite la detección precoz de deficiencias en la saturación regional en diferentes tejidos, incluso antes de que aparezcan el daño tisular y las lesiones. La mayoría de los estudios realizados han encontrado que valores bajos de la saturación de oxígeno esplácnica en prematuros se asocian al antecedente de retraso de crecimiento intrauterino y al riesgo de desarrollar enterocolitis necrosante (ECN)1–3.
La perforación gástrica neonatal es una urgencia quirúrgica infrecuente, que constituye el 7% del total de casos de perforación gastrointestinal en el período neonatal. Se asocia a una alta morbimortalidad que oscila entre el 41 y el 80%. Su etiología es multifactorial, e incluye enfermedades y traumatismos iatrogénicos del aparato digestivo. A su vez, el uso de esteroides o el estrés fisiológico intenso pueden aumentar la secreción de ácido gástrico y causar úlceras de estrés. No obstante, la fisiopatología de esta lesión no se ha establecido. La presentación clínica suele ser inespecífica. Sus posibles signos y síntomas clínicos incluyen distensión abdominal, rechazo de ingesta, actividad disminuida, alteraciones hemodinámicas y distrés respiratorio. El diagnóstico ha de confirmarse mediante radiografía abdominal, con detección de neumoperitoneo y, en algunos casos, neumoescroto4-6.
En el presente artículo se describe el papel de la monitorización abdominal continua mediante NIRS en la unidad de cuidados intensivos neonatales (UCIN) y su contribución a la predicción precoz de complicaciones gastrointestinales2,3.
Presentamos el caso de un prematuro nacido por cesárea a las 30 semanas de edad gestacional con un peso al nacer de 880g. El neonato fue ingresado en la UCIN para recibir soporte respiratorio. Antecedente de retraso de crecimiento intrauterino detectado durante el embarazo. La madre recibió un ciclo completo de corticoterapia antenatal y sulfato de magnesio. Las puntuaciones Apgar al minuto y a los 5min fueron 7 y 8, respectivamente, y el análisis de los gases del cordón detectó un pH arterial de 7,22. El neonato fue transferido a la UCIN con administración de presión continua en la vía aérea (CPAP) mediante gafas nasales con una fracción inspirada de oxígeno (FiO2) de 0,21.
El paciente sufría distrés respiratorio leve, pero se mantuvo estable sin necesidad de aumentar la FiO2 o de surfactante. Recibió ventilación nasal intermitente entre el primer y cuarto día de vida, momento en el que se cambió el soporte a CPAP con gafas nasales. Solo requirió aumentos en la FiO2 durante su manipulación/procedimientos. También se administró cafeína a partir de las 24h de vida. Se inició antibioterapia profiláctica al objetivarse neutropenia grave (neutrófilos <500μl) poco después de nacer. La nutrición enteral trófica con leche materna donada se inició a las 24h de vida. A las 48h, el médico a cargo del paciente diagnosticó ductus arterioso persistente hemodinámicamente significativo, que se trató con éxito con un curso de paracetamol de 3 días de duración, ya que el ibuprofeno estaba contraindicado por presencia de trombocitopenia.
La evacuación de meconio se consiguió a las 48h del nacimiento con enema de solución salina. En los días que siguieron, las deposiciones solo fueron posibles con la administración de enemas de solución salina. Cabe resaltar que el paciente no toleraba la nutrición enteral, ni siquiera con volúmenes mínimos de leche materna. En el cuarto día de vida se inició tratamiento con N-acetilcisteína por sospecha de síndrome de tapón meconial (STM). Las radiografías y la ecografía abdominales descartaron complicaciones adicionales del STM. El paciente se mantuvo bajo monitorización continua por NIRS con el sistema INVOS® 5100 (Medtronic®, Fridley, Minnesota, EE. UU.) y el Neonatal Oxy-Alert® NIRS Sensor (Medtronic®, Fridley, Minnesota, EE. UU.). El paciente tuvo un sensor colocado en el flanco derecho para monitorizar la oxigenación esplácnica a partir del primer día de vida.
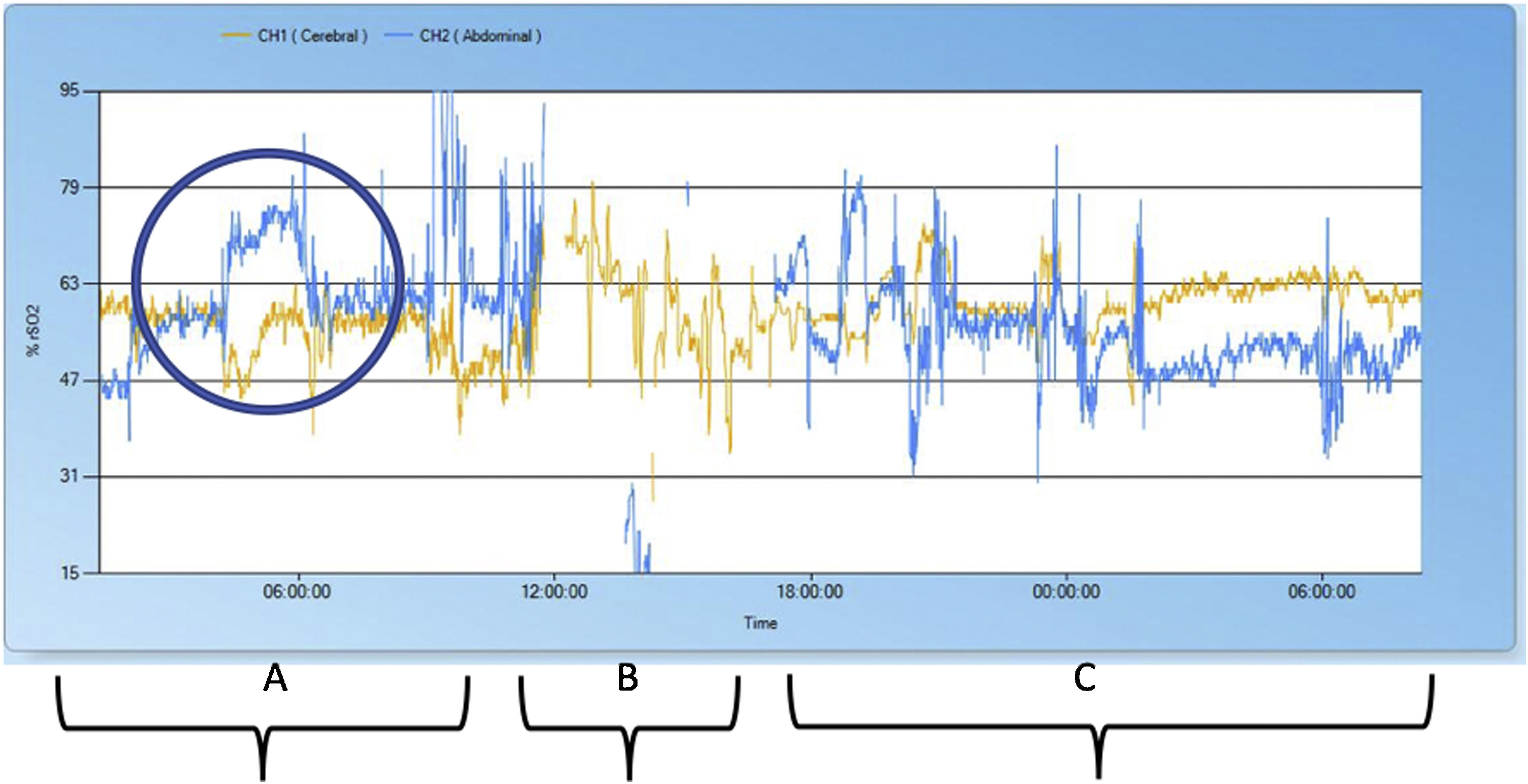
Desde las 24h de vida, las mediciones de NIRS cerebral y esplácnica se habían mantenido estables, sin cambios significativos y dentro del rango normal para la edad (55-65). Repentinamente, al quinto día de vida, el paciente desarrolló hiperglicemia, taquicardia e hipertensión arterial, con aumento de la distensión abdominal. La radiografía urgente reveló la presencia de neumoperitoneo. El registro de la NIRS mostró una caída marcada en la saturación regional cerebral de oxígeno (>25%) acompañado de un aumento significativo en la saturación de oxígeno somática (>25%) (fig. 1) en las 6h previas. La posterior revisión de los registros mostró que ambos eventos habían coincidido temporalmente con el desarrollo de la perforación gastrointestinal, que no se sospechó hasta 6h después en base a los hallazgos clínicos y radiográficos.
Registro de la saturación regional de oxígeno (rSO2). La rSO2 cerebral se muestra en amarillo y la rSO2 abdominal en azul. A) Registro de NIRS 12h antes de la cirugía con aumento significativo de la rSO2 abdominal y disminución de la rSO2 cerebral que coincidieron con el desarrollo de la perforación gástrica. B) Registro de NIRS intraoperatorio (4h). C) Registro de NIRS a las 12h de la laparotomía y reparación quirúrgica de la perforación gástrica.
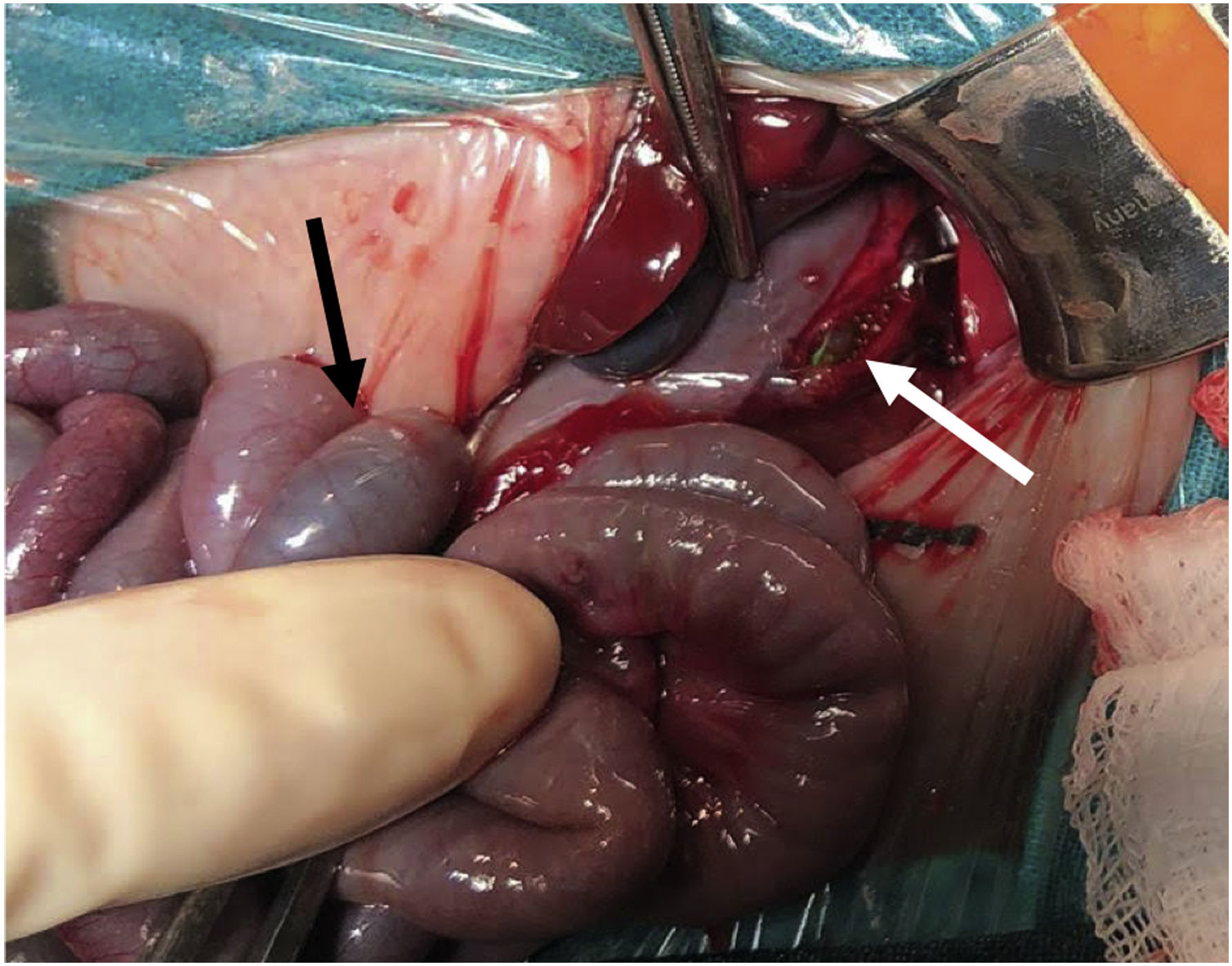
El tratamiento con enemas y N-acetilcisteína fue infructuoso. Se practicó una laparotomía media superior urgente que reveló la presencia de flujo biliar y aire libre en el peritoneo. Los hallazgos quirúrgicos fueron perforación gástrica de 2cm en la curvatura mayor extendiéndose hacia el fundus con cambios necróticos en el tejido circundante. Se realizó reparación quirúrgica del estómago. Asimismo, la exploración abdominal confirmó la obstrucción ileal por tapón de meconio. Se administró infusión de suero salino a través de una enterotomía en el íleo terminal para la extracción manual del meconio impactado. A pesar de la extracción de meconio durante la operación, no se observó mejoría en el tránsito intestinal del paciente, por lo que se realizó una ileostomía a los 29 días de vida.
La perforación gástrica es una urgencia quirúrgica rara en el período neonatal. Nuestro paciente presentó con intolerancia a la nutrición enteral, hiperglicemia y distensión abdominal. A continuación, la radiografía de urgencia detectó la presencia de neumoperitoneo. Estos signos y síntomas son los descritos con mayor frecuencia en la literatura previa4,5. Por último, la cirugía abdominal reveló la presencia de perforación gástrica e íleo meconial.
Sospechamos que la etiología de la perforación gástrica en este paciente fue multifactorial, incluyendo el bajo peso al nacer, la prematuridad, el aumento en la presión intragástrica secundario a la obstrucción meconial y el uso de ventilación mecánica no invasiva. El traumatismo iatrogénico asociado al tubo orogástrico también podría haber contribuido (fig. 2). Cada uno de estos factores involucrados en el desarrollo de la perforación gástrica se ha descrito con anterioridad4.
Entre los hallazgos de la interpretación retrospectiva del registro de NIRS, cabe destacar la elevación de la saturación regional abdominal de oxígeno que se produjo a la vez que la disminución en la saturación regional cerebral de oxígeno, que sospechamos coincidió con el desarrollo de la perforación gástrica. Sin embargo, no hubo cambios en la saturación de oxígeno medida por pulsioximetría, lo que implica un aumento en la extracción de oxígeno cerebral. Los hallazgos ecográficos excluyeron posibles causas alternativas de la caída en la saturación regional cerebral de oxígeno. No se encontró evidencia de actividad ductal o hemorragia intracraneal. Por lo tanto, sospechamos que el aumento en la extracción de oxígeno cerebral se asoció a la presencia de dolor y estrés causados por la perforación gástrica, lo que también explicaría la presencia de hiperglicemia moderada, taquicardia e hipertensión arterial.
Los neonatos extremadamente prematuros constituyen un grupo con riesgo de múltiples complicaciones. No obstante, en muchos casos sus manifestaciones son tardías, y la fragilidad de estos pacientes impone restricciones importantes en la realización de las posibles pruebas de imagen. La NIRS es un método no invasivo para la monitorización continua en tiempo real que ofrece información útil a los clínicos1–3. Lamentablemente, casi todos los estudios sobre la NIRS son retrospectivos y pocos han recogido datos de manera prospectiva1–3. En cualquier caso, la NIRS hace posible la detección precoz de cambios en la saturación de oxígeno tisular en regiones específicas incluso antes de que el daño sea significativo y sus manifestaciones aparentes, lo que permite al clínico realizar intervenciones preventivas o terapéuticas1–3.
La NIRS detecta cambios en la presión de perfusión cerebral y somática, como estados de hipoperfusión que conllevan una disminución de la oxigenación debido a la reducción en el suministro de oxígeno. Los pacientes hemodinámicamente estables también pueden mostrar alteraciones o cambios en la saturación de oxígeno tisular asociadas a un aumento en el consumo (estrés, dolor, sepsis, hipertermia, sedación, crisis convulsivas...), así como cambios en la presión parcial de oxígeno y los niveles de hemoglobina.
El presente estudio es relevante, pues demuestra que unas horas antes del diagnóstico clínico hay cambios significativos en la saturación regional de oxígeno (NIRS). También halló diferencias significativas en la oxigenación asociadas temporalmente a la perforación gástrica, una patología aguda rara, y otras enfermedades gastrointestinales insidiosas más frecuentes, como la ECN. Un estudio centrado en la ECN encontró bajadas en la saturación regional cerebral de oxígeno que se adelantaron varios días al diagnóstico clínico1–3. No obstante, en el caso de perforación gástrica que nos ocupa, los cambios en la saturación regional ocurrieron abruptamente y mostraron un aumento inesperado. Todavía se desconocen las causas de este fenómeno. Otra posible explicación es la diferencia en la fisiopatología de estas dos enfermedades intestinales.
Para optimizar el rendimiento diagnóstico de la NIRS, es necesario que el personal de enfermería notifique cualquier cambio significativo reflejado en la pantalla del monitor. Por lo tanto, la formación continua del personal médico y de enfermería es esencial.
En conclusión, la monitorización continua de la saturación regional abdominal de oxígeno mediante la NIRS ofrece una estrategia novedosa para la detección y tratamiento precoces de la perforación gástrica e intestinal en neonatos.
FinanciaciónA. Solaz-García es un investigador predoctoral en la RETICS financiado por la beca PN 2018-2021, Instituto de Salud Carlos III - Subdirección General de Evaluación y Fomento de la Investigación (España). Beca con referencia RD16/0022 del Fondo Europeo de Desarrollo Regional (FEDER), concedida a M. Vento.
Nuestro agradecimiento, especialmente, a los padres del neonato, quienes consintieron al uso de las imágenes. También a todos los profesionales que atienden a los recién nacidos en la UCIN del Hospital Universitario y Politécnico La Fe de Valencia, España.