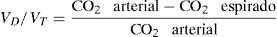El switch arterial es la intervención de elección para la transposición de grandes arterias con o sin comunicación interventricular. El objetivo ha sido la identificación de factores de riesgo de mortalidad hospitalaria.
MétodosSe intervinieron 121 niños entre enero de 1994 y junio de 2008. De ellos, 80 (66%) fueron diagnosticados de transposición con septo íntegro, y 41 (34%) con comunicación interventricular. Se recogieron variables del preoperatorio, de la intervención y del postoperatorio.
ResultadosLa edad fue de 11 [8 – 16] días y el peso de 3,5 [3,0 – 3,7] kg. A 11 niños (9,1%) se les cerró la comunicación interventricular. El 81,8% presentaba un patrón coronario normal. Se hizo cierre diferido del tórax en 38 pacientes (31,4%). La mortalidad hospitalaria fue del 11,6%, reduciéndose en los últimos 5 años al 2,1%. El peso, el patrón coronario anormal, el tiempo de circulación extracorpórea, la tensión arterial media al ingreso, el espacio muerto pulmonar y el cierre diferido del esternón fueron factores de riesgo de mortalidad. El modelo que mejor predice la muerte es el constituido por la tensión arterial media al ingreso y el cierre diferido del esternón.
ConclusionesLa reducción en el tiempo de circulación extracorpórea y en el cierre diferido del esternón han contribuido a reducir la mortalidad. El patrón coronario anormal continúa siendo un factor de riesgo de mortalidad. En los niños con cierre diferido del esternón, una tensión arterial media al ingreso ≥ 47,5 mmHg es un objetivo a conseguir.
The arterial switch is the procedure of choice for transposition of great arteries, with or without ventricular septal defect. The aim of this study was to identify risk factors for hospital mortality.
MethodsThe study included 121 children between January 1994 and June 2008. Of these, 80 (66%) were diagnosed with intact ventricular septum, and 41 (34%) with ventricular septal defect. Variables were collected pre-operatively, during surgery, and postoperatively.
ResultsThe mean age was 11 [8 to 16] days and a mean weight of 3.5 [3.0 to 3.7] kg. A ventricular septal defect was closed in 11 children (9.1%). Atotal of 81.8% had a normal coronary pattern. There was delayed closure of the chest in 38 patients (31.4%). The hospital mortality was 11.6%, decreasing over the past 5 years to 2.1%. The weight, abnormal coronary pattern, time of cardiopulmonary bypass, mean arterial pressure at admission, pulmonary dead space, and delayed closure of the chest, were risk factors of mortality. The model that best predicts the death, consists of the mean arterial pressure at admission, and delayed closure of the chest.
ConclusionsThe reduction in extracorporeal circulation time and the use of delayed closure of the chest, have helped to reduce mortality. The abnormal coronary pattern remains a risk factor for mortality. In children with delayed closure of the chest, a mean arterial pressure at admission ≥ 47.5 mmHg is a goal to achieve.
En la actualidad se considera el switch arterial, según la técnica descrita por Jatene1, el tratamiento quirúrgico de elección de la transposición de las grandes arterias (TGA). La indicación electiva del switch arterial en el periodo neonatal fue realizada por Castañeda2 en el año 1983.
Esta intervención corrige a una posición de normalidad la aorta y la arteria pulmonar, saliendo cada una de ellas de su ventrículo anatómico. La principal dificultad que presenta es la de alcanzar una correcta transferencia de las arterias coronarias. Si no se consigue, existe riesgo de que se produzca una isquemia miocárdica3.
El switch arterial se realiza en nuestro hospital desde el año 19854,5.En España, otros grupos de trabajo han obtenido experiencia y buenos resultados6,7. El impacto de esta técnica sobre la supervivencia a largo plazo no está bien definido, pues se están observando estenosis u oclusiones de las arterias coronarias8,9.
El objetivo del estudio fue la identificación de factores de riesgo de mortalidad hospitalaria, que pudieran estar relacionados con el preoperatorio, con la intervención y con el postoperatorio. La mortalidad hospitalaria se definió como la sucedida inmediatamente tras la intervención, o durante un periodo postoperatorio de 30 días.
Pacientes y métodosPoblaciónSe incluyeron 121 niños en un periodo comprendido entre enero de 1994 y junio de 2008. Se consideraron criterios de exclusión los mayores de 2 meses, los que tenían cirugía paliativa previa y los que presentaban la anomalía de Taussig-Bing.
Se incluyeron los 78 pacientes que fueron objeto del trabajo anterior5, excluyendo 1 paciente que presentaba la anomalía de Taussing-Bing. Aunque el objetivo del estudio fue el mismo, en este se han analizado mayor número de variables.
Dependiendo de que a los pacientes se les cerrara o no la comunicación interventricular (CIV), se dividieron en dos grupos: Grupo 1 (TGA/SI), en el que se incluyeron los que tenían septo íntegro; y Grupo 2 (TGA/CIV), en el que se agruparon a los que se les cerró la CIV.
DiseñoEl estudio ha sido observacional y analítico de una cohorte. Fue aprobado por la comisión de ética e investigación de nuestro hospital, obteniéndose de forma previa a la cirugía consentimiento informado.
Variables analizadasLas variables preoperatorio analizadas fueron: la edad (días) y el peso (kg), y la existencia o no de CIV.
De la intervención se recogieron: el cierre de la CIV (sí/no), la anatomía coronaria, el tiempo de circulación extracorpórea (CEC) (minutos), el tiempo de clampaje aórtico (minutos), la utilización de parada circulatoria (sí/no), el tiempo de parada (minutos) y el cierre diferido del esternón (sí/no).
Las variables postoperatorias fueron: la tensión arterial media (TAM) (mmHg), el shunt intrapulmonar (QSP/QT) (%), la fracción de espacio muerto pulmonar (VD/VT), la diferencia arterio-venosa de la saturación de oxígeno (DSO2) (%), el índice de extracción tisular de oxígeno (ETO2) (%), el tiempo de ventilación mecánica (horas), el tiempo de estancia en Unidad de Cuidados Intensivos Pediátricos (UCIP) (días), y la mortalidad (sí/no).
En esta intervención es necesario mantener la TAM en cifras normales, para obtener así una adecuada presión de perfusión coronaria10.
El QSP/QT indica la fracción del volumen minuto cardiaco que no realiza intercambio gaseoso. Valores superiores al 10% son patológicos. Se calcula mediante la siguiente fórmula:
El VD/VT estima el flujo pulmonar definiendo zonas del pulmón bien ventiladas pero mal perfundidas. Valores superiores a 0,3 indican una reducción del flujo pulmonar debido a bajo gasto11. Es calculado mediante la ecuación de Bohr12.
Donde CO2=dióxido de carbono.
La DSO2 y el ETO2 son parámetros que informan de la adecuación del aporte de oxígeno a los tejidos con relación a sus necesidades. La DSO2 se obtiene restando la SvO2 a la SaO2, y la ETO2 se calcula mediante la siguiente fórmula:
El valor normal de la DSO2 es del 30% y el de la ETO2 de un 25%. En situaciones de bajo flujo sistémico, los tejidos extraen más oxígeno, produciéndose un descenso en la saturación venosa que hace aumentar la DSO213 y la ETO214.
Anatomía coronariaLa anatomía coronaria se clasificó según los patrones descritos por Mayer15, como ya lo hicimos en estudios anteriores4,5.
Debido a la escasa frecuencia de determinados patrones coronarios, se reagruparon los pacientes en dos grupos. El grupo con patrón normal lo forman, el patrón usual (patrón 1), y el patrón de la circunfleja procedente de la coronaria derecha (patrón 2). En el grupo con patrón anormal, se incluyeron los patrones: seno coronario único (patrones 3 y 4), coronarias invertidas (patrones 5 y 6), coronarias intramurales (patrones 7 y 8), y otros patrones no descritos (patrón 9).
Intervención quirúrgicaLa técnica empleada fue la descrita por Jatene con la maniobra de Lecompte. Antes de finalizar la CEC, se realizó ultrafiltración para reducir la intensidad del síndrome de fuga capilar. Cuando esta medida es insuficiente, y el edema es importante con inestabilidad hemodinámica, se optó por el cierre diferido del esternón.
La anatomía coronaria fue determinada por el cirujano mediante visualización directa. Una vez hecha la corrección, y tras desclampar la aorta, este debe comprobar la perfusión miocárdica. Si no es adecuada, debe sospechar un problema en la anastomosis de las coronarias o en su estructura anatómica, y en la medida de lo posible resolverlo.
Recogida de datosPara calcular las variables gasométricas (QSP/QT, VD/VT, DSO2, ETO2), se hicieron gasometrías arteriales y venosas en dos momentos del postoperatorio. En el tiempo 1: al ingreso en UCIP; en él se refleja el estado clínico al finalizar la intervención. En el tiempo 2: a las 8:00 horas del día siguiente; informa del adecuado manejo clínico en las primeras horas del postoperatorio. En el instante de extraer las gasometrías, se anotó el CO2 espirado y la cifra de TAM. Las variables recogidas en el tiempo 1, se identifican con el número 1, y las recogidas en el tiempo 2, con el número 2.
Análisis estadísticoSe realizó estadística descriptiva, para ello se utilizaron frecuencias absolutas y relativas, en el caso de las variables cualitativas. Las variables cuantitativas, al no seguir una distribución normal (test de Kolmogorov-Smirnov o Shapiro-Wilk [n<50]), se expresaron mediante P50 (P25 - P75) (mediana, rango intercuartílico).
Se realizó una comparación de los grupos mediante test de χ2 de Pearson, o el test exacto de Fisher, cuando fue necesario para las variables cualitativas. La comparación de las variables cuantitativas se efectuó mediante la U de Mann-Whitney. Para analizar las variables relacionadas o apareadas se utilizó el test de Wilcoxon.
Se emleó un modelo de regresión logística bivariante para analizar los factores de riesgo (odds ratio) asociados a la muerte, indicando un 95% de intervalo de confianza (IC). Con los factores de riesgo identificados como estadísticamente significativos, se realizó una regresión logística multivariable para crear un modelo predictivo de mortalidad. Para indicar la capacidad predictiva del modelo se llevó a cabo una curva COR, obteniendo el área bajo la curva y su intervalo de confianza (IC) al 95%.
El nivel de significación estadística se estableció en p<0,05. La imputación de los datos se realizó en Access. El análisis estadístico se hizo con el paquete Stadistical Package for Social Sciences (SPSS Inc., Chicago, IL, EE.UU.) versión 16.0, de la Unidad de Apoyo a la Investigación.
ResultadosDescripción de la poblaciónLa edad a la intervención fue de 11 (8 – 16) días y el peso de 3,5 (3,0 – 3,7) kg.
Técnica quirúrgicaDe los 121 niños, 80 (66%) fueron diagnosticados de TGA con septo íntegro, y 41 (34%) de TGA con CIV, de ellos sólo a 11 niños (9,1%) se les cerró ésta.
La mediana del tiempo de CEC fue de 215 (192 – 240 minutos), la del tiempo de clampaje aórtico de 120 (105 – 132 minutos) y la del tiempo de parada circulatoria de 8,5 (7 – 10,7 minutos). Encontramos diferencias significativas en el tiempo de CEC entre los primeros 5 años (1994-1998), con respecto a los últimos 5 (2003-2007) (232 [208 – 260] min vs 203 [179 – 220] min; p<0,001).
En el estudio estadístico realizado entre los grupos 1 y 2, sólo la edad mostró diferencias significativas, siendo mayor en el grupo 2 (tabla 1).
Comparación de los grupos 1 y 2 (sin cierre y con cierre de CIV)
| Variables | Grupo 1 (d-TGA/SÍ) | Grupo 2 (d-TGA/CIV) | Valor de p |
| (n=110) (rango) | (n=11) (rango) | ||
| Edad (días) | 11 (7 - 15) | 25 (13 - 30) | 0,001 |
| (n=110) | (n=11) | ||
| Peso (kg) | 3,5 (3 - 3,7) | 3,5 (3,2 - 3,7) | 0,526 |
| (n=110) | (n=11) | ||
| Tiempo CEC (minutos) | 213 (188 - 235) | 236 (215 - 252) | 0,055 |
| (n=110) | (n=10) | ||
| Tiempo CA (minutos) | 120 (105 - 132) | 131 (114 - 137) | 0,233 |
| (n=110) | (n=10) | ||
| Tiempo de ventilación mecánica (horas) | 120 (94 - 168) | 144 (96 - 168) | 0,516 |
| (n=110) | (n=11) | ||
| Tiempo de estancia en UCIP (días) | 8 (7 - 14) | 8 (7 - 11) | 0,971 |
| (n=110) | (n=11) | ||
| Mortalidad | 14 - 12%) | 0 (0%) | 0,359 |
| (n=110) | (n=11) |
CA: clampaje aórtico; CEC: circulación extracorpórea; PC; parada circulatoria; UCIP: Unidad de Cuidados Intensivos Pediátricos.
En el 96% (116/121) de los niños ha sido posible recoger información sobre el cierre diferido del tórax, realizado en quirófano en 38 pacientes (31,4%). Esta técnica fue muy utilizada en los primeros 5 años, llegando a reducirse de forma importante en los últimos 5 (87,5% [21/24] vs 2,1% [1/47]; p<0,001).
La mortalidad fue mayor en los que se les difirió el cierre del tórax, en comparación a los que llegaron con el tórax cerrado (9/38 [23.7%] vs 2/78 [2.5%]; p=0,001). En los primeros, los tiempos de ventilación mecánica, de estancia en UCI y de CEC, fueron más prolongados con relación a los segundos (tabla 2).
Análisis del tiempo de CEC, ventilación mecánica y estancia en UCIP con respecto al cierre diferido de tórax
| Variables | Cierre diferido tórax | Valor de p | |
| Sí | No | ||
| (n=38) | (n=78) | ||
| P50 (P25 - P75) | P50 (P25 - P75) | ||
| Tiempo CEC | 224 (199 – 250) | 210 (185 – 232) | 0,034* |
| n=38 | n=77 | ||
| Horas ventilación mecánica | 132 (72 – 198) | 120 (96 – 168) | 0,731 |
| n=38 | n=78 | ||
| Días de estancia en UCIP | 10 (7 – 15,2) | 8 (7 – 14) | 0,289 |
| n=38 | n=78 | ||
La distribución de los pacientes en grupos queda reflejada en la tabla 3 y la mortalidad en la tabla 4. La mayoría de los pacientes presentaron un patrón normal (99/121; 81,8% vs 22/121; 18,2%). En el grupo con patrón anormal, las variantes anatómicas más frecuentes fueron la arteria coronaria única y la coronaria intramural (12/22; 54,5%) (tabla 3).
Análisis de la anatomía coronaria
| Patrón coronario normal | (n=99) |
| Usual (patrón 1) | 64 |
| Circunfleja de la coronaria derecha (patrón 2) | 35 |
| Patrón coronario anormal | (n=22) |
| Única (patrones 3 y 4) | 7 |
| Invertidas (patrón 5) | 2 |
| Circunfleja y coronaria derecha invertidas (patrón 6) | 4 |
| Intramural (patrones 7 y 8) | 5 |
| Otros (patrón 9) | 4 |
Análisis de la anatomía coronaria con respecto a la mortalidad
| Patrón coronario normal (n=99) | Supervivientes (n=91) | Fallecidos (n=8) |
| Usual (patrón 1) | 59 | 5 |
| Circunfleja de la coronaria derecha (patrón 2) | 32 | 3 |
| Patrón coronario anormal (n=22) | Supervivientes (n=16) | Fallecidos (n=6) |
| Única (patrones 3 y 4) | 4 | 3 |
| Invertidas (patrón 5) | 2 | 0 |
| Circunfleja y coronaria derecha invertidas (patrón 6) | 3 | 1 |
| Intramural (patrones 7 y 8) | 3 | 2 |
| Otros (patrón 9) | 4 | 0 |
La mortalidad del patrón normal fue mucho menor que la del patrón anormal [8,1% (8/99) vs. 27,3% (6/22); p=0,021]. En este último grupo, la mayor mortalidad se produjo en los niños con arteria coronaria única y con coronaria intramural (tabla 4).
Evolución en UCIPLa mediana del tiempo de ventilación mecánica fue de 120 (96-168) horas y la del tiempo de estancia en UCIP de 8 (7-14) días. La mortalidad precoz hospitalaria fue del 11,6% (14/121), reduciéndose en los últimos 5 años al 2,1%.
El fallecimiento ocurrió en quirófano en 3 casos, en 2 por problemas en la anastomosis de las coronarias. En 6 casos sucedió en las primeras 12 horas del postoperatorio por disfunción miocárdica severa. En 5 casos se produjo en los días siguientes, en 3 debido a una sepsis, y en 2 por fallo hemodinámico.
Factores predictivos de mortalidadLa comparación entre los grupos de supervivientes y fallecidos demostró que el peso, el tiempo de CEC, la TAM 1, la VD/VT 1, y la VD/VT 2, presentaron diferencias significativas (tabla 5).
Comparación de los grupos de supervivientes y fallecidos
| Variables | Fallecidos | Supervivientes | Valor de p |
| (n=14) | (n=107) | ||
| P50 (P25 - P75) | P50 (P25 - P75) | ||
| Edad (días) | 9,5 (7 - 15) | 12 (8 - 17) | 0,201 |
| n=14 | n=107 | ||
| Peso (kilogramos) | 3,12 (2,75 - 3,5) | 3,5 (3,1 - 3,7) | 0,021 |
| n=14 | n=107 | ||
| Tiempo CEC (minutos) | 260 (213 - 317) | 213 (189 - 235) | 0,005 |
| n=14 | n=106 | ||
| Tiempo CA (minutos) | 126 (106 - 148) | 119 (105 - 132) | 0,229 |
| n=14 | n=106 | ||
| TAM 1 (mm Hg) | 45 (40 - 57) | 59 (52 - 82) | 0,002 |
| n=11 | n=106 | ||
| QSP/QT 1 (%) | 7 (2 - 13) | 3 (2 - 9) | 0,309 |
| n=7 | n=103 | ||
| ETO2 1 (%) | 52 (43 - 75) | 46 (35 - 58) | 0,211 |
| n=7 | n=103 | ||
| VD/VT 1 | 0,510 (0,415-0,600) | 0,320 (0,202-0,430) | 0,009 |
| n=5 | n=100 | ||
| DSO2 1 (%) | 49 (42 - 71) | 46 (34 - 56) | 0,235 |
| n=7 | n=103 | ||
| TAM 2 (mm Hg) | 55 (37 - 60) | 53 (48 - 59) | 0,864 |
| n=5 | n=106 | ||
| QSP/QT 2 (%) | 3 (1 - 12) | 5 (3 - 10) | 0,332 |
| n=5 | n=98 | ||
| ETO2 2 (%) | 27 (18,5 - 40,5) | 29 (25 - 40) | 0,591 |
| n=5 | n=98 | ||
| VD/VT 2 | 0,405 (0,300-0,435) | 0,220 (0,160-0,305) | 0,013 |
| n=4 | n=97 | ||
| DSO2 2 (%) | 25 (21 - 41) | 28 (25 - 39,5) | 0,550 |
| n=5 | n=97 |
CA: clampaje aórtico; CEC: circulación extracorpórea; DSO2: diferencia arteriovenosa saturación de oxígeno; ETO2: extracción tisular de oxígeno; PC: parada circulatoria; QSP/QT: shunt intrapulmonar; TAM: tensión arterial media:VD/VT: fracción espacio muerto pulmonar.
1: tiempo 1; al ingreso UCIP. 2: tiempo 2; a las 8 horas del día siguiente.
Sobre aquellas variables significativas, se realizó un análisis bivariante, demostrando que el peso, el patrón coronario anormal, el tiempo de CEC, la TAM 1, la VD/VT 1, la VD/VT 2, y el cierre diferido del tórax, fueron factores de riesgo de mortalidad (tabla 6).
Análisis bivariante. Factores de riesgo asociados a la mortalidad
| Variables | Odds ratio | Intervalo de confianza 95% | Valor de p |
| Peso (n=14/121) | 0,217 | 0,062 – 0,765 | 0,017 |
| Patrón coronarias anormal (n=14/121) | 4,266 | 1,305 – 13, 943 | 0,016 |
| Tiempo CEC (n=14/120) | 1,016 | 1,006 – 1,025 | 0,001 |
| TAM 1 (n=11/117) | 0,898 | 0,838 – 0,962 | 0,002 |
| VD/VT 1 (n=5/105) | 684,471 | 2,472 – 189487,506 | 0,023 |
| VD/VT 2 (n=4/101) | 2062575,506 | 51,440 – 8,270X10 | 0,007 |
| Cierre diferido tórax (n=11/116) | 11,793 | 2,403 – 57,875 | 0,002 |
CEC: circulación extracorpórea; n: fallecidos/total; TAM: tensión arterial media;VD/VT: fracción espacio muerto pulmonar.
1: tiempo 1; al ingreso UCIP. 2: tiempo 2; a las 8 horas del día siguiente.
Se elaboró posteriormente un análisis multivariante, llegándose a la conclusión de que la TAM 1 y el cierre diferido de tórax, fueron los factores de riesgo que mejor predicen la muerte. El método utilizado es el de pasos hacia delante (n=114), obteniéndose una variabilidad explicada del 35% (R2 de Nagelkerke) (tabla 7).
Para poder determinar su poder discriminativo, calculamos la curva ROC, obteniendo un área bajo la curva de 0,853, con un intervalo de confianza al 95% de 0,728 – 0,973.
Se seleccionaron posteriormente los pacientes con cierre diferido de tórax y calculamos la curva ROC de supervivencia respecto a los valores de TAM 1 que presentaban. El área bajo la curva fue de 0,753 con un intervalo de confianza del 95% de 0,520 – 0,986. En ella comprobamos que un valor de TAM 1 ≥ 47,5, posee una sensibilidad del 93%, y una especificidad del 67% para discriminar la supervivencia.
DiscusiónEn el switch arterial, un tiempo de CEC mayor de 150 minutos es considerado un factor de riesgo independiente de mortalidad16,17. En nuestra serie también se nos mostró como un factor de riesgo (tabla 6). El tiempo de clampaje aórtico no se asoció con la mortalidad, como otros autores han expuesto17. La mayor morbilidad y mortalidad producida con los tiempos prolongados de CEC se debe a la afectación que esta técnica produce en múltiples órganos18.
Con respecto al cierre o no de la CIV, hemos de destacar que la mortalidad del grupo 2 (d-TGA/CIV) fue del 0% (tabla 1). Este resultado difiere de lo publicado por la mayoría de los autores, los cuales han obtenido una mayor mortalidad16,17,19. Otros autores20, y coincidiendo con nuestros resultados, han publicado una mortalidad similar en ambos grupos.
La edad a la intervención fue la única variable que demostró diferencias significativas entre los grupos 1 y 2 (tabla 1). La mayor edad con la que se intervienen los niños del grupo 2 fue a nuestro criterio uno de los factores que podría haber influido en los resultados. Los autores que publican una mayor mortalidad19 consideran que puede ser debida a una mayor complejidad de la técnica quirúrgica, así como al posible desarrollo de una enfermedad vascular pulmonar21.
ConEn relación a la anatomía coronaria, el alto porcentaje de niños con patrón coronario normal (99/121; 81,8%), ha influido en los buenos resultados obtenidos, ya que la presencia de un patrón coronario anormal incrementa el riesgo de muerte 17,16,19. El análisis realizado en nuestra anterior publicación demostró, que el factor que más influyó en la mortalidad fue la anatomía coronaria5, sobre todo en el grupo constituido por la arteria coronaria única e intramural. En este estudio, la presencia de un patrón coronario anormal, también ha sido un factor de riesgo de mortalidad (tabla 6). Otros autores, en cambio, no han considerado que la presencia de un patrón anormal haya sido un factor de riesgo16.
La alta mortalidad obtenida en el patrón anormal es debida a que, en esta serie, las variantes anatómicas más frecuentes fueron la arteria coronaria única (7/22; 31,8%), la arteria coronaria intramural (5/22; 22,7%), y la arteria coronaria derecha y circunfleja invertidas (4/22; 18.2%), que fueron las que presentaron mayor mortalidad (tabla 4), como también ha sido publicado anteriormente22,23.
En la actualidad, las variantes anatómicas más desfavorables, no deberían asociarse a una mayor mortalidad16,24, pero sí pueden producir mayor morbilidad, al requerir para su corrección mayor tiempo de CEC, más reintervenciones, y mayor porcentaje de cierre diferido de tórax16.
El cierre diferido de tórax también ha sido un factor de riesgo de mortalidad (tabla 6), resultado que apoya lo publicado anteriormente17,19. El descenso producido en su utilización en los últimos 5 años ha sido muy significativo (87,5% (21/24) vs 2,1% (1/47); p<0,001), encontrándonos actualmente en un nivel muy bajo en relación a otras series, en las que oscila entre el 2.9%25 y el 25%,16,20. Esta baja incidencia puede estar relacionada con la disminución conseguida en el tiempo de CEC, pues este tiempo se prolonga cuando se hace cierre diferido (tabla 2).
Respecto al análisis de VD/VT en los tiempos 1 y 2, las cifras significativamente más elevadas que presentaron los fallecidos ha sido expresión de una disminución del flujo pulmonar por un bajo gasto. La identificación como factor de riesgo de mortalidad no ha sido posible, debido a que el número de fallecidos a los que se les ha podido determinar ha sido muy reducido (tabla 6).
El tiempo medio de ventilación mecánica fue de 120 horas, cifra elevada en relación con lo publicado anteriormente19. Este aumento en el tiempo de ventilación mecánica es la causa de un aumento de la estancia en UCIP (8 días), cifra algo elevada en relación a la obtenida por otros autores (5 a 6 días)16,17,19.
La isquemia miocárdica, provocada por acodamientos, rotaciones, y estiramientos de las arterias coronarias24, es la principal causa de mortalidad precoz hospitalaria3,20,22. La alteraciones en la anatomía coronaria producidas en la intervención, puede ser el origen de la isquemia miocárdica, sobre todo en niños con un patrón coronario anormal. Esta isquemia suele manifestarse por arritmias26, bajo gasto, fallo circulatorio y dificultad en la salida de CEC.
El haber identificado la TAM 1 como factor de riesgo de mortalidad nos induce a pensar que en estos pacientes es necesario conseguir en el postoperatorio unas cifras normales de TAM, para asegurar una adecuada perfusión coronaria. Esto objetivo es más deseable en los niños con cierre diferido del esternón, que son los que mayor incidencia presentan de patrones coronarios anormales, en los que el flujo coronario puede comprometerse.
En la actualidad, la mortalidad de nuestra serie es del 2,1%, comparable a la obtenida en los mejores hospitales, en los que oscila entre 0,85% y el 6%17,25. De los 14 niños que fallecieron, 3 lo hicieron en quirófano por problemas en las coronarias, y 6 en las primeras 12 horas del postoperatorio, debido a disfunción miocárdica severa. Como sucede en otros centros17,19, estos pacientes pueden ser sometidos a soporte vital extracorpóreo (ECMO), para intentar recuperar el miocardio y mejorar la supervivencia.
En relación con el seguimiento a largo plazo, un estudio reciente27 ha demostrado que, tras un periodo de 20 años, la mayoría de los pacientes presentan una adecuada función del ventrículo izquierdo y de la válvula aórtica.
Por último, podemos concluir diciendo que la reducción en el tiempo de CEC, así como en la frecuencia de cierre diferido de tórax, han contribuido a mejorar nuestros resultados. El patrón coronario anormal continúa siendo un factor de riesgo de mortalidad. Debemos intentar conseguir en los niños con cierre diferido de tórax, una TAM al ingreso ≥ 47,5 mmHg para asegurar así una adecuada perfusión coronaria.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
AgradecimientosAl Dr. Gil-Fournier por haber sido el impulsor de la cirugía de las cardiopatías congénitas en nuestro hospital.