La encefalomielitis aguda diseminada (EMAD) es una enfermedad pediátrica infrecuente de etiología autoinmunitaria. El objetivo del presente estudio es estimar la incidencia en nuestro medio durante los últimos 10 años, analizar la forma de presentación clínica, analítica y radiológica. Estudiar la respuesta al tratamiento y su evolución.
Pacientes y métodosAnálisis retrospectivo de casos con diagnostico de EMAD según criterios actuales. De cada uno de los pacientes diagnosticados, se recogieron la edad y el mes del año al inicio de la enfermedad, el sexo, los antecedentes familiares de desmielinización, los síntomas iniciales, las enfermedades o las vacunaciones previas, las características del LCR, los estudios serológicos, la PCR frente a virus del grupo herpes en sangre y LCR, las bandas oligoclonales en LCR y EEG, las características de la neuroimagen por RMI de cráneo y/o médula, la modalidad de tratamiento seguido y la respuesta a este.
ResultadosSe encontró a 16 pacientes con una edad media de 5,6 años, con un relación varón/mujer de 11/5, con debut predominante en meses fríos del año, clínica con predominio de alteración de la marcha y de la consciencia, y convulsiones. Radiología por MRI: predominio de lesiones múltiples en la sustancia blanca profunda, en el mismo estadio visibles en T2. También en la sustancia gris profunda. Analítica sanguínea: sin elevación de reactantes y LCR normal en la mitad de los casos. La etiología se vislumbró en 7 casos.
ConclusionesLa incidencia anual en menores de 14 años se estimó en 0,64/100.000. La clínica y la radiología fueron la base del diagnóstico. El herpes virus humano 6 estuvo implicado en 4 casos. La mayoría de los pacientes se recuperó por completo.
Acute disseminated encephalomyelitis (ADEM) is a rare paediatric disease of autoimmune origin. The aim of this study is to estimate its impact in our area over the past 10 years and to analyse the clinical, laboratory and radiological presentation, as well as study the response to treatment and outcome.
Patients and methodsA retrospective analysis of cases diagnosed with current ADEM criteria. The age and month of the year at onset, sex, family history of demyelination, initial symptoms, disease or previous vaccination, CSF features, serology, PCR for herpes virus group in blood and CSF, oligoclonal bands in CSF, EEG and neuroimaging features of the skull by MRI, the type of treatment received and the response were recorded on each of the patients diagnosed.
ResultsThere were 16 patients, with a mean age of 5.6 years. Male/female: 11/5, with a dominant debut in the colder months of the year, predominantly gait disorder, changes in consciousness and seizures. The radiology by MRI showed a predominance of multiple lesions in the same T2 stage, in deep white matter and lesions in deep grey matter. There were no in blood parameters and the CSF was normal in half of the cases. The origin was determined in 7 cases.
ConclusionsThe annual incidence in children under 14 years was estimated at 0.64/100,000. The clinical and radiological findings were the basis of diagnosis. The human herpes virus 6 was involved in 4 cases. Most patients recovered completely.
La encefalomielitis aguda diseminada (EMAD) es una enfermedad generalmente monofásica, de predominio en niños prepúberes tras una enfermedad febril previa o una inmunización. Se considera una entidad inmunomediada con desmielinización aguda del SNC, pero con afectación de ganglios de la base y sustancia gris cortical1,2. Casi siempre conlleva un acentuado cuadro constitucional asociado a síntomas neurológicos de inicio abrupto y encefalopatía con afectación cortical. Su diagnóstico se basa en la clínica y en la neuroimagen, ya que carece de marcador biológico identificable.
Se relaciona etiológicamente con otras patologías inflamatorias inmunitarias, como el síndrome de Guillain-Barre, la encefalitis de Bikerstaff y la mielitis trasversa, con la que se puede asociar. Su diagnóstico diferencial plantea dificultades con la esclerosis múltiple (EM), que puede debutar de forma parecida pero con un curso recidivante polifásico. La EMAD tiene una forma recurrente de muy rara frecuencia. La neuromielitis óptica parece tener un marcador específico3,4 (NMO-IgG, o anti-acuaporinas). Está en discusión si anticuerpos contra la glucoproteína de la mielina del oligodendrocito (anti-MOG) son un indicador fiable de la EMAD5,6. Su frecuencia en menores de 18 años se estima entre 0,4 y 0,9/100.000/año7,8, por lo que la publicación de grandes series es infrecuente. La mayoría de los casos se agrupan en los meses fríos de año, lo que sugiere una influencia viral. Se admite que puede desarrollarse en relación con la infección previa por virus del grupo herpes y Mycoplasma, aunque la mayoría de los casos no presentan un agente etiológico identificable. En la actualidad, se están desarrollando estudios para buscar determinantes genómicos o epidemiológicos en relación con otros procesos, como EM. Se ha identificado cierta susceptibilidad genómica en relación con el DRB1-15, que no se identifica en otros fenómenos desmielinizantes como la EMAD9.
El conocimiento creciente sobre la patogenia de enfermedades inmunomediadas del SNC ha permitido relacionar los anticuerpos contra la acuaporinas (anti-AQP4) con la neuromielitis óptica4, contra el receptor del GABA en el síndrome del hombre rígido10, contra el receptor del NMDA en la encefalitis límbica11 y recientemente contra la glucoproteína de la mielina del oligodendrocito en la EMAD5,6.
Presentamos un estudio retrospectivo de casos de EMAD diagnosticados en un hospital de tercera referencia a lo largo de los 10 últimos años, en los que se ha seguido una sistemática de estudio, tratamiento y seguimiento homogénea. Describimos nuestra experiencia en esta enfermedad infrecuente, resaltando su forma de presentación, su estudio etiológico y su tratamiento, así como la evolución mostrada.
Pacientes y métodosSe revisaron las historias clínicas de pacientes ingresados en nuestro hospital en los últimos 10 años, que cumplieran con criterios para el diagnóstico de EMAD según las indicaciones del grupo internacional pediátrico para las enfermedades con desmielinización aguda12, considerando la siguiente forma de presentación: encefalopatía aguda y/o síntomas neurológicos multifocales, LCR sin evidencia de meningoencefalitis y neuroimagen por RMI compatible. En la RMI se contemplaron imágenes sugerentes de EMAD en caso de lesiones desmielinizantes en un mismo estadio, grandes y/o múltiples y/o asimétricas. Por lo general, se presenta con afectación de la unión corteza gris-blanca de ambos hemisferios cerebrales, cerebelo, tronco cerebral y médula espinal, y asimismo de la sustancia gris del tálamo y los ganglios basales de forma simétrica, con menor asentamiento en la sustancia blanca periventricular.
La aplicación de estos nuevos criterios propuestos en 2007 no alteró el diagnóstico previo en ninguno de nuestros pacientes, ya que no difieren de los empleados hasta ahora por nuestro grupo de trabajo.
De cada uno de los pacientes diagnosticados se recogieron la edad y el mes del año al inicio de la enfermedad, el sexo, los antecedentes familiares de desmielinización, los síntomas iniciales, las enfermedades o las vacunaciones previas y el intervalo hasta el debut de los síntomas, la estancia, las características del LCR, los estudios serológicos, la PCR frente al virus grupo herpes en sangre y el LCR, las serologías, las bandas oligoclonales en el LCR (incluidas a partir de 2005), el EEG y las características de la neuroimagen por RMI de cráneo y/o médula. Asimismo se investigó la modalidad de tratamiento seguido y la respuesta a este.
ResultadosResultados epidemiológicos generalesEntre enero de 2001 y diciembre de 2010 ingresaron 16 pacientes con criterios clínico-radiológicos de EMAD. En la tabla 1 se presenta un resumen con los datos epidemiológicos más relevantes.
Datos epidemiológicos de los pacientes con EMAD
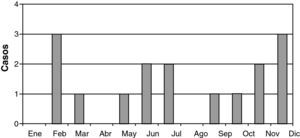
Considerando la población pediátrica bajo la atención de nuestro hospital, de referencia terciaria, con una cifra de alrededor de 255.000 niños menores de 14 años, estimamos una prevalencia aproximada de 0,63 casos de EMAD/100.000 niños/año, en consonancia con lo previamente publicado. Seis de los pacientes procedían de otros países. La edad media de presentación fue de 5,6 años (rango 6 meses a 13 años). La proporción de sexo masculino-femenino fue de 2,2:1 (11 de 16). En función del género, la edad de presentación fue más precoz en el sexo masculino (varones 5,1 años frente a mujeres 6,8 años). Trece pacientes desarrollaron la encefalomielitis antes de los 10 años de edad. No se encontraron antecedentes familiares de enfermedades neurológicas en ninguno de los casos. Diez de los casos se presentaron entre octubre y marzo (fig. 1). Durante el mes previo al inicio de la sintomatología neurológica, 12 pacientes presentaron antecedentes de enfermedades infecciosas; infecciones virales de vías respiratorias (4 pacientes), otitis media aguda (2 pacientes) gastroenteritis aguda (1 paciente), varicela (1 paciente) y enfermedad febril inespecífica (4 pacientes). Los microorganismos patógenos causantes de la enfermedad se identificaron en 7 pacientes: citomegalovirus (CMV) (1 paciente), virus varicela zóster (1 paciente), virus herpes humano 6 (HHV6) en 4 pacientes y vacunación con polio oral a los 2 y 4 meses de vida en otro. Además un caso presentó también una otitis media aguda por Pseudomonas aureginosa. En otros 3 pacientes no existía ningún antecedente previo de vacunación o enfermedad febril. El periodo medio de latencia entre el inicio de la clínica neurológica y los antecedentes de procesos infecciosos o vacunación previa fue de 9,1 días (rango de 2-30 días).
Resultados clínicosLos síntomas sistémicos que precedieron a los neurológicos incluyeron fiebre en 7 pacientes (43,8%), cefalea en 6 pacientes (37,5%) y vómitos en 4 pacientes (25%) (tabla 2). Entre los síntomas neurológicos se incluyeron la alteración del nivel de consciencia en 8 pacientes (50%), las convulsiones en 7 pacientes (43,8%), la pérdida de fuerza (paraparesia, hemiparesia y tetraparesia) en 6 pacientes (37,5%), la ataxia en 4 pacientes (25%), la alteración visual en 5 pacientes (31,2%) y la retención urinaria en 2 pacientes (12,5%). En 3 pacientes (18,8%) se evidenciaron signos piramidales. Se observó meningismo en 2 pacientes (12,5%). La afectación de los pares craneales incluyó oftalmoplejía, disartria y disfagia en 3 pacientes (18,8%). Presentaron síntomas cerebelosos 4 pacientes (25%).
Hallazgos clínicos, radiológicos y resumen del tratamiento administrado
| Total | Infección asociada | Vacuna asociada | Idiopática | |
| N=16 (%) | N=12 (%) | N=1 (%) | N=3 (%) | |
| Hallazgos clínicos | ||||
| Síntomas sistémicos | ||||
| Fiebre | 7 (44) | 5 (42) | 0 (0) | 2 (67) |
| Cefalea | 6 (38) | 4 (33) | 0 (0) | 2 (67) |
| Vómitos | 4 (25) | 2 (17) | 0 (0) | 2 (67) |
| Síntomas neurológicos | ||||
| Alteración marcha | 10 (63) | 10 (84) | 0 (0) | 0 (0) |
| Alteración consciencia | 8 (50) | 6 (50) | 0 (0) | 2 (67) |
| Crisis | 7 (44) | 5 (42) | 0 (0) | 2 (67) |
| Pérdida visual | 5 (31) | 4 (33) | 0 (0) | 1 (33) |
| Retención urinaria | 2 (13) | 2 (17) | 0 (0) | 0 (0) |
| Alteración de pares craneales | 3 (19) | 2 (17) | 1 (100) | 1 (33) |
| Síntomas cerebelosos | 4 (25) | 4 (33) | 0 (0) | 0 (0) |
| Pérdida de fuerza | 6 (38) | 6 (50) | 1 (100) | 0 (0) |
| Hallazgos RM | ||||
| Más de tres lesiones | 15 (94) | 11 (92) | 1 (100) | 3 (100) |
| Lesión cerebral | 16 (100) | 12 (100) | 1 (100) | 3 (100) |
| Sólo cerebral | 9 (56) | 8 (67) | 0 (0) | 1 (33) |
| Sustancia blanca periventricular | 3 (19) | 1 (8) | 0 (0) | 2 (67) |
| Sustancia blanca subcortical | 14 (88) | 12 (100) | 1 (100) | 1 (33) |
| Ganglios basales | 4 (25) | 3 (25) | 0 (0) | 1 (33) |
| Tálamo | 2 (13) | 1 (8) | 0 (0) | 1 (33) |
| Lesión troncoencéfalo | 3 (19) | 1 (8) | 1 (100) | 1 (33) |
| Lesión cerebelo | 4 (25) | 2 (17) | 1 (100) | 1 (33) |
| Lesión en médula espinal | 5 (31) | 5 (42) | 0 (0) | 0 (0) |
| Tratamiento | ||||
| Terapia esteroidea | 5 | 6 | 0 | 0 |
| Inmunoglobulinas iv sólo | 3 | 3 | 0 | 0 |
| Inmunoglobulinas iv+esteroides | 4 | 2 | 1 | 1 |
| Ningún tratamiento | 4 | 2 | 0 | 2 |
En 10 pacientes se realizó un EEG de vigilia en fase aguda. Todos mostraban lentificación global de la actividad bioeléctrica cerebral. En 3 de ellos focalidad irritativa de puntas en regiones temporales y en otros 3 se registró focalidad de ondas lentas de predominio témporo-occipital. Esta focalidad se correlacionó con la presencia de crisis parciales complejas con generalización secundaria en 3 pacientes. Uno de los casos mostraba los tres hallazgos, esto es, lentificación global del trazado con focalidad temporal de ondas lentas y paroxismos de ondas agudas. Clínicamente, mostraba crisis parciales secundariamente generalizadas.
Resultados analíticosLa primera analítica sanguínea mostraba leucocitosis (> 10.000/μl) en 12 pacientes (75%) (media de 20.943/μl, rango 9.100-54.770/μl) y cifra de la proteína C reactiva<7mg/dl en 10 pacientes de los 11 casos que tienen realizado el análisis. La citoquímica inicial del LCR mostraba una media de 31,8 células/μl, rango 1-121/μl con pleocitosis (> 5 células/μl) en 8 pacientes y proteinorraquia (> 40mg/dl) en 7 pacientes (43,8%) (media 51,2mg/dl, rango 24-104mg/dl). Las BOC resultaron positivas en un solo paciente de siete (tabla 3).
Hallazgos analíticos en relación con la etiología
| Caso | Edad, años | LCR células | LCR PMN (%) | LCR MN (%) | LCR glucosa (mg/dl) | LCR protein (mg/dl) | BOC LCR | Leucocitos sangre | Proteína C reactiva (mg/dl) | Etiología |
| 1 | 4,5 | 121 | 95 | 5 | 60 | 60 | 10.190 | 2,29 | HHV6 | |
| PCR en LCR | ||||||||||
| 2 | 1,41 | 34.680 | 0,68 | |||||||
| 3 | 3,75 | 3 | 46 | 104 | 10.830 | |||||
| 4 | 2,25 | 30 | 25 | 75 | 59 | 30 | 24.140 | 1,27 | ||
| 5 | 0,5 | 3 | 59 | 32 | 11.910 | 0,07 | Polio-vacuna PCR en LCR | |||
| 6 | 5,42 | 64 | 75 | 25 | 65 | 30 | 15.610 | 3,13 | ||
| 7 | 8 | 5 | 51 | 65 | 6.880 | 1,3 | ||||
| 8 | 4,41 | 62 | 20 | 80 | 50 | 65 | 19.520 | CMV serología en sangre | ||
| 9 | 13,3 | 1 | 55 | 24 | ||||||
| 10 | 6,92 | 8 | 74 | 35 | + | HHV6, PCR en sangre | ||||
| 11 | 3,58 | 1 | 21.540 | HHV6, PCR en sangre | ||||||
| 12 | 11,2 | 114 | 25 | 75 | 67 | 89 | 16.100 | 0,05 | ||
| 13 | 4,67 | 3 | 59 | 34,5 | 16.970 | 7,21 | HHV6, PCR en sangre | |||
| 14 | 3,33 | 18 | 62 | 27 | 40.970 | 0,33 | VVZ Serología en sangre | |||
| 15 | 13,91 | 4 | 71 | 73 | 91.00 | 0,12 | ||||
| 16 | 3,5 | 40 | 65 | 35 | 60 | 49 | 54.770 | 0,21 |
La reacción en cadena de la polimerasa (PCR) fue positiva en líquido cefalorraquídeo en un paciente a CMV y en otro a VHH6. La PCR en sangre resultó positiva en 3 pacientes para VHH6. El paciente con antecedente de vacunación presentó PCR positiva en LCR a virus de la poliomielitis vacunal.
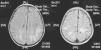
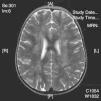
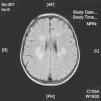
Hallazgos de neuroimagenSe encontraron más de 3 lesiones en 15 pacientes (93,8%). Todos los pacientes mostraban lesiones en el SNC, 9 de los cuales (56,2%) solo tenían lesiones cerebrales. Cuatro pacientes (25%) tenían lesiones en cerebelo, 3 pacientes (18,8%) en troncoencéfalo y 5 pacientes (31,2%) en la médula espinal. A nivel supratentorial, en 3 pacientes (18,8%) se encontraron lesiones periventriculares y en 14 pacientes (87,5%) lesiones subcorticales, en 4 pacientes (25%) lesiones en los ganglios de la base, en 2 pacientes (12,5%) lesiones talámicas, y en 4 pacientes lesiones en la cápsula interna (25%). Una descripción más detallada se presenta en la tabla 4.
Detalle de hallazgos radiológicos
| Caso | RM craneal y/o medular: descripción de los hallazgos potenciados en T2 |
| 1 | Lesiones en sustancia blanca periventricular bihemisférica sin captación de contraste y alteración señal troncoencéfalo dorsal. RMI medular: normal |
| 2 | Alteración de señal fundamental en sustancia blanca profunda y también periventricular con afectación de núcleos de la base (supratentoriales>8 lesiones) |
| 3 | Imágenes subcorticales pequeñas, no captan contraste en ambos hemisferios a nivel subcortical frontal y parietal. RMI medular: normal |
| 4 | Focos de desmielinización en sustancia blanca supra e infratentorial, cerebelo con alteración de señal en núcleos de la base. RMI medular: C2-C4, dorsal distal y cono medular |
| 5 | Lesiones nodulares milimétricas en pedúnculos cerebelosos y bulbo parasagital derecho |
| 6 | Lesiones hiperintensas talámicas bilaterales simétricas, sin otros focos de desmielinización |
| 7 | Hiperintensidad de sustancia blanca ambos lóbulos parietales y en parte superior de ambos lóbulos frontales, de forma parcheada |
| 8 | Aumento de señal en sustancia blanca de lóbulos frontales y occipitales, afectación difusa simétrica subcortical |
| 9 | Lesión hiperintensa en T2 y FLAIR desde la corona radiada derecha afectando al brazo posterior de la cápsula interna derecha, hasta el pedúnculo cerebeloso derecho, y lesión hiperintensa de 0,5cm en la hemiprotuberancia derecha |
| 10 | Aumento señal lineal en lóbulo parietal, ganglios basales izquierdos y hemisferio cerebeloso izquierdo. RMN medular: hiperintensidad T2 y ensanchamiento desde C7 hasta cono medular |
| 11 | Numerosas lesiones en sustancia blanca de localización periférica corticosubcortical, supratentoriales bihemisféricas de aproximadamente 1cm de diámetro, brillantes |
| 12 | Alteraciones focales múltiples de sustancia blanca subcortical en ambos hemisferios hiperintensas en T2 y de contorno irregular |
| 13 | Lesión nodular talámica posteromedial de 1cm y en la segunda RM a los 7 días: supratentoriales subcorticales (> 8 lesiones) |
| 14 | RM cráneo y médula: lesiones periventriculares (> 8), cerebelo y médula |
| 15 | RM cráneo: ganglios de la base, subcortical y sustancia gris de regiones témporo-occipitales |
| 16 | RMN cráneo medular: alteración de sustancia blanca subcortical en la región occipital preferentemente y también lesiones corticosubcorticales parietales y frontales. Afectación a nivel de médula cervical y dorsal |
De los 16 pacientes, se decidió no tratar en 4 casos dada la clínica y la evolución inicial mostrada. En 5 casos el tratamiento fue con esteroides durante una media de 15 días, a dosis equivalentes de 2mg/kg de metilprednisolona, con pauta descendente ulterior. En uno de los anteriores, la pauta incluyó 3 días a dosis de 30mg/kg. En otros 3 casos se siguió una pauta de 2g de inmunoglobulinas en 5 días y en 4 se pautó una terapia combinada de inmunoglobulinas mas corticoides. El tratamiento fue bien tolerado en todos los pacientes sin complicaciones relevantes.
Presentaron una evolución favorable con recuperación completa 13 pacientes (87,5%), 2 pacientes fallecieron, uno de ellos por complicaciones asociadas a secuelas neurológicas (había seguido terapia combinada de esteroides e inmunoglobulinas) y otro paciente (relacionado con polio vacunal) que fue diagnosticado de inmunodeficiencia combinada grave por déficit de HLA de clase II por sobreinfección concomitante. Un tercer caso precisó tratamiento anticomicial por persistencia de crisis parciales complejas a los 2 meses del alta. Los pacientes realizaron un seguimiento en nuestra consulta de neuropediatría durante un tiempo medio de 2 años.
DiscusiónLa baja prevalencia de EMAD que se aprecia en nuestra serie (0,64 casos/100.000 niños menores de 14 años/año) se recoge también en otras publicaciones1. Aun así, constituye la causa más común de afección de sustancia blanca en el niño2.
La edad media en nuestra serie es similar a la de otras recogidas previamente, tanto en España como en otros países que las sitúan entre los 5,3 a los 8 años1,13,14 y claramente menor a le de pacientes con EM. El predominio del sexo masculino, se refiere en otras series de nuestro medio15 y en otras más amplias13, a pesar del predominio femenino habitual en procesos autoinmunes, principal hipótesis etiológica de la EMAD. Tampoco se recogieron antecedentes personales de interés en nuestros pacientes, salvo la inmunodeficiencia demostrada en un caso. La frecuencia de pacientes inmigrados se ha relacionado con la adaptación inmune a la virología local. En nuestra serie 6 de los casos provenían de otros países. Dos tercios de nuestros casos ocurrieron en meses fríos, en clara relación epidemiológica con las viriasis respiratorias. En 7 pacientes se identificó etiológicamente algún agente relacionado temporalmente con el debut de la EMAD, en 4 de los cuales se trató de HHV6. La relación con la vacuna de poliomielitis con virus atenuado por vía oral ha sido descrita previamente16.
La clínica más habitual también es similar a la recogida por otros autores (tabla 2) destacando en nuestra serie los síntomas motores y alteración de la marcha, junto a la alteración del nivel de consciencia en la mitad de los casos. Respecto a otras series la frecuencia de crisis convulsivas es mayor. En todos los pacientes en que se registró su EEG se encontró una alteración de base con lentificación global del trazado como dato de sufrimiento cerebral, que en varios manifestaba focalidad con mayor frecuencia que lo descrito en otras series y que se tradujo en la presencia de crisis parciales complejas con o sin generalización.
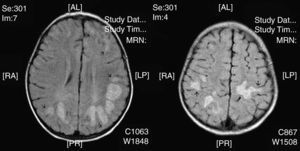
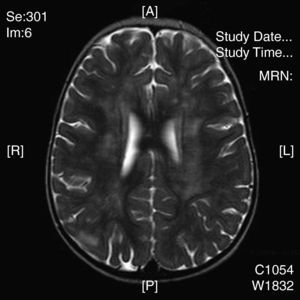
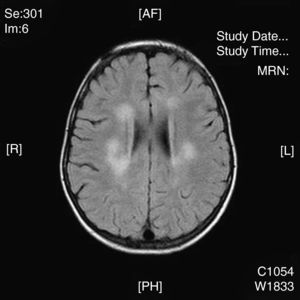
La neuroimagen forma parte fundamental en el diagnóstico y seguimiento de estos pacientes, ya que las lesiones aparecen en el 100% de los casos. El uso de la TC nos resultó útil en un primer momento para descartar otras causas que pueden ocasionar clínica similar pero no es tan sensible como la RM. La RM supone la herramienta más importante para el diagnostico de trastornos desmielinizantes inflamatorios en niños. Las alteraciones son más evidentes en T2 y FLAIR y habitualmente no captan contraste. Se están intentando dilucidar cuáles son los criterios más fiables que permitirían diferenciar el primer episodio de EM de los trastornos monofásicos como la EMAD. En general, las lesiones en la EMAD son múltiples en la sustancia blanca subcortical y mucho menos en la sustancia blanca periventricular y el cuerpo calloso. Pueden afectar al tronco y con frecuencia al cerebelo. A menudo, la sustancia gris cortical profunda y núcleos de la base presentan alteraciones. La aparición de lesiones cerebrales múltiples o la clínica en ciertos casos obliga a plantearse la ampliación del estudio a nivel medular. La repetición de neuroimagen en un intervalo amplio, así como lesiones en áreas concretas, sirve para sospechar o descartar la posibilidad de un proceso crónico como EM. Nuestros casos presentaban lesiones compatibles con lo previamente publicado en general, aunque se hallaron distintos tipos de patrones: lo más frecuente con afectación en sustancia blanca profunda subcortical (fig. 2), otros con afectación difusa en el centro semioval (fig. 3) y en otro caso predominaron las lesiones más próximas a ventrículos (fig. 4). Nuestros pacientes mostraban lesiones cerebrales en todos los casos. Solo 3 casos presentaban alteración de la sustancia blanca periventricular. Asimismo se observó en general un predominio posterior de las lesiones. La afectación medular asociada ocurrió en 5 casos (tabla 2). La afectación de fosa posterior ocurrió en 6 pacientes. Todas las lesiones se han presentado en un mismo estadio evolutivo, en consonancia con los criterios descritos para la distinción entre EM y EMAD17.
Con relación a los resultados analíticos, el LCR muestra hallazgos consistentes en pleocitosis en 8 de 15 y proteninorraquia en 7 de 15, lo que indica que el análisis citoquímico del LCR es de escasa utilidad diagnóstica, más allá de descartar un proceso infeccioso activo. Solo 1 de 7 pacientes presentaba BOC positivas. Este paciente, tras 22 meses de seguimiento, no ha presentado recaída. Otros análisis específicos de LCR, como anticuerpos anti-MOG o interleucinas (IL), no estuvieron a nuestro alcance. La PCR en el LCR frente al virus grupo herpes, enterovirus y otros agentes solo detectó en un caso el HHV6 y en otro el virus polio vacunal. Esta técnica de amplificación nucleica en paralelo con sangre no encontró dichos agentes. Por otra parte, se detectó en sangre un caso de CMV y en otros 3 el HHV6 que no habían resultado positivos en LCR.
Con respecto a la hematimetría, se ha podido apreciar tendencia a leucocitosis, en ocasiones muy elevada, sin evidencia analítica de signos de infección activa como la proteína C reactiva. Es destacable esta escasa elevación de los reactantes de fase aguda en nuestros pacientes como ocurre en ciertas enfermedades autoinmunitarias como el lupus. La asociación de la EMAD con la presencia de HHV6 en suero en 3 pacientes y en el LCR en otro parece estar en relación con la patogenia sospechada, ya que el daño por este agente parece no ser citopático directo, sino inmunomediado a través de la IL-818,19. La presencia de HHV6 en casos de EMAD con una clínica y un patrón radiológico en la MRI compatibles ya ha sido descrita con anterioridad20,21.
No se evidenció recurrencia de los episodios en nuestros pacientes, lo que indica la escasa frecuencia de la variante recurrente, así como de la variedad hemorrágica EMAD, de la que no recogimos ningún caso.
Con respecto al tratamiento, no se constataron diferencias en los resultados respecto de la terapia utilizada. El tratamiento se decidió en función del grado de afectación al diagnóstico. En los pacientes donde se constató escasa repercusión clínica y/o el inicio de la recuperación de forma precoz, se optó por una actitud expectante cuyos resultados fueron positivos. El pronóstico con una media de seguimiento de 2 años (2-60meses) fue bueno. La mortalidad en relación directa con la EMAD en nuestra serie se reduce a un caso, ya que el otro fallecimiento fue dilatado en el tiempo y se relacionó con la inmunodeficiencia de base del paciente.
Las limitaciones de nuestro estudio son varias. En primer lugar, se trata de un análisis retrospectivo. También la variabilidad en el tiempo de los avances diagnósticos con incorporación de nuevas técnicas de análisis, como la PCR a virus más extensos, la inclusión de nuevos criterios como las BOC en el protocolo de estudio a partir del 2005. También el momento evolutivo del paciente a la hora de consultar por primera vez puede modificar los hallazgos clínico-radiológicos y la decisión de iniciar tratamiento.
En resumen, nuestra revisión describe una nueva serie de casos que viene a afianzar los resultados ya obtenidos en otras series en nuestro medio. La incidencia anual en menores de 14 años se estimó en 0,64/100.000. La clínica y la radiología por RMI fueron la base del diagnóstico. La mayoría de los pacientes se recuperó por completo. Queremos resaltar la frecuencia en la implicación hallada para el HHV6, con hasta una cuarta parte de los pacientes, un nuevo caso asociado a polio vacunal y la consonancia con la aplicación de los criterios basados en la neuroimagen para distinguir la EMAD de procesos que puedan evolucionar a una EM. Son necesarios estudios inmunológicos en el LCR para detectar la presencia de marcadores que puedan ayudar a la identificación precoz de la enfermedad. La conservación de muestras para trabajos multicéntricos futuros se debe valorar si la infraestructura del centro lo permite, dado el avance de la inmunoquímica diagnostica.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.